最优混凝搅拌条件的研究
- 格式:doc
- 大小:157.50 KB
- 文档页数:8


混凝实验报告实验目的,通过混凝实验,研究混凝剂对水质的净化效果,探讨最佳混凝剂用量及混凝时间,为水处理工程提供科学依据。
实验原理,混凝是指在水中加入混凝剂后,使水中的悬浮物、胶体物质凝聚成较大的絮凝体,便于后续的沉降或过滤。
混凝剂一般为阳离子、阴离子或非离子高分子物质,其作用机理主要有吸附、中和、电中和和凝聚等。
实验材料与方法:材料,实验室自来水、混凝剂(聚合氯化铝)、搅拌器、玻璃容器、pH计、浊度计等。
方法:1. 取一定量自来水倒入玻璃容器中;2. 用搅拌器将水搅拌均匀;3. 用pH计检测水的初始pH值;4. 在搅拌的同时,向水中加入不同剂量的混凝剂;5. 混凝一定时间后停止搅拌,观察絮凝体的生成情况;6. 用浊度计检测水的浊度,记录下实验数据。
实验结果与分析:经过一系列实验,我们得出以下结论:1. 随着混凝剂用量的增加,水中絮凝体的生成量逐渐增加,浊度逐渐降低,水质得到了改善;2. 随着混凝时间的延长,絮凝体的大小逐渐增加,浊度进一步降低,但当混凝时间过长时,絮凝体又会发生分散,浊度会有所上升;3. 初始水质的pH值对混凝效果也有一定影响,一般情况下,pH值在6.5-7.5之间时,混凝效果较好。
结论:混凝实验结果表明,聚合氯化铝作为混凝剂,能够有效地改善水质,提高水的透明度,减少水中的悬浮物和胶体物质。
在实际应用中,应根据水质的不同情况,合理控制混凝剂的用量和混凝时间,以达到最佳的净化效果。
总结:通过本次混凝实验,我们对混凝剂的作用机理和影响因素有了更深入的了解,为今后的水处理工程提供了有益的参考。
同时,也为我们提供了实验操作的经验,为今后的科研工作打下了坚实的基础。
实验报告撰写人,XXX。
日期,XXXX年XX月XX日。

一、实验目的1. 了解混凝过程的基本原理及其在水质净化中的应用。
2. 探究不同混凝剂对水质净化效果的影响。
3. 通过实验确定最佳混凝条件,以优化水质净化效果。
4. 分析实验数据,总结混凝过程的关键影响因素。
二、实验原理混凝过程是利用混凝剂使水中的悬浮颗粒、胶体等杂质聚集成较大的絮体,从而实现水质净化的过程。
混凝剂通过压缩双电层、吸附架桥等作用,使杂质颗粒相互吸引、聚集,形成易于沉降的絮体。
三、实验材料与仪器1. 实验材料:原水、聚合氯化铝(PAC)、硫酸铝(SAS)、氢氧化钠(NaOH)、硫酸铁(FeSO4)、碳酸钠(Na2CO3)等。
2. 实验仪器:混凝实验装置、电子天平、pH计、浊度计、搅拌器、烧杯、玻璃棒等。
四、实验方法1. 实验步骤:(1)取一定量的原水置于烧杯中,测定初始pH值和浊度。
(2)分别向烧杯中加入不同种类和浓度的混凝剂,搅拌一定时间。
(3)测定混凝后的pH值、浊度和沉淀时间。
(4)观察沉淀物形态,记录实验数据。
2. 实验条件:(1)原水:取自某地表水体,浊度约为30NTU。
(2)混凝剂:PAC、SAS、NaOH、FeSO4、Na2CO3等。
(3)搅拌速度:100-200转/分。
(4)沉淀时间:30分钟。
五、实验结果与分析1. 不同混凝剂对水质净化效果的影响:表1:不同混凝剂对水质净化效果的影响| 混凝剂 | 投加量(mg/L) | 沉淀时间(分钟) | 浊度(NTU) || ------ | -------------- | ---------------- | ------------ || PAC | 20 | 30 | 1.5 || SAS | 20 | 30 | 2.0 || NaOH | 20 | 30 | 1.8 || FeSO4 | 20 | 30 | 1.2 || Na2CO3 | 20 | 30 | 2.5 |由表1可知,PAC和FeSO4的混凝效果较好,浊度去除率分别为50%和60%。
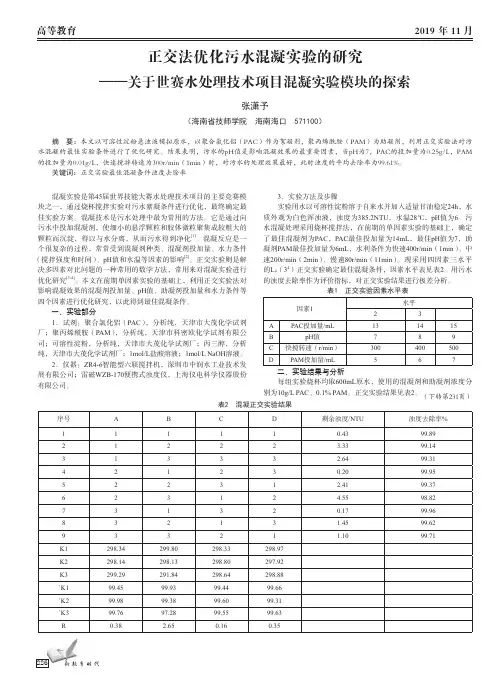
高等教育2019 年 11 月226正交法优化污水混凝实验的研究——关于世赛水处理技术项目混凝实验模块的探索张潇予(海南省技师学院 海南海口 571100)摘 要:本文以可溶性淀粉悬浊液模拟原水,以聚合氯化铝(PAC)作为絮凝剂,聚丙烯酰胺(PAM)为助凝剂,利用正交实验法对污水混凝的最佳实验条件进行了优化研究。
结果表明,污水的pH值是影响混凝效果的最重要因素,当pH为7,PAC的投加量为0.25g/L,PAM 的投加量为0.01g/L,快速搅拌转速为300r/min(1min)时,对污水的处理效果最好,此时浊度的平均去除率为99.61%。
关键词:正交实验最佳混凝条件浊度去除率混凝实验是第45届世界技能大赛水处理技术项目的主要竞赛模块之一,通过烧杯搅拌实验对污水絮凝条件进行优化,最终确定最佳实验方案。
混凝技术是污水处理中最为常用的方法。
它是通过向污水中投加混凝剂,使细小的悬浮颗粒和胶体微粒聚集成较粗大的颗粒而沉淀,得以与水分离,从而污水得到净化[1]。
混凝反应是一个很复杂的过程,常常受到混凝剂种类、混凝剂投加量、水力条件(搅拌强度和时间)、pH值和水温等因素的影响[2]。
正交实验则是解决多因素对比问题的一种常用的数学方法,常用来对混凝实验进行优化研究[3-4]。
本文在前期单因素实验的基础上,利用正交实验法对影响混凝效果的混凝剂投加量、pH值、助凝剂投加量和水力条件等四个因素进行优化研究,以此得到最佳混凝条件。
一、实验部分1.试剂:聚合氯化铝(PAC),分析纯,天津市大茂化学试剂厂;聚丙烯酰胺(PAM),分析纯,天津市科密欧化学试剂有限公司;可溶性淀粉,分析纯,天津市大茂化学试剂厂;丙三醇,分析纯,天津市大茂化学试剂厂;1mol/L盐酸溶液;1mol/L NaOH溶液。
2.仪器:ZR4-6智能型六联搅拌机,深圳市中润水工业技术发展有限公司;雷磁WZB-170便携式浊度仪,上海仪电科学仪器股份有限公司。

混凝搅拌实验报告时间:2016年4月23日实验人员:一、实验目的及要求1、通过实验观察矾花生成过程,加深对絮凝理论的理解;2、确定混凝的最佳用量及最佳pH值;3、了解影响混凝效果的因素。
二、实验原理混凝是用来去除水中无机物和有机的胶体悬浮物。
通常在废水中所见到的胶体颗粒其大小变化约在100nm-10nm之间,而其τ电位在15-20毫伏之间。
胶体悬浮物的稳定性是由于高τ电位引起的斥力,或者是由于在亲水的胶体上吸附了一层非离子的聚合物所造成的。
混凝过程包括胶体悬浮物的脱稳和接着发生的使颗粒增大的凝聚作用。
随后这些大颗粒可以用沉淀、悬浮和过滤等方法去除。
脱稳是通过投加强的用离子电解质如Al3+、Fe3+或阳离子高分子电解质来降低τ电位,或者由于形成了带正电荷的含水氧化物如Al x(OH)Y+而吸附于胶体上,或者是通过阴离子和阳离子高分子电解质的自然凝聚,或是由于胶体悬浮物被围于含水氧化物的矾花内等方式来完成的。
形成矾花最佳的条件是要求pH值在等电离点或接近等电离点(对于铝来说,要求pH值得范围为5.0-7.0),同混凝剂的反应必须有足够的碱度,对于碱度不够的废水应该投加Na2CO3、NaOH或石灰。
最有效的脱稳是使胶体颗粒同小的带正电荷含水氧化物的微小矾花接触,这种氧化物的微小矾花是在小于0.1s的时间内产生的,因此要在短时间内剧烈搅拌,在脱稳之后,凝聚促使矾花增大,从而使矾花能从水中去除。
铝和铁的矾花在搅拌时较容易破碎和离散。
投加2-5ml/L活性硅有可能提高矾花的强度。
在凝聚阶段将近结束时,投加0.2-1.0ml/L长链阴离子或非离子聚合物,通过桥联吸附作用,有助于矾花的聚集和长大。
所需混凝剂的投加量将由于盐和阴离子表面活性剂的存在而增加。
脱稳也能通过投加阳离子聚合物来完成。
混凝的通常顺序是:1、将混凝剂与水迅速剧烈的搅拌。
如果水中碱度不够,则要在快速搅拌之前投加碱性助凝剂。
2、如果使用活性硅和阳离子高分子电解质,则它们应在快速搅拌将近结束时投加。


混凝搅拌实验报告时间:2016年4月23日实验人员:一、实验目的及要求1、通过实验观察矾花生成过程,加深对絮凝理论的理解;2、确定混凝的最佳用量及最佳pH值;3、了解影响混凝效果的因素。
二、实验原理混凝是用来去除水中无机物和有机的胶体悬浮物。
通常在废水中所见到的胶体颗粒其大小变化约在100nm-10nm之间,而其τ电位在15-20毫伏之间。
胶体悬浮物的稳定性是由于高τ电位引起的斥力,或者是由于在亲水的胶体上吸附了一层非离子的聚合物所造成的。
混凝过程包括胶体悬浮物的脱稳和接着发生的使颗粒增大的凝聚作用。
随后这些大颗粒可以用沉淀、悬浮和过滤等方法去除。
脱稳是通过投加强的用离子电解质如Al3+、Fe3+或阳离子高分子电解质来降低τ电位,或者由于形成了带正电荷的含水氧化物如Al x(OH)Y+而吸附于胶体上,或者是通过阴离子和阳离子高分子电解质的自然凝聚,或是由于胶体悬浮物被围于含水氧化物的矾花内等方式来完成的。
形成矾花最佳的条件是要求pH值在等电离点或接近等电离点(对于铝来说,要求pH值得范围为5.0-7.0),同混凝剂的反应必须有足够的碱度,对于碱度不够的废水应该投加Na2CO3、NaOH或石灰。
最有效的脱稳是使胶体颗粒同小的带正电荷含水氧化物的微小矾花接触,这种氧化物的微小矾花是在小于0.1s的时间内产生的,因此要在短时间内剧烈搅拌,在脱稳之后,凝聚促使矾花增大,从而使矾花能从水中去除。
铝和铁的矾花在搅拌时较容易破碎和离散。
投加2-5ml/L活性硅有可能提高矾花的强度。
在凝聚阶段将近结束时,投加0.2-1.0ml/L长链阴离子或非离子聚合物,通过桥联吸附作用,有助于矾花的聚集和长大。
所需混凝剂的投加量将由于盐和阴离子表面活性剂的存在而增加。
脱稳也能通过投加阳离子聚合物来完成。
混凝的通常顺序是:1、将混凝剂与水迅速剧烈的搅拌。
如果水中碱度不够,则要在快速搅拌之前投加碱性助凝剂。
2、如果使用活性硅和阳离子高分子电解质,则它们应在快速搅拌将近结束时投加。

烧杯实验最优混凝剂选择烧杯实验最优混凝剂选择1、试验部分1.1 实验设备搅拌仪:(1)六联程控彩屏混凝试验搅拌仪(2)水样容器,容量V=1L(3)浊度仪:美国HACH 公司2100AN 型浊度仪1.2 试验原水与混凝剂1.2.1原水为黄河输水库水,浊度平均3-4 NTU,水温平均3.5O C;1.2.2混凝剂:(1)PAC(聚合氯化铝)(2)HACC(壳聚糖季铵盐)(3)铝铁盐助凝剂:PAM(聚丙烯酰胺)2.选择最优混凝剂的实验2.1搅拌仪转速与速度梯度G值对应值2.2 沉淀池过水时间表1 沉淀池容积表2 过水时间(以反应区计算)2.3混凝试验通过烧杯实验优选混凝剂种类,在条件恒定情况下同时确定混凝剂的最佳投药量。
搅拌转速固定,通过做PAC实验一段时间来看,在不同加药量情况下,分别固定慢速搅拌转速在10-160r/min条件下,得到结果是60r/min以上澄清后浊度接近于原水浊度,而在60r/min以下则低于原水浊度;选择絮凝时间固定在12min。
恒定条件:(1)搅拌强度分为2档:快速混合转速固定在260r/min,G1=102.4 s-1,时间T1=2min慢速搅拌转速固定在50r/min,G2=11.2s-1;时间T2=12min(2)搅拌结束后静置沉淀10min, 测定上清液的浊度。
混凝剂:PAC,助凝剂:PAM 原水浊度:3.4NTU 水温:3.5O C混凝剂:HACC,助凝剂:PAM 原水浊度:3.4NTU 水温:3.5O C混凝剂:铝铁盐, 助凝剂:PAM 原水浊度:3.4NTU 水温:3.5O C4.不同混凝剂效果比较5.实验结果分析通过对静置后浊度的测量,整体浊度相差不是很大,在相同条件下,可以看出加HACC之后浊度整体最低,其次是PAC,最后是铝铁盐;加药量在14-22mg/L范围内浊度相应较低,在接近18mg/L加药量浊度都较低;最后可以得出在相同条件下用混凝剂HACC效果最好。

混凝实验一实验目的1.了解混凝的现象及过程,净水作用及影响混凝的主要因素;2.学会求水样最佳混凝条件(包括投药量、pH值、水流速度梯度)的基本方法;3.了解助凝剂对混凝效果的影响。
二实验原理胶体颗粒带有一定电荷,它们之间的电斥力是胶体稳定性的主要因素。
胶体表面的电荷值常用电动电位ξ表示,又称为Zeta电位。
Zeta电位的高低决定了胶体颗粒之间斥力的大小和影响范围。
一般天然水中的胶体颗粒的Zeta电位约在-30mV以上,投加混凝剂之后,只要该电位降到-15mV左右即可得到较好的混凝效果。
相反,当Zeta电位降到零,往往不是最佳混凝状态。
投加混凝剂的多少,直接影响混凝效果。
水质是千变万化的,最佳的投药量各不相同,必须通过实验方可确定。
在水中投加混凝剂如Al2(SO4)3、FeCl3后,生成的Al(III)、Fe(III)化合物对胶体的脱稳效果不仅受投加的剂量、水中胶体颗粒的浓度、水温的影响,还受水的pH值影响。
如果pH值过低(小于4),则混凝剂水解受到限制,其化合物中很少有高分子物质存在,絮凝作用较差。
如果pH值过高(大于9~10),它们就会出现溶解现象,生成带负电荷的络合离子,也不能很好地发挥絮凝作用。
投加了混凝剂的水中,胶体颗粒脱稳后相互聚结,逐渐变成大的絮凝体。
混凝剂量少,达不到降低浊度的目的,混凝剂量过多,混凝效果反而下降,浊度增大,所以通过实验有最佳的投药量。
选定水样的pH,投药量从最小(确定形成矾花所用的最小混凝剂量:通过慢速搅拌烧杯中500ml的原水,并每次增加1ml混凝剂,直至出现矾花为止,这时的混凝剂作为形成矾花的最小投加量。
一般以5ml为最小混凝剂量)逐级递加,取6个药量梯度。
当单独使用混凝剂不能取得预期效果时,需投加助凝剂以提高混凝效果。
助凝剂通常是高分子物质,作用机理是高分子物质的吸附架桥,它能改善絮凝体结构,促使细小而松散的絮粒变得粗大而结实。
三实验设备仪器1.六联搅拌机(附6个800ml烧杯,实验水样选用500ml体积);2. pH计; 3.温度计; 4.浊度仪。


混凝实验报告混凝是一种常用的水处理方法,适用于去除水中悬浮物、浑浊物、色度、胶体和油脂等杂质,提高水的透明度和稳定性。
本次实验旨在通过研究不同混凝剂对水的混凝效果以及水的pH值和温度对混凝效果的影响,探究混凝过程的机理和优化混凝条件。
实验方法实验过程中使用的混凝剂为铁(Ⅲ)氯化物、铝(Ⅲ)氯化物和硫酸铵铁(Ⅲ),分别称取适量混入500mL这样的容器中,加入适量的净水搅拌使混凝剂完全溶解,然后将一定量的硬质水样液(100mL)加入其中,用漏斗过滤器过滤出混凝后的水,用透过滤纸的光线强度测定仪,测定过滤后水的透明度,并记录其透射率。
同时,记录混凝前水的pH值和温度,并在混凝后再次记录。
实验结果实验结果表明,铁(Ⅲ)氯化物、铝(Ⅲ)氯化物和硫酸铵铁(Ⅲ)均具有较好的混凝效果,其混凝后的水的透明度明显提高。
其中,铁(Ⅲ)氯化物和硫酸铵铁(Ⅲ)的混凝效果略优于铝(Ⅲ)氯化物。
不同混凝剂的混凝效果可能与其所含的氧化性、还原性离子的数量和能量、pH值等因素有关。
此外,实验表明,不同pH值下,混凝剂的混凝效果也会有所不同。
在酸性条件下,它们的混凝效果较好,其中硫酸铵铁(Ⅲ)的混凝效果最好。
但在强碱性环境下,混凝剂的混凝效果会受到一定影响,其中铁(Ⅲ)氯化物的混凝效果最差。
另外,实验还发现,温度对混凝效果也有一定影响。
随着温度的升高,混凝剂的混凝效果会逐渐下降,可能是由于温度升高后分子的热运动增强,使混合物中的悬浮物增加在粘度下降的情况下,从而不利于混凝。
讨论与结论本次实验通过分析不同混凝剂对水的混凝效果以及水的pH值和温度对混凝效果的影响,可以看出混凝剂的选择、pH值的调整和温度的控制等因素,都会直接影响混凝效果的好坏。
通过深入研究以上因素对混凝效果的影响,可以有效优化混凝工艺,并为实际水处理中的混凝工艺的优化提供一定参考价值。
此外,鉴于不同混凝剂的差异性,水处理工程师应当根据实际情况选择合适的混凝剂,提高混凝效率,降低成本。
第1篇一、实验目的1. 了解混凝搅拌的基本原理和过程。
2. 掌握混凝搅拌实验的操作方法和步骤。
3. 分析不同混凝剂和搅拌条件对混凝效果的影响。
4. 优化混凝搅拌工艺,提高水处理效果。
二、实验原理混凝搅拌实验是水处理过程中关键的一环,通过向水体中加入混凝剂,使悬浮物和胶体颗粒脱稳,相互聚集形成絮凝体,从而实现固液分离。
实验原理主要包括以下三个方面:1. 压缩双电层作用:混凝剂中的正电荷离子与悬浮物表面的负电荷离子发生中和反应,使悬浮物表面的电荷降低,从而降低悬浮物的稳定性,促进其聚集。
2. 吸附架桥作用:混凝剂分子中的桥连基团吸附在悬浮物颗粒表面,将不同颗粒连接起来,形成较大的絮凝体。
3. 电中和作用:混凝剂中的正电荷离子与悬浮物表面的负电荷离子发生中和反应,降低悬浮物的表面电荷,从而降低其稳定性。
三、实验材料与仪器1. 实验材料:原水、聚合氯化铝、硫酸铝、聚丙烯酰胺等混凝剂。
2. 实验仪器:烧杯、搅拌器、秒表、温度计、量筒、滤纸等。
四、实验步骤1. 样品准备:取一定量的原水置于烧杯中,测量水温。
2. 混凝剂投加:根据实验设计,向烧杯中加入不同种类和浓度的混凝剂。
3. 搅拌:启动搅拌器,以一定速度搅拌水样,保持搅拌时间。
4. 取样:在搅拌过程中,定时取样,观察絮凝体形成情况。
5. 过滤:将样品过滤,测量过滤后的浊度。
6. 数据分析:根据实验数据,分析不同混凝剂和搅拌条件对混凝效果的影响。
五、实验结果与分析1. 混凝剂种类对混凝效果的影响:实验结果表明,聚合氯化铝和硫酸铝对混凝效果较好,而聚丙烯酰胺的混凝效果较差。
2. 混凝剂浓度对混凝效果的影响:随着混凝剂浓度的增加,混凝效果逐渐提高,但超过一定浓度后,混凝效果变化不大。
3. 搅拌速度对混凝效果的影响:实验结果表明,搅拌速度对混凝效果有较大影响。
搅拌速度过快,容易破坏絮凝体;搅拌速度过慢,则混凝效果较差。
4. 搅拌时间对混凝效果的影响:搅拌时间对混凝效果有较大影响。
混凝实验条件下混凝剂最佳投加量的选择方法研究本文旨在研究混凝实验条件下混凝剂最佳投加量的选择方法。
通过实验室模拟混凝实验,探究不同混凝剂投加量对混凝效果的影响,进而确定最佳投加量。
实验结果表明,在混凝实验条件下,最佳混凝剂投加量应在30-50 mg/L之间。
本研究为混凝剂的合理使用提供了一定的参考。
关键词:混凝剂,投加量,混凝实验,混凝效果引言:混凝是水处理中的重要工艺之一,它通过添加混凝剂,使水中的悬浮物和胶体颗粒凝聚成较大的团块,便于沉淀和过滤。
混凝剂的使用对于提高水质具有重要的意义。
然而,混凝剂的投加量是影响混凝效果的关键因素之一。
因此,确定最佳的混凝剂投加量,对于提高混凝效果和减少混凝剂的浪费具有重要的意义。
目的:本文旨在研究混凝实验条件下混凝剂最佳投加量的选择方法。
通过实验室模拟混凝实验,探究不同混凝剂投加量对混凝效果的影响,进而确定最佳投加量。
实验方法:实验采用混凝池模拟实验室混凝实验。
实验用水采用自来水,水质稳定。
实验采用聚合氯化铝作为混凝剂,投加量分别为10 mg/L、20 mg/L、30 mg/L、40 mg/L、50 mg/L。
实验中,将混凝剂依次加入混凝池中,然后进行搅拌,搅拌时间为5分钟。
搅拌后,静置3小时,观察沉淀效果。
实验结果:实验结果如下表所示:混凝剂投加量(mg/L)沉淀效果10 未沉淀20 部分沉淀30 完全沉淀40 完全沉淀50 完全沉淀实验结果表明,在混凝实验条件下,最佳混凝剂投加量应在30-50 mg/L之间。
当投加量为10 mg/L时,混凝效果非常差,未能达到混凝的目的。
当投加量为20 mg/L时,混凝效果有所提高,但仍然不够理想。
当投加量为30 mg/L时,混凝效果达到最佳状态,完全沉淀。
当投加量继续增加到40 mg/L和50 mg/L时,混凝效果并没有显著提高。
讨论:混凝剂的投加量是影响混凝效果的重要因素之一。
过少的投加量会导致混凝效果不理想,过多的投加量会导致混凝剂的浪费。
1、实验目的(1)掌握混凝工艺基本原理;(2)独立设计混凝实验方案;(3)深入理解G值、GT值、混凝剂、助凝剂、PH值等对混凝效果的影响;(4)优化混凝工艺条件参数(原水经处理后综合去除率最高),确定PAC、PAM最佳投药量、最佳pH值,并计算处理成本,最好得到单位去除率成本最低的方案。
2、基本原理混凝剂通过电性中和或吸附架桥作用,而使分散在水中稳定状态的胶体颗粒脱稳,进而相互凝聚在一起形成矶花;混凝处理的效果不仅与混凝剂的投量有关,同时还与被处理水的pH、水温及处理过程中的水力条件(G值、GT值) 等因素有密切的关系;3、试验器材磁力搅拌机、250ml烧杯、配置好的聚合氯化铝(PAC)、聚丙烯酰胺(PAM)、硫酸溶液、氢氧化钠溶液、PH试纸、相关指标(COD cr/BOD5/TP/TN/NH3-N/PH/色度)检测,移液管、玻璃棒等其他常规试验器材4、操作步骤(1(2)确定混凝剂(PAC)最小投加量m正式开始试验前,取150ml原水,用移液管逐滴加入配置好的PAC溶液,并不停用玻璃棒搅拌,直至钒花出现,记录PAC投加量为m;(3)确定污染物去除率最高的PAC投加量M取5个烧杯依次编号,分别投加PAC的量为0、0.5m、m、2m、4m,在转速200r/min 的情况下运行直至钒花稳定,记录时间,并静置15min后取上清液,测各污染物指标并计算各污染物去除率,填入下表,选取最佳去除率的投加量记录为M:(4)确定最佳PH值取4个烧杯依次编号,分别投加PAC的量为M,通过滴加配置好的H2SO4和NaOH 溶液调整PH分别为5、7、8、10,在转速200r/min的情况下运行直至钒花稳定,记录时间,并静置15min后取上清液,测各污染物指标并计算各污染物去除率,填入下表,(5取5个烧杯依次编号,分别投加PAC的量为M,调整PH至最佳PH,在5个烧杯中分别加入不同体积的PAM,在转速200r/min的情况下运行直至钒花稳定,并静置15min后取上清液,测各污染物指标并计算各污染物去除率,填入下表,选取最佳去除率的(6)验证试验结果取3个烧杯依次编号,按照PAC、PAM的最佳投加量投加,调整PH至最佳PH,在转速200r/min的情况下运行直至钒花稳定,并静置15min后取上清液,测各污染物指标并计算各污染物去除率,与上面各步骤试验结果比较分析:。
混凝实验报告/正交设计一、实验目的1、通过实验,观察混凝现象,加深对混凝理论的理解2、选择和确定最佳混凝工艺条件。
二、实验原理天然水中存在大量胶体颗粒,使原水产生浑浊度。
我们进行水质处理的根本任务之一,则正是为了降低或消除水的浑浊度。
水中的胶体颗粒,主要是带负电的粘土颗粒。
胶体间静电斥力、胶粒的布朗运动以及胶粒表面水化作用的存在,使得它具有分散稳定性。
混凝剂的加入,破坏了胶体的散稳定性,使胶粒脱稳。
同时,混凝剂也起吸附架桥作用,使脱稳后的细小胶体颗粒,在一定的水力条件下,凝聚成较大的絮状体(矾花)。
由于矾花易于下沉,因此也就易于将其从水中分离出去,而使水得以澄清。
由于原水水质复杂,影响因素多,故在混凝过程中,对于混凝剂品种的选用和最佳投药量的决定,必需依靠原水和混凝实验来决定。
混凝实验的目的即在于利用少量原水、少量药剂。
三、实验仪器及设备1. 1000 ml 烧杯1 只2. 500 ml 矿泉水瓶6 只3. 100 ml 烧杯2 只4. 5 ml 移液管1只5. 400 ml 烧杯 2 只6. 5ml 量筒 1 台7. 吸耳球 1 个8. 温度计(0-50C)1只9. 100 ml 量筒 1 个10. 10 ml;量筒1只四、实验试剂本实验用三氯化铁作混凝剂,配制浓度2g/L, 800ml;以阴型聚丙烯酰胺为助凝剂,配制浓度0.05g/L, 500 ml。
三氯化铁用量2g,阴离子聚丙烯酰胺用量0.0250 g五、实验步骤一)配置药品1、用台秤称取2g三氯化铁,溶解,配置1000 ml,三氯化铁配制浓度2 g/L ;用电子天平称取0.05g阴离子聚丙烯酰胺,溶解,配置1000 ml,阴型聚丙烯酰胺配制浓度0.05 g/L。
2、测定原水特征。
二)混凝剂最小投加量的确定1、取6 个500 ml 瓶子,分别取400 ml 原水。
2、分别向烧杯中加入氯化铁,每次加入1.0 ml,同时进行搅拌,直至出现矶花,在表1 中记录投加量和矾花描述。
混凝实验报告/正交设计一、实验目的1、通过实验,观察混凝现象,加深对混凝理论的理解。
2、选择和确定最佳混凝工艺条件。
二、实验原理天然水中存在大量胶体颗粒,使原水产生浑浊度。
我们进行水质处理的根本任务之一,则正是为了降低或消除水的浑浊度。
水中的胶体颗粒,主要是带负电的粘土颗粒。
胶体间静电斥力、胶粒的布朗运动以及胶粒表面水化作用的存在,使得它具有分散稳定性。
混凝剂的加入,破坏了胶体的散稳定性,使胶粒脱稳。
同时,混凝剂也起吸附架桥作用,使脱稳后的细小胶体颗粒,在一定的水力条件下,凝聚成较大的絮状体(矾花)。
由于矾花易于下沉,因此也就易于将其从水中分离出去,而使水得以澄清。
由于原水水质复杂,影响因素多,故在混凝过程中,对于混凝剂品种的选用和最佳投药量的决定,必需依靠原水和混凝实验来决定。
混凝实验的目的即在于利用少量原水、少量药剂。
三、实验仪器及设备1. 1000 ml烧杯1只2. 500 ml矿泉水瓶6只3. 100 ml烧杯2只4. 5 ml移液管1只5. 400 ml烧杯2只6. 5ml量筒1台7. 吸耳球1个8. 温度计(0-50℃)1只9. 100 ml量筒1个10. 10 ml;量筒1只四、实验试剂本实验用三氯化铁作混凝剂,配制浓度2g/L,800ml;以阴型聚丙烯酰胺为助凝剂,配制浓度0.05g/L,500 ml。
三氯化铁用量2g,阴离子聚丙烯酰胺用量0.0250 g五、实验步骤(一)配置药品1、用台秤称取2g三氯化铁,溶解,配置1000 ml,三氯化铁配制浓度2 g/L;用电子天平称取0.05g阴离子聚丙烯酰胺,溶解,配置1000 ml,阴型聚丙烯酰胺配制浓度0.05 g/L。
2、测定原水特征。
(二)混凝剂最小投加量的确定1、取6个500 ml瓶子,分别取400 ml原水。
2、分别向烧杯中加入氯化铁,每次加入1.0 ml,同时进行搅拌,直至出现矾花,在表1中记录投加量和矾花描述。
3、停止搅拌,静止10min。
混凝搅拌实验条件探讨和结论摘要:随着国家和社会的发展,水厂的供水技术、工艺等方面也在提高。
混凝搅拌实验是水厂供水技术当中的一项重要的改革,提高了水厂的供水效率和质量。
本文结合乌鲁木齐市各水厂的进厂源水进行一系列的分析和讨论。
关键词:混凝搅拌实验,最优投加量,去除率1.实验设计以近两年红雁池水厂(东厂区)、石墩子山水厂、甘泉堡水厂的水源水为研究对象,对其浊度、搅拌速率和pH值范围进行统计分析后,取当地的源水用以实验。
各地表水水厂源水水质参数如表1所示。
表1 乌鲁木齐各地表水水厂源水参数根据水厂工艺经验,聚合氯化铝具有混凝效果好,对人体健康无害,使用方便,货源充足,价格低廉等优点,故采用聚合氯化铝作为试验用混凝剂。
本次试验选择源水pH值和水处理工艺中混凝剂投加量和减半前度三个参数作为实验研究对象,以源水浊度的去除率为评价标准,分析水处理工艺中混凝剂的使用条件。
由于水厂源水的水温难以控制,水温的变化不大对实验的影响很小,因此此实验不考虑水温对混凝实验的影响。
1.1实验材料及设备实验材料及设备包括:(1)六联搅拌机;(2)便携式浊度仪;(3)酸度计;(4)温度计;(5)1000mL烧杯6个;(6)聚合氯化铝(巩义市富源净水材料有限公司):配制成5 g/L的溶液;(7)水厂的源水。
1.2试验方法1.2.1单因素实验1.2.1.1混凝剂投加量对源水浊度去除率的影响首先确定形成矾花所用的最小混凝剂剂量,方法是通过慢速搅拌烧杯中1000 mL源水,并每隔10分钟投加0.5 mL混凝剂,直至出现矾花为止,这时的混凝剂用量作为形成矾花的最小投加量。
分别取6份1000 mL实验源水于六个烧杯中,向六个烧杯中分别投加不同量的聚合氯化铝(根据得出的形成矾花最小混凝剂投加量,取其0.25倍的投加量作为1号烧杯的混凝剂投加量,取其0.5,0.75,1.0,1.5,2.0倍作为2~6号烧杯的混凝剂投加量),以300 r/min的转速下快速搅拌2 min,再以60 r/min的转速下慢速搅拌10 min,静置沉降30 min,观察矾花的沉降情况,取其上清液测定其浊度。
最优混凝搅拌条件的研究————————————————————————————————作者:————————————————————————————————日期:最优混凝搅拌条件的研究混凝操作一般采用先快速搅拌(快速混合),然后慢速搅拌(絮凝)的水力条件。
快速搅拌的目的是为了使混凝剂瞬间、快速、均匀地分散到水中,以避免药剂分散不均匀,造成局部药剂浓度过高,影响混凝剂(如:硫酸铝)自身水解及其与水中胶体(或杂质颗粒)的作用。
慢速搅拌是为了使快速搅拌时生成的微絮凝体进一步成长成粗大、密实的絮凝体,以实现固液分离。
快速搅拌(混合)条件和慢速搅拌(絮凝)条件,现阶段设计和生产中,通常是按某固定值进行设计和控制的,即按某固定G值(搅拌强度)T值(搅拌时间)设计和控制,而没有考虑搅拌条件随投药量、原水浊度、水温等的变化而变化。
这样,不仅会使混凝费用增加,而且有时还会使混凝效果恶化。
本研究试图通过实验考察最优搅拌条件与投药量、原水浊度、水温等的关系,从而为生产中实时、最优地控制搅拌条件提供依据。
1 实验方法和条件混凝研究通常是通过烧杯搅拌试验,考察不同混凝条件下的除浊效果。
由于该过程经过的环节太多(快速搅拌、慢速搅拌、沉淀、测浊度),难免给实验结果带来误差。
故本实验拟采用直接测定絮凝体平均粒径,以絮凝体平均粒径为指标来研究混凝,因为混凝的目的就是为了使杂质颗粒凝聚变大。
絮凝体平均粒径的检测使用了絮凝检测仪,该仪器的检测值R(无量纲)可以相对地反映絮凝体平均粒径的大小[1],而且该值不受水样检测部分污染及电子元件漂移的影响,并且还可以实现在线连续检测。
1.1 实验装置混凝实验装置如图1所示。
混凝槽为方形槽,有效容积6.8L。
搅拌采用型号为DD60-2F型无级调速搅拌器。
用絮凝检测仪联机在线检测混凝过程中絮凝体平均粒径的变化(用检测值R反映),记录仪同时将检测信号自动记录。
原水用高岭土和哈尔滨市自来水按标准方法配制而成。
混凝剂用精制硫酸铝,用NaOH和HCl调整pH值。
图1混凝实验装置的密度1.2 搅拌强度G值的计算G值按张洪源等提出的公式(1)求搅拌器搅拌功率W,然后再由公式(2)求G值[2]。
W=14.35d4.38n2.69ρ00.69μ00.31 (1)G= (2)式中:d为搅拌叶片宽度(m);n为搅拌器转速(r/min);ρ0为水的密度(1000/9.81kg·s2/m4);μ0为水的绝对粘度(kg·s/m2);V为水样体积(m3)。
混凝实验装置中搅拌叶片的尺寸和水样体积之间的位置关系满足公式(1)的要求,不需修正。
1.3 实验资料的处理方法絮凝检测仪对混凝过程中絮凝体平均粒径变化的检测结果,可以由微机或自动记录仪在线连续记录下来。
图2是絮凝检测仪对高岭土悬浊液混凝过程检测的自动记录仪记录的结果。
图2中,投药后经过一定时间,R值开始快速增大,达到某一最大值后略有减小并趋于稳定。
由图2资料至少可以获得两个数据:一个是最大的R值(与最大絮凝体平均粒径对应);二是R值最大时的搅拌时间(从加药算起)。
在研究快速搅拌条件时,由于这时最终成长的絮凝体粒径很小,快速搅拌条件对混凝的影响难以由絮凝体粒径反映出来,故这时拟用絮凝体成长到最大(Rm值最大)所需时间t,即最优快速搅拌时间作为指标进行研究。
图2 混凝过程的检测在研究慢速搅拌条件时,由于这时絮凝体粒径大,故拟以最终成长的最大絮凝体粒径(用Rm反映)为参数进行研究。
并且为了简便,快速搅拌的G值和时间t采用固定的值,分别为106s-1和300s。
2 实验结果及分析2.1 最优快速搅拌条件2.1.1 投药量对最优快速搅拌时间的影响表1是在快速搅拌G值为106s-1,原水浊度42mg/L,水温13~14℃,不同投药量时,用絮凝检测仪测得的絮凝体平径粒径最大时的搅拌时间t(即最优快速搅拌时间)(篇幅限制,相应的图形曲线略)。
表1投药量对最优快速搅拌时间的影响Al2(SO4)3投量(mg/L) 最优快速搅拌时间tm(s)2 6806 46010 31014 16118 92原水浊度42mg/L;快搅G值106s-1;水温13~14℃;pH=7.2表1的结果有明显的规律,即随着投药量的增大,絮凝体平均粒径最大时的搅拌时间t显著减小。
实验中快速搅拌的G值固定为106s-1,由于最优快速搅拌时间随投药量的增大而减小,所以最佳GT值亦应随投药量的变化而调整,才能使快速搅拌条件最优。
表1的结果是由于低投药量时,悬浊质颗粒脱稳不充分,导致混凝速度慢、时间长。
而随着投药量的增大,悬浊质颗粒脱稳程度增大,颗粒之间凝结变得容易,使混凝速度加快,混凝时间变短。
由此,生产中快速搅拌条件应随投药量的变化而变化。
当投药量较小时,应将GT值增大;反之,可以减小GT值。
2.1.2 原水浊度对最优快速搅拌时间的影响表2是在一定的快速搅拌强度(G值为106s-1)、一定投药量、一定水温的条件下,原水浊度对最优快速搅拌时间影响的测定结果(图形略)。
共对四组不同投药量进行了研究。
表2的结果表明,当投药量较大时,随原水浊度的提高,最佳搅拌时间t略有减小,但变化较小;而投药量较小时,原水浊度对最佳搅拌时间t的影响很大;另外表2还表明,当原水浊度比较低时,最优搅拌时间随投量增大而缩短。
由此,生产中当投药量较小时,快速搅拌条件(用GT值反映)最好随原水浊度的变化适当调整;而对于低浊度原水,增加混凝剂投量,快速搅拌GT值可以减小。
表2 原水浊度对最优快速搅拌时间的影响时间(s)Al2(SO4)3投量(mg/L)浊度(mg/L)3 20 50 1003 610 504 206 1026 400 280 220 9514 170 110 98 9117 120 100 95 88快速搅拌G值106s-1;水温13~14℃;pH=7.2混凝剂必须与悬浊质碰撞才能发挥其混凝作用。
当混凝剂投量较小时,原水浊度越大,混凝剂越容易与杂质颗粒碰撞产生混凝作用,故其混凝速度快,时间短;相反,原水浊度较小时,混凝剂不易与杂质颗粒碰撞凝聚,所以混凝速度慢,时间长。
而当混凝剂投量增大时,即使原水浊度比较小,混凝剂与杂质颗粒也很容易碰撞,再加上加大投药量,可使胶粒脱稳充分,有利于提高混凝速度,缩短混凝时间,即高投药量时,最优快速搅拌时间受原水浊度影响不大。
2.1.3水温对最优快速搅拌时间的影响表3是水温对最优快速搅拌时间的影响情况(图形略)。
表3 水温对最优快速搅拌时间的影响时间(s)Al2(SO4)3投量(mg/L)水温(℃)2.1 4.8 10.2 14.9 20.33 700 650 520 400 27014 160 140 120 108 9617 120 110 105 97 90快速搅拌G值106s-1;原水浊度42mg/L;pH=7.2由表3可见,当投药量较低时,水温对最优快速搅拌时间的影响很显著,水温越高,最优快速搅拌时间越短;当投药量较大时,水温对最优快速搅拌时间的影响较小;对低温水样的混凝,投药量增大,可使最优快速搅拌时间明显缩短。
这些结果表明,对低温水的混凝,通过增加投药量可以使混凝反应更充分;而当投药量较小,水温较低时,通过延长快速搅拌时间可以保证混凝效果。
一方面水温影响混凝剂本身的水解反应速度,温度越低,水解反应速度越慢;另一方面水温还影响对混凝起关键作用的微涡旋以及水中各种微粒在水中的布朗运动,水温越低,布朗运动越慢,越不利于混凝,故而产生了上述的结果。
2.1.4 快速搅拌G值与最优快速搅拌时间t的关系表4是快速搅拌G值与最优搅拌时间t关系的实验结果(关系图略)。
由表4可见,随着快速搅拌强度G值的增大,最佳搅拌时间tm减小。
表4 G值与最佳快速搅拌时间t的关系快速搅拌G值(s-1) 最佳搅拌时间tm(s)50.8 73098.2 510148.8 370199.2 290原水浊度42mg/L;投药量14mg/L;水温13~14℃;pH=7.2以上结果与传统的GT值概念相吻合(理论不赘述)。
即在一定的G值范围内,可以以GT值为指标控制混凝的搅拌条件。
就快速搅拌的条件而言,当G值控制在一定范围时,GT值存在一个最佳值,此时的快速搅拌条件最佳,混凝效果最好,这时G值若增大,t减小;反之,t增大。
2.2 最优慢速搅拌G值2.2.1最优慢速搅拌G值混凝实验时,快速搅拌(G=106s-1)5min,慢速搅拌20min,考察慢速搅拌的G值对混凝效果的影响。
共作了两组不同投药量的试验,表5是试验结果(曲线图形略)。
表5 最优慢速搅拌G值对混凝效果的影响Al2(SO4)3投量(mg/L)G (s-1)3.24.8 7.2 10.4 15.2 20.8 353 - - 1.7 2.1 2.63 2.54 1.8514 0.7 2.5 2.6 2.4 1.8 - -原水浊度42mg/L;快速搅拌G值106s-1;快搅时间5min;pH=7.2表5表明,慢速搅拌存在最佳的G值,并且当投药量较小(如:投量3.0mg/L)时,最佳G值偏大 (15.2~20.8s-1);当投药量较大(如:14mg/L),最佳G值偏小(4.8~10.4s-1)。
合适的慢速搅拌强度既能使脱稳胶粒之间发生碰撞,又不致使絮凝体产生破碎,故存在一个最佳的慢速搅拌G值。
投药量比较小时,最佳G值偏大,可能是由于混凝剂投量小时,胶粒脱稳不充分,只有提高G值才能保证絮凝充分。
2.2.2最佳慢速搅拌时间慢速搅拌G值为15.2s-1时,慢速搅拌时间对混凝效果的影响情况如表6所示。
由表6的结果可见,当慢速搅拌时间大于15min以后,慢速搅拌时间对混凝效果几乎没有影响;当慢速搅拌时间小于10min时,混凝效果有所变差,这可能是由于搅拌时间小于10min时,脱稳胶粒之间搅拌不充分,碰撞机率小的缘故。
表6 最优慢速搅拌时间慢速搅拌时间 (s) 最大絮体粒径Rm5 1.8010 1.9015 2.620 2.430 2.350 2.5原水浊度42mg/L;慢速搅拌G值15.2s-1;水温13~14℃;pH=7.23 结论用絮凝检测仪对混凝过程进行在线检测,考察了最优的快速搅拌条件和最优的慢速搅拌条件,得到了以下结果:1.投药量对最优快速搅拌时间t影响较大,投药量越大,最优快速搅拌时间tm越小。
2.原水浊度对最优快速搅拌时间t有影响。
当投药量较小时影响较大,这时最优快速搅拌时间tm随浊度增加显著减小;当投药量较大时,浊度对最优快速搅拌时间的影响较小。
3.水温对最优快速搅拌时间tm有影响。
当投药量较小时,随水温增大,最优快速搅拌时间tm明显减小;当投药量较大时,水温对最优快速搅拌时间t影响较小;水温较低时,增加投药量,可使最优快速搅拌时间t减小。