最新化学反应热的计算盖斯定律
- 格式:pdf
- 大小:2.46 MB
- 文档页数:16


利用盖斯定律计算反应热的方法盖斯定律(Gibbs' Law)是热力学中非常重要的定律之一,它可以用来计算化学反应的热力学热变化。
该定律可以表示为以下方程式:ΔG=ΔH-TΔS其中,ΔG表示反应的自由能变化,ΔH表示反应的焓变化,ΔS表示反应的熵变化,T表示温度。
1.确定反应物和生成物:首先确定化学反应中的反应物和生成物。
这些物质在反应方程式中是明确的。
例如,对于A+B→C+D的反应,A和B 是反应物,C和D是生成物。
2.确定反应的热化学方程式:根据反应物和生成物,建立反应的热化学方程式。
这些方程式描述了反应物与生成物之间的化学反应关系,同时还包括反应的系数和状态标识。
3.确定反应的焓变化:利用已知的标准生成焓(ΔH°)值,计算反应的焓变化。
标准生成焓是指在标准状态下,1摩尔物质形成的过程中放出或吸收的热量。
通过查阅化学手册或热化学数据库确定反应物和生成物的标准生成焓,然后根据反应方程中的系数计算反应的焓变化。
4.确定反应的熵变化:确定反应的熵变化也需要一些信息。
从反应物到生成物的熵变可以通过已知的标准摩尔熵(ΔS°)值计算得出。
标准摩尔熵是指在标准状态下,1摩尔物质的熵变。
5. 确定温度:在应用盖斯定律计算反应热时,还需要确定反应发生的温度。
温度的单位通常是Kelvin(K)。
6.应用盖斯定律计算反应热:根据以上确定的ΔH,ΔS和温度值,应用盖斯定律进行计算。
7.解释结果:根据计算所得的反应热ΔG值,可以判断反应是自发进行的还是不自发进行的。
当ΔG<0时,反应是自发进行的,反应具有较大的发生倾向性。
当ΔG>0时,反应是不自发进行的,需要提供能量才能发生。
需要注意的是,在进行计算时要确保所有物质的标准生成焓和标准摩尔熵都是在相同温度下进行计算的。
此外,这种计算方法适用于理想气体和溶液的状态,对于其他复杂的体系可能需要考虑更多因素。
总而言之,利用盖斯定律计算反应热的方法是根据盖斯定律的方程式和已知的物质的焓变化和熵变化,应用热力学原理进行计算,以确定反应的自发性和热力学热变化。
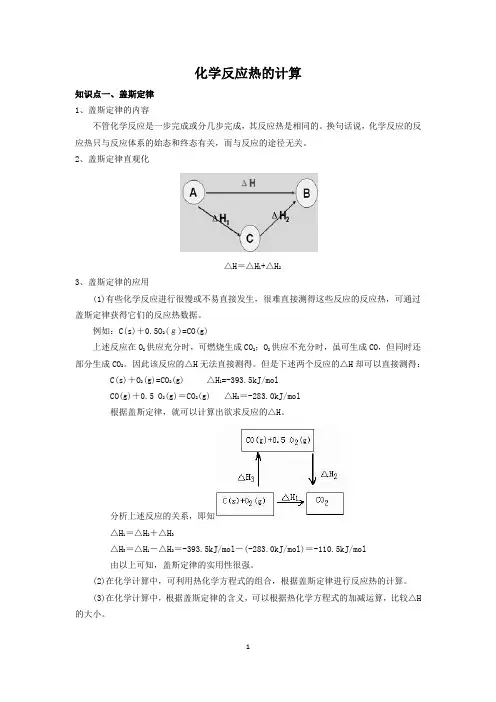
化学反应热的计算知识点一、盖斯定律1、盖斯定律的内容不管化学反应是一步完成或分几步完成,其反应热是相同的。
换句话说,化学反应的反应热只与反应体系的始态和终态有关,而与反应的途径无关。
2、盖斯定律直观化△H=△H1+△H23、盖斯定律的应用(1)有些化学反应进行很慢或不易直接发生,很难直接测得这些反应的反应热,可通过盖斯定律获得它们的反应热数据。
例如:C(s)+0.5O2(g)=CO(g)上述反应在O2供应充分时,可燃烧生成CO2;O2供应不充分时,虽可生成CO,但同时还部分生成CO2。
因此该反应的△H无法直接测得。
但是下述两个反应的△H却可以直接测得:C(s)+O2(g)=CO2(g) △H1=-393.5kJ/molCO(g)+0.5 O2(g)=CO2(g) △H2=-283.0kJ/mol根据盖斯定律,就可以计算出欲求反应的△H。
分析上述反应的关系,即知△H1=△H2+△H3△H3=△H1-△H2=-393.5kJ/mol-(-283.0kJ/mol)=-110.5kJ/mol由以上可知,盖斯定律的实用性很强。
(2)在化学计算中,可利用热化学方程式的组合,根据盖斯定律进行反应热的计算。
(3)在化学计算中,根据盖斯定律的含义,可以根据热化学方程式的加减运算,比较△H 的大小。
知识点二、反应热的计算根据热化学方程式、盖斯定律和燃烧热的数据,可以计算一些反应的反应热。
反应热、燃烧热的简单计算都是以它们的定义为基础的,只要掌握了它们的定义的内涵,注意单位的转化即可。
热化学方程式的简单计算的依据:(1)热化学方程式中化学计量数之比等于各物质的物质的量之比,还等于反应热之比。
(2)热化学方程式之间可以进行加减运算。
知识点三、有关反应热的计算依据归纳1、根据实验测得热量的数据求算反应热的定义表明:反应热是指化学反应过程中放出或吸收的热量,可以通过实验直接测定。
2、根据物质能量的变化求算根据能量守恒,反应热等于生成物具有的总能量与反应物具有的总能量的差值。






高三化学一轮复习——盖斯定律反应热的计算知识梳理1.盖斯定律内容:对于一个化学反应,无论是一步完成还是分几步完成,其反应热都是相同的。
即:化学反应的反应热只与反应体系的始态和终态有关,而与反应的途径无关。
(2)意义:间接计算某些反应的反应热。
(3)应用aA B2.反应热计算的四种方法(1)由H值计算ΔHΔH=∑H生成物-∑H反应物(2)由键能计算ΔHΔH=反应物的总键能-生成物的总键能如H2(g)+Cl2(g)===2HCl(g)ΔH由能量守恒知E H—H+E Cl—Cl=2E H—Cl+ΔH或ΔH=E H—H+E Cl—Cl-2E H—Cl(3)由反应中的热量变化Q计算ΔH如1 g H2充分燃烧生成H2O(l)时放出Q kJ的热量,H2的燃烧热为________kJ·mol -1。
H2(g)+12O2(g)===H2O(l)ΔH1 mol |ΔH|12mol Q故|ΔH|=2Q kJ·mol-1ΔH=-2Q kJ·mol-1,故H2的燃烧热为2Q。
(4)由分式结合盖斯定律计算ΔH(见应用)[考在课外]教材延伸判断正误(1)一个反应一步完成或几步完成,两者相比,经过的步骤越多,放出的热量越少(×)(2)H—H、O===O和O—H键的键能分别为436 kJ·mol-1、496 kJ·mol-1和462kJ·mol-1,则反应H2(g)+12O2(g)===H2O(g)的ΔH=-916 kJ·mol-1(×)(3)已知:O3+Cl===ClO+O2ΔH1ClO+O===Cl+O2ΔH2则反应O3+O===2O2ΔH=ΔH1+ΔH2(√)拓展应用(1)标准摩尔生成焓是指在25 ℃和101 kPa时,最稳定的单质生成1 mol化合物的焓变。
已知25 ℃和101 kPa时下列反应:①2C2H6(g)+7O2(g)===4CO2(g)+6H2O(l)ΔH=-3 116 kJ·mol-1②C(石墨,s)+O2(g)===CO2(g)ΔH=-393.5 kJ·mol-1③2H2(g)+O2(g)===2H2O(l)ΔH=-571.6 kJ·mol-1写出乙烷标准摩尔生成焓的热化学方程式:____________________________________________________________________________________________。