【重点推荐】人教版高中化学选修四第一章
- 格式:docx
- 大小:174.51 KB
- 文档页数:8

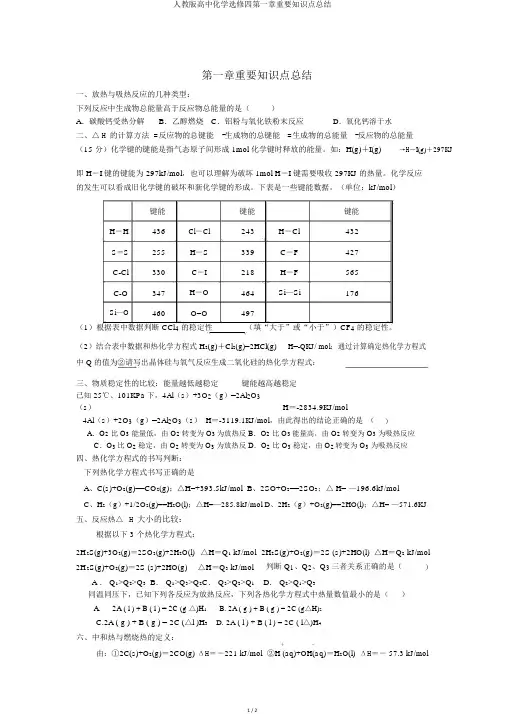
第一章重要知识点总结一、放热与吸热反应的几种类型:下列反应中生成物总能量高于反应物总能量的是()A.碳酸钙受热分解B.乙醇燃烧C.铝粉与氧化铁粉末反应D.氧化钙溶于水二、△ H 的计算方法 =反应物的总键能-生成物的总键能=生成物的总能量-反应物的总能量(15 分)化学键的键能是指气态原子间形成 1mol 化学键时释放的能量。
如:H(g)+I(g)→H-I(g)+297KJ即 H-I 键的键能为 297kJ/mol,也可以理解为破坏 1mol H-I 键需要吸收 297KJ的热量。
化学反应的发生可以看成旧化学键的破坏和新化学键的形成。
下表是一些键能数据。
(单位:kJ/mol)键能键能键能H-H 436 Cl-Cl 243 H-Cl 432S=S 255 H-S 339 C-F 427C-Cl 330 C-I 218 H-F 565C-O 347 H-O 464 Si—Si 176Si—O 460 O=O 497(1)根据表中数据判断 CCl4的稳定性(填“大于”或“小于”)CF4的稳定性。
(2)结合表中数据和热化学方程式 H2(g)+Cl2(g)=2HCl(g) H=-QKJ/ mol;通过计算确定热化学方程式中 Q 的值为②请写出晶体硅与氧气反应生成二氧化硅的热化学方程式:三、物质稳定性的比较:能量越低越稳定键能越高越稳定已知 25℃、101KPa下,4Al(s)+3O2(g)=2Al2O3(s)H=-2834.9KJ/mol4Al(s)+2O3(g)=2Al2O3(s) H=-3119.1KJ/mol,由此得出的结论正确的是()A.O2比 O3能量低,由 O2转变为 O3为放热反 B.O2比 O3能量高,由 O2转变为 O3为吸热反应C.O3比 O2稳定,由 O2转变为 O3为放热反 D.O2比 O3稳定,由 O2转变为 O3为吸热反应四、热化学方程式的书写判断:下列热化学方程式书写正确的是A、C(s)+O2(g)==CO2(g);△H=+393.5kJ/molB、2SO+O2==2SO3;△ H= —196.6kJ/molC、H2(g)+1/2O2(g)==H2O(l);△H=—285.8kJ/molD、2H2(g)+O2(g)==2HO(l);△H= —571.6KJ五、反应热△H 大小的比较:根据以下 3 个热化学方程式:2H 2S(g)+3O2(g)=2SO2(g)+2H2O(l) △H=Q1 kJ/mol 2H2S(g)+O2(g)=2S (s)+2HO(l) △H=Q2 kJ/mol2H 2S(g)+O2(g)=2S (s)+2HO(g) △H=Q3 kJ/mol 判断 Q1、Q2、Q3三者关系正确的是()A . Q1>Q2>Q3 B. Q1>Q3>Q2C. Q3>Q2>Q1 D. Q2>Q1>Q3同温同压下,已知下列各反应为放热反应,下列各热化学方程式中热量数值最小的是()A.2A ( l ) + B ( l ) = 2C (g △)H1 C.2A ( g ) + B ( g ) = 2C (△l )H3B. 2A ( g ) + B ( g ) = 2C (g△H)2 D. 2A ( l ) + B ( l ) = 2C ( l△)H4六、中和热与燃烧热的定义:由:①2C(s)+O2(g)=2CO(g) ΔH=-221 kJ/mol+-②H (aq)+OH(aq)=H2O(l) ΔH=- 57.3 kJ/mol可知:()A.①的反应热为 221 kJ/mol B.稀硫酸与 Ba(OH)2稀溶液反应的中和热为 57.3 kJ/molC.碳的燃烧热大于 110.5 kJ/mol D.稀醋酸与稀 NaOH溶液反应生成 1 mol 水,放出 57.3 kJ热量七、 n mol 可燃物放出的热量 =n 乘以它的燃烧热已知 H2(g)、C2H4(g)和 C2H5OH(1)的燃烧热分别是 -285.8 kJ·mol-1、-1411.0 kJ·mol-1和-1366.8 kJ mol-1,则由等质量的各物质放出的热量比()A .4.8:1.5:1B. 1:3.2:1.5 C. 3.2:5:1D.1.5:1:2八、能源探究问题:未来新能源的特点是资源丰富,在使用时对环境无污染或污染很小,且可以再生。


人教版化学选修四第一章知识点人教版化学选修四第一章知识点化学是自然科学的一支,研究物质的组成、结构、性质、变化以及与能量的关系。
而选修四是一门高中课程,涉及到化学领域的深入探究。
本文将会就人教版化学选修四第一章知识点作一个详细的梳理,以期让同学们能够更好的掌握和应用这些知识,更好的掌握这一门课程。
一、电子结构电子是构成原子最基本的粒子,也是化学反应中决定反应物性质、反应规律和反应结果的主要粒子之一。
电子的数量和电子的排布方式决定了元素的化学性质以及周期性定律。
原子的电子组态是指原子的每个电子所占据的能级及其角量子数的数字值。
原子的电子组态可以用法则或图形来表示。
对于许多元素来说,外层电子尤其关键。
1. 电子排布(a) 能级:原子中存在若干不同能量水平,称为电子能级。
第一个能级的电子数量为2,从第二能级开始分别是8,18,32等。
原子的电子能级是以原子核为中心的一系列球形壳层。
电子在不同能级的能量是不同的,内层能级的电子能量比外层能级的电子能量低。
(b) 湮灭原理:对于一定量的电子,要想达到稳定最低能量,即电子排布最稳定,要遵循以下规则:1、泡利不相容原理:在同一个原子内,任何两个电子所处的状态无论是四量子数还是角量子数,都不相同。
2、Aufbau起建原理:原子电子的排布顺序是按照原子能量级逐渐升高,一个原子的多层电子能够同时存在,而内层电子的能量低于外层电子。
3、范德瓦尔斥力原理:两个原子之间的相互作用能与电子的离子间距相关。
(c) 电子互斥原理:不允许在某一轨道上的电子数超过二。
(d) 同壳层电子间的屏蔽效应同壳层电子的屏蔽作用,也就是来自内层电子的电子云对来自外层电子的电子云的屏蔽作用,会导致外层电子的电性质随着原子核序数的增加而减弱。
2. 周期表和元素周期性现代周期表以元素的原子序数来排列元素,可以清晰地显示元素的电子排布和周期性变化。
在元素周期性的基础上,人们进一步推导出了周期表的各种性质。


人教版高中化学选修四知识点总结篇一:新课标高中化学选修4知识点总结(很全)化学选修4化学反映与原理章节知识点大全第一章化学反映与能量一、焓变反映热1.反映热:必然条件下,必然物质的量的反映物之间完全反映所放出或吸收的热量2.焓变(ΔH)的意义:在恒压条件下进行的化学反映的热效应(1).符号:△H(2).单位:kJ/mol3.产生缘故:化学键断裂——吸热化学键形成——放热放出热量的化学反映。
(放热>吸热) △H 为“-”或△H 吸收热量的化学反映。
(吸热>放热)△H 为“+”或△H >0☆常见的放热反映:①所有的燃烧反映②酸碱中和反映③大多数的化合反映④金属与酸的反映⑤生石灰和水反映⑥浓硫酸稀释、氢氧化钠固体溶解等☆常见的吸热反映:①晶体Ba(OH)2·8H2O与NH4Cl ②大多数的分解反映③以H二、CO、C为还原剂的氧化还原反映④铵盐溶解等二、热化学方程式书写化学方程式注意要点:①热化学方程式必需标出能量转变。
②热化学方程式中必需标明反映物和生成物的聚集状态(g,l,s别离表示固态,液态,气态,水溶液中溶质用aq表示)③热化学反映方程式要指明反映时的温度和压强。
④热化学方程式中的化学计量数能够是整数,也能够是分数⑤各物质系数加倍,△H加倍;反映逆向进行,△H改变符号,数值不变三、燃烧热1.概念:25 ℃,101 kPa时,1 mol纯物质完全燃烧生成稳固的化合物时所放出的热量。
燃烧热的单位用kJ/mol表示。
※注意以下几点:①研究条件:101 kPa②反映程度:完全燃烧,产物是稳固的氧化物。
③燃烧物的物质的量:1 mol④研究内容:放出的热量。
(ΔH 四、中和热1.概念:在稀溶液中,酸跟碱发生中和反映而生成1mol H2O,这时的反映热叫中和热。
2.强酸与强碱的中和反映其实质是H+和OH-反映,其热化学方程式为:H+(aq) +OH-(aq) =H2O(l) ΔH=-/mol3.弱酸或弱碱电离要吸收热量,因此它们参加中和反映时的中和热小于/mol。




高中化学学习材料第一章重要知识点总结一、放热与吸热反应的几种类型:下列反应中生成物总能量高于反应物总能量的是()A.碳酸钙受热分解 B.乙醇燃烧 C.铝粉与氧化铁粉末反应 D.氧化钙溶于水二、△H的计算方法=反应物的总键能-生成物的总键能=生成物的总能量-反应物的总能量(15分)化学键的键能是指气态原子间形成1mol化学键时释放的能量。
如:H(g)+I(g)→H-I(g)+297KJ 即H-I键的键能为297kJ/mol,也可以理解为破坏1mol H-I键需要吸收297KJ的热量。
化学反应的发生可以看成旧化学键的破坏和新化学键的形成。
下表是一些键能数据。
(单位:kJ/mol)(14的稳定性(填“大于”或“小于”4(2)结合表中数据和热化学方程式H2(g)+Cl2(g)=2HCl(g) ΔH=-QKJ/ mol;通过计算确定热化学方程式中Q的值为②请写出晶体硅与氧气反应生成二氧化硅的热化学方程式:三、物质稳定性的比较:能量越低越稳定键能越高越稳定已知25℃、101KPa下,4Al(s)+3O2(g)=2Al2O3(s)ΔH=-2834.9KJ/mol4Al(s)+2O3(g)=2Al2O3(s)ΔH=-3119.1KJ/mol,由此得出的结论正确的是()A.O2比O3能量低,由O2转变为O3为放热反 B.O2比O3能量高,由O2转变为O3为吸热反应C.O3比O2稳定,由O2转变为O3为放热反D.O2比O3稳定,由O2转变为O3为吸热反应四、热化学方程式的书写判断:下列热化学方程式书写正确的是A、C(s)+O2(g)==CO2(g);△H=+393.5kJ/molB、2SO2+O2==2SO3;△H= —196.6kJ/molC、H2(g)+1/2O2(g)==H2O(l);△H=—285.8kJ/molD、2H2(g)+O2(g)==2H2O(l);△H= —571.6KJ五、反应热△H大小的比较:根据以下3个热化学方程式:2H 2S(g)+3O 2(g)=2SO 2(g)+2H 2O(l) △H =Q 1 kJ/mol 2H 2S(g)+O 2(g)=2S (s)+2H 2O(l) △H =Q 2 kJ/mol 2H 2S(g)+O 2(g)=2S (s)+2H 2O(g) △H =Q 3 kJ/mol 判断Q 1、Q 2、Q 3三者关系正确的是( )A . Q 1>Q 2>Q 3B . Q 1>Q 3>Q 2C . Q 3>Q 2>Q 1D . Q 2>Q 1>Q 3同温同压下,已知下列各反应为放热反应,下列各热化学方程式中热量数值最小的是( )A. 2A ( l ) + B ( l ) = 2C (g ) △H 1B. 2A ( g ) + B ( g ) = 2C (g ) △H 2C.2A ( g ) + B ( g ) = 2C ( l ) △H 3D. 2A ( l ) + B ( l ) = 2C ( l ) △H 4六、中和热与燃烧热的定义:由:①2C(s)+O 2(g)=2CO(g) ΔH =-221 kJ/mol ②H +(aq)+OH -(aq)=H 2O(l) ΔH =-57.3kJ/mol 可知:( )A .①的反应热为221 kJ/molB .稀硫酸与Ba(OH)2稀溶液反应的中和热为57.3 kJ/molC .碳的燃烧热大于110.5 kJ/molD .稀醋酸与稀NaOH 溶液反应生成1 mol 水,放出57.3 kJ 热量七、n mol 可燃物放出的热量=n 乘以 它的燃烧热已知H 2(g)、C 2H 4(g)和C 2H 5OH(1)的燃烧热分别是-285.8 kJ ·mol -1、-1411.0 kJ ·mol -1和-1366.8 kJ mol -1,则由等质量的各物质放出的热量比( )A .4.8:1.5:1B .1:3.2:1.5C . 3.2:5:1D .1.5:1:2八、能源探究问题:未来新能源的特点是资源丰富,在使用时对环境无污染或污染很小,且可以再生。
第二节燃烧热能源大地二中张清泉一、燃烧热1、概念:25℃,101KPa时,1mol纯物质完全燃烧生成稳定的化合物时放出的热量,单位用kJ/mol表示。
2、注意要点:○1反应条件:25℃,101KPa;○2反应程度:完全燃烧;○3反应物的量:燃烧物的物质的量:1mol。
○4反应产物:元素完全燃烧时对应的氧化物3、燃烧热热化学方程式的书写原则:燃烧热是以1mol物质完全燃烧所放出的热量来定义的,因此在书写它的热化学方程式时,应以1mol燃烧物质为标准来配平其余物质的化学计量数3、燃烧热的计算:=n(可燃物)(为可燃物燃烧反应所放出的热量,n为可燃物的物质的量,为可燃物的燃烧热)【习题一】(2017秋•武昌区期中)下列关于燃烧热的说法正确的是()A.燃烧反应放出的热量就是该反应的燃烧热B.1 mol可燃物质发生氧化反应所放出的热量就是燃烧热C.1 mol可燃物质完全燃烧生成稳定的化合物时所放出的热量就是燃烧热D.在25℃、101 kPa时,1 mol纯物质完全燃烧生成稳定的氧化物时所放出的热量是燃烧热【考点】燃烧热.【专题】燃烧热的计算.【分析】燃烧热的条件是在25℃、1.01×105Pa下,必须是1mol物质完全燃烧并且生成的物质为最稳当的氧化物,燃烧热的热化学方式的计量系数必须是1,燃烧是发光发热的剧烈的氧化还原反应,不一定有氧气参加,据此解答.【解答】解:A.燃烧热必须是可燃物质完全燃烧生成稳定的氧化物放出的热量,故A错误;B.1 mol可燃物质发生氧化反应生成最稳当的氧化物所放出的热量就是燃烧热,故B错误;C.25℃、1.01×105Pa下,必须是1mol物质完全燃烧并且生成的物质为最稳当的氧化物时所放出的热量,故C错误;D.25℃、101 kPa时,1 mol纯物质完全燃烧生成稳定的氧化物时所放出的热量是燃烧热,故D正确;故选:D。
【习题二】(2016秋•朝阳区校级期末)已知H2的燃烧热是akJ/mol,由H2、CO按3:1比例组成的混合物2mo,完全燃烧并恢复常温吋,放出的热量为bkJ,则CO的燃烧热为(kJ/mol)为()A.2b-3a B.3a-2b C. D.【考点】燃烧热.【专题】化学反应中的能量变化.【分析】设CO的燃烧热为xkJ•mol-1,又H2的燃烧热是akJ/mol,所以由H2、CO按3:1比例组成的混合物2mol,完全燃烧并恢复到常温吋,放出的热量为bkJ,可得,据此计算.【解答】解:设CO的燃烧热为xkJ•mol-1,又H2的燃烧热是akJ/mol,所以由H2、CO按3:1比例组成的混合2mol,完全烧并恢复到常温吋,放出的热量为bkJ,可得,则解得x=2b-3a,故选:A。
目录第一章化学反应与能量_________________________________________________________________________________ 1 第二章化学反应速率和化学平衡_________________________________________________________________________ 6 第三章水溶液中的离子平衡___________________________________________________________________________ 21 第四章电化学基础____________________________________________________________________________________ 41章节知识点梳理第一章化学反应与能量化学反应中的能量变化(1)化学反应的实质:反应物化学键断裂和生成物化学键形成。
其中旧键断裂要吸收能量,新键形成会释放能量。
(2)化学反应的特征:既有物质变化,又有能量变化。
(3)化学反应中的能量转化形式:热能、光能和电能等,通常主要表现为热能的变化。
一、焓变反应热1.反应热:化学反应过程中所放出或吸收的热量,任何化学反应都有反应热,因为任何化学反应都会存在热量变化,即要么吸热要么放热。
反应热可以分为(燃烧热、中和热、溶解热)2.焓变(ΔH)的意义:在恒压条件下进行的化学反应的热效应.符号:△H.单位:kJ/mol ,即:恒压下:焓变=反应热,都可用ΔH表示,单位都是kJ/mol。
3.产生原因:化学键断裂——吸热化学键形成——放热放出热量的化学反应。
(放热>吸热) △H 为“-”或△H <0,表示的时候“-”,“kJ/mol”不能省略吸收热量的化学反应。
(吸热>放热)△H 为“+”或△H >0,表示的时候“+”,“kJ/mol”不能省略放热反应和吸热反应判断方法①能量图像左图反应物总能量大于产物总能量,为放热反应;右图为反应物总能量低于产物总能量,为吸热反应注意:a.图中可以得知物质的能量越高越不稳定;b.一定是所有物质的能量之和,而不是某一个物质的能量高于产物或者低于产物的能量②通过键能的计算△H也可以利用计算△H来判断是吸热还是放热。
人教版化学选修四第一章知识点(实用版)编制人:__________________审核人:__________________审批人:__________________编制单位:__________________编制时间:____年____月____日序言下载提示:该文档是本店铺精心编制而成的,希望大家下载后,能够帮助大家解决实际问题。
文档下载后可定制修改,请根据实际需要进行调整和使用,谢谢!并且,本店铺为大家提供各种类型的实用范文,如学习资料、英语资料、学生作文、教学资源、求职资料、创业资料、工作范文、条据文书、合同协议、其他范文等等,想了解不同范文格式和写法,敬请关注!Download tips: This document is carefully compiled by this editor.I hope that after you download it, it can help you solve practical problems. The document can be customized and modified after downloading, please adjust and use it according to actual needs, thank you!In addition, this shop provides various types of practical sample essays, such as learning materials, English materials, student essays, teaching resources, job search materials, entrepreneurial materials, work examples, documents, contracts, agreements, other essays, etc. Please pay attention to the different formats and writing methods of the model essay!人教版化学选修四第一章知识点具体地说,学习化学可以了解化学变化的原理,搞清发生在我们身边的许多“为什么”,比如溶洞中的钟乳石、石笋、石柱是怎样形成的?金属为什么容易生锈?下面是本店铺为大家整理的有关人教版化学选修四第一章知识点试题,希望对你们有帮助!化学选修四第一章知识点试题1.下列说法正确的是A.HD、CuSO4•5H2O都是化合物B.由同种元素组成的物质一定是纯净物C.NaHSO4在溶液中能电离出H+,所以NaHSO4是酸D.浊液、胶体、溶液三种分散系的本质区别是分散质微粒直径的大小不同2.下列过程属于物理变化的是A.平行光照射胶体产生丁达尔效应B.紫外线照射下,液态蛋白质凝固C.铁在潮湿的空气中生锈D.铝遇到冷的浓发生钝化3.下列化学符号正确的是A.二氧化硅的结构式O=Si=OB.聚乙烯的结构简式C.过氧化钠的电子式D.羟基的电子式4.NA代表阿伏加德罗常数的值。
高中化学学习材料(精心收集**整理制作)人教版选修4第一章《化学反应与能量》测试题广州市高二化学中心组提供2008.9 本试卷分第一部分(选择题)和第二部分(非选择题),满分100分,考试时间40分钟。
第一部分选择题(共50分)一、选择题(每小题5分,每小题有1.~.2.个.选项符合题意,错选0分,漏选2分,共50分。
)1.未来新能源的特点是资源丰富,在使用时对环境无污染或污染很小,且可以再生。
下列属于未来新能源标准的是①天然气②煤③核能④石油⑤太阳能⑥生物质能⑦风能⑧氢能A.①②③④B.⑤⑥⑦⑧C.③⑤⑥⑦⑧D.③④⑤⑥⑦⑧2.下列说法中正确的是A.在化学反应过程中,发生物质变化的同时不一定发生能量变化B.生成物全部化学键形成时所释放的能量大于破坏反应物全部化学键所吸收的能量时,反应为吸热反应C.反应产物的总焓大于反应物的总焓时,反应吸热,ΔH>0D.ΔH的大小与热化学方程式的计量系数无关3.下列过程中△H小于零的是A. 氯酸钾分解制氧气B. 氯化铵分解得氨气C.碳酸钙分解得二氧化碳D. 实验室制备氢气4.已知1 g氢气完全燃烧生成水蒸气时放出热量121 kJ。
且氧气中1 mol O=O键完全断裂时吸收热量496 kJ,水蒸气中1 mol H-O键形成时放出热量463 kJ,则氢气中1mol H-H键断裂时吸收热量为A.920 kJ B.557 kJ C.436 kJ D.188 kJ5.同温同压下,已知下列各反应为放热反应,下列各热化学方程式中反应热最小的是A.2A ( l ) + B ( l ) = 2C (g ) △H1 B.2A ( g ) + B ( g ) = 2C (g ) △H2C.2A ( g ) + B ( g ) = 2C ( l ) △H3 D.2A ( l ) + B ( l ) = 2C ( l ) △H46.强酸与强碱的稀溶液发生中和反应的热效应为:H+(aq)+OH-(aq)=H2O(l)△H =-57.3KJ·mol-1。
分别向1L 0.5mol·L-1的Ba(OH)2的溶液中加入①浓硫酸;②稀硫酸;③稀硝酸,恰好完全反应的热效应分别为△H1、△H2、△H3,下列关系正确的是A.△H1>△H2>△H3B.△H1<△H2<△H3C.△H1>△H2=△H3D.△H1=△H2<△H37.将铁粉和硫粉混合后加热,待反应一发生即停止加热,反应仍可持续进行,直至反应完全生成新物质硫化亚铁。
这现象说明了A. 该反应是吸热反应B. 该反应是放热反应C. 铁粉和硫粉在常温下难以发生反应D. 硫化亚铁的总能量高于铁粉和硫粉的总能量8.以N A代表阿伏加德罗常数,则关于热化学方程式C2H2 ( g ) +5/2O2 ( g ) →2CO2 ( g )+H2O ( l )△H = —1300kJ / mol 的说法中,正确的是A. 当10 N A个电子转移时,该反应放出1300kJ的能量B. 当1 N A个水分子生成且为液体时,吸收1300kJ的能量C. 当2 N A个碳氧共用电子对生成时,放出1300kJ的能量D. 当8 N A个碳氧共用电子对生成时,放出1300kJ的能量9.下列说法或表示法正确的是A.等量的硫蒸气和硫固体分别完全燃烧,后者放出热量多B.由C(石墨)→C(金刚石) ΔH = +119 kJ·mol—1可知,石墨比金刚石稳定C.在稀溶液中:H++OH-===H2O ΔH = -57.3 kJ·mol—1,若将含1mol CH3COOH的醋酸溶液与含1 mol NaOH的溶液混合,放出的热量小于57.3 kJD.在101 kPa时,2 g H2完全燃烧生成液态水,放出285.8 kJ热量,氢气燃烧的热化学方程式表示为2H2(g)+ O2(g)===2H2O(l)ΔH = +285.8 kJ·mol—110.一些盐的结晶水合物,在温度不太高时就有熔化现象,即熔溶于自身的洁净水中,又同时吸收热量。
他们在塑料袋中经日晒就熔化,又在日落后缓慢凝结而释放热量。
故可用于调节室内温度,或用作夏日防暑的枕垫或坐垫,这些物质可称之为热材料。
现有几种盐的结晶水合物有关数据如下:根据上述数据和实用性考虑,实际运用时常采用的物质应该是A.① B.②C.③ D.④高二班姓名学号成绩第二部分非选择题(共50分)二、非选择题(共50分)11。
(12分)实验室利用右图装置进行中和热的测定,请回答下列问题:(1)在操作正确的前提下,提高中和热测定准确性的关键是(2)做1次完整的中和热测定实验,温度计需使用次,某同学为了省去清洗温度计的麻烦,建议实验时使用两支温度计分别测量酸和碱的温度,你是否同意该同学的观点,为什么?(3)请为本实验设计数据记录表格:12.(15分)已知化学反应N2+3H2=2NH3的能量变化如图所示,(1)1mol N 和3mol H 生成1mol NH3① Na2S2O3·5H2O ②CaCl2·6H2O ③Na2SO4·10H2O ④ Na2HPO4·10H2O 熔点/℃40~50 29.92 32.38 35.1 熔化热/kJ· mol-149.7 37.3 77 100.1(g)是--------------------------------能量的过程(填“吸收”或“释放”)。
(2)12N2(g)+32H2(g)=NH3(g);△H= ;(3)N2(g)和H2生成NH3(1)的热化学方程式为------------------------------------------------------13.(13分)某同学发现在灼热的煤炭上洒少量水,煤炉中会产生淡蓝色火焰,煤炭燃烧更旺,因此该同学得出结论“煤炭燃烧时加少量水,可使煤炭燃烧放出更多的热量。
”(已知煤炭的燃烧热为-393.15 kJ/mol,氢气的燃烧热为-242 kJ/mol,一氧化碳的燃烧热为-283 kJ/mol)(1)写出该同学看到燃烧现象所涉及到的所有热化学反应方程式;;你认为该同学的结论是否正确,请简要说明理由。
14.(10分)已知2H2(g)+ O2(g)===2H2O(l)ΔH = —571.6 kJ·mol—1CO(g) + 1/2O2(g) == CO2(g) △H = -283 kJ·mol—1某H2和CO的混合气体完全燃烧时放出113.74 kJ热量,同时生成3.6 g液态水,求原混合气体中H2和CO的物质的量。
人教版选修4第一章《化学反应与能量》测试题参考答案一、选择题(每小题5分,每小题有1.~.2.个.选项符合题意,错选0分,漏选2分,共50分。
)题号 1 2 3 4 5 6 7 8 9 10答案 B C D C C B BC AD BC C二、非选择题(共50分)11.(1)保温(2分)(2)3次(2分)不同意,因为不同的温度计误差不同。
(3分)(3)(5分)温度实验次数起始温度t1/℃终止温度t2/℃温度差(t2—t1)/℃HCl NaOH 平均值12312(1)释放(2)(a-b) kJ·mol-1(3)N2(g)+3H2(g)=2NH3(1); △H=2(a-b-c)kJ·mol-113.(1)C(s) +O2 (g) =CO2(g) △H = -393.15 kJ/mol (2分)H2 (g) +1/2 O2 (g) =H2O (l) △H = -242 kJ/mol(2分)CO(g) +1/2 O2 (g) =CO2(g) △H = -283 kJ/mol(2分)C(g) +H2O (l) =CO(g) +H2 (g) △H = +131.85 kJ/mol(4分)(2)不正确。
因为根据盖斯定律,反应过程中的热效应与途径无关,只与反应物和生成物的能量差有关。
(3分)14.n(H2) ==0.2mol n(co)==0.20mol备选题1.下列反应中反应物总能量高于生成物总能量的是A.二氧化碳与碳生成一氧化碳B.碳与水蒸气生成一氧化碳和氢气C.碳酸钙受热分解D.盐酸与氢氧化钠反应2.氢气是人类最理想的能源。
已知在25℃、101kPa下,1 g氢气完全燃烧生成液态水时放出热量142.9kJ,则下列热化学方程式书写正确的是A.2H2 + O2==2H2O;△H= –142.9 kJ/molB.2H2(g) + O2(g)==2H2O(l);△H= – 142.9 kJ/molC.2H2(g) + O2(g) 2H2O(l);△H=– 571.6 kJ/molD.2H2(g) + O2(g) 2H2O(l);△H = + 571.6 kJ/mol3.氢气(H2)、一氧化碳(CO)、辛烷(C8H18)、甲烷(CH4)的热化学方程式分别为:H2(g) + 1/2O2(g) == H2O (l) △H = -285.8 KJ/molCO(g) + 1/2O2(g) == CO2(g) △H = -283 KJ/molC8H18 (l) + 25/2O2(g) == 8CO2(g) + 9H2O (l) △H = -5518 KJ/molCH4 (g) + 2O2(g) == CO2(g) + 2H2O (l) △H = -890.3 KJ/mol相同质量的H2、CO、C8H18、CH4完全燃烧时,放出热量最少的是A.H2(g) B.CO(g) C.C8H18 (l) D.CH4 (g)4.下列关于热化学反应的描述中正确的是A.HCl和NaOH反应的中和热△H=-57.3kJ/mol,则H2SO4和Ca(OH)2反应的中和热△H=2×(-57.3)kJ/molB.CO(g)的燃烧热是283.0kJ/mol,则2CO2(g)===2CO(g)+O2(g)反应的△H=+566.0kJ/mol C.需要加热才能发生的反应一定是吸热反应D.1mol甲烷燃烧生成气态水和二氧化碳所放出的热量是甲烷的燃烧热5.下列有关能量转换的说法正确的是A、煤燃烧是化学能转化为热能的过程B、化石燃料和植物燃料燃烧时放出的能量均来源于太阳能C、动物体内葡萄糖被氧化成CO2是热能转变成化学能的过程反应过程能量(kJ/mol )反应物分子 生成物 分子 活化 分子反应物的总能量(E 1) 生成物的 总能量(E 2)(Ⅰ)(Ⅱ) 活化分子的最低能量12D 、植物通过光合作用将CO 2转化为葡萄糖是太阳能转变成热能的过程 6.已知:(1)Zn (s )+1/2O 2(g )==ZnO(s),ΔH = -348.3kJ/mol(2)2Ag(s)+1/2 O 2(g )== Ag 2O(s),ΔH = -31.0kJ/mol 则Zn (s )+ Ag 2O(s) == ZnO(s) + 2Ag(s) 的ΔH 等于A .-317.3kJ/molB .-379.3kJ/molC .-332.8 kJ/molD .317.3 kJ/mol 7.甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是 ①CH 3OH(g)+H 2O(g) = CO 2(g)+3H 2(g) △H = + 49. 0 kJ ·mol -1②CH 3OH(g)+1/2O 2(g) = CO 2(g)+2H 2(g) △H =-192. 9 kJ ·mol -1下列说法正确的是A .CH 3OH 的燃烧热为192. 9 kJ ·mol -1B .反应①中的能量变化如右图所示C .CH 3OH 转变成H 2的过程一定要吸收能量D .根据②推知反应:CH 3OH(l) +1/2O 2(g) = CO 2(g) +2H 2(g) △H >-192. 9kJ ·mol -18.(16分)在化学反应中,只有极少数能量比平均能量高得多的反应物分子发生碰撞时才可能发生化学反应,这些分子被称为活化分子。