2012中考试题汇编(物质分离与除杂)精选
- 格式:doc
- 大小:219.00 KB
- 文档页数:5

2012年中考真题分类汇编——物质的分离与提纯一、选择题1(2012•湖北黄石,26题,1分)26.下列除杂方法正确的是()物质所含杂质除杂方法A O2CO2通过灼热的铜网B Cu(NO3)2溶液AgNO3加过量铜粉,过滤C KCl溶液BaCl2加适量Na2S04溶液,过滤D CO2HCl 通过盛有NaOH溶液的洗气瓶2(2012年江苏盐城,14题,2分)下表列出了除去物质中所含少量杂质的方法,其中错误的是()选项物质杂质除杂方法A CO2CO 点燃B Cu粉Fe粉磁铁吸引C CaO CaCO3高温D CaCl2溶液稀盐酸加入足量的CaCO3 ,过滤3(2012年湖南衡阳,17题,2分)下表中,除去物质中所含杂质的方法正确的是()物质所含杂质除杂方法A CuO Cu 滴加足量盐酸,然后过滤B CO2CO 将气体通过灼热的氧化铜C HCl 水蒸气将气体通过生石灰D NaCl溶液Na2CO3加适量的氢氧化钙溶液4(2012年四川广安,20题,2分)下列做法不正确的是A.用稀盐酸检验氢氧化钠是否变质B.点燃氢气前一定要先检验氢气的纯度C.除去氧化钙中的碳酸钙,加入足量的水,然后过滤D.家中天然气装置漏气时,应先关闭阀门,并打开门窗5(2012年江苏淮安,10题2分)下列实验操作中,不能达到实验目的的是实验目的实验操作A 鉴别涤纶和羊毛面料分别取样灼烧、闻气味B 提纯粗盐(含少量泥沙) 将粗盐加适量水溶解、过滤、蒸发结晶C 除去氯化钙溶液中少量盐酸加入过量的碳酸钙粉末,充分反应后过滤D 分离硫酸钠和硫酸铜的混合溶液加入过量氢氧化钠溶液后过滤,将滤渣溶于稀硫酸6(2012年四川德阳,15题,3分)列除去混合物中少量杂质的方法或加入试剂合理的是()选项物质所含杂质除去杂质的方法或加入的试剂A KClK2S04Ba(NO3)2B CuOCu粉空气中灼烧C CO2N2澄清石灰水D Ca(OH)2CaCO3盐酸7.(2012年江苏苏州,23题,2分)除去下列物质中的少量杂质(括号内为杂质)的方法错误的是A. O2(H2O)—用生石灰B. NaCl溶液(KNO3 )—降温结晶C. CaCO3粉末(N a2CO3 )—加水过滤D. KCI溶液(K2CO3)—加适量盐酸8(2012年甘肃兰州,20题,2分)下列除去杂质的方法中正确的是()选项物质杂质除杂质的方法A CaCl2溶液稀盐酸过量碳酸钙、过滤B KOH溶液KCl适量稀盐酸C NaCl溶液Na2CO3适量硝酸钙溶液、过滤D O2CO 通过灼热的氧化铜9.(2012年四川眉山,6题,2分)除去下列物质中的杂质,选用试剂或操作方法不正确是( )物质所含杂质除去杂质的试剂或方法A Na2C03固体NaHC03固体加热B Cu Fe 加过量稀盐酸后过滤、洗涤、干燥C 02H20 通人盛有过量浓H2S04的洗气瓶D C02HC1 通入盛有NaOH溶液的洗气瓶,然后干燥10(2012年湖北武汉,7题,3分)某化学小组的同学利用混有少量CO2的CO一氧化碳气体还原氧化铁,并验证反应后的气体产物。

专题十一物质的除杂、分离1. 除去下列物质中混入的少量杂质(括号中的物质为杂质)所涉及的实验方案或操作中,合理的是__________A. KNQ晶体(NaCl):将固体溶于水配制成热的饱和溶液,采用降温结晶的方法B. CQ气体(HCl):将气体通过盛有NaOH溶液的洗气瓶C. BaC b溶液(Ba(OH»加入适量的稀硫酸,过滤D. O2 (N2):将混合气体通过炽热的铜网2. 下列各组括号内除杂质的方法或试剂错误的是A. CO2中混有CO (点燃)B. Cu粉中混有CuO (稀硫酸)C. CO中混有CO2 (氢氧化钠溶液)D. Cu粉中混有Fe粉(用磁铁吸引)3. 除去下列物质中混有的少量杂质(括号内为杂质),所用方法正确的是A. CO2 (CO ——通入氧气点燃B. SO2 (HCl)——通过足量的氢氧化钠溶液C. KCl固体(KClQ)——加少量二氧化猛固体并加热D. NaCl溶液(NaHCO3)——滴加稀盐酸恰好完全反应4. 除去下列物质中混有的少量杂质,所选用的试剂及操作方法不正确的是5. 欲除去氯化钙溶液中的少量稀盐酸,在没有指示剂的条件下应选用的试剂是A. 碳酸钙粉末B. 生石灰粉末C.熟石灰粉末D. 硝酸银粉末6. 除去下列物质中混有的少量杂质(括号内为杂质),所用的方法正确的是A. CQ气体(CO气体)一一通入氧气点燃B. CaO固体(CaCQ固体)一一加水充分溶解,过滤C. KCl固体(MnO2固体)一一加水充分溶解,过滤,蒸发结晶D. NaCl溶液(CaCl溶液)一一滴加碳酸钾溶液至恰好完全反应,过滤7. 分离氯化铁、氯化钠、硫酸彻的固体混合物,得到三种纯净物,应选用的一组试剂是A. 水、硝酸银、稀硝酸B. 水、氢氧化钠、盐酸C. 水、氢氧化钠、稀硝酸D. 水、氢氧化钾、盐酸8. 要收集得到较纯净的物质,下列除去指定杂质(括号中为杂质)方法正确的是①CO (CQ)——通过装有烧碱溶液的洗气瓶;②CO2 (CO)——导出,在空气中点燃;③。
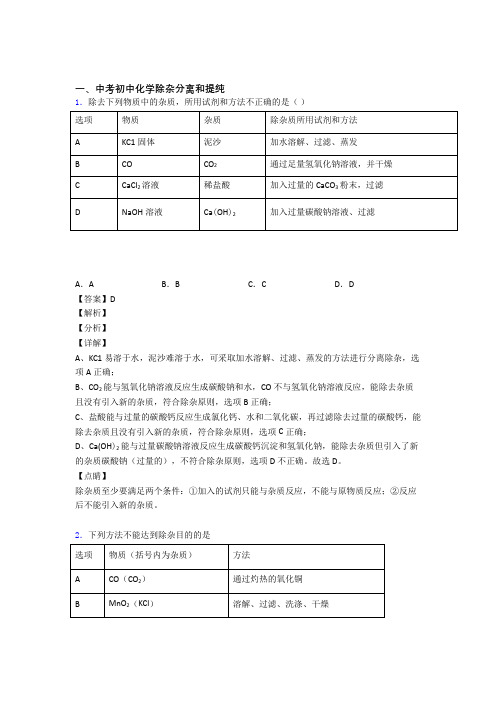
一、中考初中化学除杂分离和提纯1.除去下列物质中的杂质,所用试剂和方法不正确的是()A.A B.B C.C D.D【答案】D【解析】【分析】【详解】A、KC1易溶于水,泥沙难溶于水,可采取加水溶解、过滤、蒸发的方法进行分离除杂,选项A正确;B、CO2能与氢氧化钠溶液反应生成碳酸钠和水,CO不与氢氧化钠溶液反应,能除去杂质且没有引入新的杂质,符合除杂原则,选项B正确;C、盐酸能与过量的碳酸钙反应生成氯化钙、水和二氧化碳,再过滤除去过量的碳酸钙,能除去杂质且没有引入新的杂质,符合除杂原则,选项C正确;D、Ca(OH)2能与过量碳酸钠溶液反应生成碳酸钙沉淀和氢氧化钠,能除去杂质但引入了新的杂质碳酸钠(过量的),不符合除杂原则,选项D不正确。
故选D。
【点睛】除杂质至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质。
2.下列方法不能达到除杂目的的是A.A B.B C.C D.D【答案】A【解析】【分析】【详解】A、CO能与灼热的氧化铜反应生成铜和二氧化碳,反而会把原物质除去,不符合除杂原则,故选项所采取的方法错误。
B、氯化钾易溶于水,MnO2难溶于水,可采取加水溶解、过滤、洗涤、干燥的方法进行分离除杂,故选项所采取的方法正确。
C、CaCO3在高温下煅烧生成氧化钙和二氧化碳,能除去杂质且没有引入新的杂质,符合除杂原则,故选项所采取的方法正确。
D、足量的铁粉能与CuCl2溶液反应生成氯化亚铁溶液和铜,再过滤,能除去杂质且没有引入新的杂质,符合除杂原则,故选项所采取的方法正确。
故选:A。
【点睛】根据原物质和杂质的性质选择适当的除杂剂和分离方法,所谓除杂(提纯),是指除去杂质,同时被提纯物质不得改变.除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质。
3.除去下列物质中的少量杂质,所选用的试剂和操作方法都正确的是()A.A B.B C.C D.D【答案】D【解析】【分析】A、FeCl3溶液和CuCl2均能与铁粉反应,不但能把杂质除去,也会把原物质除去,不符合除杂原则,故选项所采取的方法错误。
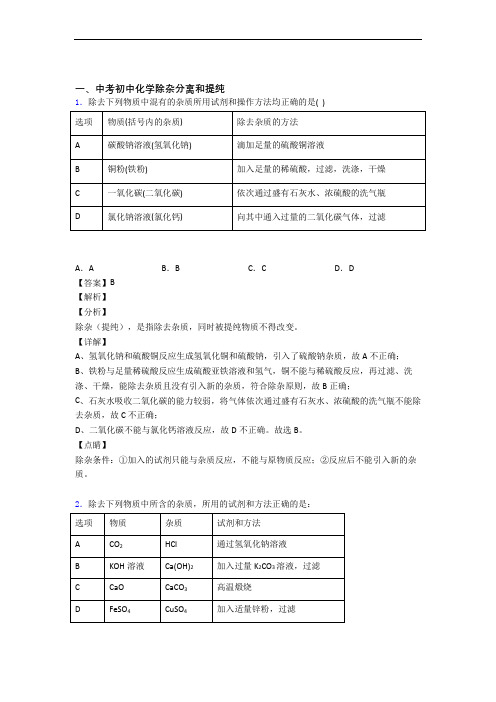
一、中考初中化学除杂分离和提纯1.除去下列物质中混有的杂质所用试剂和操作方法均正确的是( )A.A B.B C.C D.D【答案】B【解析】【分析】除杂(提纯),是指除去杂质,同时被提纯物质不得改变。
【详解】A、氢氧化钠和硫酸铜反应生成氢氧化铜和硫酸钠,引入了硫酸钠杂质,故A不正确;B、铁粉与足量稀硫酸反应生成硫酸亚铁溶液和氢气,铜不能与稀硫酸反应,再过滤、洗涤、干燥,能除去杂质且没有引入新的杂质,符合除杂原则,故B正确;C、石灰水吸收二氧化碳的能力较弱,将气体依次通过盛有石灰水、浓硫酸的洗气瓶不能除去杂质,故C不正确;D、二氧化碳不能与氯化钙溶液反应,故D不正确。
故选B。
【点睛】除杂条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质。
2.除去下列物质中所含的杂质,所用的试剂和方法正确的是:A.A B.B C.C D.D【答案】C【解析】【分析】【详解】A、CO2和HCl气体均能与NaOH溶液反应,不但能把杂质除去,也会把原物质除去,不符合除杂原则,故选项所采取的试剂错误。
B、Ca(OH)2能与过量K2CO3溶液反应生成碳酸钙沉淀和氢氧化钾,能除去杂质且入了新的杂质碳酸钾(过量的),不符合除杂原则,故选项所采取的方法错误。
C、CaCO3固体高温煅烧生成氧化钙和二氧化碳,能除去杂质且没有引入新的杂质,符合除杂原则,故选项所采取的方法正确。
D、FeSO4和CuSO4均能与适量的锌粉反应,不但能把杂质除去,也会把原物质除去,不符合除杂原则;故选项所采取的方法错误。
故选:C。
【点睛】根据原物质和杂质的性质选择适当的除杂剂和分离方法,所谓除杂(提纯),是指除去杂质,同时被提纯物质不得改变.除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质。
3.除去下列物质中含有的少量杂质,所用试剂或方法不正确的是()A.A B.B C.C D.D【答案】D【解析】【分析】除杂(提纯),是指除去杂质,同时被提纯物质不得改变。

一、中考初中化学除杂分离和提纯1.除去下列物质中混有的杂质所用试剂和操作方法均正确的是( )A.A B.B C.C D.D【答案】B【解析】【分析】除杂(提纯),是指除去杂质,同时被提纯物质不得改变。
【详解】A、氢氧化钠和硫酸铜反应生成氢氧化铜和硫酸钠,引入了硫酸钠杂质,故A不正确;B、铁粉与足量稀硫酸反应生成硫酸亚铁溶液和氢气,铜不能与稀硫酸反应,再过滤、洗涤、干燥,能除去杂质且没有引入新的杂质,符合除杂原则,故B正确;C、石灰水吸收二氧化碳的能力较弱,将气体依次通过盛有石灰水、浓硫酸的洗气瓶不能除去杂质,故C不正确;D、二氧化碳不能与氯化钙溶液反应,故D不正确。
故选B。
【点睛】除杂条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质。
2.下表列出了除去物质中所含少量杂质的方法,其中正确的是()A.A B.B C.C D.D【答案】D【解析】【分析】【详解】A、CaO能与水反应生成氢氧化钙,碳酸钙难溶于水,反而会把原物质除去,不符合除杂原则,故选项所采取的方法错误。
B、除去二氧化碳中的一氧化碳不能够点燃,这是因为当二氧化碳(不能燃烧、不能支持燃烧)大量存在时,少量的一氧化碳是不会燃烧的;故选项所采取的方法错误。
C、Na2CO3能与过量的氢氧化钙溶液反应生成碳酸钙沉淀和氢氧化钠,能除去杂质但引入了新的杂质氢氧化钙(过量的),不符合除杂原则,故选项所采取的方法错误。
D、氯化钠易溶于水,泥沙难溶于水,可采取加水溶解、过滤、蒸发的方法进行分离除杂,故选项所采取的方法正确。
故选:D。
【点睛】根据原物质和杂质的性质选择适当的除杂剂和分离方法,所谓除杂(提纯),是指除去杂质,同时被提纯物质不得改变.除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质。
3.下列实验方案不能达到实验目的的是()A.A B.B C.C D.D【答案】D【解析】【分析】【详解】A、Na2CO3+2HCl=2NaCl+H2O+CO2↑,选项A正确;B、NaCl溶于水溶液温度不变,NaOH固体溶于水溶液温度升高,选项B正确;C、CO2可以使澄清石灰水变浑浊,CO则不能,选项C正确;D、CaO和CaCO3都与稀盐酸反应,选项D不正确。

一、中考初中化学除杂分离和提纯1.要除去氯化钠溶液中含有的少量碳酸钠,可采用的方法是①通入适量的二氧化碳②加入适量的氯化钡溶液③加入适量的稀盐酸④加入适量的石灰水()A.①或③B.②或③C.②或④D.③或④【答案】B【解析】【分析】【详解】①二氧化碳不和碳酸钠溶液反应,不能除去杂质,此项错误;②氯化钡能和碳酸钠反应生成碳酸钡沉淀和氯化钠,反应时不会带入新的杂质,故此项正确;③盐酸能和碳酸钠反应,且生成氯化钠,不会带入新的杂质,此项正确;④氢氧化钙溶液能和碳酸钠反应,但反应时会生成氢氧化钠,带入新的杂质,此项错误,故选B。
2.下表中,除去物质所含少量杂质的方法和反应类型归类均正确的是A.A B.B C.C D.D【答案】A【解析】【分析】【详解】A、铜和氧气加热生成氧化铜,反应为化合反应,氧化铜和氧气加热不反应,可以除去铜粉,故A正确;B、一氧化碳和氧化铜反应生成铜和二氧化碳,反应不属于置换反应,故B不正确;C、盐酸和氢氧化钠反应生成氯化钠和水,反应类型为复分解反应,故C不正确;D、硫酸钾和硝酸钡反应生成硫酸钡和硝酸钾,引进新杂质硝酸钾,故D不正确。
故选A。
3.下列除去杂质所用的药品或方法,不正确的是()A.A B.B C.C D.D【答案】A【解析】【分析】【详解】A、Na2SO4能与过量的BaCl2溶液反应生成硫酸钡沉淀和氯化钠,能除去杂质但引入了新的杂质氯化钡,不符合除杂原则。
A错误;B、CaCO3固体高温煅烧生成氧化钙和二氧化碳,能除去杂质且没有引入新的杂质,符合除杂原则。
B正确;C、氧气通过灼热的铜网时可与铜发生反应生成氧化铜,而氮气不与铜反应,能除去杂质且没有引入新的杂质,符合除杂原则。
C正确;D、碳酸钠能溶于水形成溶液,碳酸钙难溶于水。
加水溶解后过滤,得到碳酸钠溶液,再将溶液蒸发即可得到纯净的碳酸钠晶体,符合除杂原则。
D正确。
故选A。
【点睛】除杂的原则:不除去原物质、不引入新的杂质、易于分离4.下列实验操作中(括号内为待检验物质或杂质)不能达到实验目的是()A.A B.B C.C D.D【答案】B【解析】【分析】【详解】A. 鉴别C、CuO,加入稀硫酸,氧化铜会与硫酸反应逐渐溶解,生成蓝色的硫酸铜溶液,而木炭不反应,所以通过观察溶液颜色变化可以鉴别它们,方案可行。
一、中考初中化学除杂分离和提纯1.某混合溶液含有一定量的硝酸银、硝酸铜和硝酸钡,为逐一分离其中的金属元素,所加试剂均过量,且理论上氢氧化钠的消耗量最少。
所加试剂1-3顺序正确的是A.氢氧化钠、氯化钠、硫酸钠B.氯化钠、氢氧化钠、硫酸钠C.氯化钠、稀硫酸、氢氧化钠D.硫酸钠、氯化钠、氢氧化钠【答案】B【解析】【分析】【详解】A、先加入氢氧化钠,氢氧化钠会和硝酸铜反应生成蓝色沉淀和硝酸钠,但同时也会和硝酸银反应生成氢氧化银后迅速分解成氧化银,无法将金属元素逐一分离,故A错误;B、先加入氯化钠,氯化钠只和硝酸银反应生成白色沉淀和硝酸钠,不与其他物质反应,将沉淀过滤出来即可分离出银元素,再加入氢氧化钠,氢氧化钠只和硝酸铜反应生成氢氧化铜的沉淀和硝酸钠,将沉淀过滤出来即可分离出铜元素,再加入硫酸钠,硫酸钠和硝酸钡反应生成硫酸钡沉淀和硝酸钠,将沉淀过滤出来即可分离出钡元素,所加试剂顺序正确,故B正确;C、第二个所加试剂为稀硫酸的话,又因试剂均过量,那么在第三种加入氢氧化钠试剂时氢氧化钠要和过量的稀硫酸反应,氢氧化钠的消耗量就比B选项中的多了,故C错误。
D、硫酸银是微溶物,溶液中多了也会沉淀下来,所以第一步试剂加入硫酸钠的话,无法将硫酸钡和硫酸银给逐一分离,故D错误。
故选B。
2.下列方法不能达到除杂目的的是选项物质(括号内为杂质)方法A CO(CO2)通过灼热的氧化铜B MnO2(KCl)溶解、过滤、洗涤、干燥C CaO 固体(CaCO3)高温煅烧A.A B.B C.C D.D【答案】A【解析】【分析】【详解】A、CO能与灼热的氧化铜反应生成铜和二氧化碳,反而会把原物质除去,不符合除杂原则,故选项所采取的方法错误。
B、氯化钾易溶于水,MnO2难溶于水,可采取加水溶解、过滤、洗涤、干燥的方法进行分离除杂,故选项所采取的方法正确。
C、CaCO3在高温下煅烧生成氧化钙和二氧化碳,能除去杂质且没有引入新的杂质,符合除杂原则,故选项所采取的方法正确。
一、中考初中化学除杂分离和提纯1.下表中,除去物质所含少量杂质的方法和反应类型归类均正确的是A.A B.B C.C D.D【答案】A【解析】【分析】【详解】A、铜和氧气加热生成氧化铜,反应为化合反应,氧化铜和氧气加热不反应,可以除去铜粉,故A正确;B、一氧化碳和氧化铜反应生成铜和二氧化碳,反应不属于置换反应,故B不正确;C、盐酸和氢氧化钠反应生成氯化钠和水,反应类型为复分解反应,故C不正确;D、硫酸钾和硝酸钡反应生成硫酸钡和硝酸钾,引进新杂质硝酸钾,故D不正确。
故选A。
2.下列依据实验目的所设计的实验方案正确的是()D除去KNO3溶液中的KCl加入过量的AgNO3溶液,过滤A.A B.B C.C D.D【答案】C【解析】【分析】【详解】A、除去CO2中的HCl气体,将混合气体通入足量NaOH溶液中,NaOH不仅与杂质氯化氢反应,还与原物质二氧化碳反应,不符合除杂的“原物质不减少”原则,不能用于除氯化氢杂质,选项说法错误,故不符合题意;B、区分尿素CO(NH2)2、NH4Cl和NH4NO3,加熟石灰研磨闻气味,只能区分出尿素,NH4Cl 和NH4NO3都与熟石灰反应产生刺激性气味的氨气,无法区分,选项说法错误,故不符合题意;C、区分稀HCl( 酸性)、Na2CO3溶液(碱性)、NaCl溶液(中性),滴加紫色石蕊溶液,紫色石蕊遇稀HCl显红色,遇Na2CO3溶液显蓝色,遇NaCl溶液显紫色,可以通过观察颜色区分开,选项说法正确,故符合题意;D、除去KNO3溶液中的KCl,加入过量的AgNO3溶液,AgNO3只与KCl生成硝酸钾和沉淀氯化银,但AgNO3溶液是过量的,引入了新杂质,不符合除杂的“不引入新杂质”原则,不能用于除去KCl,选项说法错误,故不符合题意,故选C。
【点睛】该题为除杂和鉴别的综合题,解题关键是:把握除杂时,要根据物质的性质,选择合适的方法,不能除去主要物质,也不能引入新的杂质;鉴别物质,要根据物质的性质不同,通过不同的实验现象来区分物质。
一、中考初中化学除杂分离和提纯1.除去下列物质中混有的杂质所用试剂和操作方法均正确的是( )A.A B.B C.C D.D【答案】B【解析】【分析】除杂(提纯),是指除去杂质,同时被提纯物质不得改变。
【详解】A、氢氧化钠和硫酸铜反应生成氢氧化铜和硫酸钠,引入了硫酸钠杂质,故A不正确;B、铁粉与足量稀硫酸反应生成硫酸亚铁溶液和氢气,铜不能与稀硫酸反应,再过滤、洗涤、干燥,能除去杂质且没有引入新的杂质,符合除杂原则,故B正确;C、石灰水吸收二氧化碳的能力较弱,将气体依次通过盛有石灰水、浓硫酸的洗气瓶不能除去杂质,故C不正确;D、二氧化碳不能与氯化钙溶液反应,故D不正确。
故选B。
【点睛】除杂条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质。
2.下表列出了除去物质中所含少量杂质的方法,其中正确的是()A.A B.B C.C D.D【答案】D【解析】【分析】【详解】A、CaO能与水反应生成氢氧化钙,碳酸钙难溶于水,反而会把原物质除去,不符合除杂原则,故选项所采取的方法错误。
B、除去二氧化碳中的一氧化碳不能够点燃,这是因为当二氧化碳(不能燃烧、不能支持燃烧)大量存在时,少量的一氧化碳是不会燃烧的;故选项所采取的方法错误。
C、Na2CO3能与过量的氢氧化钙溶液反应生成碳酸钙沉淀和氢氧化钠,能除去杂质但引入了新的杂质氢氧化钙(过量的),不符合除杂原则,故选项所采取的方法错误。
D、氯化钠易溶于水,泥沙难溶于水,可采取加水溶解、过滤、蒸发的方法进行分离除杂,故选项所采取的方法正确。
故选:D。
【点睛】根据原物质和杂质的性质选择适当的除杂剂和分离方法,所谓除杂(提纯),是指除去杂质,同时被提纯物质不得改变.除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质。
3.某混合溶液含有一定量的硝酸银、硝酸铜和硝酸钡,为逐一分离其中的金属元素,所加试剂均过量,且理论上氢氧化钠的消耗量最少。
物质的分离和提纯模拟预测·演练基础性试题调研1.除去下列各组物质中的杂质,所用试剂和方法均正确的是()。
()。
A.食盐和细沙B.水和酒精C.石灰石和石灰水D.蔗糖和味精3.将下列各操作名称的序号填在后面的横线上(每个序号只填写一次):①搅拌②蒸发③过滤④加热(1)由饱和的食盐水得到食盐晶体______;(2)将饱和的硝酸钾溶液变为不饱和溶液______;(3)除去食盐中的泥沙,先溶解,再____;(4)将浓硫酸注入水中,为使热量迅速散发____。
4.实验小组的同学欲对一粗盐样品进行初步提纯。
所用实验仪器或用品如下:(1)A的名称是__________;(2)提纯的步骤是:溶解、过滤、______、计算产率;(3)“过滤”操作的要点可概括为“一贴、二低、三靠”,其中“二低”的含义是__________;(4)实验小组通过正确的计算发现,所得实验结果对与该粗盐的实际含量对比,实验测得的结果比实际偏低,请分析可能的原因:______________________________。
5.某自来水厂用源水处理成自来水的流程如下:(1)加入活性炭的作用是________;在乡村没有活性炭,常加入____________来净水。
(2)实验室中,静置、吸附、过滤、蒸馏等操作中可以降低水硬度的是____________。
(3)若该地区源水中含有较多的MgCl 2,请写出在源水处理流程中加入CaO 时的有关化学方程式:①________________________________________________________________________; ②________________________________________________________________________。
能力性试题调研1.下列实验方案中,设计合理的是( )。
A .用过滤的方法软化硬水B .用燃烧木炭的方法制备纯净的二氧化碳气体C .用浓硫酸除去氢气中的水蒸气D .用紫色石蕊溶液鉴别澄清石灰水和氢氧化钠溶液2.某同学对下列4个实验都设计了两种方案,其中方案1合理、方案2不合理的是( )。
2012中考试题汇编(物质分离与除杂)精选
一、选择题:(每小题有1——2个选项符合题意)
1.(宜昌)除去下列物质中混有的少量杂质(括号内为杂质),所用方法正确的是()
A.二氧化碳(一氧化碳)——将气体点燃B.氧化钙(碳酸钙)——加入适量的稀硫酸
C.氯化钠溶液(碳酸氢钠)——滴加入稀盐酸至恰好完全反应D.二氧化硫(氯化氢)——通过足量的氢氧化钠溶液2.()
3.()
()
()
6、()
7.(2012•()
8.()A.CaO中的CaCO3(高温煅烧)B.CO2中的CO(点燃)
C.N2中的O2(灼热铜丝)D.Na2SO4溶液中的NaOH(H2SO4)
9.(无锡)下列除杂所用药品不正确(括号内的是杂质)的是()A.FeSO4溶液(CuSO4)铁粉B.H2(HCl )NaOH C.CaO (CaCO3)水D.KCl(K2CO3)盐酸
()
()A. O2(H2O)—用生石灰 B. NaCl溶液(KNO3 )—降温结晶
C. CaCO3粉末(Na2CO3 )—加水过滤
D. KCl溶液(K2CO3)—加适量盐酸
()
()A.AgNO3溶液B.NaOH溶液C.稀醋酸D.KNO3溶液
14.( )
15、()
16.( ) (CO)
17()A.区分硝酸铵与磷矿粉---观察外观B.除去生石灰中含有的杂质石灰石---水或稀盐酸
C.检验长期露置的氢氧化钠溶液是否变质---稀盐酸或澄清石灰水
D.从过氧化氢溶液制氧气的残余物中分离出二氧化锰---过滤或蒸发
18.(2012遵义)要除去下列四种物质中的少量杂质(括号内的物质为杂质)
甲:CaCO3(KCl)乙:Na2SO4(CuSO4)丙:KCl(KOH)丁:碳粉(CuO)
可选用的试剂及操作方法有:①加适量水,搅拌,过滤;②加过量稀H2SO4,过滤;③溶解后加适量KOH溶液,过滤;
④溶解后加适量盐酸,蒸发;⑤加热(或高温灼烧).下列组合中正确的是()A.甲-⑤B.乙-③C.丙-④D.丁-①
19.(黑龙江龙东)欲除去下列物质中的少量杂质,所用的试剂正确的是()
20.( )
( )
22( )
23.()
Na
通过
24.()
硫酸钠
25.
A.CO2气体(CO气体)——通入氧气B.CaO固体(CaCO3固体)——加水充分溶解,过滤
C.KCl固体(MnO2固体)——加水充分溶解,过滤,蒸发结晶
D.NaCl溶液(CaCl2溶液)——滴加碳酸钾溶液至恰好完全反应,过滤
、(哈尔滨)除去下列物质中的少量杂质,所选用的试剂及操作方法均正确的是(
适量稀硫酸
27.(百色)除去下列物质中混有的少量杂质(括号内为杂质)所用方法正确的是()
A.CO 2( CO )──通入氧气点燃
B.SO 2( HCl )──通过足量的氢氧化钠溶液
C.KCl 固体( KClO 3 )── 加少量二氧化锰固体并加热
D.NaCl 溶液( NaHCO 3 )──滴加稀盐酸至恰好完全反应 28.(2012•烟台)下列各组物质分离提纯的步骤,与粗盐提纯(只除去不溶性杂质)的三个实验步骤相同的是( )
A .从空气中分离出氧气
B .从医用酒精中提纯酒精
C .从草木灰中提取碳酸钾(不考虑其他可溶性杂质)
D .从双氧水制取氧气的废液中回收二氧化锰 29.(菏泽)除去下列物质中含有的杂质所选用试剂或操作方法不正确...
的一组是 ( )
1.(随州)实验室制取气体所需的装置如图所示.请回答一下问题:
(1)写出装置中标号仪器的名称:a , b .
(2)用大理石和稀盐酸制取一瓶干燥的二氧化碳气体时,应选用装置 (填字母代号)组合.F 装置中浓硫酸的作用是 .
2.(12泸州)已知草酸(H 2C 2O 4)固体与浓硫酸供热发生化学反应:H 2C 2O 4
△
浓硫酸 CO 2↑+CO↑+H 2O 。
某化学兴趣
小组同学设计如下实验装置,用于制取纯净干燥的的CO 气体来还原氧化铁。
请根据题目要求回答下列问题:
(1)实验开始时,应首先点燃 处的酒精灯(填装置序号)。
(2)装置B 中NaOH 的作用是 ;C 中所盛的液体是 。
(3)B 装置玻璃管中观察的现象是 ,反应的方程式为_________ _ _______(4)从E 装置出来的尾气要进行处理,是因为尾气中含有 。
2012中考试题汇编(物质分离与除杂)精选
参考答案
一、选择题
1、C
2、B
3、C
4、C
5、C
6、AC
7、A
8、B
9、C10、D11、B12、D13、B14、D15、B16、C17、B18、C19、D20、D21、A22、AC23、BC24、B25、C26、D27、D28、C29、C。