消毒产品微生物检测实验记录表
- 格式:doc
- 大小:65.50 KB
- 文档页数:5
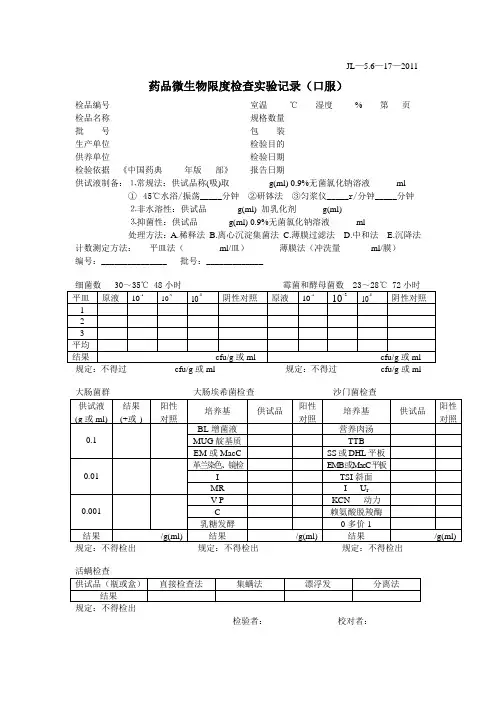
药品微生物限度检查实验记录(口服)检品编号_____________________________ 室温_____℃湿度_____% 第___页检品名称_____________________________ 规格数量____________________________ 批号_____________________________ 包装____________________________ 生产单位_____________________________ 检验目的____________________________ 供养单位_____________________________ 检验日期____________________________ 检验依据《中国药典年版部》报告日期____________________________ 供试液制备:⒈常规法:供试品称(吸)取_________g(ml) 0.9%无菌氯化钠溶液______ml①45℃水浴/振荡_____分钟②研钵法③匀浆仪_____r/分钟_____分钟⒉非水溶性:供试品_______g(ml) 加乳化剂______g(ml)⒊抑菌性:供试品_______g(ml) 0.9%无菌氯化钠溶液______ml处理方法:A.稀释法B.离心沉淀集菌法C.薄膜过滤法 D.中和法 E.沉降法计数测定方法:平皿法(________ml/皿)薄膜法(冲洗量_______ml/膜)编号:_______________ 批号:_____________大肠菌群大肠埃希菌检查沙门菌检查规定:不得检出规定:不得检出规定:不得检出规定:不得检出检验者:__________ 校对者:__________药品微生物限度检查实验记录(局部用药)检品编号_____________________________ 室温_____℃湿度_____% 第___页检品名称_____________________________ 规格数量____________________________ 批号_____________________________ 包装____________________________ 生产单位_____________________________ 检验目的____________________________ 供养单位_____________________________ 检验日期____________________________ 检验依据《中国药典年版部》报告日期____________________________ 供试液制备:⒈常规法:供试品称(吸)取_________g(ml) 0.9%无菌氯化钠溶液______ml②45℃水浴/振荡_____分钟②研钵法③匀浆仪_____r/分钟_____分钟⒉非水溶性:供试品_______g(ml) 加乳化剂______g(ml)⒊抑菌性:供试品_______g(ml) 0.9%无菌氯化钠溶液______ml处理方法:A.稀释法B.离心沉淀集菌法C.薄膜过滤法 D.中和法 E.沉降法规定:不得过__________cfu/g或ml 规定:不得过_________cfu/g或ml 金黄色葡萄球菌检查铜绿假单胞菌检查规定:不得检出规定:不得检出规定:不得检出规定:不得检出检验者:__________ 校对者:__________。

消毒产品检验技术规范
1. 消毒产品检验方法:包括对产品成分、理化性质、杀菌效果等方面进行检测的具体方法和步骤。
2. 消毒产品化学成分分析:通过分析消毒产品的化学成分,确定产品是否符合相关要求。
3. 消毒产品理化性质检验:包括对消毒产品的外观、pH值、溶解性、稳定性等方面进行检测。
4. 消毒产品杀菌效果评价:通过实验室测试,评估消毒产品对不同细菌、的杀灭能力。
5. 消毒产品毒性评价:通过实验评估消毒产品对人体的毒性和刺激性,确保产品对人体无害。
6. 消毒产品贮存稳定性评价:评估产品在贮存期间的性能变化和稳定性。
7. 消毒产品标签标识检验:检验产品的标签上是否包含正确的使用说明、成分信息等,并确保标签和包装符合相关法规要求。
8. 消毒产品包装检验:检验产品包装的完整性、防伪性能等。
9. 消毒产品微生物检验:通过培养和检测微生物,评价产品的无菌性和抗菌效果。
10. 消毒产品残留物检验:检验产品使用后是否有残留物,确保产品不会对环境和使用者产生不良影响。
通过进行上述检验,可以确保消毒产品的质量和安全性符合相关标准和法规要求,保护公众的健康安全。

卫生用品微生物限度记录表单家庭卫生用品微生物限度记录
(1)海绵
1. 菌落总数:海绵的菌落总数检测结果为:100cfu/g。
2. 指示菌:检测结果显示,海绵内无指示菌存在。
3. E. coli:海绵内无E. coli检测。
4. Staphylococcus aureus:海绵无Staphylococcus aureus检测。
(2)肥皂
1. 菌落总数:肥皂的菌落总数检测结果为:25cfu/g。
2. 指示菌:检测结果显示,肥皂内无指示菌存在。
3. E. coli:肥皂内无E. coli检测。
4. Staphylococcus aureus:肥皂无Staphylococcus aureus检测。
(3)漱口杯
1. 菌落总数:漱口杯的菌落总数检测结果为:150 cfu/g。
2. 指示菌:检测结果显示,漱口杯内无指示菌存在。
3. E. coli:漱口杯内无E. coli检测。
4. Staphylococcus aureus:漱口杯内无Staphylococcus aureus检测。
(4)卷筒纸
1. 菌落总数:卷筒纸的菌落总数检测结果为:40 cfu/g。
2. 指示菌:检测结果显示,卷筒纸内无指示菌存在。
3. E. coli:卷筒纸内无E. coli检测。
4. Staphylococcus aureus:卷筒纸内无Staphylococcus aureus检测。

紫外线消毒效果实验报告一、引言随着健康意识的提高,对于消毒的需求也越来越迫切。
紫外线消毒作为一种高效、无化学残留的消毒方式,备受关注。
本实验旨在研究紫外线消毒对微生物的杀灭效果,以及不同因素对紫外线消毒效果的影响。
二、实验目的探究紫外线消毒在杀灭微生物方面的效果,并分析不同因素对紫外线消毒效率的影响。
三、实验步骤1. 实验准备:a. 准备所需实验材料:紫外线消毒灯、灭菌培养皿、试管、无菌滴管等。
b. 搭建实验装置:将紫外线消毒灯固定在实验室专用支架上,确保距离合适。
2. 实验设计:a. 分别取两个灭菌培养皿,标记为“对照组”和“实验组”。
b. 在“对照组”培养皿中分别滴加适量的无菌培养基。
c. 在“实验组”培养皿中也滴加适量的无菌培养基,并将其置于紫外线消毒灯下照射一段时间。
3. 实验操作:a. 置于紫外线照射一段时间后,将实验组和对照组培养皿分别密封,存放在适当的环境中。
b. 接下来的几天,观察培养皿中微生物的生长情况。
四、实验结果经过观察和记录,我们得到如下实验结果:在对照组中,微生物开始呈现规律性生长,培养基的颜色逐渐变深。
而对于实验组,观察到紫外线消毒后的培养皿中微生物的生长受到抑制,培养基的颜色较为浅淡。
五、数据分析从实验结果中,我们可以得出以下结论:紫外线消毒对微生物具有较好的杀灭效果。
与对照组相比,实验组的培养基颜色浅淡,说明紫外线照射后能够明显抑制微生物的生长。
六、实验讨论1. 实验中的影响因素a. 紫外线照射时间:实验过程中,我们发现照射时间越长,微生物的生长受到的抑制效果越明显。
b. 紫外线照射距离:合适的照射距离能够确保紫外线能够有效达到杀菌杀灭微生物的效果。
2. 紫外线消毒的优点:a. 高效:紫外线消毒作用迅速,能够在短时间内杀灭微生物。
b. 无化学残留:相比其他消毒方式,紫外线消毒不需要使用化学药剂,避免了化学残留对环境和人体的影响。
c. 广泛应用:紫外线消毒适用于多种场所,如水处理、医疗设备、空气净化等。
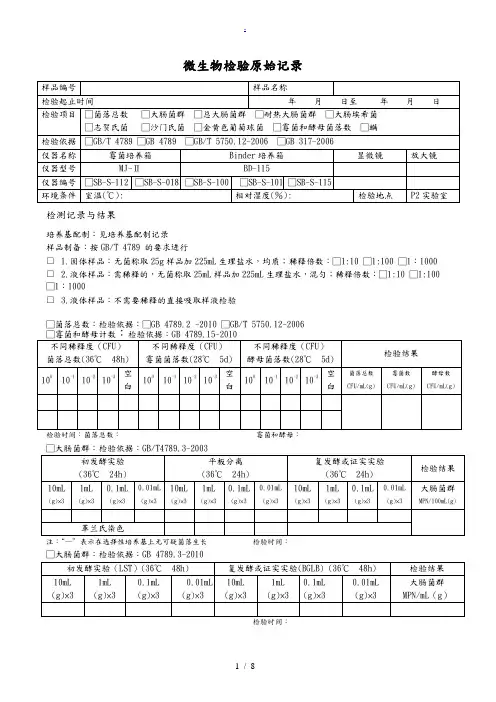
微生物检验原始记录
检测记录与结果
培养基配制:见培养基配制记录
样品制备:按GB/T 4789 的要求进行
□ 1.固体样品:无菌称取25g样品加225mL生理盐水,均质;稀释倍数:□1:10 □1:100 □1:1000 □ 2.液体样品:需稀释的,无菌称取25mL样品加225mL生理盐水,混匀;稀释倍数:□1:10 □1:100 □1:1000
□ 3.液体样品:不需要稀释的直接吸取样液检验
□菌落总数:检验依据:□GB 4789.2 -2010 □GB/T 5750.12-2006
检验时间:菌落总数:霉菌和酵母:
□大肠菌群:检验依据:GB/T4789.3-2003
注:“—”表示在选择性培养基上无可疑菌落生长检验时间:
检验时间:
□总大肠菌群:检验依据:GB/T 5750.12-2006
注:“—”表示在选择性培养基上无可疑菌落生长检验时间:
□耐热大肠菌群:检验依据:GB/T 5750.12-2006
注:“—”表示在选择性培养基上无可疑菌落生长检验时间:
□大肠埃希氏菌:检验依据:GB/T 5750.12-2006
检验时间:
□致病菌□沙门氏菌□志贺氏菌□金黄色葡萄球菌
检验依据 GB 317.4-.10-2006
检测人:复核人:
微生物限度检验记录(复合膜)
检验人:复核人:
微生物限度检验记录(辅料)
检验人:复核人:
微生物限度检验记录(铝箔、PVC硬片)
微生物限度检验记录(半成品、成品)
检验人:复核人:
微生物限度检验记录(辅料)
检验人:复核人:。
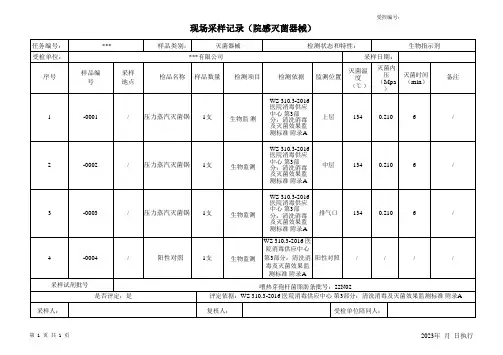
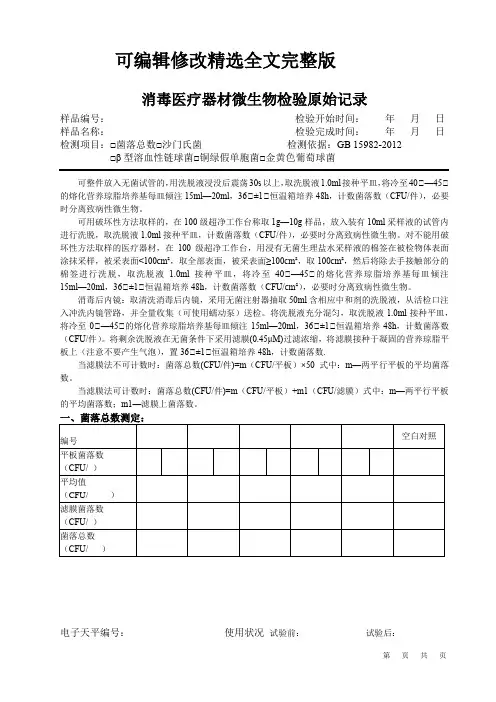
可编辑修改精选全文完整版消毒医疗器材微生物检验原始记录样品编号:检验开始时间:年月日样品名称:检验完成时间:年月日检测项目:□菌落总数□沙门氏菌检测依据:GB 15982-2012□β型溶血性链球菌□铜绿假单胞菌□金黄色葡萄球菌可整件放入无菌试管的,用洗脱液浸没后震荡30s以上,取洗脱液1.0ml接种平皿,将冷至40℃—45℃的熔化营养琼脂培养基每皿倾注15ml—20ml,36℃±1℃恒温箱培养48h,计数菌落数(CFU/件),必要时分离致病性微生物。
可用破坏性方法取样的,在100级超净工作台称取1g—10g样品,放入装有10ml采样液的试管内进行洗脱,取洗脱液1.0ml接种平皿,计数菌落数(CFU/件),必要时分离致病性微生物。
对不能用破坏性方法取样的医疗器材,在100级超净工作台,用浸有无菌生理盐水采样液的棉签在被检物体表面涂抹采样,被采表面<100cm²,取全部表面,被采表面≥100cm²,取100cm²,然后将除去手接触部分的棉签进行洗脱,取洗脱液 1.0ml接种平皿,将冷至40℃—45℃的熔化营养琼脂培养基每皿倾注15ml—20ml,36℃±1℃恒温箱培养48h,计数菌落数(CFU/cm²),必要时分离致病性微生物。
消毒后内镜:取清洗消毒后内镜,采用无菌注射器抽取50ml含相应中和剂的洗脱液,从活检口注入冲洗内镜管路,并全量收集(可使用蠕动泵)送检。
将洗脱液充分混匀,取洗脱液1.0ml接种平皿,将冷至0℃—45℃的熔化营养琼脂培养基每皿倾注15ml—20ml,36℃±1℃恒温箱培养48h,计数菌落数(CFU/件)。
将剩余洗脱液在无菌条件下采用滤膜(0.45μM)过滤浓缩,将滤膜接种于凝固的营养琼脂平板上(注意不要产生气泡),置36℃±1℃恒温箱培养48h,计数菌落数.当滤膜法不可计数时:菌落总数(CFU/件)=m(CFU/平板)×50式中:m—两平行平板的平均菌落数。
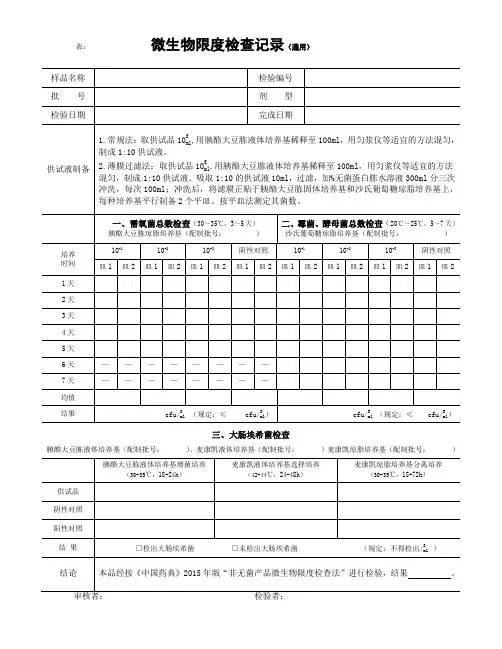
表:微生物限度检查记录(通用)三、大肠埃希菌检查胰酪大豆胨液体培养基(配制批号:)、麦康凯液体培养基(配制批号:)麦康凯琼脂培养基(配制批号:)微生物限度检查记录(30~35℃,3~5天)20℃~25℃,5~7天)沙氏葡萄糖琼脂培养基(配制批号:)三、控制菌检查(30-35℃)表:胰酪大豆胨液体培养基(配制批号:)、麦康凯液体培养基(配制批号:)麦康凯琼脂培养基(配制批号:)(30℃~35℃)胰酪大豆胨液体培养基(配制批号:)、RV沙门增菌液体培养基(配制批号:),木糖赖氨酸脱氧胆酸盐琼脂培养基(配制批号:)、三糖铁琼脂(配制批号:)五、耐胆盐革兰阴性菌检查胰酪大豆胨液体培养基(配制批号:)、肠道菌增菌液体培养基(配制批号:),紫红胆盐葡萄糖琼脂培养基(配制批号:)表:(含药材原粉的片剂)胰酪大豆胨液体培养基(配制批号: )、麦康凯液体培养基(配制批号: )麦康凯琼脂培养基(配制批号: )(30℃~35℃)胰酪大豆胨液体培养基(配制批号: )、RV 沙门增菌液体培养基(配制批号: ),木糖赖氨酸脱氧胆酸盐琼脂培养基(配制批号: )、三糖铁琼脂(配制批号: )五、耐胆盐革兰阴性菌检查胰酪大豆胨液体培养基(配制批号: )、肠道菌增菌液体培养基(配制批号: ),紫红胆盐葡萄糖琼脂培养基(配制批号: )表:微生物限度检查记录(蛇胆川贝液)三、大肠埃希菌检查胰酪大豆胨液体培养基(配制批号:)、RV沙门增菌液体培养基(配制批号:),木糖赖氨酸脱氧胆酸盐琼脂培养基(配制批号:)、三糖铁琼脂(配制批号:)表:微生物限度检查记录(30~35℃,3~5天)20℃~25℃,5~7天)沙氏葡萄糖琼脂培养基(配制批号:)胰酪大豆胨液体培养基(配制批号:)、麦康凯液体培养基(配制批号:)麦康凯琼脂培养基(配制批号:)表:微生物限度检查记录(内包材)三、大肠埃希菌检查胰酪大豆胨液体培养基(配制批号:)、麦康凯液体培养基(配制批号:)麦康凯琼脂培养基(配制批号:)。

洗浴场所用品用具微生物检测原始记录管理编号:xxx/XX-XXX报告编号:第页/ 共页检测项目真菌总数送检日期检毕日期检测环境温度:ºС 相对湿度:% 检测地点样品来源样品编号仪器型号及编号检测方法或依据参照GB/T 18204.4-2013 《公共场所卫生检验方法第4部分:公共用品用具微生物》检验方法将经灭菌的规格板放在被检物体表面,用一浸有灭菌生理盐水的棉签在其内涂抹次,然后剪去手接触部分棉棒,将棉签放入含10ml灭菌生理盐水的采样管内,于h内送实验室。
1.菌落总数检测每支采样管充分混匀后取1ml样液,放入灭菌平皿内,倾注营养琼脂培养基,每个样品平行接种两块平皿,置℃±1℃培养h后观察结果,计数平板上菌落数。
表1 菌落总数测试结果(空白对照cfu /皿)检测人:校核人:洗浴场所用品用具微生物检测原始记录管理编号:xxx/XX-XXX报告编号:第页 / 共页2.真菌总数检测在每只鞋的鞋内前端与脚趾接触处cm× cm面积范围内分别均匀涂抹次,左、右鞋各采样 cm2,采样总面积为 cm2,双鞋为同份样品。
将采样后棉拭子放入装有 ml生理盐水的试管充分振摇,此液为1:10的样品匀液。
用1mL无菌吸管或微量移液器吸取1:10样品匀液1mL,沿管壁缓慢注于盛有9mL生理盐水稀释液的无菌试管中(注意吸管或吸头尖端不要触及稀释液面),振摇试管或换用1支无菌吸管反复吹打使其混合均匀,制成1:100的样品匀液。
按同法制备10倍系列稀释样品匀液,每递增稀释1次,换用1次1mL 无菌吸管或吸头。
选择样品匀液原液及 ~ 个适宜稀释度的样品匀液,分别吸取mL样品匀液于个无菌平皿内。
同时分别取 mL不添加样品的稀释液加入两个无菌平皿作空白对照。
将溶化并冷却至℃左右的孟加拉红琼脂或沙氏琼脂注入灭菌的平皿中,待琼脂凝固后,倒置于℃~ ℃温箱中, d后开始观察,共培养观察一周。
表2 真菌总数测试结果(空白对照cfu /皿)检测人:校核人:洗浴场所公共用品用具微生物检测原始记录管理编号:xxx/XX-XXX报告编号:第页 / 共页3.大肠菌群检测采用乳糖胆盐发酵法进行大肠菌群的检验,如不产酸不产气,则记录该发酵管阴性,如产酸产气则进行确证试验;根据试验结果查MPN表,报告检验结果。

消毒剂微生物限度的检测标准通常遵循相关的国家标准或行业标准。
在中国,消毒剂的微生物限度检测通常遵循《消毒技术规范》(2002年版)或《消毒产品卫生安全评价技术要求》(WS/T 668-2016)等标准。
这些标准规定了消毒剂在特定条件下,如一定时间内、一定浓度下,对微生物(如细菌、真菌、病毒等)的杀灭效果或抑制作用。
检测方法通常包括微生物培养法、荧光法、酶联免疫法等,以确定消毒剂的微生物限度。
具体的检测方法、标准限量、合格判定等要求会根据消毒剂的种类、使用范围和标准的不同而有所差异。
因此,在进行消毒剂微生物限度检测时,需要严格按照相应的标准和方法进行操作,并由具备相应资质和能力的检测机构出具检测报告。

消毒产品检测项目
消毒产品的检测项目可以包括以下几个方面:
1. 性能指标检测:包括有效成分、有效成分浓度、pH值、相对密度、溶解度等性能指标的检测,以确保产品的有效性和稳定性。
2. 微生物检测:消毒产品的主要功能是杀灭细菌和病毒,因此需要对产品进行微生物检测,包括常规菌落总数、大肠杆菌和金黄色葡萄球菌等致病菌的检测。
3. 毒理学检测:消毒产品的使用对人体和环境是否有毒副作用是需要关注的问题,可以进行急性和慢性毒性测试,包括对小鼠、大鼠等动物的生存状况、器官损害等进行评估。
4. 气味检测:消毒产品往往会有一定的气味,因此需要进行气味检测,以确保产品的气味无害或无刺激性。
5. 包装标签检测:检测消毒产品的包装信息是否准确、清晰,包括产品名称、生产日期、有效期等信息。
6. 腐蚀性检测:检测消毒产品对金属和其他材料的腐蚀情况。
综上所述,消毒产品的检测项目主要涉及性能指标、微生物、毒理学、气味、包装标签和腐蚀性等方面的检测。
根据具体产品的特点和用途,也可能有其他相关的检测项目。
目录1 消毒剂与消毒器械 1 1.1消毒剂与消毒器械检验时限 1 1.2 灭菌医用包装材料检验时限 21.3说明 22 消毒剂与消毒器械等检验所需样品数量及规格3 2.1 消毒剂检验所需样品数量及规格 3 2.2 消毒器械检验所需样品数量及规格 42.3 灭菌医用包装材料检验所需样品数量及规格 43 消毒剂与消毒器械检验项目及要求4 3.1消毒剂与消毒器械检验项目及要求 4 3.2消毒器械检验项目及要求 6 3.3 指示物检验项目及要求73.4 灭菌医用包装材料检验项目及要求74.卫生用品和一次性使用医疗用品检验规定7 4.1卫生用品和一次性使用医疗用品检验时限、检验所需样品数量及规格7 4.2一次性使用医疗用品检验时限、检验所需样品数量及规格8 4.3 卫生用品和一次性使用医疗用品检验项目及要求9 4.4卫生用品和一次性使用医疗用品检验报告编制要求12 5.消毒产品检验报告编制原则12 5.1本检验报告体例共分三个类型12 5.2本检验报告体例要求12 5.3本检验报告体例12 5.4检验单位报告体例12 5.5检验机构应出具检验报告数目125.6 消毒剂与消毒器械等检验报告编制原则136 消毒剂与消毒器械等检验报告体例13 6.1封面13 6.2说明14 6.3检验结论15 6.4理化检验16(1)消毒产品检验理化性能检验结论16(2)消毒剂有效成分含量测定17(3)消毒剂pH 值测定19(4)消毒剂稳定性测定(化学法)20(5)消毒剂对金属腐蚀性试验21(6)消毒器械消毒因子的强度测定22 6.5微生物试验23(1)消毒剂杀微生物试验结论23(2)细菌定量杀灭试验24(3)脊髓灰质炎病毒灭活试验26(4)能量试验28(5)有机物对消毒剂杀菌效果的影响试验29(6)消毒剂稳定性测定(微生物法)30(7)消毒剂空气消毒效果鉴定试验31(8)消毒器械空气消毒效果鉴定试验33(9)毒剂空气消毒效果现场试验35(10)消毒器械空气消毒效果现场试验36(11)饮水消毒剂杀菌试验37(12)饮水消毒器杀菌试验38(13)压力蒸汽灭菌生物指示物鉴定试验39(14)压力蒸汽灭菌化学指示卡鉴定试验40(15)紫外线强度化学指示卡鉴定试验41(16)消毒剂浓度试纸鉴定试验42(17)消毒剂对手消毒效果现场试验43(18)手消毒效果现场试验44(19)皮肤消毒效果模拟现场试验45(20)皮肤消毒效果现场试验46(21)消毒剂对物体表面消毒模拟现场试验47(22)消毒剂对物体表面消毒现场试验48(23)消毒剂对食(饮)具消毒模拟现场试验49(24)消毒碗柜对食(饮)具消毒大肠杆菌模拟现场试验50(25)消毒剂对医疗器械消毒模拟现场试验51(26)消毒剂对医疗器械灭菌模拟现场试验52(27)抑菌环试验53(28)振荡烧瓶试验54(29)奎因试验55(30)浸渍试验56(31)滞留抑菌效果试验57(32)洗衣粉抗(抑)菌效果鉴定方法试验58(33)最小抑菌浓度测定试验59(34)灭菌医用包装材料一般检查60(35)灭菌医用包装材料质量测定61(36)灭菌因子穿透性能测定62(37)灭菌对包装标识的影响试验63(38)灭菌医用包装材料不透气性试验64(39)透气性材料微生物屏障试验65(40)灭菌医用包装材料无菌有效期试验66 6.6 毒理学检验67(1)急性经口毒性试验67(2)急性吸入毒性试验68(3)皮肤刺激试验69(4)急性眼刺激试验70(5)阴道粘膜刺激试验73(6)皮肤变态反应试验74(7)亚急性毒性试验75(8)体外哺乳动物细胞基因突变试验77(9)体外哺乳动物细胞染色体畸变试验78(10)小鼠骨髓嗜多染红细胞微核试验79(11)小鼠精子畸形试验807.卫生用品、一次性使用医疗用品检验报告体例(1)卫生用品检验结论81 81(2)卫生用品微生物污染检测(3)隐形眼镜护理用品渗透压测定8283(4)隐形眼镜护理用品澄清度检查(5)溶出性抗(抑)菌卫生用品抑菌试验(6)隐形眼镜护理用品开封产品抛弃日期测定848586(7)隐形眼镜护理用品模拟现场试验87(8)环氧乙烷残留量测定(9)一次性使用医疗用品检验结论8889(10)一次性使用医疗用品细菌菌落总数测定、致病菌检测(11)一次性使用医疗用品无菌试验(12)一次性使用医疗用品环氧乙烷灭菌程序验证试验(13)一次性使用医疗用品电离辐射灭菌程序验证试验90919293(14)几点说明94消毒产品检验规定1.消毒剂和消毒器械1.1消毒剂和消毒器械检验时限消毒剂和消毒器械检验时限见表11.2 灭菌医用包装材料检验时限灭菌医用包装材料检验时限见表21.3 说明(1)表1、表2项目中所需时间只适用于单项检测。
表消毒产品微生物检测实验记录表检品名称规格生产单位包装供样单位检品数量批号收检日期检验目的检验日期检验依据报告日期检验员复核人用无菌方法打开用于检测的至少3个包装,从每个包装中取样,准确称取10 g±1g样品,剪碎后加入到200 mL灭菌生理盐水中,充分混匀,得到一个生理盐水样液。
液体产品用原液直接做样液。
样品制备:样品:g(ml);0.9%无菌氯化钠溶液ml。
细菌菌落总数原始记录表培养温度培养时间菌落数cfu 原液10-110-2阴性对照平板1 2 3 4 5 1 2 3 4 5 1 2 3 4 5 1 2 24h48h真菌落总数原始记录表培养温度培养时间菌落数cfu 原液10-110-2阴性对照平板1 2 3 4 5 1 2 3 4 5 1 2 3 4 5 1 2 3d5d7d致病性化脓菌试验原始记录表致病菌项目结果大肠菌群乳糖胆盐发酵培养产酸:是□否□产气:是□否□伊红美蓝琼脂培养是否长菌:是□否□若长菌,菌落形态为:革兰氏染色镜检革兰氏菌:阴性□阳性□芽孢:有□无□乳糖发酵培养产酸:是□否□产气:是□否□结果判定大肠杆菌:检出□未检出□绿脓杆菌SCDLP培养培养液是否呈黄绿色或蓝绿色:是□否□十六烷基三甲基溴化铵平板培养是否长菌:是□否□若长菌,菌落形态为:革兰氏染色镜检革兰氏菌:阳性□阴性□(阴性则进行下列试验)氧化酶试验阴性□阳性□绿脓菌素试验阴性□阳性□硝酸盐还原产气试验阴性□阳性□明胶液化试验阴性□阳性□42℃生长试验阴性□阳性□结果判定绿脓杆菌:检出□未检出□金黄色葡萄球菌SCDLP培养是否长菌:是□否□血琼脂平板是否长菌:是□否□若长菌,菌落形态为:革兰氏染革兰氏菌:阴性□阳色镜检性□是否葡萄状:是□否□芽孢与荚膜:是□否□若为革兰氏阳性球菌,排列成葡萄状,无芽孢与荚膜,进行下列试验。
甘露醇发酵试验阴性□阳性□血浆凝固酶试验阴性□阳性□结果判定溶血性链球菌葡萄糖肉汤培养是否长菌:是□否□血琼脂平板是否长菌:是□否□若长菌,菌落形态为:革兰氏染色镜检革兰氏菌:阴性□阳性□是否为链状排列球菌:是□否□若为革兰氏阳性,呈链状排列的球菌,进行下列试验。