脱羧反应
- 格式:doc
- 大小:29.50 KB
- 文档页数:2


羧化反应和脱羧反应
羧化反应和脱羧反应是有机化学中非常重要的两种反应类型。
羧化反应是指将一个含有羟基的化合物(如醇)氧化为一个羧酸化合物的反应。
这个反应通常需要一种氧化剂,如酸性高锰酸钾(KMnO4)或过氧化氢(H2O2)。
羧化反应是有机合成中非常常见的一种反应,因为羧酸化合物是许多生物大分子(如脂肪酸、蛋白质等)的重要组成部分。
相反,脱羧反应是指将一个羧酸化合物转化为一个含有一个碳原子少的化合物的反应。
这种反应通常需要一种还原剂,如锌或铝。
脱羧反应也是有机合成中非常常见的一种反应,因为它可以用来制备一些有用的化合物,如醛、酮等。
总的来说,羧化反应和脱羧反应是有机合成中非常重要的两种反应类型,可以用来制备许多重要的化合物。
- 1 -。

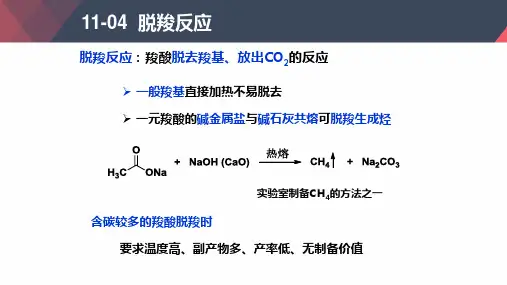
脱羧反应,加热无水醋酸钠和碱石灰的混合物:CH3COONa+NaOH=(Δ;CaO)=Na2CO3+CH4↑其它方法还有,通过生物原料像麦秸等,通过分解等一系列流程可以制得甲烷,一般用作天然气,当然,过程很复杂的写不出方程式。
另外某些区域海底有可燃冰CH4•H2O,从深海开采出来后,降低压强调整温度就可以得到大量的甲烷。
(1)氧化反应:CH4 + 2O2 ---> CO2 + 2H2O(2)取代反应:CH4 + Cl2 ---> CH3Cl + HCl (反应条件:光)CH3Cl + Cl2 ---> CH2Cl2 + HClCH2Cl + Cl2 ---> CHCl3 + HClCHCl3 + Cl2 ---> CCl4 + HCl(3)分解反应:CH4 ---> C + 2H2 (反应条件:加热)(1)还原反应把制得的甲烷气体通入盛有高锰酸钾溶液(加几滴稀硫酸)的试管里,没有变化。
再把甲烷气体通入溴水,溴水不褪色。
甲烷可以发生氧化反应(燃烧反应)。
(2)取代反应把一个大试管分成五等分,或用一支有刻度的量气管,用排饱和食盐水法先收集1/5体积的甲烷,再收集4/5体积的氯气,把它固定在铁架台的铁夹上,并让管口浸没的食盐水里。
然后让装置受漫射光照射。
在阳光好的日子,约半小时后可以看到试管内氯气的黄绿色逐渐变淡,管壁上出现油状物,这是甲烷和氯气反应的所生成的一氯甲烷、二氯甲烷、三氯甲烷、四氯化碳(或四氯甲烷)和少量的乙烷的混和物。
试管中液面上升,这是反应中生成的氯化氢溶于水的缘故。
食盐水中白色晶体析出。
因为氯气极易溶于水,溶于水后增加了水中氯离子的浓度,是氯化钠晶体析出。
用大拇指按住试管管口,提出液面,管口向上,向试管中滴入紫色石蕊试液或锌粒,可验证它是稀盐酸。
如果在阴暗的天气需1到2小时才能观察到反应的结果。
CH4+Cl2→(光照)CH3Cl(气体)+HClCH3Cl+Cl2→(光照)CH2Cl2(油状物)+HClCH2Cl2+Cl2→(光照)CHCl3(油状物)+HClCHCl3+Cl2→(光照)CCl4(油状物)+HCl最后生成的hcl最多(3)氧化反应点燃纯净的甲烷,在火焰的上方罩一个干燥的烧杯,很快就可以看到有水蒸气在烧杯壁上凝结。

脱酸反应羧酸分子脱去羧基 (一COOH)放出二氧化碳的反应叫脱羧反应:R-COOH→RH+CO₂脱羧反应是有机化学的一类重要反应,随着研究的不断深入 , 对不同脱羧反应的机理与调控途径有了更细微的了解 ,脱羧反应的应用也越来越广,现已广泛地应用于化工、生物、医药、食品等领域。
脱羧反应之所以能够发生 ,是由其分子结构决定的。
一般情况下 ,羧酸中的羧基较为稳定 ,不易发生脱羧反应 ,但在特殊条件下 ,羧酸能脱去羧基(失去二氧化碳) 而生成烃。
一、从分子结构来分析脱羧反应为什么能够发生在羧酸分子中,羧基中的碳原子是 SP2杂化的,它的三个 SP2杂化轨道分别与烃基及两个氧原子形成三个σ键,这三个σ键同在一个平面上,碳原子剩下的一个 P电子与氧原子的一个 P电子形成了羰基 ( )中的π键,羧基中的一OH的氧上有一对孤电子,可与羰基上的π键形成 P一π共轭体系。
羧基的结构羧基负离子的结构由于 P一π共轭效应,OH的氧原子的电子云向羰基移动,增强了0一H键的极性,有利于氢原子的离解,使羧酸比醇酸性强。
当羧基上的H离解后,P一π共轭作用更加完全,两个C一0键的键长完全平均化,羧酸根负离子更加稳定。
从上可见,羧酸分子结构的一个特点是:具有 P一π共轭效应的是比较稳定的部分,当受热时可以作为CO2整体脱去。
CO2脱去后,中心碳原子转为SP杂化,碳原子的两个SP杂化轨道分别与两个氧原子形成两个σ键,分子呈直线型,碳原子以未参与杂化的两个P轨道,分别与两个氧原子的 P轨道形成两个四电子三中心大π键(π43)。
这是一个非常稳定的结构。
从热力学的观点看,越稳定的越容易形成,所以脱羧反应能够发生。
脱羧反应的共价键断裂有两种方式:一种是异裂,即反应按离子型反应历程进行;一种是均裂,即反应按游离基型反应历程进行。
1、离子型反应历程大多数脱羧反应属于离子型反应历程。
有实验表明:这类脱羧反应属于单分子反应。
反应过程大致为:羧酸先离解生成羧酸根负离子和氢离子,羧基负离子()具有一个π43键一并且是一个供电的基团,使共价键发生异裂,生成烃基负离子并释放出CO2 ,最后烃基负离子获得氢离子使反应完成。

乙二酸脱羧反应方程式
乙二酸脱羧反应方程式是指将乙二酸(C2H2O4)进行脱羧反应,生成二氧化碳(CO2)和乙烯醇(C2H4O2)的化学反应。
其方程式如下:
C2H2O4 → CO2 + C2H4O2
在这个反应中,乙二酸分子经过加热或加入催化剂后发生脱羧反应,其中一个羧基(COOH)被去除,形成一个羰基(C=O),同时释放出一个CO2分子。
此时,产生的中间体可进一步发生水解反应,生成乙烯醇。
乙二酸脱羧反应是一种重要的有机合成反应,在化学工业上具有广泛的应用。
它可以用于合成各种含有羰基和醇基的有机物,如甲基丙烯酸、丁二醇、苯甲酸等。
此外,在医药、染料、香料等领域也有着重要的应用。
总之,乙二酸脱羧反应方程式是一种重要的有机合成反应,在化学工业和其他领域具有广泛的应用。
了解这个反应方程式的特点和应用,对于化学工作者和相关领域的从业者都是非常重要的。

脱酸反应羧酸分子脱去羧基 (一COOH)放出二氧化碳的反应叫脱羧反应:R-COOH→RH+CO₂脱羧反应是有机化学的一类重要反应,随着研究的不断深入 , 对不同脱羧反应的机理与调控途径有了更细微的了解 ,脱羧反应的应用也越来越广,现已广泛地应用于化工、生物、医药、食品等领域。
脱羧反应之所以能够发生 ,是由其分子结构决定的。
一般情况下 ,羧酸中的羧基较为稳定 ,不易发生脱羧反应 ,但在特殊条件下 ,羧酸能脱去羧基(失去二氧化碳) 而生成烃。
一、从分子结构来分析脱羧反应为什么能够发生在羧酸分子中,羧基中的碳原子是 SP2杂化的,它的三个 SP2杂化轨道分别与烃基及两个氧原子形成三个σ键,这三个σ键同在一个平面上,碳原子剩下的一个 P电子与氧原子的一个 P电子形成了羰基 ( )中的π键,羧基中的一OH的氧上有一对孤电子,可与羰基上的π键形成 P一π共轭体系。
羧基的结构羧基负离子的结构由于 P一π共轭效应,OH的氧原子的电子云向羰基移动,增强了0一H键的极性,有利于氢原子的离解,使羧酸比醇酸性强。
当羧基上的H离解后,P一π共轭作用更加完全,两个C一0键的键长完全平均化,羧酸根负离子更加稳定。
从上可见,羧酸分子结构的一个特点是:具有 P一π共轭效应的是比较稳定的部分,当受热时可以作为CO2整体脱去。
CO2脱去后,中心碳原子转为SP杂化,碳原子的两个SP杂化轨道分别与两个氧原子形成两个σ键,分子呈直线型,碳原子以未参与杂化的两个P轨道,分别与两个氧原子的 P轨道形成两个四电子三中心大π键(π43)。
这是一个非常稳定的结构。
从热力学的观点看,越稳定的越容易形成,所以脱羧反应能够发生。
脱羧反应的共价键断裂有两种方式:一种是异裂,即反应按离子型反应历程进行;一种是均裂,即反应按游离基型反应历程进行。
1、离子型反应历程大多数脱羧反应属于离子型反应历程。
有实验表明:这类脱羧反应属于单分子反应。
反应过程大致为:羧酸先离解生成羧酸根负离子和氢离子,羧基负离子()具有一个π43键一并且是一个供电的基团,使共价键发生异裂,生成烃基负离子并释放出CO2 ,最后烃基负离子获得氢离子使反应完成。


水杨酸脱羧反应方程式
水杨酸脱羧反应是一种常见的有机合成反应,其反应方程式如下:
C6H4(OH)COOH + NaOH → C6H4(OH)COONa + H2O
其中,水杨酸(C6H4(OH)COOH)与氢氧化钠(NaOH)在适当的条件下反应,生成水杨酸钠(C6H4(OH)COONa)和水。
这个反应是一个酸碱中和反应,其中氢氧化钠作为碱,中和了水杨酸中的羧基(-COOH),使其失去一个羰基(-CO)并形成相应的盐。
该反应通常在碱性条件下进行,在高温和高压下可以加速反应速率。
该反应具有广泛的实际意义。
例如,在制药工业中,水杨酸脱羧反应被广泛用于生产阿司匹林等药物。
此外,在化妆品工业中,该反应也用于制备具有抗炎、抗菌等功效的化妆品原料。
总之,水杨酸脱羧反应是一种重要的有机合成反应,具有广泛的实际意义。
掌握该反应的原理和操作方法对于有机合成和应用研究都具有重要意义。

三羧酸循环中的脱羧反应和脱氢反应一、引言三羧酸循环(TCA循环)是生物体内一种非常重要的代谢途径,它在细胞呼吸中发挥着至关重要的作用。
在三羧酸循环中,脱羧反应和脱氢反应是两个核心步骤,它们负责将乙酰辅酶A氧化成二氧化碳和水,并产生大量还原型辅酶NADH和FADH2。
这两种辅酶又很大程度上参与了线粒体内细胞呼吸链的工作。
本文将就三羧酸循环中的脱羧反应和脱氢反应展开全面的评估,并从浅入深地探讨这一主题。
二、脱羧反应(一)脱羧反应的定义和作用脱羧反应是三羧酸循环中的一种重要反应,它主要发生在异丙酰辅酶A脱羧酶作用下。
在这一反应中,乙酰辅酶A经过一系列酶催化作用,失去两个碳原子,生成丙酮酸。
这是三羧酸循环中的第一步脱羧反应,也是将有机物氧化为二氧化碳的关键步骤。
(二)脱羧反应的化学方程式和催化酶脱羧反应的化学方程式如下:乙酰辅酶A + GDP + Pi + NAD+ →羧基-辅酰胺 + CoA + NADH + CO2 + GTP脱羧反应主要由异丙酰辅酶A脱羧酶催化。
(三)脱羧反应的生物学意义脱羧反应将乙酰辅酶A氧化成丙酮酸的也产生了两分子还原型辅酶NADH。
这些还原型辅酶又可以进入线粒体内的细胞呼吸链,产生更多的三磷酸腺苷(ATP),为细胞提供充足的能量。
三、脱氢反应(一)脱氢反应的定义和作用脱氢反应是三羧酸循环中的另一个重要反应,它主要包括4个脱氢酶作用。
这些脱氢反应将丙酮酸、柠檬酸等有机酸氧化成了辅酰胺、嘌呤核苷酸二磷酸酶和α-麦角甾酮。
这是三羧酸循环中的另一关键步骤,也是细胞呼吸链所需的还原剂NADH和FADH2的主要生成途径。
(二)脱氢反应的化学方程式和催化酶脱氢反应的化学方程式如下:A酶-乙酰辅酶A + NAD+ ⇒ A酶-辅酰胺 + NADH + CO2脱氢反应主要由乳酸脱氢酶、苹果酸脱氢酶、橙酸脱氢酶和莽草酸脱氢酶催化。
(三)脱氢反应的生物学意义脱氢反应将有机酸氧化成了辅酰胺、嘌呤核苷酸二磷酸酶和α-麦角甾酮,产生了很多还原型辅酶NADH和FADH2。

脱酸反应羧酸分子脱去羧基(一 COOH 放出二氧化碳的反应叫脱羧反应:R-COO H RH+CO ?脱羧反应是有机化学的一类重要反应,随着研究的不断深入 , 对不同脱羧反应的机理与调控途径有了更细微的了解 ,脱羧反应的 应用也越来越广,现已广泛地应用于化工、生物、医药、食品等领域。
脱羧反应之所以能够发生,是由其分子结构决定的。
一般情况 下,羧酸中的羧基较为稳定,不易发生脱羧反应,但在特殊条件下, 羧酸能脱去羧基(失去二氧化碳)而生成烃。
一、从分子结构来分析脱羧反应为什么能够发生在羧酸分子中,羧基中的碳原子是 SP 2杂化的,它的三个SP 2杂化轨道分别与烃基及两个氧原子形成三个 (T 键,这三个(T 键同在一 个平面上,碳原子剩下的一个P 电子与氧原子的一个P 电子形成了 羰基(')中的n 键,羧基中的一 0H 的氧上有一对孤电子,可 与羰基上的n 键形成P 一 n 共轭体系。
由于P 一 n 共轭效应,0H 的氧原子的电子云向羰基移动,增强 了 0一H 键的极性,有利于氢原子的离解,使羧酸比醇酸性强。
当羧羧基的结构羧基负离子的结构基上的H 离解后,P 一n 共轭作用更加完全,两个C 一0键的键长完 全平均化,羧酸根负离子更加稳定。
从上可见,羧酸分子结构 的一个特点是:具有P 一n 共轭效应 —0的 是比较稳定的部分,当受热时可以作为 CQ 整体脱去。
CO 脱去后,中心碳原子转为 SP 杂化,碳原子的两个SP 杂化轨 道分别与两个氧原子形成两个。
键,分子呈直线型,碳原子以未参 与杂化的两个P 轨道,分别与两个氧原子的P 轨道形成两个四电子 三中心大n键(n 43)。
这是一个非常稳定的结构。
从热力学的观点看, 越稳定的越容易形成,所以脱羧反应能够发生。
脱羧反应的共价键断裂有两种方式: 一种是异裂,即反应按离子型反应历程进行;一种是均裂,即反应按游离基型反应历程进行。
1、离子型反应历程大多数脱羧反应属于离子型反应历程。
二元羧酸的脱羧反应机理一、引言脱羧反应是有机化学中一种重要的反应类型,它能够将羧酸分子中的羧基(-COOH)脱除,生成相应的羰基化合物。
而对于二元羧酸,其脱羧反应的机理相对复杂一些。
本文将以二元羧酸的脱羧反应机理为标题,详细介绍其反应过程。
二、二元羧酸的结构与性质二元羧酸是指含有两个羧基的有机酸,其分子结构中有两个羧基分别连接在不同的碳原子上。
由于二元羧酸分子中存在两个羧基,使得它们在反应过程中具有特殊的性质和反应路径。
三、脱羧反应的机理1. 脱羧反应的起始脱羧反应的起始是由于羧基的离去,形成一个羧酸根离子(RCOO-)。
这一步骤通常需要外界的刺激,如加热、溶剂催化等。
羧酸根离子的生成是通过羧基的负电荷在共轭体系中稳定而实现的。
2. 羧酸根离子的进一步反应羧酸根离子进一步参与反应,经过质子的转移和电荷的重新分配,形成共轭碳离子中间体(共轭负离子)。
共轭碳离子中间体的生成能够进一步增加反应的稳定性和速率。
3. 共轭碳离子的负电荷重新分布共轭碳离子中间体的负电荷重新分布,使得其负电荷能够更加稳定地分布在分子结构中。
这一步骤通常涉及到电子的重排和负电荷的共轭效应。
4. 生成羰基化合物在负电荷重新分布的过程中,共轭碳离子中间体失去一个氧原子,形成相应的羰基化合物。
这个过程是通过氧原子的离去和负电荷的重新分布实现的。
四、实例分析以乙二酸为例,其脱羧反应的机理如下:1. 乙二酸分子中的两个羧基离去,生成两个乙二酸根离子(C2H3O2-)。
2. 乙二酸根离子进一步参与反应,形成共轭碳离子中间体。
3. 共轭碳离子中间体的负电荷重新分布,使得其负电荷能够更加稳定地分布在分子结构中。
4. 最终生成乙酰醛(CH3CHO)和二氧化碳(CO2)。
五、结论二元羧酸的脱羧反应机理是一个复杂的过程,它涉及到羧基的离去、羧酸根离子的生成、共轭碳离子中间体的形成以及最终生成羰基化合物等多个步骤。
通过对二元羧酸脱羧反应机理的研究,能够更好地理解有机化学中的脱羧反应以及相关的反应机制。
羧酸脱羧反应
羧酸脱羧反应是一种有机化学转化反应,通过在羧酸分子上引入外部能量或催化剂的作用下,将羧基(-COOH)从羧酸分子中去除,生成一个碳氧双键,同时释放出一个二氧化碳分子(CO2)。
这个反应可以用以下化学方程式表示:
R-COOH → R-CO + CO2
其中,R代表一个有机基团。
羧酸脱羧反应是羧酸衍生物的重要转化反应,可以应用于有机化学合成的不同方面。
常见的脱羧反应包括热解脱羧、光解脱羧、酶催化脱羧等。
脱羧反应通常发生在酸性或碱性条件下,某些特定的功能化基团或化合物能够促进该反应的进行。
羧酸脱羧反应的应用广泛,例如,在药物合成中,脱羧反应可以用于构建药物分子的骨架或引入特定的官能团。
此外,脱羧反应还可以用于合成香料、染料、高分子材料等有机化合物。
脱羧反应ph一、脱羧反应的概述脱羧反应是有机化学中的一种重要反应类型,它是指有机酸中的羧基(-COOH)被去除,生成相应的烯烃或炔烃。
这种反应在有机合成中具有广泛的应用,可以用于制备各种有机化合物,如醛、酮、乙烯、丙烯等。
脱羧反应一般需要催化剂和适当的条件才能进行。
二、脱羧反应的分类1. 热解法:将含羧基的化合物加热至高温,使其发生分解而生成相应的烯或炔。
2. 光解法:利用紫外线或可见光辐射使有机酸分子内部发生裂解。
3. 电解法:利用电流通过含羧基化合物溶液时,在阳极上发生氧化还原反应而实现脱羧。
4. 化学方法:通过添加特定试剂或催化剂来促进脱羧反应。
三、常见脱羧反应及其机理1. 酸催化下的脱羧反应酸催化下的脱羧反应是一种常见的脱羧反应类型,它可以用于制备醛、酮等化合物。
以苯甲酸为例,其脱羧反应机理如下:(1)初步生成苯甲酸的负离子;(2)负离子中的羟基被质子化,形成稳定的离子;(3)水分子进攻,使得C—O键断裂,生成苯乙酮。
2. 金属催化下的脱羧反应金属催化下的脱羧反应是一种重要的脱羧反应类型,常用于制备烯烃和炔烃。
以丙二酸为例,其脱羧反应机理如下:(1)丙二酸在钠乙二硫和氢氧化钠存在下发生去质子化反应;(2)产生稳定的负离子;(3)钠和乙二硫还原负离子中的一个羰基,并使其发生消除反应;(4)生成丙烯。
四、脱羧反应在有机合成中的应用1. 制备烯烃和炔烃:通过金属催化法或其他方法可以制备各种不同结构的烯烃和炔烃,这些化合物在有机合成中具有广泛的应用。
2. 制备醛、酮等化合物:通过酸催化法可以制备各种不同结构的醛、酮等化合物,这些化合物在药物、农药等领域有着重要的应用。
3. 制备芳香族羧酸:通过芳香族羧酸的脱羧反应可以制备各种不同结构的芳香族烯烃和炔烃,这些化合物在医药、农药等领域具有广泛的应用。
五、脱羧反应ph值对反应速率的影响脱羧反应ph值对反应速率有着较大的影响。
一般来说,在弱酸性条件下,脱羧反应速率较慢;而在强碱性条件下,脱羧反应速率较快。
barton自由基脱羧反应Barton自由基脱羧反应Barton自由基脱羧反应是一种重要的有机合成反应,由英国化学家Derek Harold Richard Barton于1950年首次提出。
它被广泛应用于天然产物的合成和药物化学领域。
该反应通过产生Barton自由基,将羧酸或酮酸分子转化为相应的烯烃,从而实现脱羧的目的。
1. 反应机理Barton自由基脱羧反应是一种光化学反应,主要依赖于紫外线或可见光的照射。
反应的关键步骤是通过紫外线激发羧酸分子中的一个电子,使其跃迁至高能级的激发态。
在激发态下,羧酸分子会经历一个内部过程,形成一个稳定的Barton自由基。
这个自由基能够与其他分子发生反应,最常见的是与另一个羧酸分子发生偶联反应,形成烯烃并释放二氧化碳。
2. 反应条件Barton自由基脱羧反应的反应条件相对温和,主要包括适当的溶剂、光源和温度。
常用的溶剂有二氯甲烷、四氢呋喃等,它们既能溶解反应物,又能够吸收紫外线或可见光。
光源通常选择可见光或紫外线灯,以提供所需的激发能量。
反应温度一般在室温至低温范围内进行。
3. 反应应用Barton自由基脱羧反应在有机合成中具有广泛的应用价值。
通过该反应,可以高效地将羧酸转化为烯烃,从而合成复杂的有机分子。
此外,该反应还可以应用于天然产物合成领域,用于合成天然产物的结构类似物或类似骨架的化合物。
例如,通过Barton自由基脱羧反应,可以合成香豆素类天然产物的合成前体。
4. 反应优势Barton自由基脱羧反应相对于传统的脱羧反应具有一些优势。
首先,该反应条件温和,不需要高温或强酸碱条件,从而避免了其他反应可能导致的副反应或分子结构破坏。
其次,该反应具有高效性和选择性,可以在较短的时间内高产率地完成脱羧反应。
此外,该反应的副产物仅为二氧化碳,无害环境,具有较好的环境友好性。
5. 反应的限制尽管Barton自由基脱羧反应具有诸多优势,但也存在一些限制。
首先,该反应对于某些羧酸的适应性较差,特别是含有其他官能团或取代基团的复杂羧酸。
目前位置:首页—>羧酸及其衍生物—>K
5羧酸的脱羧反应
羧酸的脱羧反应
教学目标:掌握脱羧反应和应用范围。
教学重点:β-羰基酸的脱羧反应、己二酸脱羧反应
教学安排:K
1—>K5;10min
羧酸盐在碱存在下受热,发生脱羧反应。
乙酸钠与碱石灰共熔,发生脱羧,生成甲烷和碳酸钠,这是实验室中制取少量甲烷的方法。
乙酸的钙盐或钡盐在强烈受热时,发生部分脱羧的反应生成丙酮,这个反应可用于综合利用含羧酸的废水:
当羧酸的C上连有强吸电子基时,加热可使它较顺利地脱羧。
如:
草酸是不稳定的二元羧酸,它受热时,脱去一分子CO
2生成甲酸,少量的CO2可由此法制得,丙二酸及取代丙二酸在受热时,容易发生脱羧,生成一元羧酸:
已二酸在高温下脱水环化,生成环戊酮酸,后者在受热下脱羧,生成环戊酮,已二酸的钡盐
在受热时脱去一分子CO
2生成环戊酮,都具有制备间意义。
关键词脱羧反应。