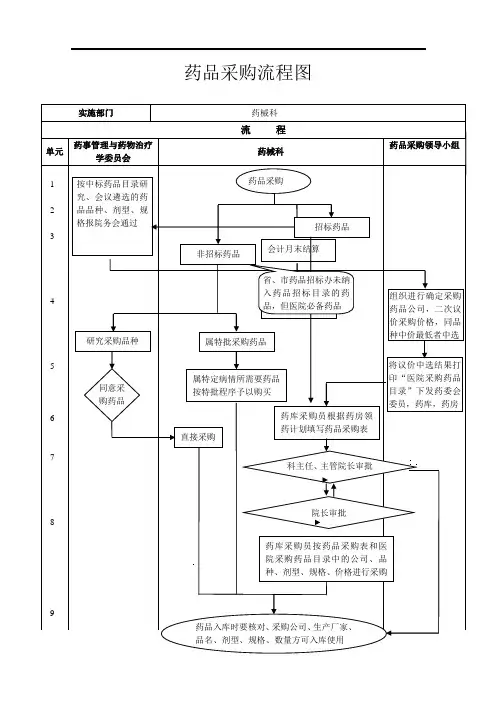
药品采购流程图
- 格式:doc
- 大小:28.00 KB
- 文档页数:1

医院药品采购流程图医院药品采购流程图医院药品采购流程图药库形成采购计划书药剂科审核采购计划书提交采购办公室审核、签字主管院长签字采购计划书提交采购领导小组研究、批准网上采购供应商最后凭采购计划书和发票与医院结算注:因突发疫情、事故或紧急抢救需临时采购的药品,可在采购领导小组的指示下,由采购办紧急调拨,调拨后2-5天内补齐计划书。
扩展阅读:药品进医院的流程图药品进医院的流程医院好比一座山,来到山前,首先要知道的是山的整体轮廓是什么?而医药销售人员面对的是一家医院,只有明确掌握医院的架构、人员的组成以及患者的组成,才能成功地销售医药产品。
一.医院的架构每一家医院的架构基本上是相似的。
首先是院长,在院长之下有党委书记,有很多的业务副院长,他们分管不同的事务,一般都有一个专门分管药品的副院长,一个管理临床的副院长等;每家医院都分许多科室,大概可以分为四大类,即:临床科室、医技科室、行政科室和后勤科室。
例如临床的科室有内科、外科、妇科等,还有行政的有医务科、财务科、科教科、档案管理处、医保办、医院办公室、护理部等,医技科有药剂科、检验科、放射科、器械科等;后勤科室有保卫处、膳食科、后勤部等。
临床的科室和药剂科对于做临床推广的医药销售人员来说很重要。
在临床科室里的外科还可以分普外科、心外科、胸外科、神经外科、泌尿外科、肝胆外科、烧伤科等;内科可以分心内科、内分泌科、呼吸内科、消化内科、肾内科、风湿免疫科、血液内科等等。
二.医院的人员组成医院的基本架构是由掌握不同专业知识的人员组成的,首先是院长,医药销售主管应该经常去拜访院长,接下来就是副院长、药剂师、医生、行政人员,另外还有**,**也可以提供很多医务处方信息。
三.患者的构成医药产品的最终购买者是患者,所以走进一家医院,首先要清楚该医院患者的组成情况,是专科还是综合?它有没有自费的患者,或者是医保的患者,各占多大比例?按就诊地点来分可以分为住院和门诊的患者;按患者来源来分可以分为外地和本地的患者。
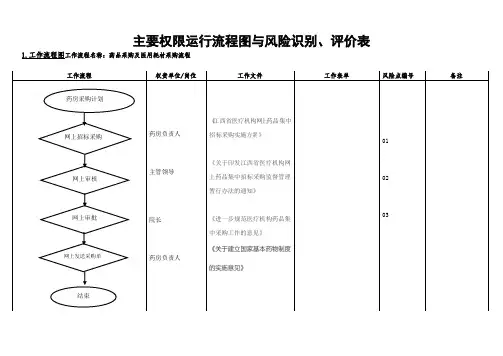
主要权限运行流程图与风险识别、评价表1.工作流程图工作流程名称:药品采购及医用耗材采购流程工作流程权责单位/岗位工作文件工作表单风险点编号 备注药房负责人 主管领导 院长药房负责人《江 西 省 医 疗 机 构 网 上 药 品 集 中招 标 采 购 实 施 方 案 》《关于印发江西省医疗机构网上药品集中招标采购监督管理暂行办法的通知》《进一步规范医疗机构药品集中采购工作的意见》 《关于建立国家基本药物制度的实施意见》01 02 03网上招标采购网上审核 药房采购计划结束网上审批 网上发送采购单2.一般性物品采购流程风险识别评价表编号风险点 原因分析现有控制措施建议措施防范措施1审核1、制度意识淡薄;2、制度执行不到位严格按照医院章程,进行实事求是的调查后审核。
采取多人分工协作,相互监督的工作机制采取多人分工协作,相互监督的工作机制。
审批 1、制度意识淡薄;2、制度执行不到位贯彻执行《江西省医疗机构药品集中采购实施方案》采取多人分工协作,相互监督的工作机制采取多人分工协作,相互监督的工作机制。
采购1、制度意识淡薄;2、道德水平低下、3外部环境恶劣采取多人分工协作,相互监督的工作机制加强自身修养,廉洁自律、分工协作,相互监督的工作机制贯彻执行 《 江 西 省 医 疗 机 构 网 上 药 品 集 中招 标 采 购 实 施 方 案 》;加强自身修养,廉洁自律。
科室意见 主管领导审核意见 风险防范小组审批意见签字: 日期:签字: 日期:签字: 日期:编号风险点 风险点描述(主要内容与表现形式)风险类型风险评价风险等级岗位风险 道德风险 制度风险流程风险外部风险发生可能性 (1-5)风险后果(1-5)高中低1 审核 因为审核材料过程中不细心、不严格,可能导致不符合条件的采购通过。
√ √2 5 √ 2 审批因为存在私心,审批签字时把关不严,可能导致不符合条件的采购,产生不良影响。
√ √ 3 3√ 3采购因为监督不严,道德水平低下,外部环境恶劣,可能导致采购的药品不符合要求、贪污受贿。
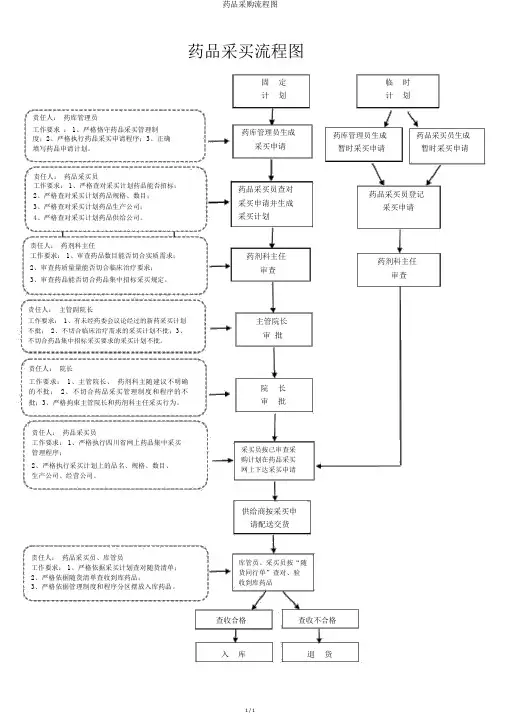
药品采购流程图1 / 1药品采买流程图责任人: 药库管理员工作要求 : 1、严格恪守药品采买管理制度;2、严格执行药品采买申请程序;3、正确填写药品申请计划。
责任人: 药品采买员 工作要求: 1、严格查对采买计划药品能否招标;2、严格查对采买计划药品规格、数目;3、严格查对采买计划药品生产公司;4、严格查对采买计划药品供给公司。
责任人: 药剂科主任工作要求: 1、审查药品数目能否切合实质需求; 2、审查药质量量能否切合临床治疗要求; 3、审查药品能否切合药品集中招标采买规定。
责任人: 主管副院长工作要求: 1、有未经药委会议论经过的新药采买计划不批; 2、不切合临床治疗需求的采买计划不批;3、不切合药品集中招标采买要求的采买计划不批。
责任人: 院长工作要求: 1、主管院长、 药剂科主随建议不明确的不批; 2、不切合药品采买管理制度和程序的不批;3、严格拘束主管院长和药剂科主任采买行为。
责任人: 药品采买员 工作要求: 1、严格执行四川省网上药品集中采买管理程序;2、严格执行采买计划上的品名、规格、数目、生产公司、经营公司。
固 定 计 划药库管理员生成采买申请药品采买员查对 采买申请并生成 采买计划药剂科主任审查主管院长 审 批院 长 审 批采买员按已审查采购计划在药品采买网上下达采买申请临 时 计 划药库管理员生成 药品采买员生成暂时采买申请 暂时采买申请药品采买员登记采买申请药剂科主任审查责任人: 药品采买员、库管员工作要求: 1、严格依据采买计划查对随货清单;2、严格依据随货清单查收到库药品;3、严格依据管理制度和程序分区摆放入库药品。
供给商按采买申 请配送交货库管员、采买员按“随 货同行单”查对、验 收到库药品查收合格 查收不合格入 库 退 货。

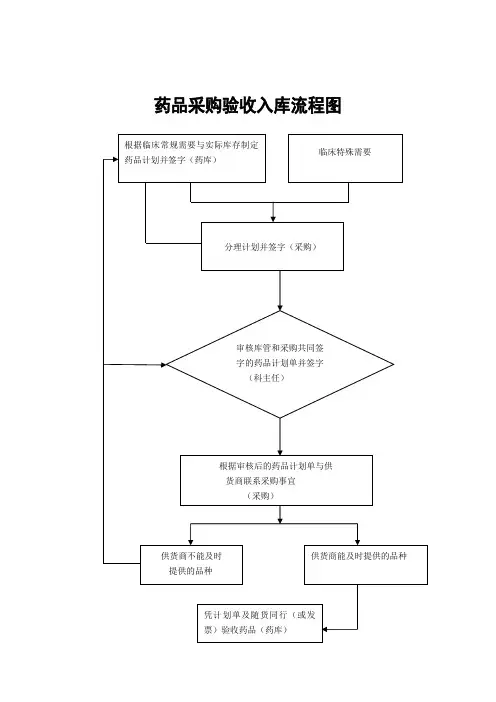
药品采购流程图药品采购流程图药品采购是医院、药店等医疗单位必不可少的一项工作,其流程图如下:1. 采购需求确认:- 医疗单位根据临床需要和库存情况,确定药品的采购需求。
- 确定药品的品种、规格、数量等。
2. 药品供应商选择:- 医疗单位根据药品的品质、价格、信誉等因素,选择合适的药品供应商。
- 可以通过招标、询价等方式选择药品供应商。
3. 询价和比较:- 医疗单位向选定的药品供应商发送询价函,要求其提供药品的报价和其他相关信息。
- 医疗单位根据不同供应商提供的药品报价和其他信息,进行比较和评估。
4. 采购合同签订:- 医疗单位根据选定的供应商,与其签订药品采购合同。
- 合同中应明确药品的品种、规格、数量、价格、支付方式、交货时间等内容。
5. 付款和交货:- 医疗单位按照合同约定的付款方式和时间,支付采购款项给供应商。
- 供应商按照合同约定的交货时间和地点,将药品送达给医疗单位。
6. 药品验收和入库:- 医疗单位对采购的药品进行验收,核实药品的品种、规格、数量等是否与合同一致。
- 验收合格后,将药品入库,并进行相应的记录和管理。
7. 药品库存管理:- 医疗单位对药品进行库存管理,包括定期盘点、跟踪库存数量和质量、及时补充库存等。
8. 供应商绩效评估:- 医疗单位定期评估供应商的绩效,包括药品质量、供货能力、服务态度等因素。
- 根据评估结果,决定是否继续与该供应商合作或者选择其他供应商。
以上是药品采购的基本流程图,不同的医疗单位可能会有一些细微的差别,具体流程还需根据实际情况进行调整。
药品采购是一项关系到医疗单位运行和患者安全的重要工作,需要高度重视和严格执行。
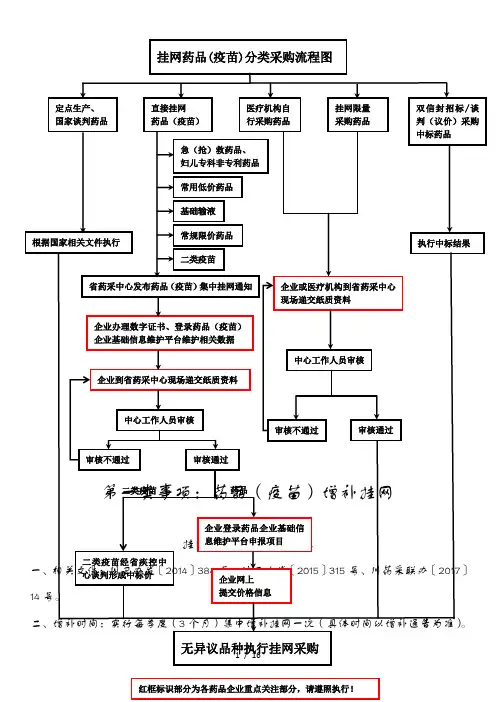
三、申报流程常用低价药品增补要求一、相关文件:川卫办发〔2014〕384号、川卫办发〔2015〕315号、川药械采〔2016〕33号。
二、增补时间:实行每季度(3个月)集中增补挂网一次(具体时间以增补通告为准)。
三、申报流程妇儿专科非专利药、急抢救药品增补要求一、相关文件:川药械采〔2015〕69号。
二、增补时间:随时增补。
三、申报流程挂网限量采购药品、医疗机构自行采购药品增补要求一、相关文件:川基药采〔2015〕91号二、增补时间:随时增补。
三、所需资料:1、产品封面(格式见川基药采〔2015〕91号附件1)。
2、产品说明书原件。
3、进口药品由集团内企业维护药品信息的,需提供声明书(格式见川基药采〔2015〕91号附件2);由集团外的一级代理商维护药品信息的,需提供进口药品生产厂对一级代理商的授权书。
4、挂网限量采购药品/医疗机构自行采购药品企业法人授权书(格式见川基药采〔2015〕91号附件3,如递交资料人员为四川省药品基础信息库的被授权人则无须递交)。
5、被授权人本人带身份证原件递交资料。
6、每页纸质资料均需盖申报企业鲜章。
第二类疫苗增补要求一、相关文件:川卫办发〔2016〕56号、川药械采〔2016〕50号、川药械采〔2016〕67号二、增补时间:具体时间以相关增补通告为准。
三、申报流程第二类事项:药品及生产企业信息变更企业申请撤销挂网资料要求1、药品企业撤销药品挂网授权委托书(在“四川药械采购与监管平台”的“下载中心”里下载固定格式)。
2、被授权人身份证复印在《药品企业撤销药品挂网授权委托书》背面,并加盖申请企业鲜章。
3、申请企业开具的关于撤销挂网的有编号的正式红头文件(内容要求:①写明收文单位全称:四川省药械集中采购服务中心。
②写明我公司接受不良记录一次。
③写明撤销品种(具体名称、规格)一年内不再参加四川省集中采购工作。
(属于限量采购药品、妇儿专科(非专利)药品、急抢救药品、自行采购药品无需提供第②、③点资料)4、国产药品生产企业:最新有效的生产许可证、GMP证书和拟撤网药品的药品生产批件的复印件(企业变更名称的需递交相关企业更名的《药品补充申请批件》),并提供相应的生产许可证、GMP证书、药品生产批件其中之一的原件核查,如果企业变更名称的需递交相关企业更名的《药品补充申请批件》原件。