有机化学清华大学李艳梅版课后习题答案
- 格式:docx
- 大小:1.51 MB
- 文档页数:68

第九章1.苯乙酮(1)(2) 2-(1-甲基)丙基苯甲醛(3)环己酮缩乙二醇(4)1,5,5-三甲基-2-氧代环己甲醛(5)1-苯基-2-甲基-3-羟基-1-丁酮(6)4-甲基-7-氧代-辛醛(7)5-乙基-6-庚烯醛(8)3-丁烯-2-酮(9)(E)-1,4-二苯基-2-丁烯-1,4-二酮苯基苯基甲酮肟(11)5-硝基-2-萘甲醛2.(1)CH=CHCHO (2)CH3OCH(CH3)2(10)对溴(12)1-环丙基-2-丙酮(3)OCH2CCH2CH3(4)OBrCCH2CHCH3(5)CH3CH3O (6)OCH3O(7)NCONH2CH3CH2CCH3(8)CH3CH=CHC=NNHC6H53.(1)乙醛丁醛环戊酮I2NaOH(-)(-)土伦试剂(+)黄色沉淀(+) 银镜反应(-)(2)CH 2CH 2CHO O CH 2CCH 3C 2H 5 CHO土伦试剂(-) (+) 银镜反应 (+) 银镜反应斐林试剂(+) 银镜反应(-)无变化(3)丙醛 丙酮 丙醇 异丙醇I 2 NaOH(-) (+) 黄色沉淀 (-) (+) 黄色沉淀土伦试剂(+) 银镜反应(-)白色固体丙酮饱和亚硫酸氢钠(-)异丙醇(4)戊醛 2-戊酮 环戊酮 (-) (+) 黄色沉淀I 2 NaOH(-)(+) 银镜反应 (-)斐林试剂饱和亚硫酸氢钠(+) 白色固体苯甲醛(-) (-) (-)4.(1)正丁醇>丁酮>乙醚>正戊烷OO H>OO CH 2CHO(2) (3)H> CH 3CHO >O CH 3CCH 3O CH 3CCH 3O CH 3CH 2CCH 3CHO >CHO >>(4)丙酮>丁酮>2-戊酮5.(CH 3)3CCOCH 3COCH 3CH 2CHCH 3 OH以上化合物能发生碘仿反应 6.O-CH 2CCH 2CH 3OCH 3CCH 2CH 3OH -O -CH 3CCH 2CH 3OH-优先进攻酸性强和立体位阻小的氢OHC CH 2CH 3 (I) OHC CH 2CH 3 (II) (I) 烯醇式结构更稳定OCH 2CCHCH 3 BrBr 2OBrCH 2CCH 2CH 3OCH 3CCH 2CH 3H ++ OHCH 3CCH 2CH 3CH 3Br 2CH 27.(1)CH 3CH=CH-CH 2CH 2CH(OCH 3)2 (3) OH C 6H 5COCHCN(4)NHOH CH 3CCH 2CH 3OH(5) CHO CHO(2)BrOCH 3(6)OMgBr Ph (8)OH OOPhPh (9) OH Ph(7)CH 3CH 2OHCH 3COOH(10)CH 2CH 3 OH O(11)OO CH3CH3(12)CH3BrO8.(1)BrOCCH3CH2OHCH2OHHClBrO OCH31) Mg, 无水乙醚2) CO23) H3O+OHOOOCH3H3O+HOO OCCH3CH3OHH2SO4 OCH3O OCCH3NaBH4CH3OO OHCHCH3(2)H2SO4, H2O C CHHgSO4OC CH3NaCNOHC CH3CNH3O+OHC CH3COOH (3)Br +CH3CH2CHO1) Mg, 无水乙醚2)H3O+OH48% HBrBr 1) Mg, 无水乙醚2)D2ODO(4)KMnO4H+OO1) NaOH2)(5)OCH3CH2CH2COClAlCl3Zn-HgHClBr(6)CH3CH2Br(7)HC CHNaNH2NH3H2SO4, H2O HgSO4OCH3CH2CH2CCH2CH2CH2CH3NaC CNaOBr2FeBr+PPh3Ph3P-CH2CH3Br-OPh C CH3CHCH3Ph C CH3CH3CH2CH2BrCH3CH2CH2 C C CH2CH2CH3(8)O3 Zn CHOCHO1) NaOH2)CHO9.(1)OCOOC2H5C2H5ONaOCOOC2H5-Na+CH2OCHCCH3COOC2H5C2H5OHMichael加成COOC2H5-H2OOCH3OC2H5ONa COOC2H5COOC2H5OH3C-O HOOO(2)OONaOH CH 3CCH 2CH 2CCH 3- OOCH 2CCH 2CH 2CCH 3O OH CH 3-H 2OO(3) CH 3HO CCH PhH + -H +CH 3H OH CCH Ph +重排CH 3HH C C OH + Ph重排CH 3H OH C C Ph H+-H + H +PhCOCH 2CH 310.CH 3 CH 3 (A)O CH 3CH 3+CH 3CHOOH CH 3CH 3 CH 3(B)O CH 3 CH 3 CH 3(C)CH 311.OCH 3 OCH 3 CH 3 (A)(B)CHO HClCH 3KMnO 4COOH COOH12.HO(I)HOCH 2CH 2CH 3 (III)O CH 2CCH 3HOOH CH 2CHCH 3 (II)CH 3OCH 2CH 2CH 3 (IV)13.CH3O (I)HOO(II)OCH314.(1)红外光谱,后者在1700 cm-1 附近有醛羰基的红外吸收峰。



有机化学课后习题参考答案
一、选择题
1. 答案:B
解析:选择题的题目解析。
2. 答案:A
解析:选择题的题目解析。
二、填空题
1. 答案:催化剂
解析:填空题的题目解析。
2. 答案:氧化还原
解析:填空题的题目解析。
三、判断题
1. 答案:正确
解析:判断题的题目解析。
2. 答案:错误
解析:判断题的题目解析。
四、解答题
1. 答案:解答内容的答案。
解析:解答题的题目解析。
2. 答案:解答内容的答案。
解析:解答题的题目解析。
五、综合题
答案:综合题的答案。
解析:综合题的题目解析。
六、总结
本文提供了有机化学课后习题的参考答案,包括选择题、填空题、判断题、解答题和综合题等不同类型的题目。
通过学习这些题目的解析,可以帮助读者更好地理解有机化学的相关知识点,并提高解题能力。
希望这些参考答案能够对大家有所帮助。

有机化学第二版答案李艳梅【篇一:有机化学教案】txt>2014 至 2015 学年第二学期________有机化学________课程教案课程编码:_______________________________________总学时/周学时:48 / 3开课时间:年月日第周至第周授课年级、专业、班级:2014级烹饪营养与教育专业推荐教材:有机化学系别/教研室:________________/____________________授课教师:曾习本次课教学组织与设计教学内容及时间分配:第一章绪论(一) 有机化合物和有机化学 5min(二) 有机化合物的特性 5min(三) 有机化合物的分子结构和结构式 15min(四) 共价键 10min(五)有机化合物的分类 10min第二章饱和烃(烷烃)(一) 烷烃的通式和构造异构 5min(二) 烷烃的命名 20min(三) 烷烃的结构 5min(四) 烷烃的物理性质 5min(五) 烷烃的化学性质 20min(六) 烷烃的主要来源和制法 5min第三章(一) 脂环烃的分类 5min(二) 环烷烃的命名 5mim(三) 环烷烃烃的性质 5min(四) 环烷烃的结构与稳定性 10min(五) 环己烷及其衍生物的构象 5min教学互动设计:一、课堂提问:1.何谓有机化学?f.wohler有何贡献?2.与无机化合物相比较,有机化合物主要具有哪些特点?3.写出反-1,3-二甲基环己烷的优势构象。
二、课堂讨论:2.电负性:sp杂化碳 sp2杂化碳 sp3杂化碳 !5.用化学方法鉴别丙烷和环丙烷。
板书设计:一、常用的有化合物书写方法hhhh h hh-c-hhch3chch2oh3或(ch3)2chch2oh二、sp,sp2,sp3杂化 oh【篇二:有机合成工具书清单】当当价格 73.5作者:(德)施韦特利克等编著,万均等译基础有机化学(第三版)上册(新版)当当价格 37.9作者:邢其毅等著基础有机化学(第三版)下册(新版)当当价格 43作者:邢其毅等著出版社:高等教育出版社现代有机合成试剂:性质、制备和反应(第二卷)当当价格 66作者:胡跃飞主编出版社:化学工业出版社高等有机化学--反应、机理与结构当当价格 126作者:(美)史密斯,马奇编著,李艳梅译现代有机合成试剂(1)--氧化反应试剂当当价格 22.5作者:胡跃飞主编出版社:化学工业出版社现代有机合成试剂(2)--还原反应试剂当当价格 21作者:胡跃飞主编出版社:化学工业出版社现代有机合成试剂(3)--保护基和酸碱试剂当当价格 27作者:胡跃飞主编现代有机合成试剂(5)金属盐和有机金属试剂当当价格 27作者:胡跃飞主编出版社:化学工业出版社。



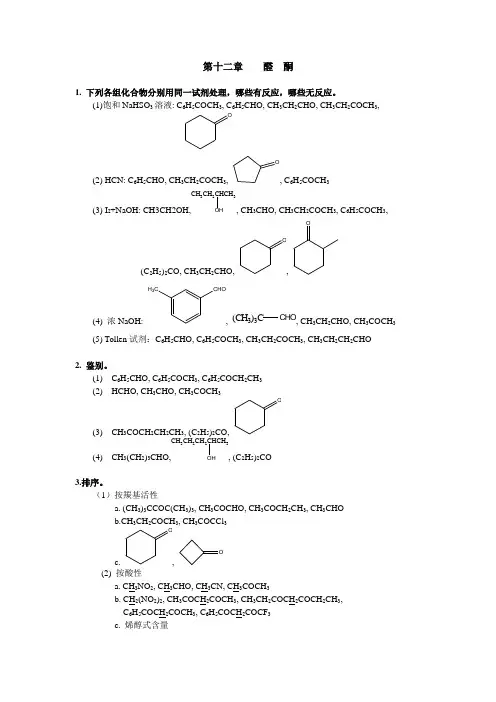
第十二章 醛 酮1. 下列各组化合物分别用同一试剂处理,哪些有反应,哪些无反应。
(1)饱和NaHSO 3溶液: C 6H 5COCH 3, C 6H 5CHO, CH 3CH 2CHO, CH 3CH 2COCH 3,O(2) HCN: C 6H 5CHO, CH 3CH 2COCH 3,O, C 6H 5COCH 3(3) I 2+NaOH: CH3CH2OH,CH 3CH 2CHCH 3OH, CH 3CHO, CH 3CH 2COCH 3, C 6H 5COCH 3,(C 2H 5)2CO, CH 3CH 2CHO,O, O(4) 浓NaOH:H 3CCHO, (CH 3)3C CHO , CH 3CH 2CHO, CH 3COCH 3(5) Tollen 试剂:C 6H 5CHO, C 6H 5COCH 3, CH 3CH 2COCH 3, CH 3CH 2CH 2CHO2. 鉴别。
(1) C 6H 5CHO, C 6H 5COCH 3, C 6H 5COCH 2CH 3 (2) HCHO, CH 3CHO, CH 3COCH 3(3) CH 3COCH 2CH 2CH 3, (C 2H 5)2CO,O(4) CH 3(CH 2)3CHO,CH 3CH 2CH 2CHCH 3OH , (C 2H 5)2CO3.排序。
(1)按羰基活性a. (CH 3)3CCOC(CH 3)3, CH 3COCHO, CH 3COCH 2CH 3, CH 3CHOb.CH 3CH 2COCH 3, CH 3COCCl 3c. O, O(2) 按酸性a. CH 3NO 2, CH 3CHO, CH 3CN, CH 3COCH 3b. CH 2(NO 2)2, CH 3COCH 2COCH 3, CH 3CH 2COCH 2COCH 2CH 3,C 6H 5COCH 2COCH 3, C 6H 5COCH 2COCF 3c. 烯醇式含量CH 3COCH 2COOC 2H 5, CH 3COCH 2CH 3,CH 3COCH 2COCH 3, CH(COCH 3)3,(CH 3CO)2CHCOOC 2H 54. 从指定原料合成。


习题答案第一章1.(1)有机化合物:含碳化合物(一氧化碳、二氧化碳、碳酸盐、金属碳化物等少数简单含碳化合物除外)或碳氢化合物及其衍生物的总称。
有机物是生命产生的物质基础。
(2)共价键:共价键(covalent bond)是化学键的一种,两个或多个原子共同使用它们的外层电子,在理想情况下达到电子饱和的状态,由此组成比较稳定的化学结构叫做共价键。
(3)同分异构:同分异构是一种有相同化学式,有同样的化学键而有不同的原子排列的化合物的现象。
(4)杂化:在形成多原子分子的过程中,中心原子的若干能量相近的原子轨道重新组合,形成一组新的轨道,这个过程叫做轨道的杂化。
(5)偶极矩:正、负电荷中心间的距离r 和电荷中心所带电量q 的乘积,叫做偶极矩μ=r×q。
它是一个矢量,方向规定为从负电荷中心指向正电荷中心。
(6)诱导效应:诱导效应是指在有机分子中引入一原子或基团后,使分子中成键电子云密度分布发生变化,从而使化学键发生极化的现象,称为诱导效应(Inductive Effects)。
(7)异裂:共价键断裂时,共用电子对完全转移给成键原子中的某个原子,形成了正、负离子,这种断键方式称为异裂。
(8)范德华力:在化学中通常指分子之间的作用力。
(9)键角:分子中和两个相邻化学键之间的夹角。
(10)Lewis 酸:路易斯酸(Lewis Acid,LA)是指电子接受体,可看作形成配位键的中心体。
(11)疏水作用:非极性分子间或分子的非极性基团间的吸引力。
导致这些基团在水性环境中的缔合。
(12)官能团:决定有机物性质的原子或原子团称为官能团。
2.(1)(2)(3)(4)(5)(6)(7)(8)(9)3.具有偶极的分子:(1)两 H 原子中心指向 O 原子方向;(2)又 H 原子指向 Br 原子;(4)H 原子指向三个 Cl 原子的中心方向;(5)乙基指向羟基方向4.(1)正庚烷;(2)异丁烷;(3)异己烷;(4)新戊烷5.(1)(3)6.(4)(2)酸:Cu2+ FeCl3 CH3CN碱:NH3 CH3NH2 C2H5OC2H5加合物:CH3COOH CH3OHH3O+/ H2O 7.(1)CH3COOH/CH3COO-(2)H2SO4/HSO4-(3)HNO3/NO3-8. (3) CH3Cl > (1) CH4CH3OH2+/CH3OH (CH3)3NH+/(CH3)3N(2) CH3F >(4)CH3Br >(5)CH3I > 9. 单键最长,双键次之,叁键最短.单键中两个原子间的电子云密度小,叁键两个原子间的电子云密度最大,共同的电子把两个原子吸引得最近.所以说,叁键最短,单键最长,双键处于中间.10. C5H12O11. C8H10N4O2第二章1. ⑶>⑵>⑴>⑸>⑷3. 2-甲基丁烷较稳定的构象是:CH3H⑴HCH3HCH3⑵HCH3CH3H⑶HCH3HCH3CH3CH3HCH3其中⑴和⑵更稳定。
目录•有机化学概述•碳原子结构与性质•官能团及其反应活性•立体异构现象与手性分子识别•有机合成策略与方法•绿色化学原理在有机合成中应用有机化学概述有机化学定义与发展历程定义研究有机化合物结构、性质、合成、反应机理及其应用的科学发展历程从早期对天然产物的提取和分离,到合成有机化合物的探索,再到现代有机化学的飞速发展有机化合物分类及特点分类按碳骨架分类(开链化合物、碳环化合物、杂环化合物等)、按官能团分类(烃类、醇类、醛类、酮类等)特点种类繁多、结构复杂、性质各异,具有广泛的应用价值有机化学在科研与工业中应用科研应用研究生命现象的本质、探索新药物和新材料、发展高效低毒的农药和化肥等工业应用合成纤维、塑料、橡胶等高分子材料,生产染料、香料、涂料等精细化学品,制备医药、农药等中间体。
碳原子结构与性质碳原子杂化类型及空间构型sp杂化碳原子形成两个σ键,呈直线型构型,如乙炔中的碳原子。
sp²杂化碳原子形成三个σ键,呈平面三角形构型,如乙烯中的碳原子。
sp³杂化碳原子形成四个σ键,呈四面体构型,如甲烷中的碳原子。
0102 03σ键由两个原子轨道沿键轴方向重叠而形成,具有方向性和饱和性。
π键由两个原子轨道垂直于键轴方向重叠而形成,具有方向性和不饱和性。
共价键的极性由成键原子的电负性差异决定,差异越大,极性越强。
共价键形成与性质分析03疏水作用非极性分子间的相互作用力,使非极性分子在水溶液中相互聚集。
01范德华力普遍存在于分子间的相互作用力,与分子的大小和极性有关。
02氢键存在于含有氢原子的分子间的一种特殊相互作用力,具有方向性和饱和性。
碳原子间相互作用力探讨官能团及其反应活性卤素原子(-X )具有亲电性,可发生亲核取代、消除等反应。
-NH2)具有亲核性和碱性,可参与亲核取代、缩合等反应。
羧基(-COOH )具有酸性,可发生酯化、酰卤化等反应。
羟基(-OH )具有亲核性,可参与亲核取代、消除等反应。
第一章绪论 (1)第二章饱和烃 (3)第三章不饱和烃 (7)第四章环烃 (14)第五章旋光异构 (22)第六章卤代烃 (27)第七章波谱分析 (33)第八章醇酚醚 (34)第九章醛、酮、醌 (41)第十章羧酸及其衍生物 (50)第十一章取代酸 (58)第十二种含氮化合物 (65)第十三章含硫和含磷有机化合物 (72)第十四章碳水化合物 (74)第十五章氨基酸、多肽与蛋白质 (78)第十六章类脂化合物 (82)第十七章杂环化合物 (88)第一章绪论1.1 扼要归纳典型的以离子键形成的化合物与以共价键形成的化合物的物理性质。
1.2是否相同?如将CH4 及CCl4各1mol混在一起,与CHCl3及CH3Cl各1mol的混合物是否相同?为什么?答案:NaCl与KBr各1mol与NaBr及KCl各1mol溶于水中所得溶液相同。
因为两者溶液中均为Na+ , K+ , Br-, Cl-离子各1mol。
由于CH4 与CCl4及CHCl3与CH3Cl在水中是以分子状态存在,所以是两组不同的混合物。
1.3 碳原子核外及氢原子核外各有几个电子?它们是怎样分布的?画出它们的轨道形状。
当四个氢原子与一个碳原子结合成甲烷(CH4)时,碳原子核外有几个电子是用来与氢成键的?画出它们的轨道形状及甲烷分子的形状。
答案:C+624HCCH 4中C 中有4个电子与氢成键为SP 3杂化轨道,正四面体结构CH 4SP 3杂化2p y2p z2p x2sH1.4 写出下列化合物的Lewis 电子式。
a. C 2H 4b. CH 3Clc. NH 3d. H 2Se. HNO 3f. HCHOg. H 3PO 4h. C 2H 6i. C 2H 2j. H 2SO 4答案:a.C C H H H HCC HH HH或 b.H C H H c.H N HHd.H S He.H O NO f.O C H Hg.O P O O H H Hh.H C C HHH H HO P O O H HH或i.H C C Hj.O S O HH OO H H或1.5 下列各化合物哪个有偶极矩?画出其方向。
习题答案第一章1. (1)有机化合物:含碳化合物(一氧化碳、二氧化碳、碳酸盐、金属碳化物等少数简单含碳化合物除外)或碳氢化合物及其衍生物的总称。
有机物是生命产生的物质基础。
(2)共价键:共价键(covalent bond )是化学键的一种,两个或多个原子共同使用它们的外层电子,在理想情况下达到电子饱和的状态,由此组成比较稳定的化学结构叫做共价键。
(3)同分异构:同分异构是一种有相同化学式,有同样的化学键而有不同的原子排列的化合物的现象。
(4)杂化:在形成多原子分子的过程中,中心原子的若干能量相近的原子轨道重新组合,形成一组新的轨道,这个过程叫做轨道的杂化。
(5)偶极矩:正、负电荷中心间的距离r 和电荷中心所带电量q的乘积,叫做偶极矩尸r的。
它是一个矢量,方向规定为从负电荷中心指向正电荷中心。
6)诱导效应:诱导效应是指在有机分子中引入一原子或基团后,使分子中成键电子云密度分布发生变化,从而使化学键发生极化的现象,称为诱导效应(Inductive Effects )。
(7)异裂:共价键断裂时,共用电子对完全转移给成键原子中的某个原子,形成了正、负离子,这种断键方式称为异裂。
(8)范德华力:在化学中通常指分子之间的作用力。
(9)键角:分子中和两个相邻化学键之间的夹角。
(10)Lewis 酸:路易斯酸(Lewis Acid ,LA )是指电子接受体,可看作形成配位键的中心体。
(11)疏水作用:非极性分子间或分子的非极性基团间的吸引力。
导致这些基团在水性环境中的缔合。
(12)官能团:决定有机物性质的原子或原子团称为官能团。
2.(1)(2)(3)4)5)6)7)8)9)3.具有偶极的分子:(1)两H 原子中心指向O 原子方向;(2)又H 原子指向Br 原子;(4)H 原子指向三个Cl 原子的中心方向;(5)乙基指向羟基方向4.(1)正庚烷;(2)异丁烷;(3)异己烷;(4)新戊烷5.(1)(2)(3)(4)6.酸:Cu2+ FeCl3 CH3CN碱:NHCHNH2 GH5OCH5加合物:CH3COOH CH3OH7.(1)CH3COOH/C3HCOO- H3O+/H 2O(2)H2SO4/HSO4- CH3OH2+/CH3OH(3)HNO3/NO3- (CH3)3NH+/(CH 3)3N 8.(3) CH 3Cl > (2) CH 3F >(4)CH3Br > (5)CH3I > (1) CH 49. 单键最长, 双键次之, 叁键最短. 单键中两个原子间的电子云密度小, 叁键两个原子间的电子云密度最大, 共同的电子把两个原子吸引得最近.所以说,叁键最短, 单键最长, 双键处于中间.10.C 5H12O11.C 8H10N4O2第二章1. ⑶〉⑵,⑴^心⑷3. 2- 甲基丁烷较稳定的构象是:其中⑴和⑵更稳定。
7. ⑵乂心⑷皿8. ⑴7 , 7-二甲基三环[221.02,6]庚烷 ⑵ 三环 [3.3.1.1 3, 7]癸烷11. 该烷烃的分子式为 C 8H 18 。
由于只能生成一种一氯 产物,说明该烷烃中的 18 个氢原子是等性的,其结构 式为: 3)3C — C (CH 3) 3(CH 12. 2- 甲基-1- 溴丙烷的含量为 0.6% ,2-甲基-2- 溴丙 烷的含量为 CH 3 ⑶ CH 3CH3 HHCH 3H⑵H99.4% 。
第三章2. ⑶、⑷为共轭化合物;⑴、⑶、⑷有顺反异构。
3. ⑴E型⑵E型⑶Z型⑷E型4. ⑴熔点:顺-2- 丁烯〉反-2- 丁烯,因为顺式的偶极矩大;沸点:反式〉顺式,因为反式的对称性好,分子排列紧密。
⑵ 熔点:2- 丁炔〉1-丁炔,因为2- 丁炔对称性好,分子排列紧密。
沸点:2- 丁炔〉1- 丁炔,因为末端炔烃具有较低的沸点5.7. 生成的主要产物是4- 甲基-3- 溴环戊烯。
反应机理为自由基取代历程(略)。
10. ⑴ 第一步用顺丁烯二酸酐检验,有沉淀生成者为1,3-丁二烯;第二步用溴水检验,不褪色者为丁烷;第三步用酸性高锰酸钾溶液检验,褪色者为1- 丁烯;余者为甲基环丙烷。
⑵第一步用硝酸银的氨溶液或氯化亚铜的氨溶液检验,有沉淀者为1- 戊炔;第二步用溴水检验,不褪色者为环戊烷;第三步用酸性高锰酸钾溶液检验,褪色者为环戊烯。
余者为乙基环丙烷。
11. ⑴p- n共轭,c -p 共轭⑵p- n 共轭,c - n共轭⑶p- n共轭n - n 共轭,p- n 共轭,c -p 共轭13. ⑶〉⑴皿15•⑴后一个式子是错误的,原子排列顺序发生改变。
⑵ 后一个式子是错误的,它的未成对电子数目不对。
⑶正确。
⑷ 两个式子间不是单纯的电子转移,原子位置发生了改变2.B .甲基环丙烷C . 1—丁烯 E 、F 为顺式和反式2 —丁烯第四章1.⑴ ⑷ Br Cl Cl H 3 Br Cl ⑵ CCH HO CH 3 H 3 Br H 3 Cl ⑶ ⑹ Cl Br Br17. A .环丁烷 D . 2—甲基丙烯BrCH36.BrCl3.⑴对叔丁基甲苯⑶对乙烯基苯甲酸⑷2 , 4, 6-三硝基甲苯烷⑵2-硝基4⑸2-甲基-3-氯甲苯苯基丁⑼CH3(7)『〒CH(CH3)2CHCICH3COOHCOCH2CH2CH2CIC >A >D >BC >D > B >A13.四甲基苯的异构体有:H 3CPh CH 3H 3C CH 3AICI 39.⑴CH 2C0CIH 2⑵ 0CH 3OB > D > E >A >C10.⑴ ⑸ ⑵ ⑹⑶⑺⑷⑻及其对映体11.⑴ 3 6-二甲基-2硝基萘⑵9 , 10-二溴菲0HCH3CH3CH⑶/CH3CH3其中⑶的对称性最好,熔点最高。
14. A. CH 3CH3 CHCH3 B. HOOC COOH C. HOOC COOHN02反应式略。
C2H5CIAlCl3浓H2SO4HNO3H2SO4C12C12FeNaOHH+/H2O(CH3)2C=CH2 / H +■HNO3Fe H2SO416.⑴有⑵无⑶无⑷无⑸有⑹有CH2CH319.茚18. A为CH3茚满第五章1.(略)2. (1)正确。
(2)不正确。
S构型是人为规定的,(+)R、而、(-)是测定得到的,二者没有必然联系。
(3)不正确。
分子中没有对称面、对称轴与对称中心,也可以有旋光性如螺环化合物,有空间为阻的联苯类化合物、丙二烯型化合物等。
(4)不正确。
如2,3-二溴丁烷,含有2个不对称碳原子,只有一对对映异构体,一个内消旋体。
只有 3 个立体异构体。
(5)不正确。
如内消旋体,分子内有手性碳,但因其有对称面并不具有光学活性。
(6)不正确。
如内消旋体,分子内虽具有不对称碳原子,但无旋光性。
(7)正确。
3. +2.3.0 °4. (4)(7)不同,其他相同5.⑴(CH3)2CHCHCICH 2CH3NH2 H(4)0H H **(2) CH3CHBrCH XHCICHOHCH 3⑶H 2NCH 2CHBrCOOHH3C CI*Cl(5) &6.薄荷醇分子中有3手性碳原子,可能有8个异构体。
7. (1)(4)(6)有对称元素,没有手性。
(5)CH3;CH3H3C⑶ 1HHO XD aCH3 ⑸H CD a C OHCH38.四个构型异构体,分别是H3P CH3 ClBrf H3HCH3ClHCH3r HBrCH3HBrCH3C1CH3(2S,3R) (2R,3S) (2R,3R) (2S,3S)9.用R/S 标记下列化合物中不对称碳原子的构型。
(1) S (2) S (3) S (4) R (5) 2R,3R (6) 2S,3R (7) 1S,2R (8)(9) R (10)R10.(1)C6H5HdCH2CH3CH3(3)HOHHC1-CHClCH 2CH3HH\H C CBr(6)H3C C|COOH⑷ C(CH 3)3 HCl J. C H 2CH(CH 3)22R,3S (有旋光性)2S,3R 2R,3R (有旋光性)2S,3SC 6H 5HC H 3 C2R,3R (有旋光性)2S,3S (无旋2R,3S光性)内消旋体3R,6R (有旋光性)3S,6S3R,6S (无旋光性)内消旋体11. CH 2CH 3 1 ■I ■ CH 2CH 3 (1)BrH t …一CH 2CH 2CH 3■ 1 1 ■ HB J■ I I ■ CH 2CH 2CH 3R1S(2) 无对映异构体12.(1)⑶cq 2CH Br 1 cH 2BrS⑵R(有旋光性)C 2H 5H 3C F" H 十-HlH CH 3C 2H 5C 2H 5C 2H 5H 3C HH HB- « m -B '3« 'B B &H HH 3C H石H 5C(CH 3)3 CH 2CH(CH 3)2ClCH 3 H CH 3 ■ ■ ■ ] ■ IH CH 3 C H 3 CH 2CH 2CICIHC H 2CH 3 6H 513. (3)相同,其它为对映体。
14.( 1)( A ) BrCH=CBrCH(CHCH 2CH 3,CH 2=CHCH(CH 3)CH 2CH 3,(C ) CH 3COCH(CH 3)CH 2CH 3,CH 2=CClCH(CH 3)CH 2CH 3,(E) CH CCH(CH 3)CH 2CH(2)都是旋光体(3) 都具有相同构型 (4) 都不能预测15.(2)无,其它有。
16.(1)使用旋光性酸形成两个非对映体,然后进行分级结晶,得到结晶后,再用碱水解得到纯净的产物(如CH 20HHO HHOH-,— H OH CH 2OH Cp 2OH HHO HOH-.-HO^- CH 2OH CH 2OHCH 2OH HO H HOH 卜 HO中CH 2OH2R,4R(有旋光性)2S,4S2S,4R (无旋光性)内消旋体2S,4R (无旋光性)内消旋体⑺彳IJ Cl C|1R,2S (无旋光性)内消旋体(8) Cl :ClI1R,2R(有旋光性)1S,2SCl分子具有对称面,无旋光性(B)(D )酒石酸)(2) 使用旋光性碱形成两个非对映体,然后进行 分级结晶,得到结晶后,再用酸水解得到纯净的产物(如 生物碱类)。
(3) 先与丁二酸酐作用形成半酯,再与具有旋光 性的碱作用,形成非对映体,然后进行分级结晶,得到 结晶后,再用酸水解得到纯净的产物。
17. 略18.( A 2H 5CH(CH 3)CC 三 CH(B) C 2H 5CH(CH 3)CH 2CH 319. (A) CH 3CH=CHCH(C)C CCH 3 三(B) CH 3CHCHCH(CH)CH 2CH!CH第六早1. (略)2. (1)正戊基碘(2)正丁基溴 (3)正庚基溴 (4)间溴甲苯沸点相对较高。