高考化学试题解析
- 格式:ppt
- 大小:591.00 KB
- 文档页数:24
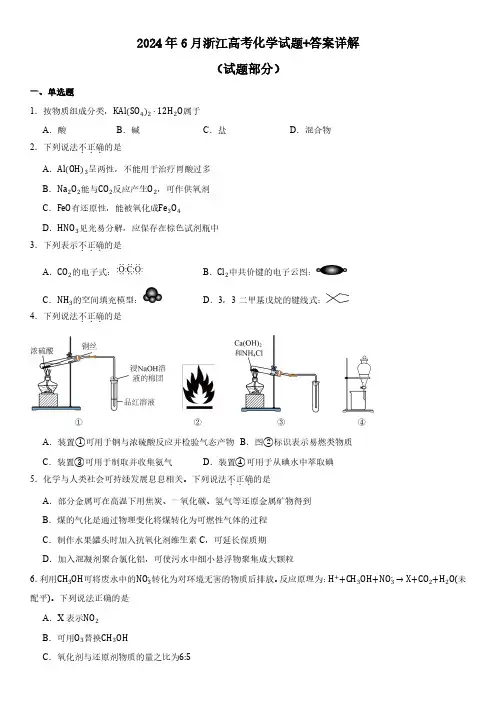
2024年6月浙江高考化学试题+答案详解(试题部分)一、单选题1.按物质组成分类,KAl(SO4)2⋅12H2O属于A.酸B.碱C.盐D.混合物2.下列说法不正确...的是A.Al(OH)3呈两性,不能用于治疗胃酸过多B.Na2O2能与CO2反应产生O2,可作供氧剂C.FeO有还原性,能被氧化成Fe3O4D.HNO3见光易分解,应保存在棕色试剂瓶中3.下列表示不正确...的是A.CO2的电子式:B.Cl2中共价键的电子云图:C.NH3的空间填充模型:D.3,3-二甲基戊烷的键线式:4.下列说法不正确...的是A.装置①可用于铜与浓硫酸反应并检验气态产物B.图②标识表示易燃类物质C.装置③可用于制取并收集氨气D.装置④可用于从碘水中萃取碘5.化学与人类社会可持续发展息息相关。
下列说法不正确...的是A.部分金属可在高温下用焦炭、一氧化碳、氢气等还原金属矿物得到B.煤的气化是通过物理变化将煤转化为可燃性气体的过程C.制作水果罐头时加入抗氧化剂维生素C,可延长保质期D.加入混凝剂聚合氯化铝,可使污水中细小悬浮物聚集成大颗粒6.利用CH3OH可将废水中的NO3-转化为对环境无害的物质后排放。
反应原理为:H++CH3OH+NO3-→X+CO2+H2O(未配平)。
下列说法正确的是A.X表示NO2B.可用O3替换CH3OHC.氧化剂与还原剂物质的量之比为6:5D .若生成标准状况下的CO 2气体11.2L ,则反应转移的电子数为2N A (N A 表示阿伏加德罗常数的值) 7.物质微观结构决定宏观性质,进而影响用途。
下列结构或性质不能解释....其用途的是 (A .AB .BC .CD .D8.下列离子方程式正确的是A .用CuSO 4溶液除H 2S 气体:Cu 2++S 2-=CuS ↓B .H 2SO 3溶液中滴加Ba (NO 3)2溶液:H 2SO 3+Ba 2+=BaSO 3↓+2H +C .NaHCO 3溶液中通入少量Cl 2:2HCO 3-+Cl 2=2CO 2+Cl -+ClO -+H 2OD .用FeCl 3溶液刻蚀覆铜板制作印刷电路板:2Fe 3++Cu =2Fe 2++Cu 2+9.有机物A 经元素分析仪测得只含碳、氢、氧3种元素,红外光谱显示A 分子中没有醚键,质谱和核磁共振氢谱示意图如下。

全国统一高考化学试卷(全国卷Ⅰ)一、选择题1.(3分)下列判断错误的是()A.熔点:Si3N4>NaCl>SiI4B.沸点:NH3>PH3>AsH3C.酸性:HClO4>H2SO4>H3PO4D.碱性:NaOH>Mg(OH)2>Al(OH)32.(3分)下列叙述正确的是()A.Li在氧气中燃烧主要生成Li2O2B.将CO2通入次氯酸钙溶液可生成次氯酸C.将SO2通入BaCl2溶液可生成BaSO3沉淀D.将NH3通入热的CuSO4溶液中能使Cu2+还原成Cu3.(3分)能正确表示下列反应的离子方程式是()A.将铁粉加入稀硫酸中2Fe+6H+═2Fe3++3H2↑B.将磁性氧化铁溶于盐酸Fe3O4+8H+═3Fe3++4H2OC.将氯化亚铁溶液和稀硝酸混合Fe2++4H++NO3﹣═Fe3++2H2O+NO↑D.将铜屑加Fe3+溶液中2Fe3++Cu═2Fe2++Cu2+4.(3分)下列叙述正确的是()A.某醋酸溶液的pH=a,将此溶液稀释1倍后,溶液的pH=b,则a>bB.在滴有酚酞溶液的氨水中,加入NH4Cl的溶液恰好无色,则此时溶液pH<7C.常温下,1.0×10﹣3mol/L盐酸的pH=3.0,1.0×10﹣8mol/L盐酸pH=8.0D.若1mLpH=1盐酸与100mLNaOH溶液混合后,溶液pH=7,则NaOH溶液的pH=115.(3分)如图是一种染料敏化太阳能电池的示意图。
电池的一个电极由有机光敏燃料(S)涂覆在TiO2纳米晶体表面制成,另一电极由导电玻璃镀铂构成,电池中发生的反应为:TiO2/s→TiO2/S﹡(激发态)TiO2/S﹡→TiO2/S++e﹣I3﹣+2e﹣→3I﹣2TiO2/S++3I﹣→2TiO2/S+I3﹣下列关于该电池叙述错误的是()A.电池工作时,是将太阳能转化为电能B.电池工作时,I﹣离子在镀铂导电玻璃电极上放电C.电池中镀铂导电玻璃为正极D.电池的电解质溶液中I﹣和I3﹣的浓度不会减少6.(3分)如图表示4﹣溴环己烯所发生的4个不同反应.其中,有机产物只含有一种官能团的反应是()A.①④B.③④C.②③D.①②7.(3分)一定条件下磷与干燥氯气反应,若0.25g磷消耗掉314mL氯气(标准状况),则产物中PCl3与PCl5的物质的量之比接近于()A.1:2B.2:3C.3:1D.5:38.(3分)下面关于SiO2晶体网状结构的叙述正确的是()A.存在四面体结构单元,O处于中心,Si处于4个顶角B.最小的环上,有3个Si原子和3个O原子C.最小的环上,Si和O原子数之比为1:2D.最小的环上,有6个Si原子和6个O原子二、非选题9.在溶液中,反应A+2B⇌C分别在三种不同实验条件下进行,它们的起始浓度均为c(A)=0.100mol/L、c(B)=0.200mol/L 及c(C)=0mol/L.反应物A的浓度随时间的变化如图所示.请回答下列问题:(1)与①比较,②和③分别仅改变一种反应条件.所改变的条件和判断的理由是:②;.③;.(2)实验②平衡时B的转化率为;实验③平衡时C的浓度为;(3)该反应的△H0,其判断理由是(4)该反应进行到4.0min时的平均反应速率:实验②:v B=实验③:v c=.10.有A、B、C、D、E和F六瓶无色溶液,它们是中学化学中常用的无机试剂.纯E为无色油状液体;B、C、D和F是盐溶液,且它们的阴离子均不同.现进行如下实验:①A有刺激性气味,用沾有浓盐酸的玻璃棒接近A时产生白色烟雾;②将A分别加入其它五种溶液中,只有D、F中有沉淀产生;继续加入过量A时,D中沉淀无变化,F中沉淀完全溶解;③将B分别加入C、D、E、F中,C、D、F中产生沉淀,E中有无色、无味气体逸出;④将C分别加入D、E、F中,均有沉淀生成,再加入稀HNO3,沉淀均不溶.根据上述实验信息,请回答下列问题:(1)能确定溶液是(写出溶液标号与相应溶质的化学式):(2)不能确定的溶液,写出其标号、溶质可能的化学式及进一步鉴别的方法:.11.请设计CO2在高温下与木炭反应生成CO的实验.(1)在下面方框中,A表示有长颈漏斗和锥形瓶组成的气体发生器,请在答题卡上的A后完成该反应的实验装置示意图(夹持装置,连接胶管及尾气处理不分不必画出,需要加热的仪器下方用△标出),按气流方向在每件仪器下方标出字母B、C…;其他可选用的仪器(数量不限)简易表示如下:(2)根据方框中的装置图,在答题卡上填写该表仪器符号仪器中所加物质作用A石灰石、稀盐酸石灰石与盐酸生成CO2(3)有人对气体发生器作如下改进:在锥形瓶中放入一小试管,将长颈漏斗下端插入小试管中.改进后的优点是;(4)验证CO的方法是.12.有机化合物A~H的转换关系如下所示:请回答下列问题:(1)链烃A有支链且只有一个官能团,其相对分子质量在65~75之间,1 mol A完全燃烧消耗7mol氧气,则A的结构简式是,名称是;(2)在特定催化剂作用下,A与等物质的量的H2反应生成E.由E转化为F的化学方程式是;(3)G与金属钠反应能放出气体.由G转化为H的化学方程式是;(4)①的反应类型是;③的反应类型是;(5)链烃B是A的同分异构体,分子中的所有碳原子共平面,其催化氢化产物为正戊烷,写出B所有可能的结构简式;(6)C也是A的一种同分异构体,它的一氯代物只有一种(不考虑立体异构).则C的结构简式为.全国统一高考化学试卷(全国卷Ⅰ)参考答案与试题解析一、选择题1.(3分)下列判断错误的是()A.熔点:Si3N4>NaCl>SiI4B.沸点:NH3>PH3>AsH3C.酸性:HClO4>H2SO4>H3PO4D.碱性:NaOH>Mg(OH)2>Al(OH)3【考点】75:金属在元素周期表中的位置及其性质递变的规律;76:非金属在元素周期表中的位置及其性质递变的规律;77:元素周期律的作用;9H:晶体熔沸点的比较.【专题】51C:元素周期律与元素周期表专题;51D:化学键与晶体结构.【分析】A、从晶体的类型比较;B、从是否含有氢键的角度比较;C、从非金属性强弱的角度比较;D、从金属性强弱的角度比较;【解答】解:A、Si3N4为原子晶体,NaCl为离子晶体,SiI4为分子晶体,一般来说,不同晶体的熔点高低按照原子晶体>离子晶体>分子晶体的顺序,故有Si3N4>NaCl>SiI4,故A 正确;B、NH3含有氢键,沸点最高,PH3和AsH3不含氢键,沸点的高点取决于二者的相对分子质量大小,相对分子质量越大,沸点越高,应为AsH3>PH3,故顺序为NH3>AsH3>PH3,故B错误;C、元素的非金属性越强,其对应的最高价氧化物的水化物的酸性就越强,由于非金属性Cl>S>P,所以最高价氧化物的水化物的酸性的强弱顺序为:HClO4>H2SO4>H3PO4,故C 正确;D、元素的金属性越强,其对应的最高价氧化物的水化物的碱性就越强,由于金属性Na>Mg>Al,所以最高价氧化物的水化物的碱性的强弱顺序为:NaOH>Mg(OH)2>Al(OH),故D正确。

2024年普通高中学业水平选择性考试(贵州卷)化学本卷满分100分,考试时间75分钟。
可能用到的相对原子质量:H 1C 12O 16Na 23Si 28Cl 35.5W 184一、选择题:本题共14小题,每小题3分,共42分。
在每小题给出的四个选项中,只有一项符合题目要求。
1.历史文物见证了中华民族共同体在发展中的交往交流交融。
下列贵州出土的文物中主要由天然高分子材料制成的是A .青陶罐B .带盖铜托杯C .鹭鸟纹蜡染百褶裙D .九凤三龙嵌宝石金冠A.AB.BC.CD.D2.下列叙述正确的是A.KBr 的电子式:[]K :Br -+ B.聚乙炔的结构简式:C.23SO -的空间结构:平面三角形D.()3232CH CH C CH CH =的名称:2-甲基-2-丁烯3.厨房中处处有化学。
下列说法错误的是选生活情境涉及化学知识项A 清洗餐具时用洗洁精去除油污洗洁精中的表面活性剂可使油污水解为水溶性物质B炒菜时不宜将油加热至冒烟油脂在高温下容易生成对身体有害的稠环化合物C长期暴露在空气中的食盐变成了糊状食盐中常含有容易潮解的2MgCl D 久煮的鸡蛋蛋黄表面常呈灰绿色蛋白中硫元素与蛋黄中铁元素生成的FeS 和蛋黄混合呈灰绿色A.AB.BC.CD.D4.贵州盛产灵芝等中药材。
灵芝酸B 是灵芝的主要活性成分之一,其结构简式如图。
下列说法错误的是A.分子中只有4种官能团B.分子中仅含3个手性碳原子C.分子中碳原子的杂化轨道类型是2sp 和3spD.该物质可发生酯化反应、加成反应和氧化反应5.下列装置不能达到实验目的的是A.图①可用于实验室制3NHB.图②可用于除去22C H 中少量的2H SC.图③可用于分离22CH Cl 和4CCl D.图④可用于制备明矾晶体6.二氧化氯()2ClO 可用于自来水消毒。
实验室用草酸()224H C O 和3KClO 制取2ClO 的反应为22432422242H C O 2KClO H SO 2ClO 2CO K SO 2H O =++↑+↑++。

2024年全省普通高中学业水平等级考试化学注意事项:1.答卷前,考生务必将自己的姓名、考生号等填写在答题卡和试卷指定位置。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑。
如需改动,用橡皮擦干净后,再选涂其他答案标号。
回答非选择题时,将答案写在答题卡上。
写在本试卷上无效。
3.考试结束后,将本试卷和答题卡并交回。
可能用到的相对原子质量:H 1 C 12 O 16 S 32一、选择题:本题共10小题,每小题2分,共20分。
每小题只有一个选项符合题目要求。
1. 中国书画是世界艺术瑰宝,古人所用文房四宝制作过程中发生氧化还原反应是 A. 竹管、动物尾毫→湖笔 B. 松木→油烟→徽墨 C. 楮树皮→纸浆纤维→宣纸 D. 端石→端砚【答案】B 【解析】【详解】A .湖笔,以竹管为笔杆,以动物尾毫为笔头制成,不涉及氧化还原反应,A 不符合题意; B .松木中的C C 单质,存在元素化合价的变化,属于氧化还原反应,B 符合题意;C .宣纸,以楮树皮原料,得到纸浆纤维,从而制作宣纸,不涉及氧化还原反应,C 不符合题意;D .端砚以端石为原料经过采石、维料、制璞、雕刻、磨光、配盒等步骤制成,不涉及氧化还原反应,D 不符合题意; 故选B 。
2. 化学品在食品工业中也有重要应用,下列说法错误的是 A. 活性炭可用作食品脱色剂 B. 铁粉可用作食品脱氧剂 C. 谷氨酸钠可用作食品增味剂 D. 五氧化二磷可用作食品干燥剂 【答案】D 【解析】【详解】A .活性炭结构疏松多孔,具有吸附性,能够吸附一些食品中的色素,故A 正确; B .铁粉具有还原性,能与O 2反应,可延长食品的保质期,作食品脱氧剂,故B 正确;的为C.谷氨酸钠是味精的主要成分,能增加食物的鲜味,是一种常用的食品增味剂,故C正确;D.P2O5吸水后的产物有毒,不能用作食品干燥剂,故D错误;故选D。
3. 下列化学用语或图示正确的是A. 的系统命名:2-甲基苯酚B. 3O分子的球棍模型:C. 激发态H原子的轨道表示式:D. p-pπ键形成的轨道重叠示意图:【答案】A【解析】【详解】A.含有的官能团为羟基,甲基与羟基相邻,系统命名为:2-甲基苯酚,故A正确;B.臭氧中心O原子的价层电子对数为:622232−×+=,属于sp2杂化,有1个孤电子对,臭氧为V形分子,球棍模型为:,故B错误;C.K能层只有1个能级1s,不存在1p能级,故C错误;D.p-pπ键形成的轨道重叠示意图为:,故D错误;故选A。

江苏省2024年普通高中学业水平选择性考试化学限时75分钟 满分100分可能用到的相对原子质量:H —1 B —11 C —12 N —14 O —16 Cl —35.5 Cr —52 Fe —56 Ag —108 Nd —144一、单项选择题:共13题,每题3分,共39分。
每题只有一个选项最符合题意。
1. 我国探月工程取得重大进展。
月壤中含有Ca 、Fe 等元素的磷酸盐,下列元素位于元素周期表第二周期的是 A. O B. P C. Ca D. Fe【答案】A 【解析】【详解】A .O 元素位于元素周期表第二周期ⅥA ,A 符合题意; B .P 元素位于元素周期表第三周期ⅤA ,B 不符合题意; C .Ca 元素位于元素周期表第四周期ⅡA ,C 不符合题意; D .Fe 元素位于元素周期表第四周期Ⅷ族,D 不符合题意; 综上所述,本题选A 。
2. 反应2242PbS+4H O =PbSO O 可用于壁画修复。
下列说法正确的是 A. 2-S 的结构示意图为B. 22H O 中既含离子键又含共价键C. 24SO −中S 元素的化合价为6+ D.2H O 的空间构型为直线形【答案】C 【解析】【详解】A .2-S 核外有18个电子,其结构示意图为,A 错误;B .22H O 是共价化合物,其中只含共价键,B 错误;C .24SO −中O 元素化合价为-2,S 元素的化合价为+6,C 正确;D .2H O 中的O 的杂化类型为3sp ,O 有2个孤电子对,因此2H O 的空间构型为V 形,D 错误; 综上所述,本题选C 。
3. 实验室进行铁钉镀锌实验。
下列相关原理、装置及操作不正确的是 ABCD配制NaOH 溶液 铁钉除油污铁钉除锈铁钉镀锌A. AB. BC. CD. D【答案】A 【解析】【详解】A .配制一定物质的量浓度的溶液时,溶质要放在烧杯中溶解,不能直接放在容量瓶中溶解,A 不正确;B .油污的主要成分是油脂,油脂在碱性条件下可以发生水解反应生成可溶于水的甘油和高级脂肪酸盐,因此,铁钉放在NaOH 溶液中加热后可以除去其表面的油污,B 正确;C .铁锈的主要成分是232Fe O nH O ⋅,其可溶于盐酸,因此,将铁钉放在盐酸中可以除去其表面的铁锈,C 正确;D .该装置为电解池,铁钉与电源负极相连作阴极,锌片与电源的正极相连作阳极,电解质溶液为2ZnCl 溶液,因此,该装置为电镀装置,可以实现铁钉上镀锌,D 正确; 综上所述,本题选A 。

高考化学试题及解析答案一、选择题1. 下列关于化学反应速率的说法正确的是()A. 温度升高,反应速率一定加快B. 反应物浓度越大,反应速率一定加快C. 催化剂可以改变化学反应速率D. 反应物的接触面积越大,反应速率一定加快答案:C解析:催化剂可以改变化学反应速率,但不一定加快反应速率,也可能减慢反应速率。
温度升高、反应物浓度增大和接触面积增大通常都会加快反应速率,但并非绝对。
2. 某化学反应的平衡常数为K,当温度升高时,K值增大,该反应()A. 吸热反应B. 放热反应C. 不是吸热反应就是放热反应D. 无法判断答案:A解析:平衡常数K与反应的热效应有关。
当温度升高,平衡常数K增大,说明正反应是吸热反应。
二、填空题3. 将1.0mol/L的HCl溶液与1.0mol/L的NaOH溶液等体积混合,混合后溶液的pH值为______。
答案:7解析:HCl与NaOH等体积等浓度混合,反应生成NaCl和水,溶液呈中性,pH值为7。
4. 根据元素周期表,第三周期的元素中,最外层电子数为4的元素是______。
答案:Si解析:第三周期的元素中,最外层电子数为4的元素是硅(Si),其原子序数为14。
三、计算题5. 某化学反应的热化学方程式为:2A(g) + B(g) → 3C(g) + 4D(g),ΔH = -1200 kJ/mol。
若反应中消耗2mol A,求生成C的物质的量。
答案:3mol解析:根据热化学方程式,2mol A参与反应,生成3mol C。
因此,消耗2mol A后,生成C的物质的量为3mol。
四、实验题6. 在实验室中,为了验证氯气和水的反应,可以采用以下实验步骤:(1)将氯气通入水中;(2)观察溶液颜色变化;(3)向溶液中加入______,观察是否有白色沉淀生成。
答案:硝酸银溶液解析:氯气和水反应生成盐酸和次氯酸,加入硝酸银溶液后,盐酸中的氯离子会与银离子反应生成白色沉淀的氯化银,从而验证氯气和水的反应。

高考化学试题及答案解析一、选择题(每题3分,共30分)1. 下列物质中,属于纯净物的是()。
A. 空气B. 矿泉水C. 蒸馏水D. 石油答案:C解析:纯净物是指由单一物质组成的物质,蒸馏水是由水分子组成的纯净物,而空气、矿泉水和石油都是混合物。
2. 化学反应中,能量变化的主要形式是()。
A. 光能B. 热能C. 电能D. 机械能答案:B解析:化学反应中,能量变化的主要形式是热能,因为反应过程中通常伴随着热量的释放或吸收。
3. 下列物质中,属于电解质的是()。
A. 酒精B. 蔗糖C. 硫酸D. 醋酸答案:C解析:电解质是指在水溶液中或熔融状态下能够导电的化合物,硫酸是一种强酸,属于电解质。
4. 元素周期表中,第ⅢA族元素的价电子数是()。
A. 1B. 2C. 3D. 4答案:C解析:元素周期表中,第ⅢA族元素的最外层电子数为3,因此价电子数为3。
5. 下列反应中,属于氧化还原反应的是()。
A. 2H2O → 2H2 + O2B. NaCl + AgNO3 → AgCl + NaNO3C. 2H2 + O2 → 2H2OD. 2H2O2 → 2H2O + O2答案:C解析:氧化还原反应是指在化学反应中,元素的氧化态发生变化的反应。
选项C中,氢气与氧气反应生成水,氢元素的氧化态从0变为+1,氧元素的氧化态从0变为-2,因此属于氧化还原反应。
6. 根据勒夏特列原理,下列操作中,可以使平衡向正反应方向移动的是()。
A. 增加反应物浓度B. 减少生成物浓度C. 增加生成物浓度D. 减少反应物浓度答案:A解析:勒夏特列原理指出,如果改变影响平衡的一个条件,平衡会向减弱这种改变的方向移动。
增加反应物浓度会使得平衡向正反应方向移动。
7. 下列化合物中,属于共价化合物的是()。
A. NaClB. H2OC. NaOHD. MgO答案:B解析:共价化合物是由共用电子对形成的化合物。
水分子中,氢原子与氧原子之间通过共用电子对形成共价键,因此属于共价化合物。

2024年吉林省普通高等学校招生选择性考试化学本试卷共8页。
考试结束后,将本试卷和答题卡一并交回。
注意事项:1.答题前,考生先将自己的姓名准考证号码填写清楚,将条形码准确粘贴在考生信息条形码粘贴区。
2.选择题必须使用2B铅笔填涂;非选择题必须使用0.5毫米黑色字迹的签字笔书写,字体工整、笔迹清楚。
3.请按照题号顺序在答题卡各题目的答题区域内作答,超出答题区域书写的答案无效;在草稿纸、试卷上答题无效。
4.作图可先使用铅笔画出,确定后必须用黑色字迹的签字笔描黑。
5.保持卡面清洁,不要折叠,不要弄破、异皱,不准使用涂改液、修正带、刮纸刀。
.可能用到的相对原子质量:H 1 C 12 O 16 S 32 Cl 355 Ti 48 Cu 64一、选择题:本题共15小题,每小题3分,共45分。
在每小题给出的四个选项中,只有一项符合题目要求。
1.文物见证历史,化学创造文明。
东北三省出土的下列文物据其主要成分不能与其他三项归为一类的是A.金代六曲葵花鎏金银盏B.北燕鸭形玻璃注C.汉代白玉耳杯D.新石器时代彩绘几何纹双腹陶罐【答案】A【解析】【详解】A.金代六曲葵花鎏金银盏是合金,属于无机金属材料;B.北燕鸭形玻璃注是玻璃制品,属于硅酸盐材料;C.汉代白玉耳环是玉,属于含有微量元素的钙镁硅酸盐材料;D.新石器时代彩绘几何纹双腹陶罐是陶器,属于硅酸盐材料;综上A选项材质与其他三项材质不用,不能归为一类,答案选A。
2.下列化学用语或表述正确的是SiO的晶体类型:分子晶体A.中子数为1的氦核素:12HeB.2PCl的空间结构:平面三角形C.2F的共价键类型:p-p σ键D.3【答案】C【解析】【详解】A .中子数为1的He 核素其质量数为1+2=3,故其表示应为32He ,A 错误;B .SiO 2晶体中只含有共价键,为共价晶体,B 错误;C .两个F 原子的2p 轨道单电子相互重叠形成p-p σ键,C 正确;D .PCl 3的中心原子存在1对孤电子对,其VSEPR 模型为四面体型,PCl 3的空间结构为三角锥型,D 错误;故答案选C 。

2023年高考全国新高考I卷化学试题及答案解析选择题第一部分(共10分)1. 答案A2. 答案B3. 答案C4. 答案D5. 答案A第二部分(共30分)21. 答案B22. 答案A23. 答案D24. 答案C25. 答案D26. 答案C27. 答案A28. 答案B29. 答案A30. 答案D第三部分(共35分)31. 答案B32. 答案C33. 答案A34. 答案D35. 答案B36. 答案A37. 答案C38. 答案D39. 答案B40. 答案C第四部分(共25分)41. 答案C42. 答案D43. 答案A44. 答案B45. 答案A46. 答案D47. 答案C48. 答案B49. 答案C50. 答案B非选择题第五部分(共20分)一、填空题51. 答案:氢气52. 答案:353. 答案:1054. 答案:无色二、简答题55. 答案:煤的生成过程中会释放大量的甲烷,因此煤矿工人在采煤时一定要注意通风和排放甲烷等有害气体,以免引起矿井事故。
56. 答案:阴离子交换树脂是一种具有特殊化学结构的高分子化合物,可以通过其空腔内正离子与周围环境中的阴离子发生交换反应,在水质处理、制备高纯度的化合物、以及分离和净化生物化学物质等方面发挥重要作用。
三、应用题57. 答案略。
自主思考题58. 答案略。
总结本次考试难度适中,综合涉及了化学的各个知识领域。
希望同学们认真复习备考,取得好成绩!。

高考化学试题及答案解析一、选择题1. 下列物质中,属于纯净物的是:A. 空气B. 矿泉水C. 蒸馏水D. 碳酸钙答案:C解析:纯净物是指由单一物质组成的物质。
空气是多种气体的混合物,矿泉水含有多种矿物质,碳酸钙虽然是化合物,但通常含有杂质,而蒸馏水是经过蒸馏过程去除杂质的水,只含有水分子,因此是纯净物。
2. 根据题目所给的化学方程式:Fe + CuSO4 → FeSO4 + Cu,下列说法正确的是:A. 铁是还原剂B. 铜是氧化剂C. 硫酸根离子在反应前后不变D. 反应中没有电子转移答案:A解析:在这个置换反应中,铁原子失去了电子,被氧化成了Fe2+,因此铁是还原剂。
硫酸根离子在反应前后保持不变,而铜离子Cu2+得到了电子,被还原成了Cu,但铜本身不是氧化剂。
反应中存在电子的转移。
二、填空题1. 请写出水的化学式,并简述水的分子结构。
答案:H2O;水分子由两个氢原子和一个氧原子组成,氧原子与氢原子之间形成共价键,分子呈V形结构。
2. 什么是摩尔质量?请给出水的摩尔质量数值。
答案:摩尔质量是物质中一个摩尔的质量,单位为克/摩尔。
水的摩尔质量是18克/摩尔。
三、计算题1. 某工厂排放的废水中,含有0.05摩尔/升的硫酸根离子(SO4^2-),若要中和这些硫酸根离子,需要加入多少摩尔/升的氢氧化钠(NaOH)?答案:0.1摩尔/升解析:硫酸根离子SO4^2-与氢氧化钠NaOH反应的化学方程式为:SO4^2- + 2NaOH → Na2SO4 + 2H2O根据化学方程式,1摩尔硫酸根离子需要2摩尔氢氧化钠来中和。
因此,0.05摩尔/升的硫酸根离子需要0.05 * 2 = 0.1摩尔/升的氢氧化钠。
四、实验题1. 描述如何通过实验确定一个未知溶液是否含有氯离子。
答案:可以通过硝酸银溶液滴定法来确定未知溶液是否含有氯离子。
首先取少量未知溶液于试管中,然后逐滴加入硝酸银溶液。
如果溶液中存在氯离子,会与硝酸银反应生成白色沉淀的氯化银(AgCl),这表明未知溶液中含有氯离子。

2023年全国统一高考化学试卷(乙卷)参考答案与试题解析一、选择题:本题共7小题,每小题6分,共42分。
在每小题给出的四个选项中,只有一项是符合题目要求的。
1.(6分)(2023•乙卷)下列应用中涉及到氧化还原反应的是( )A.使用明矾对水进行净化B.雪天道路上撒盐融雪C.暖贴中的铁粉遇空气放热D.荧光指示牌被照发光【答案】C【解答】解:A.明矾作净水剂,与水解有关,没有元素的化合价变化,不发生氧化还原反应,故A错误;B.雪天道路上撒盐融雪是利用溶解吸热,没有元素的化合价变化,不发生氧化还原反应,故B错误;C.暖贴中的铁粉遇空气放热是利用铁的氧化放热原理,即铁元素的化合价发生了变化,因而发生了氧化还原反应,故C正确;D.荧光指示牌被照发光中没有元素化合价的变化,即没有发生氧化还原反应,故D错误,故选:C。
2.(6分)(2023•乙卷)下列反应得到相同的产物,相关叙述错误的是( )①②A.①的反应类型为取代反应B.反应②是合成酯的方法之一C.产物分子中所有碳原子共平面D.产物的化学名称是乙酸异丙酯【答案】C【解答】解:A.反应①中羧基上的﹣OH被取代生成CH3COOCH(CH3)2,该反应类型是取代反应,故A正确;B.反应②是乙酸和丙烯发生加成反应生成CH3COOCH(CH3)2,生成物中含有酯基,所以反应②是合成酯的方法之一,故B正确;C.连接两个甲基的碳原子具有甲烷结构特点,甲烷分子中最多有3个原子共平面,﹣COO中所有原子共平面,单键可以旋转,该分子相当于2﹣丙醇中羟基上的氢原子被CH3CO﹣取代,则生成物中所有碳原子一定不共平面,故C错误;D.CH3COOCH(CH3)2的名称是乙酸异丙酯,故D正确;故选:C。
3.(6分)(2023•乙卷)下列装置可以用于相应实验的是( )A.制备CO2B.分离乙醇和乙酸C.验证SO2酸性D.测量O2体积【答案】D【解答】解:A.碳酸钠加热不分解,不能制备二氧化碳,故A错误;B.乙醇与乙酸互溶,不分层,不能选图中分液漏斗分离,故B错误;C.二氧化硫与品红化合生成无色的物质,可知二氧化硫具有漂白性,与酸性无关,故C 错误;D.调节左右两侧的液面相平,排出水可的体积可折合为氧气的体积,图中装置可测量氧气的体积,故D正确;故选:D。
化学高考试题及答案详解一、选择题(每题3分,共30分)1. 下列物质中属于纯净物的是()。
A. 空气B. 矿泉水C. 蒸馏水D. 碳酸钙答案:C解析:纯净物是由单一物质组成的,空气和矿泉水都是混合物,含有多种物质。
蒸馏水是水的纯净形式,而碳酸钙虽然是一种化合物,但题目中未指明其纯度,因此不能确定是否为纯净物。
2. 物质的量浓度相同的NaOH溶液和HCl溶液混合后,溶液呈()。
A. 酸性B. 中性C. 碱性D. 不确定答案:B解析:当等物质的量浓度的NaOH溶液和HCl溶液混合时,两者会发生中和反应生成水和氯化钠,溶液最终呈中性。
3. 以下哪个反应是氧化还原反应()。
A. CO2 + H2O → H2CO3B. 2H2 + O2 → 2H2OC. NaCl → Na+ + Cl-D. CaCO3 → CaO + CO2答案:B解析:氧化还原反应是指在化学反应中,原子或离子的氧化态发生变化的反应。
选项B中的氢气和氧气反应生成水,氢和氧的氧化态发生了变化,因此是氧化还原反应。
二、填空题(每空2分,共20分)1. 写出下列物质的化学式:- 氢氧化钠:________- 硫酸铜:________- 硝酸银:________答案:NaOH、CuSO4、AgNO3解析:氢氧化钠的化学式为NaOH,硫酸铜的化学式为CuSO4,硝酸银的化学式为AgNO3。
2. 写出下列物质的电子式:- 氢气:________- 氮气:________- 氟气:________答案:H:H、N≡N、F:F解析:氢气分子中两个氢原子共享一对电子,氮气分子中两个氮原子之间有三对共用电子,氟气分子中两个氟原子之间没有共用电子。
三、计算题(共50分)1. 计算100g质量分数为10%的NaOH溶液中NaOH的质量。
(10分)答案:10g解析:根据质量分数的定义,NaOH的质量为100g × 10% = 10g。
2. 计算在标准状况下,22.4L氧气的物质的量。