2012年全国高中学生化学竞赛(安徽赛区)初赛试题(word版)
- 格式:doc
- 大小:1.08 MB
- 文档页数:8

年全国高中化学竞赛(安徽赛区)初赛试题H 1.008 元素周期表He4.003Li 6.941Be9.012B10.81C12.01N14.01O16.00F19.00Ne20.18Na 22.99Mg24.31Al26.98Si28.09P30.97S32.07Cl35.45Ar39.95K 39.10Ca40.08Sc44.96Ti47.88V50.94Cr52.00Mn54.94Fe55.85Co58.93Ni58.69Cu63.55Zn65.39Ga69.72Ge72.61As74.92Se78.96Br79.90Kr83.80Rb 85.47Sr87.62Y88.91Zr91.22Nb92.91Mo95.94Tc[98]Ru101.1Rh102.9Pd106.4Ag107.9Cd112.4In114.8Sn118.7Sb121.8Te127.6I126.9Xe131.3Cs 132.9Ba137.3La-LuHf178.5Ta180.9W183.8Re186.2Os190.2Ir192.2Pt195.1Au197.0Hg200.6Tl204.4Pb207.2Bi209.0Po[210]At[210]Rn[222]Fr [223]Ra[226]Ac-La......................一、本题包括25小题,每小题2分,共50分。
每小题有1个或2个选项符合题意。
若该题只有1个选项合题意,多选或错选均不得分。
若该题有2个选项合题意,选对1个得1分,选对2个得2分;选错1个,该题不得分。
⒈我国有些煤矿的坑道中具有丰富的可燃性气体。
目前已建成利用坑道气的发电厂,这样既充分利用了能源,又保证了煤矿的安全生产,坑道中的可燃性气体是A.H2B.COC.CH4D. CH4和CO的混合气体⒉A是烷烃,B是单烯烃,B分子中的碳原子数比A分子中多。
常温下1L该混合气体充分燃烧可得到同温同压下的二氧化碳气体2.5L,则原混合气体中A和B的组合方式可能有A.2和B.3和C.4和D.5和⒊某种混合气体,可能含有N2、HCl、CO。

第-26-届中国化学奥林匹克(初赛)试题及答案中国化学会第26 届全国高中学生化学竞赛(省级赛区)试卷(2012 年9 月2 日9:00~12:00)题号 1 2 3 4 5 6 7 8 9 10 11 总分满分7 7 10 5 8 7 10 16 12 6 12 100 得分评卷人签名·竞赛时间3 小时。
迟到超过半小时者不能进考场。
开始考试后1 小时内不得离场。
时间到,将试卷背面朝上放于桌面,立即起立离开考场。
·姓名、报名号和所属学校等必须写于首页左侧指定位置,写于其他位置者按废卷论处。
·所有解答必须写于卷面指定位置,写于其他位置者无效。
·凡要求计算的,须给出计算过程,无计算过程即使结果正确也不得分。
·用铅笔解答的部分(包括作图)无效。
·禁用涂改液和修正带。
否则,整个答卷无效。
·试卷已装订成册,不得拆散。
·附草稿纸一张,不得将任何纸张带入考场。
·允许使用非编程计算器以及直尺等文具。
·写有与试题内容无关的任何文字的答卷无效。
H 1.008 元素周期表He4.003Li Be B C N O F Ne 6.941 9.012 10.81 12.01 14.01 16.00 19.00 20.18 Na Mg Al Si P S Cl Ar 22.99 24.31 26.98 28.09 30.97 32.07 35.45 39.95 K Ca Sc Ti V Cr Mn Fe Co Ni Cu Zn Ga Ge As Se Br Kr 39.10 40.08 44.96 47.87 50.94 52.00 54.94 55.85 58.93 58.69 63.55 65.38 69.72 72.64 74.92 78.96 79.90 83.80 Rb Sr Y Zr Nb Mo TcRu Rh Pd Ag Cd In Sn Sb Te I Xe 85.47 87.62 88.91 91.22 92.91 95.96 [98]101.07 102.91 106.42 107.87 112.41 114.82 118.71 121.76 127.60 126.90 131.29 Cs Ba La Hf Ta W Re Os Ir Pt Au Hg Tl Pb Bi Po At Rn 132.91 137.33 138.91 178.49 180.95 183.84 186.21 190.23 192.22 195.08 196.97 200.59 204.38 207.2 (209) (210) (222) 208.98Fr Ra Ac Rf Db(223) 226.0 (227) (261) (262)Ce Pr Nd Pm Sm Eu Gd Tb Dy Ho Er Tm Yb Lu140.12 140.91 144.24 (145)150.36 151.96 157.25 158.93 162.50 164.93 167.26 168.93 173.05 174.97 Th Pa U Np Pu Am Cm Bk Cf Es Fm Md No Lr 232.04 231.04 238.03 237.05 (244) (243) (247) (247) (251) (254) (257) (256) (254) (257)第1 题(7 分)1-1 向硫酸锌水溶液中滴加适当浓度的氨水至过量,发生两步主要反应。

2004年全国中学生化学竞赛(安徽赛区)初赛试题一、本题包括25小题,每小题2分,共50分。
每小题有1个或2个选项符合题意。
若该题只有1个选项符合题意,多选或错选均不得分。
若该题有2个选项符合题意,选对1个得1分,选对2个得2分;选错1个,该题不得分。
1.下列卤素互化物中,最不稳定的是(A)ClI3(B)ClF3(C)BrF3(D)ICl32.下列各结构式中,最有可能的N2OLewis结构式为(A)N=N=O —O (C)N—(D)N=O=N3.下列各金属碳化物中,与水反应能生成C3H4的是(A)Be2C (B)Na2C3(C)Mg2C3(D)A14C34.在一定温度下,某浓度的硝酸与金属锌反应,生成NO2和NO的物质的量之比为1:3 则要使1摩金属锌完全反应,需要HNO3的物质的量为(A)0.8 (B)2.4 (C)2.6 (D)2.85.在恒温条件下,有甲、乙两容器,甲容器为体积不变的密闭容器,乙容器为一个带有理想活塞(即无质量、无摩擦力的刚性活塞)的体积可变的密闭容器,两容器起始状态完全相同,都充有C气体,若发生可逆反应C(g) A(g)+B(g),经一段时间后,甲、乙两容器反应都达到平衡。
下列说法中正确的是(A)平均反应速度:乙>甲(B)平衡时nc(甲)>nc(乙)(C)平衡时C的转化率:乙>甲(D)平衡时A的物质的量甲>乙6.对手由CrO42—转化为Cr2O72—的下列各叙述中,正确的是(A)这是Lewis酸碱反应(B)这是氧化还原反应(C)加酸,该反应向右移动(D)加酸,该反应向左移动7.在水溶液中,KHSO3(aq)的电荷平衡式为(A)[H3O+]十[K+]=[OH—]+[HSO3—]+[SO32—](B) [H3O+]十[K+]=[OH—]+[HSO3—]+2[SO32—](C) [H3O+]十[K+]=[OH—]+[HSO3—]+1/2[SO32—](D) [H3O+]十2[K+]=[OH—]+[HSO3—]+2[SO32—]8.下列各组离子中,能在强碱性溶液中共存,且在滴加盐酸过程中会生成气体和沉淀的是(A)Na+、CrO2—、SO42—、CO32—(B)NH4+、A1O2—、SO42—、CO32—(C)K+、A1O2—、SO42—、HCO3—(D)K+、ZnO2—·、SO42—、CO32—9.已知Al和Ga是同族元素,且都是两性元素,并知A1(OH)3的碱性比Ga(OH)3大。
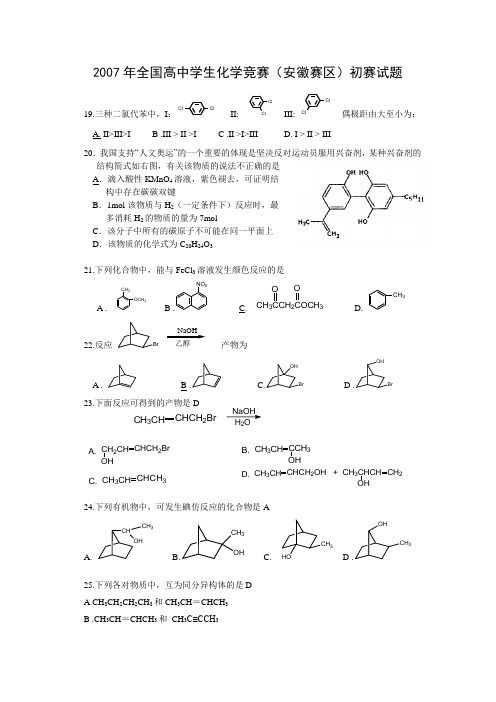
2007年全国高中学生化学竞赛(安徽赛区)初赛试题19.三种二氯代苯中,I :ClCl II:ClClIII:ClCl偶极距由大至小为:A. II>III>I B .III > II >I C .II >I>III D. I > II > III20.我国支持“人文奥运”的一个重要的体现是坚决反对运动员服用兴奋剂,某种兴奋剂的结构简式如右图,有关该物质的说法不正确的是 A .滴入酸性KMnO 4溶液,紫色褪去,可证明结 构中存在碳碳双键B .1mol 该物质与H 2(一定条件下)反应时,最 多消耗H 2的物质的量为7molC .该分子中所有的碳原子不可能在同一平面上D .该物质的化学式为C 20H 24O 321.下列化合物中,能与FeCl 3溶液发生颜色反应的是A . CH 3OCH 3B .NO 2C. CH 3CCH 2COCH 3 O OD.CH 322.反应 BrNaOH乙醇产物为A .B . C.BrOHD .BrOH23.下面反应可得到的产物是D24.下列有机物中,可发生碘仿反应的化合物是AA. CHOHCH 3 B.CH 3OHC.CH 3HOD .CH 3OH25.下列各对物质中,互为同分异构体的是D A.CH 3CH 2CH 2CH 3和CH 3CH =CHCH 3 B .CH 3CH =CHCH 3和 CH 3C≡CCH 3CH 3CH CHCH 2Br H 2ONaOHCH 2CH OHCHCH 2Br A.CH 3CH CCH 3B.OH CH 3CH CHCH 3C.CH 3CH CHCH 2OH +D. CH 3CHCH OHCH 2CH 3CH CHCH 3C.和 CH 3CH CCH 3CH 3CH 3CH 2CH 2OH 和CH 3CHCH 3D.OH32.(6分)请将反应中间产物填入框内CH 3COH + CH 3OHOH +AH +CH 3CH 2OHB+C33. (10分)请将反应中间产物填入框内,并将各产物用系统命名法命名CH 3CH CH 2Cl 2400℃ ANaOHBCHOClDECa(OH)2H 2O34. (9分)以甲苯为原料,合成 CH 2COOH,并写出各步反应的反应类型。

乱shi 佳人编辑整理学校 班级 考号 姓名_________________试场号______________装订线内不要答题 ◆◆◆◆◆◆◆◆◆◆◆◆◆装◆◆◆◆◆◆◆◆◆◆◆◆◆◆◆◆◆◆◆◆◆订◆◆◆◆◆◆◆◆◆◆◆◆◆◆◆◆◆◆线◆◆◆◆◆◆◆◆◆◆◆◆◆◆◆◆◆2010年全国高中学生化学竞赛(安徽赛区)初赛试题注意:考试时间3小时,满分150分。
直接在试卷上答题,允许使用非编程计算器。
1. 化学作为一门实用性很强的学科与社会、环境等密切相关。
下列有关说法中正确的是( ) A 、“低碳经济”主要是指减少对化石能源的依赖B 、光导纤维主要成分是晶体硅C 、制作航天服的聚酯纤维属于有机高分子化合物D 、甲型H1N1流感病毒的蛋白质由C 、H 、O 元素组成 2.下列溶液中,一定能大量共存的离子组是( ) A 、pH=1的溶液中:Na +、Mg 2+、SO 42- 、HCO 3-B 、含有大量Fe 3+的溶液中:Al 3+、Cu 2+、Cl - 、SO 42- C 、加入铝能放出H 2的溶液中:K + 、NH 4+ 、NO 3- 、Cl -D 、水电离产生的c (H +)=10-12mol ²L -1的溶液中:K + 、Ba 2+ 、NO 3- 、OH - 3.用N A 表示阿伏伽德罗常数,一下叙述正确的是( )A 、1mol 甲烷中的氢原子被氯原子完全取代,需要氯气分子数为2N AB 、1.7g H 2O 2中含有的电子数为0.9N AC 、2mol 的NO 2与水完全反应转移电子数为N AD 、在pH=13的NaOH 溶液中,OH -数目为0.1 N A一、本题包括25小题,每小题2分,共50分。
每小题有1个或2个选项符合题意,若该题只有1个选项符合题意,多选或错选均不得分。
若该题有2个选项符合题意,选对1个得1分,选对2个得2分;错选1个该题不得分。
4.科学解释能力是科学素养的重要组成部分。

年全国高中化学竞赛(安徽赛区)初赛试题及参考答案————————————————————————————————作者:————————————————————————————————日期:22001年全国高中化学竞赛(安徽赛区)初赛试题(考试时间3小时,满分150分)注意:⒈本试卷分试题卷和答题卷两部分,所有的答案必须写在答题卷上,写在试题卷上无效......................。
⒉考生开始答题前,请先将答题卷上密封线内的项目填写完整。
⒊有关计算中,请遵循近似数计算法则。
H1.008 元素周期表He 4.003Li 6.941Be9.012B10.81C12.01N14.01O16.00F19.00Ne20.18Na 22.99Mg24.31Al26.98Si28.09P30.97S32.07Cl35.45Ar39.95K 39.10Ca40.08Sc44.96Ti47.88V50.94Cr52.00Mn54.94Fe55.85Co58.93Ni58.69Cu63.55Zn65.39Ga69.72Ge72.61As74.92Se78.96Br79.90Kr83.80Rb 85.47Sr87.62Y88.91Zr91.22Nb92.91Mo95.94Tc[98]Ru101.1Rh102.9Pd106.4Ag107.9Cd112.4In114.8Sn118.7Sb121.8Te127.6I126.9Xe131.3Cs 132.9Ba137.3La-LuHf178.5Ta180.9W183.8Re186.2Os190.2Ir192.2Pt195.1Au197.0Hg200.6Tl204.4Pb207.2Bi209.0Po[210]At[210]Rn[222]Fr [223]Ra [226]Ac-La一、本题包括5小题,每小题1分,共5分。
每小题只有一个选项符合题意。
⒈下列各组离子中,能大量共存的是A.H+、Cl-、HPO42-、K+B.OH-、Zn2+、Al3+、Mn2+C.OH-、HPO42-、Na+、SO42-D.OH-、CO32-、AlO2-、Na+⒉现有X、Y、Z、W四种主族元素。
第27届中国化学奥林匹克(初赛)试题、解答、评分标准及评分细则第1题(12分) 写出下列化学反应的方程式1-1 加热时,三氧化二锰与一氧化碳反应产生四氧化三锰。
1-2 将KCN 加入到过量的CuSO 4水溶液中。
1-3 在碱性溶液中,Cr 2O 3和K 3Fe(CN)6反应。
1-4 在碱性条件下,Zn(CN)42?和甲醛反应。
1-5 Fe(OH)2在常温无氧条件下转化为Fe 3O 4。
1-6 将NaNO 3粉末小心加到熔融的NaNH 2中,生成NaN 3(没有水生成)。
1-1 3Mn 2O 3+CO =2Mn 3O 4+CO 2 2分 1-2 4CN ?+2Cu 2+=2CuCN +(CN)2 2分 1-3 Cr 2O 3+6Fe(CN)63?+10OH ? =2CrO 42?+6Fe(CN)64?+5H 2O 2分 1-4 Zn(CN)42?+4H 2CO +4H 2O =4 HOCH 2CN +Zn(OH) 42?? 2分 1-5 3Fe(OH)2=Fe 3O 4+H 2+2H 2O 2分 1-6 NaNO 3+3NaNH 2=NaN 3+NH 3+3NaOH 2分 1方程式正确才能得满分。
2若全部物质皆写对而未配平,可得1分。
第2题(23分) 简要回答或计算2-1 Bi 2Cl 82-离子中铋原子的配位数为5,配体呈四角锥型分布,画出该离子的结构并指出Bi 原子的杂化轨道类型。
Bi 2Cl 82-的结构:ClClBiClClCl2-或ClClClClCl2- 2分.......未画成楔形键不扣分;不画电子对不扣分;若画了电子对且画成如上图(蓝)所示的连线,则与电子对相连的线不画成虚线(左)、虽画成虚线但远离Bi 原子,扣0.5分杂化轨道类型:sp 3d 2 1分2-2在液氨中,E θ(Na +/Na)=-1.89V ,E θ(Mg 2+/Mg)=-1.74V ,但可以发生Mg 置换Na 的反应:Mg +2NaI =MgI 2+2Na ,指出原因。
2015年全国中学生化学竞赛(安徽赛区)初赛试题注意:考试时间2.5小时,满分150分。
请在答题卡上答题,允许使用非编程计算器。
一、本题包括15小题,每小题2分,共30分。
每小题仅有1个选项符合题意。
1.下列生活常识与化学原理有关,正确的选项是①福尔马林具有防腐杀菌的作用,是因为甲醛可以使蛋白质变性②人体血液pH保持弱碱性(7.35-7.45),主要是血液中存在H2CO3—HCO3-缓冲体系③硫酸亚铁补铁剂应与维生素C同服,是因为维生素C可以防止Fe2+被氧化④油炸食品容易产生“哈喇”味而不能食用,是因为被氧化产生过氧化物和醛类A.①②③④B.①②③C.②③④D.①③④2.缺铁性贫血是世界上最普遍的营养性问题,一个简单的解决办法是生产铁强化酱油,即在酱油中加入易吸收的铁添加剂——Na2FeY,其中Y4-是乙二胺四乙酸(H4Y)的酸根形式,H4Y结构如下左图。
生产铁强化酱油产生的废水可用绿色消毒剂X(如下右图)来杀菌。
下列有关说法正确的是A.从酸碱质子理论来说,H4Y只有酸性B.X能够杀菌的原因是其水解可产生次氯酸C.H4Y和X在一定条件下均能发生水解反应D.可用萃取法从铁强化酱油中分离出Na2FeY3.某未知溶液可能含Cl-、CO32-、Na+、SO42-、Al3+等离子中的一种或多种。
将溶液滴在蓝色石蕊试纸上.试纸变红。
取少量试液,滴加硝酸酸化的氯化钡溶液,有白色沉淀生成;在上层清液中滴加硝酸银溶液,产生白色沉淀。
下列判断不合理...的是A.一定有Cl-B.一定有SO42- C.一定有Al3+ D.一定没有CO32-4.下列有关实验操作中错误..的是A.萃取分液时,分液漏斗中下层液体从下口放出,上层液体从上口倒出B.检查容量瓶是否漏水的方法是:往容量瓶中加水,塞好瓶塞,将容量瓶倒过来,若不漏水,将瓶塞旋转180°,再倒过来,看是否漏水C.为加速固体物质的溶解常采取搅拌、加热等措施D.酸式滴定管装入标准溶液前,必须用蒸馏水润洗三次,不得用标准溶液润洗5.“酸化”是实验中经常采用的方法,下列酸化过程正确的是A.增强高锰酸钾的氧化能力,用浓盐酸酸化B.抑制Fe2+的水解,用稀硝酸酸化C.检验卤代烃中的卤元素,加碱溶液并加热后,用稀硫酸酸化,再检验D.确认溶液中含有SO42-时,用盐酸酸化,再检验6.近年来,科学家合成了一系列具有独特化学特性的氢铝化合物(AlH3)n。
2012年全国高中学生化学竞赛(安徽赛区)初赛试题注意:考试时间3小时,满分150分。
直接在试卷上答题,允许使用非编程计算器第一大题(选择题)答案写在下表中,其余题答案写在试卷上一、本题包括25小题,每小题2分,共50分。
每小题有1个或2个选项符合题意。
若该题只有1个选项符合题意,多选或错选均不得分。
若该题有2个选项符合题意,选对1个得1分,选对2个得2分;选错1个,该题不得分。
1.为了缓解石油危机,科学家正在进行“生物质油”代替柴油的试验。
所谓“生物质油”是指以光合作用产生的植物、农作物等富含纤维素、半纤维素和木质素的物质为原料,采用生物热解液化技术而产生的新能源。
下列有关说法错误..的是 A .生物质油是一种有机化合物 B .这一类能源属于可再生能源C .利用生物质能就是间接利用太阳能D .生物质油提炼技术中主要利用的是化学变化 2.一块铜板被等分成两块,Cu(a)和Cu(b);捶打Cu(a),Cu(b)不动。
再由Cu(a)、Cu(b)及CuSO 4溶液组成电池:Cu(a )︱CuSO 4(cmol/L) ︱Cu(b),测得电动势E>0,因为Cu(a)的A .△S>0,△H=0B .△S>0,△H<0C .△S<0, △H=0D .△S<0, △H<0 3.空间实验室“天宫一号”的供电系统中有再生氢氧燃料电池(RFC),RFC 是一种将水电技术与氢氧燃料电池技术相结合的可充电电池。
下图为RFC 工作原理示意图,有关说法正确的是 A .当有0.1mol 电子转移时,a 极产生1.12LH 2(标准状况下) B .b 极上发生的电极反应是:4H 2O + e - = 2H 2↑+ 4OH - C .c 极上进行还原反应,B 池中的H+可以通过隔膜进入A 池D .d 极上发生的电极反应是:O 2 + 4H + + 4e - = 2H 2O 4.室温下,下列各组离子在指定溶液中一定能大量共存的是A .pH=12的溶液中:AlO 2-、Na +、SO 24-、SO 23-B .水电离出的()c H +=10-17mol/L 的溶液中:K +、Na +、SO 24-、AlO 2-C .能与铝反应生成氢气的溶液中:Mg 2+、Na +、Cl -、NO 3-D .()c H +=0.10mol/L 的溶液中:CH 3COO -、NH 4+、Cl -、Na +5.已知化学反应A 2(g)+B 2(g)=2AB(g)的能量变化如右图所示,下列叙述中正确的是A .每生成2分子AB 吸收bkJ 热量 B .该反应焓变为△H =+(a+b)kJ/molC .该反应中反应物的总能量高于生成物的总能量D .断裂1molA —A 键和1molB —B 键,放出akJ 能量6.中学化学教材中有大量的数据材料,下面是某学生对数据的利用情况,其中错误..的是 A .利用K sp 数据可判断BaCO 3与Na 2SO 4溶液能否反应B .利用沸点数据可推测将一些液体混合物分离出来的可能性C .利用第一电离能数据可判断同周期元素的金属性强弱D .利用液体密度可以判断液体物质挥发性的难易 7.As 2S 3和HNO 3有如下反应:As 2S 3 + 10H + + 10NO 3- → 2H 3AsO 4 + 3S +10NO 2↑+2H 2O ,下列说法正确的是A .生成1molH 3AsO 4时,转移电子个数为10N AB .将该反应设计成一原电池,则NO 2应该在正极附近逸出C .该反应的氧化产物之一为SD .反应产物NO 2与11.2L O 2(标准状况)混合后用水吸收全部转化成浓HNO 3,然后与过量的碳反应,所产生的CO 2的量为0.5mol 8.关于下列各装置图的叙述中,错误的是 A .装置①中,d 为阳极、c 为阴极 B .装置②可用于收集H 2、CO 2C .装置③中X 若为CCl 4,可用于吸收氨气或氯化氢,并能防倒吸D .装置④可用于干燥、收集NH 3,并吸收多余的氨气9.可逆反应2A(g) + B(g) ƒ 2C(g),根据下表中的数据判断下列图像错误的是10.能正确表示下列反应的离子方程式的是A .足量的硫酸铝溶液与纯碱溶液反应:2Al 3+ + 3 CO 23- + 3H 2O = 2Al(OH)3↓ + 3CO 2↑B .NaHS 溶液的水解方程式:HS - + H 2O ƒ H 3O + + S 2-C .Fe(OH)3与足量的HI 溶液反应:Fe(OH)3 + 3H + = Fe 3+ + 3H 2OD .向饱和亚硫酸氢钡溶液中加入足量的NaOH 溶液:Ba 2++2HSO 3-+2OH -=BaSO 3 +2H 2O+SO 23-11.在室温下,向氢硫酸中通入二氧化硫气体,溶液的pH 发生变化。
下列图示能正确反映通入SO 2后在很短时间内通入SO 2体积与溶液pH 的关系的是12.下列各溶液中,微粒的物质的量浓度关系表述正确的是A .0.1mol/LNa 2CO 3溶液中:c(Na +)=2c(HCO 3-)+2c(H 2CO 3)+2c(CO 23-)B .常温下pH=4的醋酸与pH=10的NaOH 溶液等体积混合后pH>7C .将0.2mol/LNaA 溶液和0.1mol/L 盐酸等体积混合所得碱性溶液中 c(Na +)+c(H +)=c(A -)+c(Cl -)D .pH=12的Ba(OH)2溶液和pH=12的Na 2CO 3溶液中,水电离的c(H +)相等14.华法林(Warfarin ,右图)是一种鼠药。
该分子的立体中心数目为 A .0 B .1 C .2 D .316.Mg(ClO 3)2在农业上常用作脱叶剂、催熟剂,可采用复分解反应制备:MgCl 2+2NaClO 3=Mg(ClO 3)2+2NaCl ,已知四种化合物的溶解度(S)随温度(T)变化曲线如下图所示。
下列叙述正确的是A .四种化合物的溶解度随温度变化最小的是Mg(ClO 3)2B .300K 时,MgCl 2的溶解度约为55gC .300K 时,100gNaCl 饱和溶液中约含NaCl 36gD .该反应能够进行的条件是生成沉淀,该沉淀是Mg(ClO 3)217.下列关于电解质溶液的叙述正确的是A .室温下,将稀氨水逐滴加入稀硫酸中,当溶液pH=7时,c(SO 24-)>c(NH 4+)B .室温下,pH=3的氢氟酸加水稀释后,电离常数K a (HF)和pH 均减小C .室温下,pH=11的NaOH 溶液与pH=3的醋酸溶液等体积混合,滴入石蕊溶液呈红色D .向0.1mol/L 的氨水中加入少量硫酸铵固体,则溶液中32()()OH NH H O c c -g 增大甲乙丙丁18.下列物质的转化在给定条件下不能..实现的是 A .MgCl 2(aq)−−−→石灰乳Mg(OH)2−−−→燃烧MgO B .S O −−−−→2/点燃SO 3H O−−−→2H 2SO 4 C .Al 2O 3Na ()OH aq ∆−−−−→NaAlO 2(aq) CO−−−→2Al(OH)3 D .饱和NaCl(aq) 3NH ,CO −−−−→2NaHCO 3∆−−→Na 2CO 3 19.ClO 3-离子中O —Cl —O 的键角为A .109°28ˊB .小于109°28ˊC .120°D .小于120°,大于109°28ˊ20.水溶液X 中只可能溶有K +、Mg 2+、Al 3+、AlO 2-、SiO 23-、CO 23-、SO 24-中的若干种离子。
某同学对该溶液进行了如下实验:下列判断错误..的是 A .有气体甲生成,表明溶液X 中一定有CO 23- B .沉淀甲不可能是硅酸镁 C .Al 3+一定存在于溶液X 中 D .不能确定SO 24-是否存在于溶液中 21.乙二胺(N N)是双齿配体,X 和Y 是单齿配体,下面配合物属对映体的是A .(Ⅰ)和(Ⅱ)B .(Ⅱ)和(Ⅲ)C .(Ⅰ)和(Ⅲ)D .(Ⅱ)和(Ⅳ) 22.M 的名称是乙烯雌酚,它是一种激素类药物,结构简式如下。
下列叙述不正确...的是 A .M 的分子式为C 18H 20O 2 B .M 与NaOH 溶液或NaHCO 3溶液均能反应 C .1molM 最多能与7molH 2发生加成反应 D .1molM 与饱和溴水混合,最多消耗5molBr 223.对反应AsBr 3+BrOTeF 5+As(OTeF 5)5=[AsBr 4]+[As(OTeF 5)6]-,下面正确的叙述是 A .该反应不是氧化还原反应 B .该反应是氧化还原反应C .所有化合物中溴的氧化数都为-1D .所有化合物中砷的氧化数都为+5 24.为防治“白色污染”,有一条重要途径是将合成高分子化合物重新变为小分子化合物:目前对结构简式为 的化合物已成功实现了这种处理,其运用的 原理是酯交换反应(即酯与醇在酸或碱的催 化下生成一个新酯和一个新醇的反应)。
试分析若用CH3OH 来处理这种化合物能得到的有机物可能是 A .苯 B .乙二醇 C .对苯二甲酸二甲酯 D .苯甲酸25.甲基胺与过量的氧气反应,生成氮气、水和二氧化碳。
与1mol 甲基胺完全反应所需的氧气的物质的量为A .2.25B .2.5C .3.00D .4.5 二、本题包括4小题,共24分26.(3分)设气相反应物和生成物为理想气体,若需求111PV P V T T ,则反应方程式中反应物的计量系数之和必须 (填等于、大于或小于)生成物的计量系数之和,因为。
27.(6分)NO -、NO 、NO +中,键能由大到小的次序为 ,NO +键级数为 级;含有单电子轨道的是 ,键长最长的是 。
配合物[PtCl 3(C 2H 4)]- 中,Pt 原子周围有 电子;Cr 2(CO)4(C 5H 5)2中,Cr 与Cr 之间为三键,则每个Cr 原子周围有 电子。
28.(9分)在低温下液态SO2溶剂中,点单子与五氟化锑反应,生成[I 4]2+[Sb 3F 14]-[SbF 6]-。
其反应方程式为 。
在[Sb 3F 14]-中Sb 的平均氧化数为 ,Sb 的实际氧化数为 和 。
[Sb 3F 14]-可以看作由2个离子团(A) 与1个离子团(B) [(A)和(B)用化学式表示]连接而成。
试画出[Sb 3F 14]-的结构式,并指明结构式中每个Sb 原子的杂化类型。
29(6分)(1)画出配合物PtCl 2A(A 为1,2-二氨基环丁烯二酮)的结构式,指明所有原子是否共面?说明原因。
(2)若A 中环丁烯中双键被加氢,画出PtCl 2A ′的二种结构式。