天然沸石对氨氮的动态去除过程研究(精)
- 格式:pdf
- 大小:849.77 KB
- 文档页数:5

沸石吸附水体中氨氮的热力学和动力学过程研究袁时珏;黄远星;李亮;马腾飞;薛磊【期刊名称】《水资源与水工程学报》【年(卷),期】2013(24)4【摘要】随着近年来各大自然水体富营养化程度的加重,废水中氨氮的处理显得尤为重要。
我国浙江缙云有丰富的沸石矿藏,研究其对于沸石的吸附过程有着明显的应用价值。
实验结果显示:在288~318 K范围内的温度对沸石吸附氨氮过程影响较小,在氨氮初始浓度为30 mg/L的条件下,小粒径沸石对氨氮的48 h吸附容量为1.13±0.06 mg/g,去除率为91%。
大粒径沸石对氨氮的48 h吸附容量为1.10±0.06 mg/g,去除率为87%。
沸石对氨氮的吸附过程遵循二级吸附动力学方程,Freundlich和Langmuir等温吸附方程均适用于描述沸石吸附氨氮的热力学过程。
本研究表明天然沸石是一种合适的吸附剂,可用于废水或者天然水体中氨氮的去除。
【总页数】4页(P11-14)【关键词】氨氮;吸附;沸石;废水处理【作者】袁时珏;黄远星;李亮;马腾飞;薛磊【作者单位】上海理工大学环境与建筑学院【正文语种】中文【中图分类】X703【相关文献】1.改性粘土预处理垃圾渗滤液中氨氮的吸附热力学和动力学研究 [J], 吕利;唐艳妮;姜丽丽2.白银斜发沸石的改性及其对氨氮的吸附热力学和动力学 [J], 马明广;魏云霞;赵国虎;张力;尚琼3.氨氮在土壤中吸附/解吸的动力学与热力学研究 [J], 孙大志4.活化沸石吸附水中氨氮影响因素及动力学研究 [J], 李卉;韩占涛;李雄光;黄冰5.硅藻土/沸石复合颗粒吸附材料脱氮除磷的吸附动力学及热力学分析 [J], 段宁;吴依远;张银凤因版权原因,仅展示原文概要,查看原文内容请购买。


天然沸石是含水多孔铝硅酸盐的总称,其结晶构造主要由(SiO)四面体组成,其中部分Si4+为Al3+取代,导致负电荷过剩,因此,结构中有碱金属(碱土金属)等平衡电荷的离子。
同时沸石构架中有一定孔径的空腔和孔道,决定了其具有吸附、离子交换等性质,因此其对氨氮具有很强的选择性吸附能力,因而可被应用于氨氮废水的处理。
对沸石处理氨氮废水进行了许多研究,但是吸附动力学和等温吸附的研究结果不尽相同,尤其是对沸石饱和吸附量的研究鲜见报道,因此有必要做进一步研究。
本实验探讨了氨氮浓度、温度、时间、沸石粒径对天然沸石吸附氨氮的影响,研究了沸石对氨氮的动态吸附过程,旨在探索沸石对氨氮吸附的规律,为沸石用于氨氮废水处理奠定基础。
吸附动力学研究通过在不同温度下进行试验,研究不同时间内沸石对氨氮的吸附量,进而得出反应速率变化的规律和物质浓度随时间变化的规律。
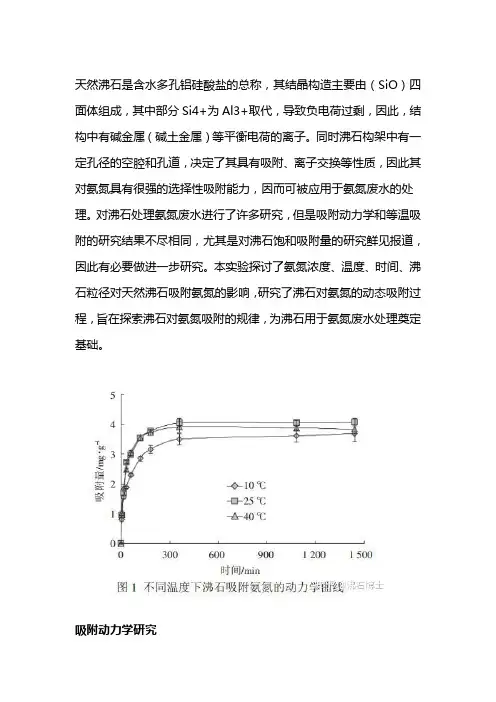
沸石对氨氮的吸附量随时间而变化见图1。
在不同温度下,沸石对氨氮的吸附量都是随着时间的增加而增加,但并不一定随着温度的升高而增加。
在吸附反应初始阶段(0~60min),沸石对氨氮的吸附速率较大,吸附量上升很快,随着吸附反应的不断进行,吸附速率降低,在360min后吸附基本达到平衡。
沸石对氨氮的快速吸附阶段是氨氮在沸石表面和内部孔隙中的扩散吸附过程,第二阶段为平衡吸附过程,此时吸附速率随着溶液中氨氮浓度的降低而变慢,最终达到固液两相平衡。
10、25℃和40℃下的平衡吸附容量分别为3.60、4.05mg·g-1和3.87mg·g-1左右。
采用SPSS软件进行处理间多重比较LSD分析,结果表明在3种温度下沸石对氨氮的吸附容量有显著性差异(P<0.05)。
为了进一步描述沸石对氨氮吸附过程的动力学特征,利用图1中的数据,用以下准二级动力学方程进行拟合:t/Qt=1/(k·2Qe2)+t/Qe式中:t为吸附时间(min);Qt为t时刻的吸附量(mg·g-1);Qe为平衡吸附量(mg·g-1);k2为二级吸附速率常数(g·mg-1·min-1)。

天然沸石吸附氨氮和磷的研究
天然沸石吸附氨氮和磷的研究
选用浙江缗云产颗粒状天然沸石为材料对氨氮和磷进行吸附动力学和吸附等温试验,考察初始浓度、振荡时间对吸附量、去除率的影响.试验结果表明:沸石对氨氮和磷吸附显示出"快速吸附,缓慢平衡"的`特点;吸附动力学过程符合准二级动力学模型;吸附等温线更符合Freundlich 方程;氨氮初始浓度小于7 mg/L、振荡时间在1h内和磷初始浓度小于30 mg/L、振荡时间在15 min内,吸附量、去除率随初始浓度、振荡时间增加而增加,当超过此阶段后,吸附量增加缓慢、去除率下降.
作者:胡细全胡志操王春秀金洁郭静林惠凤 Hu Xiquan Hu Zhicao Wang Chunxiu Jin Jie Guo Jing Lin Huifeng 作者单位:湖北大学资源环境学院,湖北,武汉,430062 刊名:环境科学与管理英文刊名: ENVIRONMENTAL SCIENCE AND MANAGEMENT 年,卷(期):2009 34(4) 分类号:X703.1 关键词:天然沸石氨氮磷吸附动力学试验吸附等温试验。

沸石对氨氮的吸附行为研究作者:符露来源:《丝路视野》2016年第20期【摘要】本文研究了斜发沸石对氨氮吸附行为,探讨了水力停留时间、pH值对吸附效果的影响,同时考察了吸附氨氮前后的沸石的性能及结构变化。
结果表明,准二级吸附动力学方程能够很好地描述沸石吸附氨氮的过程,沸石在1.0 g/L的氨氮溶液中的理论吸附值为8.69 mg·g-1。
沸石吸附氨氮的最佳水力停留时间为40min,最佳pH值为6,并且氨氮去除率随着浓度的升高而降低,随着沸石投加量的增加而升高。
沸石吸附氨氮前后形态及结构并未发生变化,比表面积、孔容、孔径则明显降低。
【关键词】斜发沸石;氨氮氨氮是水体中重要耗氧物质、是引起水体富营养化的污染物。
近年来,随着社会生产水平的提高,氨氮的排放量与日俱增。
由于水污染事件频繁发生,严重威胁着社会日常生产工作,对于水污染较严重的地区,逐渐实行更加严格的标准控制污水中氨氮的排放,不少污水处理厂面临标准提高的严峻现状。
因此,在兼顾经济的条件下提高处理效率,成为了研究的重点。
目前国内解决高浓度氨氮污染主要使用吹脱法、生物法、离子交换法。
其中吹脱法容易造成二次污染,生物法条件要求高、反应缓慢,而离子交换法较易控制。
天然沸石是一种含水的碱或碱土金属的铝硅酸盐矿物,是由硅氧四面体和铝氧四面体组成的架状硅酸盐,具有比表面积大,吸附性能好,离子交换能力强,化学性能稳定等特点。
沸石对氨氮的去除有着较好的效果,对浓度具有普适性,并且由于沸石资源在我国储量丰富、成本低廉,是一种具有前景的水处理方式,因此沸石吸附氨氮受到较多的关注。
一、材料与方法(一)实验装置静态吸附采用摇床,动态吸附采用沸石柱装置,如图1所示。
实验装置主要由PVC管、蠕动泵、水箱三部分组成,其中PVC管高为100cm,(二)动态吸附实验室温下,在不同的滤速下将含氨氮废水通过沸石吸附柱,每隔20分钟取水样并用0.4μm 滤膜过滤后测定氨氮的浓度。

沸石分子筛吸附污水中氨氮的研究进展沸石分子筛吸附污水中氨氮的研究进展随着工农业的发展,污水处理成为了一项重要的环保任务。
氨氮是污水中常见的一种污染物,具有毒性和刺激性,对水环境和生态系统造成严重危害。
因此,研究高效、经济的氨氮去除技术成为了当前环境保护领域的热点。
沸石分子筛作为一种常用的吸附剂,受到了广泛关注,并在氨氮吸附领域取得了显著的研究进展。
沸石是一种富含硅酸盐的多孔矿物,具有较高的比表面积和丰富的通道系统。
由于其独特的化学结构和物理性质,沸石分子筛具备了良好的吸附能力,可以有效地吸附污水中的氨氮。
沸石分子筛吸附氨氮的机制主要包括离子交换和物理吸附两种方式。
在离子交换中,沸石分子筛表面的阳离子与氨氮中的氨离子发生交换反应,将氨离子固定在其孔隙结构中。
物理吸附则是通过静电力、范德华力等相互作用力,将氨氮吸附到沸石分子筛表面。
这两种吸附方式形成了丰富的吸附位点,大大提高了沸石分子筛对氨氮的吸附能力。
研究者们通过调控沸石分子筛的孔径、表面性质和晶体结构等参数,进一步提高了其对氨氮的吸附效果。
其中,改变孔径是一种较为常见的方法。
研究发现,较小孔径的沸石分子筛具有较高的氨氮吸附能力。
这是因为小孔径可以增加分子筛表面积与体积的比值,提高了吸附位点的密度,从而增强了吸附效果。
此外,研究者还通过改变分子筛表面的官能团,引入诸如羟基、胺基等亲水官能团,增加了分子筛与水中氨氮之间的亲和力,提高了吸附效果。
除了调控分子筛本身的性质外,研究者还通过改变吸附条件,进一步优化了吸附效果。
例如,调节溶液的pH值、温度和初始氨氮浓度等。
实验证明,酸性条件下沸石分子筛的吸附效果较好,这是因为在酸性环境中,氨氮更容易解离为氨离子,便于其与分子筛表面的阳离子发生离子交换反应。
另外,适当提高温度可以增加活化能,促进吸附过程的进行;而增大初始氨氮浓度可以增加吸附位点的利用率,提高吸附效果。
近年来,沸石分子筛在氨氮去除领域得到了广泛应用。

天然沸石去除废水中氨氮的研究作者:方佳丽李荣寨来源:《科学与财富》2017年第05期摘要:随着社会经济的迅速发展,大量含氨氮的生活和工业废水排入天然水体,造成环境污染日益严重。
天然沸石由于具有较好的吸附和离子交换性能,被应用于废水中氨氮的去除。
本文通过单因素实验法,研究分析了沸石粒径、投加量、振荡时间、PH值、再生等因素对氨氮去除率的影响。
研究结果表明,天然沸石在处理模拟低浓度氨氮废水时,废水氨氮浓度≤100mg/L,沸石粒径>60目,投加量为50g/L,振荡时间为1h,PH值为4-8时效果最佳;实验还发现,在处理实际生活和工业的氨氮尾水时同样具备较好的去除效果,且循环3次再生使用后天然沸石仍具有一定的氨氮去除能力。
关键词:天然沸石;生活废水;工业废水;氨氮废水Abstract: With the rapid development of social economy, a large number of industrial and domestic wastewater containing ammonia nitrogen discharged into natural water, Environmental pollution is becoming increasingly serious. The natural zeolite has good adsorption and ion exchange properties, study on the application of nature zeolite in treatment of ammonia nitrogen wastewater has been carried out. Through single factor experiment method, research and analysis of the particle size of zeolite, dosage,oscillation time, pH value, zeolite recycling study on ammonia removal. The results show that nature zeolite removal ammonia nitrogen from simulation wastewater, the condition of ammonia nitrogen concentration is less than 100mg/L, the particle size of zeolite is more than 60 mesh, dosage is 50g/L, oscillation time is 1 hour, pH value is 4-8 has the best effect; The experimental results also show that the treatment process has a better effect in the treatment of the actual life and industrial ammonia nitrogen tail water. And the natural zeolite still has a certain removal capacity after 3 cycles.Key words: nature zeolite; domestic wastewater; industrial wastewater; ammonia nitrogen wastewater.前言水环境中的氨氮是指以游离氨(NH3)和铵离子(NH4+)形式存在的氮。

第30卷 第1期 上海第二工业大学学报 V ol.30 No.1 2013年3月 JOURNAL OF SHANGHAI SECOND POLYTECHNIC UNIVERSITY Mar. 2013 文章编号: 1001-4543(2013)01-0025-06天然斜发沸石对水中氨氮的吸附研究田 震,李奕怀,沈娇雯,许中平,邴乃慈(上海第二工业大学环境建设与环境工程学院,上海201209)摘 要:研究了天然斜发沸石对废水中氨氮的吸附行为,比较了pH 值、温度、氨氮浓度等条件对吸附性能的影响。
对沸石的吸附等温线用Langmuir 和Freundlich 模型分析拟合表明,其吸附等温线更符合Langmuir 模型;不同pH 环境和不同温度下氨氮的吸附量比较表明,适宜的pH 值和较低的温度有利于沸石具有较高的吸附量,在温度低于30 ℃、pH 在4~8的范围内,沸石的吸附性量可达2 mg·g -1以上。
关键词:天然沸石;氨氮;吸附等温线;pH 值;吸附量 中图分类号:TB14 文献标志码:A0 引言含氨氮废水是日常生活和多个生产行业排放的主要污染物之一。
近年来,随着国家对氮、磷等有机污染的重视,各种含氨废水的脱氮技术也成为了研究热点。
目前对含氨废水的处理尤其是低浓度含氨废水的处理尚未有十分有效的处理技术。
由于天然沸石来源广泛,对NH 4 +具有很强的选择吸附能力,在处理含氨氮较低的微污染水处理中有良好的应用前景[1]。
天然沸石对NH 4 +的吸附能力主要是基于它的强离子交换能力。
交换能力的大小决定了其吸附容量,其大小不仅与沸石的种类有关,而且还与沸石的硅铝比、孔径大小、孔道畅通情况、阳离子的位置和性质以及交换过程中的温度、压力、离子浓度、pH 值等诸多因素有关[2-3]。
不同的离子由于其电荷及结构的不同,其离子交换选择性顺序为Cs + >Rb + >K + >NH 4+ >Ba 2+ >Sr 2+ >Na + >Ca 2+ >Fe 3+ >Al 3+ >Mg 2+ >Li +斜发沸石(Clinoptilolite)是一类分布及应用较广的天然沸石,其主体结构是由硅(铝)氧四面体连成三维的格架,格架中有各种大小不同的空穴和通道,其化学式表示为R 1+R 2+[Al x +2y Si (n -x -2y )O 2n ]·m H 2O 的一族含水架状结构铝硅酸盐矿物。

沸石去除氨氮试验方案一、沸石改性预处理首先对沸石进行清洗,用清水对沸石进行10次淘洗,待沉淀后,倒去上部浑水,洗去沸石中混有的杂质,然后用纯水对沸石进行二次清洗,再将清洗后的沸石在烘箱105℃下干燥5小时,期间要将沸石拿出搅拌数次,防止结块。
二、改性沸石的制备1. 无机酸改性沸石的酸改性试验,选用盐酸作为改性剂,改性对象为经过与处理的沸石。
通过此改性试验得到H型沸石。
配置一定量的盐酸(1mol/L),称取一定量的经过预处理的沸石。
将沸石在盐酸中浸泡24小时,倒出上清液,用去离子水将沸石清洗至中性,然后将沸石放入烘箱在105℃下烘干,制得HCl改性沸石即H型沸石。
2. 无机碱改性为了得到P型沸石,对经过预处理的沸石进行碱改性试验,选用改性剂是氢氧化钠。
称取一定量的经过预处理的沸石,放入配置好的1 mol/L 的NaOH溶液中浸泡24小时,倒出上清液,用去离子水将沸石清洗至中性,然后将沸石放入烘箱在105℃下烘干,制得碱改性沸石即P型沸石。
3. 无机盐改性沸石的无机盐改性试验,选用的改性剂是氯化钠,改性对象是经过预处理的沸石。
称取一定量的经过预处理的沸石和HCl改性沸石,分别加入1 mol/L的NaCl溶液,浸泡24小时,倒出上清液,用去离子水将沸石清洗至中性,然后将沸石放入烘箱在105℃下烘干,制得氯化钠改性沸石即Na型沸石。
三、改性沸石去除氨氮的效果研究1. 定性分析试验设计用NH4Cl和纯水配置浓度为10mg/L的氨氮水样。
分别称取三种改性沸石10g,投入1L配置好的10mg/L的NH4Cl溶液中进行烧杯试验,设计搅拌速度为200r/min,搅拌时间为30分钟,分析氨氮的去除率,对比三种改性沸石对氨氮的去除效果。
若改性沸石对氨氮有较好的去除效果,则往下继续开展下述试验步骤。
2. 改性沸石去除氨氮的影响因素2.1 三种改性沸石投加量对去除率的影响针对三种不同的改性沸石分选用不同投加量,进行烧杯试验,观察、对比其在不同投加量下去除氨氮的效果,确定三种改性沸石在NH4+浓度为10mg/L时的最佳投加量,并尝试采用模拟水绘制Langmuir等温线或者Freundlich等温线。
第22 卷第2 期环境化学VoI. 22,No. 2 2003 年 3 月ENVIRONMENTAL CHEMISTRY Marc1 2003 !!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!氨氮在天然沸石上的吸附及解吸l)张曦吴为中温东辉李文奇唐孝炎(北京大学环境科学中心,北京,l0087l)摘要研究了氨氮浓度、温度、时间、共存阳离子等对氨氮在天然沸石上吸附的影响,比较了HCI 及NaC I 溶液对氨氮解吸的效果,初步探讨了沸石吸附氨氮后自然硝化的规律.结果显示,随着氨氮浓度的增大或温度的升高,沸石吸附量上升,最大可达ll.5mg・g - l;沸石吸附的初始阶段(0—81),沸石吸附量随时间显著上升,此后趋于平缓;在不同阳离子共存的情况下,K +可使沸石吸附量降低50%以上;HC I 溶液对氨氮解吸的效果好于NaCI溶液,解吸率最高可达到60%;沸石吸附的氨氮在硝化细菌作用下可转化为硝氮,溶液中硝氮浓度l201 后可达9mg・I - l,在总氮中比率达到27% .关键词氨氮,沸石,吸附,解吸,硝化 .天然沸石是含水多孔铝硅酸盐的总称,其结晶构造主要由(SiO)四面体组成,其中部分Si4 +为AI3 +取代,导致负电荷过剩,因此,结构中有碱金属(或碱土金属)等平衡电荷的离子 . 同时沸石构架中有一定孔径的空腔和孔道,决定了其具有吸附、离子交换等性质[l,2],其离子交换选择性顺序为:CS + > Rb + > K + > NH4+ > Ba2 + > Sr2 + > Na + > Ca2 + > Fe3 + > AI3 + > Mg2 + > Li +可见其对氨氮具有很强的选择性吸附能力,因而可被应用于氨氮废水的处理[3,4].本实验探讨了氨氮浓度、温度、时间、共存阳离子对天然沸石吸附氨氮的影响,研究了不同化学洗脱液对氨氮解吸的效果,考察了沸石所吸附的氨氮在溶液中的自然硝化作用,旨在探索氨氮在沸石上吸附及解吸的规律,为沸石用于氨氮废水处理奠定基础.l l.l 实验部分沸石的静态吸附实验6材料. 其主要物理特性为:Si / AI 为 4.2—5.3,粒径为2—3cm,孔隙率为30—40%,动力学直径为 3.9 .称取30g 沸石放入500mI 锥形瓶中,加入不同浓度(!0)的NH4CI 溶液200mI,置恒温水浴振荡器中振荡,使氨氮在液相和沸石固相间的分配达到平衡,721 后取出样品,静置l5min,取上清液测定NH3 - N的平衡浓度(!e),计算沸石对NH3 - N的吸附2002 年5 月l7 日收稿.l)基金项目:科技部重大专项“滇池流域农业面源污染控制技术”(K99053502).・选取浙江缙云产斜发沸石(典型晶胞组成为:Na[(AIO2)6(Si O2)30]24H2O)为试验2 期张曦等:氨氮在天然沸石上的吸附及解吸167量 . 实验中改变NH4CI 溶液浓度、温度、振荡时间、共存阳离子等实验条件,进行不同条件下的吸附实验对比 . 吸附量(!,mg・g - 1)计算公式如下:! =(C0 - C e)V / m式中,C0:NH4CI 溶液起始浓度,mg・I - 1;C e:吸附后NH4CI 溶液平衡浓度,mg・I - 1;V:溶液体积,I;m:沸石重量,g.1.2 化学解吸实验将不同NH3-N 浓度下吸附达到平衡的沸石置于恒温箱中,75C下干燥121,然后在干燥器中静置至室温 . 按上述步骤放入锥形瓶,加入NaCI 或HCI 溶液恒温振荡721,取出后测定沸石的吸附量,以新鲜沸石吸附量为对比计算解吸率(",)."=(1 -! /!0)X 100%式中,!0:新鲜沸石氨氮吸附量,mg・g - 1;!:解吸后沸石残留的氨氮吸附量,mg・g - 1 . 1.3 自然硝化实验在与阳光及大气接触的开放条件下,将30g 沸石浸没于5g・I - 1 NH4CI 溶液中,使之静置吸附,3d 后沸石表面生长出绿色藻类,此时取出沸石,缓慢清洗沸石表面残留的NH4CI 溶液,于75C下干燥121,在干燥器中静置至室温,然后置于500mI 50mg・I - 1的NH4CI 溶液中,20C恒温并光照条件下培养,定期检测溶液pH 值、溶解氧(DO)以及溶液中NH3-N 及NO3- -N 的浓度,考察沸石吸附氨氮的自然硝化作用 .2 2.1 结果与讨论吸附等温线图 1 显示了不同温度下沸石在NH3-N 起始浓度为5mg・I - 1—10g・I - 1的NH4CI 溶液中的吸附量 . 从图 1 可见,随着氨氮浓度的增大,吸附平衡后沸石上氨氮的吸附量上升.NH3-N 起始浓度小于1000mg・I - 1时,随着浓度的增大,沸石吸附量上升趋势明显,曲线较陡;NH3-N 起始浓度大于1000mg・I - 1后,吸附量随浓度的上升趋势减缓;NH3-N 起始浓度大于5000mg・I - 1后,曲线形成一平台,表明沸石吸附达到最大值,约为11.5 mg・g - 1 . 同时,随着温度的升高,沸石吸附量亦增大,但在10C 的变化范围内,吸附量增加不多. 沸石这种吸附特性符合FreundIic1 吸附规律[5],即吸附量与溶液浓度的对数关系为线性 . 根据FreundIic1 吸附等温式(! = KC1 / I),可拟合出以上三条等温线的吸附方程式,结果见表 1.表1 不同温度下的吸附等温式Table 1 Adsorption eGuations in t1e different temperaturesT /C25 35 45吸附等温式In! = 0.8005 InC - 4.4389In! = 0.7916 InC - 4.3317In! = 0.7915 InC - 4.2479相关系数0.98830.98830.9850K0.01180.01310.0143I1.24921.26331.2634168 环境化学22 卷氨氮在沸石上的吸附机理以化学吸附作用与离子交换作用为主 . 溶液中氨氮浓度愈大,可供交换的氨氮较多,而且溶液本体与沸石表面形成的浓度差愈大,造成氨氮向沸石内部迁移并进行交换反应的动力也愈大,因此,沸石的吸附量增加;当温度升高时,不仅使得氨氮克服沸石表面界膜阻力的能力增加,而且促使沸石表面吸附的氨氮沿沸石微孔向沸石内部迁移,因而沸石吸附量也增大.图 2 显示吸附前后溶液pH 值的变化,随着温度的上升pH 值升高的趋势变得明显. 根据氨氮在沸石上吸附的离子交换机理,加上对沸石结构组成的综合分析,可认为是沸石晶体中Na +等平衡电荷离子被NH4+取代而进入溶液,造成溶液pH 值升高 .图1 不同温度下氨氮在沸石上的吸附等温线图2 吸附前后溶液pH 值的变化Fig. 1 Adsorption isotherms of ammonia-nitrogen Fig. 2 pH vaIues in NH4CI soIution before onto the zeoIite in the different temperatu res and after adsorption2.2 吸附速率图 3 是25C,氨氮浓度为5mg・I - 1时溶液中沸石吸附量随时间变化的曲线 . 在沸石吸附的初始阶段(0—8h),沸石吸附量随时间显著上升,此后趋于平缓,8—48h 内吸附量增加不大,显示了沸石“快速吸附,缓慢平衡”的特点 . 根据时间等温线,可计算此条件下沸石吸附速率,发现其符合班厄姆公式:d! / d! =!(" )其中! 表示吸附量,! 表示时间," 为吸附速率常数. 本实验中吸附量和时间取对数后具有较好的线性关系:In! = 0.132 In! - 3.8412(# = 0.9715).2.3 共存阳离子的影响多种阳离子都存在对氨氮的吸附竞争,尤其是K +,沸石对其吸附能力在氨氮之上 . 实验选择K +,Na +,Ca2 +,Mg2 +四种金属离子(浓度均为0.1moI・I - 1)与氨氮共存,分别在5mg・I - 1和50mg・I - 1两种氨氮浓度下,测定沸石吸附量的变化. 结果见图 4. 由图 4 可见,在阳离子共存的情况下,沸石对氨氮的吸附量降低,而以K +的影响最大,使得沸石对氨氮的吸附量降低50% 以上,Na +,Ca2 +,Mg2 +三种离子的影响相仿,差" ! .别不大 .2.4 化学洗脱作用下沸石的解吸氨氮在沸石上的吸附主要基于离子交换和化学吸附作用,同样地,如果采用较高浓 度的洗脱液使沸石上的氨氮被交换下来,则能够达到解吸的目的 . 图 5 显示了在 250 mg ・I - 1的 NaCI 和 HCI 溶液洗脱作用下沸石上氨氮的解吸情况 . HCI 溶液对沸石解吸的效果较好,在不同的氨氮浓度下其解吸率均高于 NaCI 溶液,最高达到 60%,这是由于2 期张曦等:氨氮在天然沸石上的吸附及解吸169H +比Na +更容易取代NH4+的缘故;而在两种洗脱液中都呈现出沸石解吸率随着沸石吸附量的增大而增大的现象,其原因在于初始吸附的氨氮不仅在沸石表面结合较牢固,而且向沸石内部迁移,因此,不易被其它离子取代,而沸石表面被氨氮完全占据后,吸附作用愈来愈弱,结合不甚牢固,因此,后吸附的氨氮容易被洗脱.图3 沸石吸附量随时间的变化曲线图4 共存阳离子对吸附量的影响Fig. 3 Curve of adsorption capacity Fig. 4 Effects of coexisting cations onvariation with tim e图5the adsorption capacity 不同溶液对氨氮解吸的效果Fig. 5 Effects of different soiution on the desorption efficiency2.5 氨氮的自然硝化实验中沸石吸附氨氮后暴露于大气和阳光之中,以满足自然硝化细菌生长的条件 . 在这种自然硝化过程中,沸石表面氨氮在硝化细菌作用下转化为硝氮,致使溶液中硝氮浓度升高,同时,沸石孔径中的氨氮向外部迁移,逐步转化为硝氮,这实际上是一种微生物作用下的解吸作用 . 而新鲜沸石上由于没有细菌生长,因而只有吸附作用发生.由图 6 可见,自然硝化过程中溶液pH 值先升后降,其原因在于表面生长有大量硝化细菌的沸石浸没在NH4Ci 溶液中,沸石由于未达到其吸附容量,因此,继续吸附氨氮,造成溶液pH 值升高. 此后由于硝化作用的进行,溶液中硝氮浓度增大,因此,pH 值降低;与此同时,与新鲜沸石形成对比,生长有硝化菌的沸石在溶液中出现DO 显著降低的现象,这是硝化过程中氨氮被氧化成硝氮而耗氧的结果 . 图7 显示了自然硝化过程中硝氮浓度明显上升的趋势,开始为零,120h 后接近9mg・i - 1,在所有氮形态中比率达到27%(见表2),此后硝氮的增长趋于平缓.170图6环自然硝化过程中溶液pH 值和境化学图722 卷自然硝化过程中溶液中NH3-N 和DO 的变化NO3- -N 浓度的变化Fig. 6 pH and DO of soIutions within the Fig. 7 NH3-N and NO3- -N concentrations nitrification process variation within the nitrification process表2 自然硝化过程中各形态氮占总氮的比率随时间的变化Table 2 R atio of NH3-N,NO2- -N and NO3- -N in tot aI nit rog en withi n the nitri fic ation p ro ce sst /h!NH3-N / %-21002489.780.087282.270.1312072.780.1421671.830.1736071.670.22- % 0 10.14 12.60 27.08 28.00 28.123 结论(1)随着溶液氨氮浓度的增大或温度的升高,沸石吸附量上升,沸石的吸附特性符合FreundIich 吸附规律. 吸附前后溶液pH 值升高,这是由于沸石晶体中Na +等平衡电荷离子被NH4+取代而进入溶液的结果 .(2)沸石具有“快速吸附,缓慢平衡”的特点,即沸石吸附的初始阶段(0—8h),沸石吸附量随时间显著上升,此后趋于平缓 . 在阳离子共存的情况下,沸石对氨氮的吸附量降低,而以K +的影响最大,其使沸石的吸附量降低50%以上 .(3)HCI 溶液对沸石的解吸效果较好,在不同的氨氮浓度下其解吸率均高于NaCI溶液,最高达到60%;而在两种洗脱液中都呈现出沸石解吸率随着沸石吸附量的增加而增加的现象 .(4)沸石吸附的氨氮在硝化细菌作用下转化为硝氮,其浓度呈明显上升的趋势,20C恒温光照培养120h 后硝氮浓度接近9Mg・I - 1,在所有氮形态中比率达到27%;同时出现溶液pH 值先升后降及DO 显著降低的现象 .参考文献[ 1 ]Zorpas A,Constantinid es T,VIyssid es A G et aI. ,H eavy Met aI Uptak e by Natu raI ZeoIi te and MetaIs Partitioning inSewage SIudge CoMpost[J]. Bioresource Technology,2000,72I113—119感谢您试用AnyBizSoft PDF to Word。
天然斜发沸石对水中氨氮吸附影响因素研究摘要:本实验研究了天然沸石对氨氮的吸附影响因素及机理,结果表明,沸石投加量为2g,粒径由20目增加到100目时,其qe从0.341上升到0.512mg/g;沸石投加量1g,初始氨氮浓度10mg/L增大到100mg/L时,qe从0.112上升0.595mg/g;氨氮初始浓度为100mg/L,投加量为有1g增大到15g时,qe从0.595mg/g下降到0.268mg/g,;沸石吸附氨氮更适合用Langmuir吸附等温线和准二级反应动力学进行描述,其R2分别为0.997和0.998。
关键词:天然沸石;氨氮;吸附容量Study on Influencing Factors by Natural Stellerite AdsorptingAmmoniumDianbo-XuChina Railway Fifth Survey And Design Institute Group Co.,Ltd. Abstract: This study investigated the influencing factors and mechanism of natural zeolite adsorptin ammonia nitrogen.The results show that: zeolite dosage 2g and particle size increased from 20 mesh to 100 mesh, qe increased from 0.341 to 0.512mg / g; zeolitedosage 1g, initial ammonia concentration of 10 mg / L increased to 100mg / L, qe roses from 0.112 to 0.595mg / g; ammonia initial concentration is100 mg / L and the dosage from 1g increased to 15g,qe decreased from 0.595mg / g to 0.268mg / g; the zeolite adsorbed ammonia is more suitable to describe Langmuir adsorption isotherm and pseudo-second reaction kinetics, R2is 0.997 and 0.998 respectively.Keywords:Natural Stellerite;Ammonium;Adsorption capacity引言:近年来,随着城市化进程的加快,化工厂废水的过度排放,使得水体中的氮元素含量过多,导致水体富营养化现象日益严重,已经成为当今世界面临的全球性的重大环境问题[1]。
农业资源与环境学报2015年6月·第32卷·第3期:250-256June 2015·Vol.32·No.3:250-256Journal of Agricultural Resources and Environment随着城市人口的日益膨胀和工农业的迅速发展,氨氮污染的来源越来越广泛,排放量也越来越大,氨氮的污染日益严重。
氨氮排入水体,容易引起水中藻类及其他微生物大置繁殖,形成富营养化污染,这不但会使水中溶解氧下降,鱼类大量死亡,严重时甚至会影响饮水安全[1-3]。
因此,去除水体中的氨氮对于防治水体富营养化和保障水产养殖生产至关重要。
天然沸石是含水多孔铝硅酸盐的总称,其结晶构造主要由(SiO )四面体组成,其中部分Si 4+为Al 3+取代,导致负电荷过剩,因此,结构中有碱金属(碱土金属)等平衡电荷的离子。
同时沸石构架中有一定孔径的空腔和孔道,决定了其具有吸附、离子交换等性质,因此其对氨氮具有很强的选择性吸附能力,因而可被应用于氨氮废水的处理[4-7]。
对沸石处理氨氮废水进行了许多研究,但是吸附动力学和等温吸附的研究结果不尽相同,尤其是对沸石饱和吸附量的研究鲜见报道[8-11],因此有必要做进一步研究。
本实验探讨了氨氮天然沸石对水中氨氮吸附特性的研究许育新,喻曼,陈喜靖,安文浩,王云龙,肖华,沈阿林(浙江省农业科学院环境资源与土壤肥料研究所,浙江杭州310021)摘要:以浙江缙云天然沸石为原料,分别用摇床和吸附柱实验研究了天然沸石对氨氮的静态和动态吸附特性。
结果显示,在10、25、40℃温度下沸石吸附氨氮有显著差异(P <0.05)。
在25℃、氨氮初始浓度为50mg ·L -1的条件下,1~2mm 沸石对氨氮的360min 吸附容量为4.05±0.02mg ·g -1。
沸石对氨氮的吸附过程遵循二级吸附动力学方程,沸石对氨氮的等温吸附可用Langmuir 和Fre -undlich 等温吸附方程拟合,相关性分析结果表明Langmuir 方程达到极显著相关(P <0.01),可以更好地描述沸石吸附氨氮的热力学过程。
沸石吸附氨氮技术研究进展摘要:介绍了沸石脱除氨氮的原理和再生机制,综述了国内外应用沸石在改良常规污水处理工艺、作为氨氮污水处理系统的介质与最终出水的氨氮控制环节等方面的研究进展。
炼油催化剂生产过程中产生的污水氨氮浓度高,先后试验了多种处理方法,但水中的氨氮很难达标。
研究经济合理的工艺去除催化剂生产污水中的氨氮是紧迫而实际的。
沸石吸附可作为组合工艺予以试验。
关键词:沸石污水处理氨氯氨氮对人体和水体具有一定的危害,水质指标中氨氮是引起水体富营养化和环境污染的一种重要污染物。
去除污水中氨氮的方法有生物硝化法、气体吹脱法和离子交换法”等.生物法无污染,耗能低,但其转换作用缓慢,去除难于彻底;气体吹脱法工艺简单,投资少,但易造成二次污染;而离子交换法却没有以上不足,且反应过程稳定、易控,吸附剂可再生利用,处理成本较低,特别是使用沸石作为吸附剂时.沸石具有稳定的硅氧四面体结构、大小均一的宽阔空间和连通孔道,能够吸附大量的氨氮,因此被认为是最有应用前景的去除氨氮吸附剂.。
鉴于沸石有着良好的吸附与离子交换性能,而我国是世界上少数几个富产沸石的国家之一,美、日等发达国家已将沸石应用在污水处理、特效干燥剂、土壤饲料改良剂等方面,而我们大部分停留在出卖原矿为主甚至干脆闲置不用。
因此加强对沸石的开发和利用研究非常必要。
沸石脱氨氮技术是近年来引起人们重视的一种生物物化相结合实现污水脱氨氮的新技术,这一技术就是把沸石对铵根离子的选择性吸附能力和生物硝化反硝化结合起来,加强生物脱氨氮系统的性能和效率一、沸石对污水中氨氮的去除机理沸石是具有四面体骨架结构的多孔性含水硅铝酸盐晶体,有良好的吸附及离子交换性能;同时沸石比表面积大,对微生物无毒害,易于附着微生物作为生物载体。
生物沸石脱氨氮工艺中,一方面沸石用于生物载体富集硝化菌;另一方面沸石通过离子交换作用吸附水中的铵,还有很重要的一方面就是沸石表面生物膜中的硝化菌将吸附在沸石上的氨氮转化为硝酸盐,形成了一个自我吸收、自我消化的循环过程。
沸石改性及其去除水中氨氮的实验研究随着水环境污染的日益严重,水质的改善已成为迫切的社会问题。
氨氮是最常见的非颗粒态污染物之一,它会伤害人类健康,破坏水体生态系统,从而影响生产和生活环境。
因此,去除水中氨氮变得十分重要。
很多研究表明,沸石是一种有效的去除水中氨氮的方法。
沸石具有优良的吸附性能,能够吸附氨氮,从而改善水质。
然而,沸石本身具有较弱的强度和耐久性,这限制了它的使用。
为了使沸石更适应水质改善的应用,一种改性技术被提出和研究,即将沸石的外表覆盖一层改性剂,以改善沸石的强度和耐久性。
近年来,沸石改性技术受到关注,被用于改善水质,特别是去除水中氨氮。
然而,沸石改性及其去除水中氨氮的研究尚未完全了解和完善。
因此,本研究旨在通过实验研究,深入探讨沸石改性技术对去除水中氨氮的作用及其原理。
首先,将沸石与多种改性剂结合,进行改性处理,以改善沸石的强度和耐久性。
其次,通过采样、样品处理、氨氮定量测定等方法,对改性沸石的吸附性能进行测试,探究其沸石改性对去除水中氨氮的作用。
结果表明,改性沸石具有良好的吸附性能,能够显著降低氨氮含量,从而改善水质。
此外,通过X射线衍射、扫描电子显微镜等方法研究了改性沸石的结构及其去除氨氮的机理。
结果表明,与未改性的沸石相比,改性沸石的表面更加粗糙疏松,比表面积更大,具有更好的吸附性能。
改性沸石的孔径表面能改变氨氮的构型,增加氨氮分子的活性位,从而有效去除水中氨氮。
综上所述,本研究表明沸石改性技术是一种有效去除水中氨氮的方法。
改性沸石具有优良的强度和耐久性,同时拥有良好的吸附性能。
此外,本研究还探讨了改性沸石去除氨氮的机理,为进一步研究和开发改性沸石技术提供了重要参考。
①动态法研究天然沸石去除氨氮效果何 杰,刘玉林(淮南工业学院,安徽淮南 232001)摘 要:本文研究了天然沸石在动态下去除N H 4-N 效果及一些影响因素。
结果表明,杂质明显影响着沸石床层的穿透点,小颗粒样品的效果优于大颗粒沸石,最小床层深度较小,特别是在低温条件下效果更显著,同时,小颗粒沸石有利于再生。
在床层压力降允许的条件下,尽可能使用小粒径沸石。
关键词:沸石;N H 4-N ;动态法;穿透曲线中图分类号:TQ 028.7 文献标识码:A 文章编号:100023770(1999)0620358204天然沸石为去除水中的N H 4-N 提供了一种行之有效的手段。
但对其离子交换过程还缺乏彻底了解,特别是动力学数据。
鉴于此,本文比较详细地研究了N H +4在天然沸石上的穿透曲线,为吸附工程设计提供了有益的帮助。
1 实验部分1.1 材 料选用皖南天然沸石矿,粉碎筛分,洗净备用。
其化学组成为:Ca 0.032K 0.030N a 0.108(Si 1.200A l 0.262Fe 0.011)O 2.917・0.356H 2O 。
1.2 装 置取一定量的沸石样品装柱,水自上而下流经床层,测定出水N H 4-N 随出水体积的变化。
1.3 N H +4浓度测定N H +4浓度采用电极法测定。
仪器:pXSJ -216型离子分析仪(上海雷磁)2 结果和讨论2.1 吸附等温线采用静态吸附法测得N H +4在沸石样品上的吸附等温线,求得N H +4在该沸石的吸附等温方程为:x m =2.68C0.71根据吸附理论,该方程的k 和1 n 值表明,N H +4在该沸石上易于交换,该沸石可以在较宽的N H +4浓度范围内使用。
2.2 水质对穿透曲线的影响分别以去离子水、自来水和经过活性炭过滤水(简称炭滤水)配制N H 4C l 溶液作为进水,第25卷 第6期1999年12月 水处理技术 T ECHNOLO GY O F WA T ER TR EA TM EN T V o l .25N o.6D ec .,1999①收稿日期:1998208207测得不同水质等条件下沸石固定床交换N H +4的穿透曲线,结果如图1所示。