氯化物原始记录
- 格式:doc
- 大小:54.00 KB
- 文档页数:2

氯化物(Cl -)指标的监测规程——硝酸银滴定法1.目的为了规范化验人员在污水处理厂中的监测方法和操作程序,提高水质监测数据的准确性,特制定本规程。
2.适用范围本监测规程适用于东莞市中堂溢源水务有限公司。
3.原理在中性或者弱碱性范围内(PH=6.5~10.5),以铬酸钾为指示剂,用硝酸银滴定氯化物时,由于氯化银的溶解度小于铬酸银的溶解度,氯离子首先被完全沉淀出来后,然后铬酸盐才以铬酸银形式沉淀出来,产生砖红色物质,指示氯离子滴定的终点达到。
沉淀滴定反应如下:()+2442Ag Ag Cl AgCl CrO AgCrO +--+→↓+→↓砖红色铬酸银离子的浓度与沉淀形成的快慢有关,必须加入足量的指示剂。
且由于有稍过量的硝酸银与铬酸钾形成铬酸银沉淀的终点较难判断,所以需要以蒸馏水作空白滴定,以作对照判断(使终点色调一致)。
4.试剂监测时氯化钠标准试剂的氯化钠应符合国家标准的基准或优级纯试剂,其他监测试剂除非另有说明,均为符合国家标准的分析纯试剂;监测用水均为蒸馏水或同等纯度的水。
4.1 氯化钠标准溶液C(NaCl)=0.0141mol/L,相当于500mg/L 氯化物含量:将基准试剂氯化钠置于坩埚内,在500~600℃加热40~50min。
在干燥器中冷却后称取8.2400g溶于蒸馏水中,在容量瓶中稀释至1000mL。
吸取10.0mL,用水定容至100mL,此溶液每毫升含0.500mg氯化物(Cl-)。
4.2 硝酸银标准溶液C(AgNO3)=0.0141mol/L:称取于105℃烘干半小时的硝酸银2.3950g,溶于蒸馏水并稀释至1000mL,贮存于棕色瓶中。
用氯化钠标准溶液标定其准确浓度,步骤如下:吸取25.00mL氯化钠标准溶液置锥形瓶中,加蒸馏水25mL。
另取一锥形瓶,取50mL蒸馏水作为空白。
各加入1mL铬酸钾溶液指示剂,在不断摇动下用硝酸银标准溶液滴定,至刚出现砖红色沉淀为终点。
计算每毫升硝酸银溶液所相当的氯化物量,然后校正其浓度,再做最后标定。

仪器:□电子天平型号:编号:试液:硝酸溶液批号:浓度:沉淀剂Ⅰ批号:沉淀剂Ⅱ批号:硫酸铁铵饱和溶液批号:硝酸银标准滴定溶液批号:浓度:硫氰酸钾标准滴定溶液批号:浓度:操作过程:试样制备:称取混合均匀的试样g(精确至1mg)于100mL具塞比色管中(V),加入50mL约70℃热水,振荡分散样品,水浴中沸腾15min,并不时摇动,取出,超声处理20min,冷却至室温,依次加入2mL沉淀剂I 和2mL沉淀剂II ,每次加后摇匀。
用水稀释至刻度,摇匀,在室温静置30min。
用滤纸过滤,弃去最初滤液,取部分滤液测定。
必要时也可用离心机于5000r/ min 离心10min,取部分上清液测定。
测定试样氯化物的沉淀:移取50.00mL上清液( V2 ),氯化物含量较高的样品,可减少取样体积,于100mL比色管中。
加入5mL硝酸溶液。
在剧烈摇动下,用酸式滴定管滴加ml 硝酸银标准滴定溶液,用水稀释至刻度,在避光处静置5min。
用快速滤纸过滤,弃去10mL 最初滤液。
加入硝酸银标准滴定溶液后,如不出现氯化银凝聚沉淀,而呈现胶体溶液时,应在定容、摇匀后,置沸水浴中加热数分钟,直至出现氯化银凝聚沉淀。
取出,在冷水中迅速冷却至室温,用快速滤纸过滤,弃去10mL最初滤液。
过量硝酸银的滴定:移取50.00mL滤液于250mL锥形瓶中,加入2mL硫酸铁铵饱和溶液。
边剧烈摇动边用0.1mol/ L 硫氰酸钾标准滴定溶液滴定,淡黄色溶液出现乳白色沉淀,终点时变为淡棕红色,保持1min不褪色。
记录消耗硫氰酸钾标准滴定溶液的体积(V1 )。
同时做空白试验,记录消耗硫氰酸钾标准滴定溶液的体积(V0)检验人:日期:复核人:日期:。
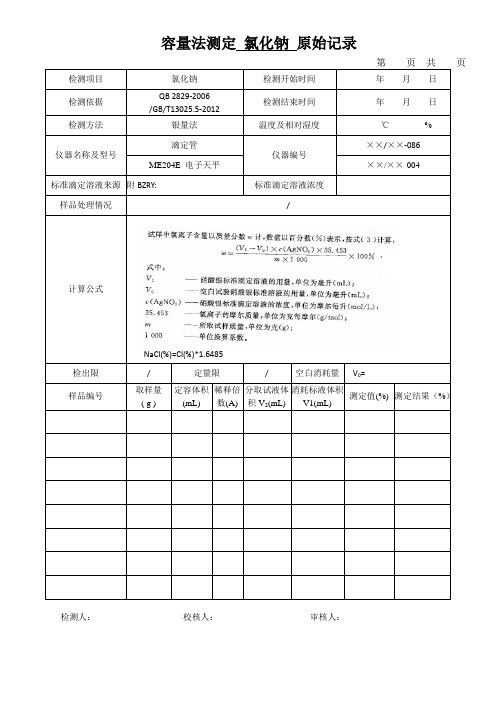
容量法测定氯化钠原始记录
页检测项目氯化钠检测开始时间年月日
检测依据
QB 2829-2006
/GB/T13025.5-2012
检测结束时间年月日
检测方法银量法温度及相对湿度℃%
仪器名称及型号
滴定管
仪器编号
××/××-086 ME204E 电子天平××/××-004
标准滴定溶液来源附BZRY: 标准滴定溶液浓度样品处理情况/
计算公式
NaCl(%)=Cl(%)*1.6485
检出限/ 定量限/ 空白消耗量V0=
样品编号取样量
( g )
定容体积
(mL)
稀释倍
数(A)
分取试液体
积V2(mL)
消耗标液体积
V1(mL)
测定值(%) 测定结果(%)
检测人:校核人:审核人:
容量法测定氯化物原始记录
页
检测人:校核人:审核人:
容量法测定氯化物原始记录(续表)
页
检测人:校核人:审核人:。



二次供水检测原始记录
检验项目:氯化物检验日期:年月日
检验方法:硝酸汞容量法室内温度:℃室内湿度: % 检验依据:《生活饮用水标准检验方法》GB/T 5750.5.2—2006
1.试剂
标准溶液(自配)浓度:c[1/2Hg(NO3)2]= mol/L ;配制过程:称取g硝酸汞溶于含mL 硝酸(ρ20=1.42g/mL)的纯水中,用纯水稀释至mL;c(NaCl)= mol/L :配制过程:称取经700℃烧灼1h的氯化钠(NaCl)g,溶于纯水中并稀释至mL。
吸取mL,用纯水稀释至mL。
2. 仪器:锥形瓶,250mL;滴定管,25mL;无分度吸管,50mL。
3. 分析步骤
3.1水样的预处理
3.2取氯化钠标准溶液25.00mL加纯水至50mL,水样及纯水各50mL,分别置于250mL锥形瓶中,加0.2mL指示剂,用硝酸(1.0mol/L)调节水样PH值,使溶液由蓝色变成纯黄色,再加硝酸(0.1mol/L)0.6mL,此时溶液PH值为3.0±0.2。
3.3用硝酸汞标准溶液滴定,当溶液呈淡橙红色,泡沫呈紫色时即为终点。
记录氯化钠标准溶液消
耗硝酸汞的量V1mL,水样消耗硝酸汞的量V2;标定时,纯水消耗硝酸汞的量V0 mL。
滴定样品时,纯水消耗硝酸汞的量V0′ mL。
4结果计算
硝酸汞标准溶液的浓度:m=错误!未找到引用源。
= mg/mL
m—1.00mL硝酸汞标准溶液相当于以mg表示的氯化物(Cl-)质量
V0—标定时,纯水消耗硝酸汞的体积,mL
V1—滴定氯化物标准溶液消耗的硝酸汞的体积,mL
校正硝酸汞标准溶液浓度,使1.00ml含氯化物0.50mg:需取纯水mL加原硝酸汞标准溶液定容至mL。
氯化物计算公式:ρ(Cl-)=错误!未找到引用源。
ρ(Cl-)—水样中氯化物的质量浓度,mg/L
V—水样体积,mL
V0′—滴定空白消耗的硝酸汞的体积,mL
V2—滴定氯化物标准溶液消耗的硝酸汞的体积,mL
检验者:复核者:
日期:年月日日期:年月日
本法检出限: 1.0mg/L
检验者:复核者:
日期:年月日日期:年月日。