(完整版)标准滴定溶液的配制与标定记录
- 格式:doc
- 大小:14.34 KB
- 文档页数:1

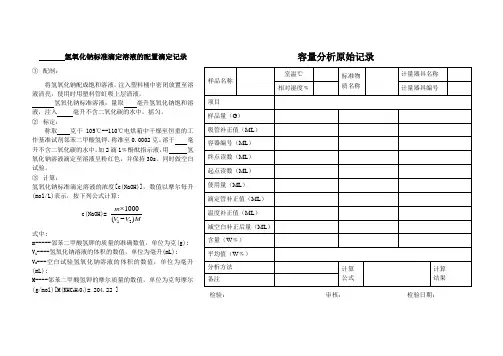
氢氧化钠标准滴定溶液的配置滴定记录 ① 配制:将氢氧化钠配成饱和溶液,注入塑料桶中密闭放置至溶液清亮,使用时用塑料管虹吸上层清液。
氢氧化钠标准溶液:量取 毫升氢氧化钠饱和溶液,注入 毫升不含二氧化碳的水中,摇匀。
② 标定:称取 克于105℃--110℃电烘箱中干燥至恒重的工作基准试剂邻苯二甲酸氢钾,称准至0.0002克。
溶于 毫升不含二氧化碳的水中,加2滴1﹪酚酞指示液,用 氢氧化钠溶液滴定至溶液呈粉红色,并保持30s 。
同时做空白试验。
③ 计算:氢氧化钠标准滴定溶液的浓度[c(NaOH)],数值以摩尔每升(mol/L)表示,按下列公式计算:c(NaOH)=121000()m V V M⨯-式中:m-----邻苯二甲酸氢钾的质量的准确数值,单位为克(g); V 1----氢氧化钠溶液的体积的数值,单位为毫升(mL); V 2---空白试验氢氧化钠溶液的体积的数值,单位为毫升(mL);M----邻苯二甲酸氢钾的摩尔质量的数值,单位为克每摩尔(g/mol)[M(KHC 8H 404)= 204.22 ]容量分析原始记录检验: 审核: 检验日期:盐酸标准滴定溶液的配置滴定记录① 配制:盐酸标准溶液,量取 毫升盐酸,注入 毫升水中。
② 标定:称取 克于270℃--300℃高温炉中灼烧至恒重的工作基准试剂无水碳酸钠,称准至0.0002克。
,溶于50mL 水中,加10滴溴甲酚绿一甲基红指示液,用配制好的盐酸溶液滴定至溶液由绿色变为暗红色,煮沸2min ,冷却后继续滴定至溶液再呈暗红色,同时做空白试验。
③ 计算:盐酸标准滴定溶液的浓度[c(HCl)]数值以摩尔每升(mol/L)表示,按下列公式计算:c(HCl)=121000()m V V M⨯-式中:m----无水碳酸钠的质量的准确数值,单位为克(g) V 1---盐酸溶液的体积的数值,单位为毫升(mL)V 2---空白试验盐酸溶液的体积的数值,单位为毫升(mL) M---无水碳酸钠的摩尔质量的数值,单位为克每摩尔(g/mol)[M (12Na 2CO 3)=52.994]容量分析原始记录检验: 审核: 检验日期:硫酸标准滴定溶液的配置滴定记录①配制:硫酸标准溶液,量取毫升硫酸,注入毫升水中。

硫酸标准溶液的配制和标定1.各浓度硫酸标准滴定溶液的配制按表1所示,量取硫酸慢慢注入600mL烧杯内的400mL水中,混匀。
冷却后转移入1L量瓶中,用水稀释至刻度,混匀。
贮存于密闭的玻璃容器内。
表 1 量取硫酸体积硫酸标准滴定溶液浓度mol/L 配制1L硫酸溶液所需硫酸体积mL0.05 1.50.1 3.00.2 6.00.5 15.01.0 30.02.标定按表2所示,准确称量已在270-300℃干燥过4h的基准无水碳酸钠分别置于250mL锥形瓶中,各加入蒸馏水50mL使其溶解,再加2滴甲基红指示液,用硫酸溶液滴定至红色刚出现,小心煮沸溶液至红色褪去,冷却至室温。
继续滴定、煮沸、冷却,直至刚出现的微红色在再加热时不褪色为止。
表 2 标定所需无水碳酸钠质量硫酸标准滴定溶液浓度mol/L 无水碳酸钠质量g0.05 0.11±0.0010.1 0.22±0.010.2 0.44±0.010.5 1.10±0.011.02.20±0.013.计算硫酸标准滴定溶液浓度按式(1)计算:c(1/2H2SO4)=m/0.05299×V式中:硫酸标准滴定溶液之物质的量浓度,mol/L;c(1/2H2SO4)──m──称量无水碳酸钠质量,g;V──滴定用去硫酸溶液实际体积,mL;0.05299──与1.00mL硫酸标准滴定溶液〔c(1/2H2SO4)=1.000mol/L〕相当的以克表示的无水碳酸钠的质量。
4.精密度做五次平行测定。
取平行测定的算术平均值为测定结果。
五次平行测定的极差,应小于表3规定的容许差r。
表3 硫酸标准滴定溶液标定的容许差c,mol/L 0.05 0.1 0.2 0.5 1.0r,mol/L 0.000 200 0.000 30 0.000 40 0.001 00 0.002 0 硫酸标准滴定溶液每月重新标定一次。
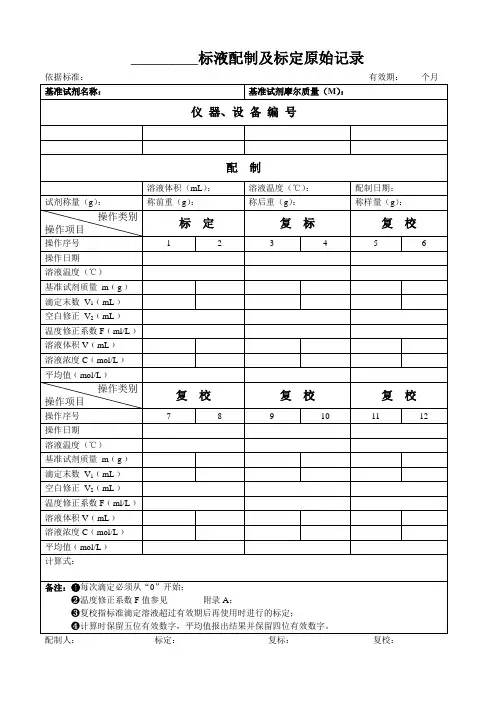
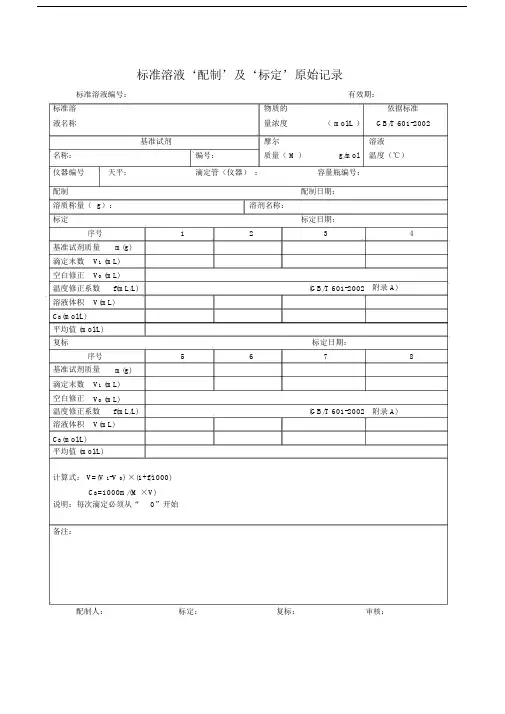
标准溶液‘配制’及‘标定’原始记录标准溶液编号:有效期:标准溶物质的依据标准液名称量浓度( mol/L )GB/T 601-2002基准试剂摩尔溶液名称:编号:质量( M )g/mol温度(℃)仪器编号天平:滴定管(仪器):容量瓶编号:配制配制日期:溶质称量( g):溶剂名称:标定标定日期:序号1234基准试剂质量m(g)滴定末数V1 (mL)空白修正V0 (mL)温度修正系数f(mL/L)(GB/T 601-2002附录 A)溶液体积V(mL)C B(mol/L)平均值 (mol/L)复标标定日期:序号5678基准试剂质量m(g)滴定末数V1 (mL)空白修正V0 (mL)温度修正系数f(mL/L)(GB/T 601-2002附录 A)溶液体积V(mL)C B(mol/L)平均值 (mol/L)计算式: V=(V 1-V 0) ×(1+f/1000)C B=1000m/(M ×V)说明:每次滴定必须从“0”开始备注:配制人:标定:复标:审核:标准物质配制(标定)记录编号: CHEC/ QBG-075名称:、配制方法:使用天平型号编号室温℃、湿度%RH配制:取定溶mL标定:取份:⑴⑵⑶⑷用溶液滴定,滴定消耗量( mL)V1=、 V2=、 V3=、V4=、V0=。
标准溶液浓度计算公式: C=计算结果():C1=C2=C3=C4= C =相对偏差( %):S1=S2=S3=S4=备注:。
配制人:复核人:配制日期:年月日有效期年月日标准溶液配制记录编号: CHEC/QBG-147标准溶液名称:规格:配制方法:仪器名称:溯源标准:温度:℃、湿度:%RH标准溶液拟配浓度:配制或稀释过程:配制日期:年月日有效期:年月日配制人:复核人:0.1mol/L盐酸标准滴定溶液的标定编号: JL/LJ-001-01一、标定方法: GB/T5009.1-2003二、使用仪器: AEL-200 电子天平(仪器编号: JYB001)马弗炉 (仪器编号:JYC009)三、操作1、量取 9ml 盐酸,加适量水并稀释至 1000ml 。
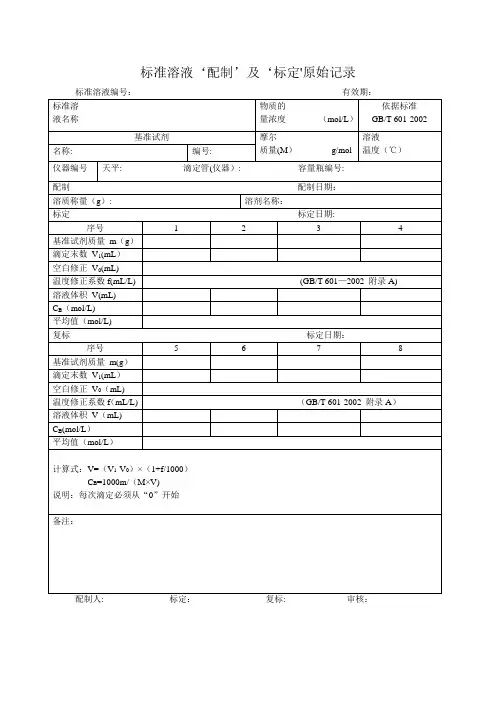
标准溶液‘配制’及‘标定'原始记录配制人: 标定:复标: 审核:标准物质配制(标定)记录编号: CHEC/QBG-075名称:、配制方法:使用天平型号编号室温℃、湿度%RH 配制:取定溶mL 标定:取份:⑴⑵⑶⑷用溶液滴定,滴定消耗量(mL) V1= 、V2= 、V3= 、V4= 、V0= 。
标准溶液浓度计算公式:C=计算结果():C1= C2= C3= C4= C =相对偏差(%):S1= S2= S3= S4=备注:.配制人:复核人:配制日期:年月日有效期年月日标准溶液配制记录编号: CHEC/QBG—147标准溶液名称:规格:配制方法:仪器名称:溯源标准:温度: ℃、湿度:%RH标准溶液拟配浓度:配制或稀释过程:配制日期:年月日有效期:年月日配制人:复核人:0。
1mol/L盐酸标准滴定溶液的标定编号:JL/LJ-001-01一、标定方法:GB/T5009。
1-2003二、使用仪器:AEL—200电子天平(仪器编号:JYB001)马弗炉(仪器编号:JYC009)三、操作1、量取9ml盐酸,加适量水并稀释至1000ml。
混匀,待标定.2、标定:精密称取约0.15g在270~300℃干燥至恒量的基准无水碳酸钠,加50ml水使之溶解,加10滴溴甲酚绿-甲基红混合指示液,用本溶液滴定至溶液由绿色转变为紫红色,煮沸2min,冷却至室温,继续滴定至溶液由绿色变为暗紫色.四、记录和结果1、计算公式:c(HCl)=m/[(V1-V2)×0。
0530]0。
0530……与1.00ml盐酸标准滴定溶液[c(HCl)=1mol/L]相当的基准无水碳酸钠的质量,g配制人: 复核人:配制日期:复核日期:标准溶液(滴定液)管理工作的基本要求关键词(必填项目):标准溶液、滴定液目的(必填项目):对标准溶液的使用等制定统一的要求,便于统一的管理.背景知识(选填项目):无。
原理(选填项目):无主体内容(操作步骤,必填项目):1 内容1.1 标准溶液的配制1.1。
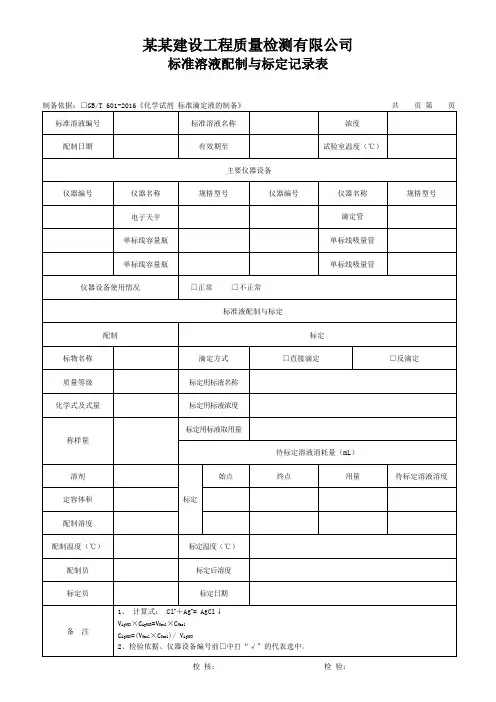

edta标准溶液的配制和标定数据记录 EDTA(乙二胺四乙酸)是一种常用的配位试剂,广泛应用于化学分析和环境监测等领域。
为了准确测定目标物质的含量,必须配制和标定EDTA标准溶液。
本文将详细描述EDTA标准溶液的配制过程和标定数据记录方法,以期为读者提供准确、可靠的实验结果。
一、EDTA标准溶液的配制1. 根据实验需求确定所需浓度和体积。
2. 准备清洁、干燥的容器,精确称量所需质量的EDTA固体。
注:应使用分析纯的EDTA以确保溶液的纯度和精确度。
3. 将EDTA固体加入容器中,加入适量的去离子水溶解,定容至所需体积。
注:在溶解过程中应充分搅拌,确保EDTA充分溶解并均匀分布。
二、EDTA标准溶液的标定1. 标定前的准备工作:a. 清洁、干燥容器,准备所需量的标定溶液。
b. 根据实验需求,选择相应的指示剂和溶剂。
c. 准备一定浓度的化学指示剂溶液(例如:钙碳酸盐指示剂等)。
d. 准备一定浓度的酸溶液(例如:0.1 mol/L盐酸溶液)用于调节溶液的pH值。
e. 清洁、干燥滴定管和滴定管架。
2. 标定过程: a. 取一定体积的待测样品(例如:10 mL)加入滴定瓶中。
b. 加入适量的酸溶液调节待测样品的pH值。
确保待测样品中没有其他影响滴定反应的离子。
c. 加入一定体积的化学指示剂溶液,使其与待测样品反应产生可观察的颜色变化。
d. 使用滴定管分次向待测样品中滴定EDTA标准溶液,直至颜色变化,记录滴定所用的EDTA标准溶液的体积(V1)。
e. 等颜色变化稳定后,再缓慢滴定,直到颜色消失,记录滴定所需的EDTA标准溶液的体积(V2)。
f. 重复上述滴定步骤2-3次,计算平均用量,提高测量结果的准确性。
三、标定数据记录 1. 记录待测样品用量、酸溶液浓度、化学指示剂体积以及EDTA 标准溶液滴定数据。
例如:待测样品用量:10 mL,酸溶液浓度:0.1 mol/L,化学指示剂体积:2 mL,EDTA标准溶液滴定体积:V1 = 8.5 mL,V2 = 12.3 mL。
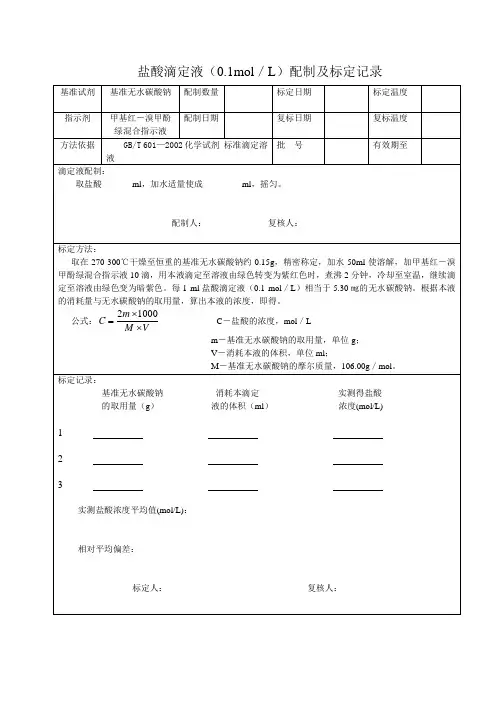

标准溶液的配制和标定方法品控中心一、氢氧化钠标准溶液的配制和标定(依据国标GB/T5009.1-2003)C(NaOH)= 1mol/LC(NaOH)= 0.5mol/LC(NaOH)= 0.313mol/LC(NaOH)= 0.1mol/L(一)氢氧化钠标准溶液的配制:称取 120gNaOH,溶于 100mL无 CO2的水中,摇匀,注入聚乙烯容器中,密闭放置至溶液清亮。
用塑料管吸取下列规定体积的上层清液,注入用无 CO2的水稀释至1000mL,摇匀。
C(NaOH), mol/L NaOH饱和溶液, mL1560.5280.31317.5280.1 5.6(二)氢氧化钠标准溶液的标定:1.测定方法:称取下列规定量的、于 105—110。
C电烘箱烘至恒重的工作基准试剂邻苯二甲酸氢钾,称准至 0.0001 g ,溶于下列规定体积的无 CO2的水中,加 2 滴酚酞指示液( 10 g/L ),用配制好的 NaOH溶液滴定至溶液呈粉红色并保持 30S。
同时做空白试验。
C(NaOH),mol/L基准邻苯二甲酸氢钾 ,g无 CO水 ,mL21 6.0800.5 3.0800.313 1.878800.10.6802.计算:氢氧化钠标准溶液浓度按下式计算:MC( NaOH)= ------------------------(V—V0)× 0.2042式中: C(NaOH)——氢氧化钠标准溶液之物质的浓度,mol/L ;V——消耗氢氧化钠的量,mL;V0——空白试验消耗氢氧化钠的量,mL;M——邻苯二甲酸氢钾的质量,g;0.2042 ——邻苯二甲酸氢钾的摩尔质量。
Kg/ mol 。
二、盐酸标准溶液的配制和标定(依据国标 GB/T5009.1-2003)C(HCl)= 1mol/LC(HCl)= 0.5mol/LC(HCl)= 0.1mol/L(一)盐酸标准溶液的配制:量取下列规定体积的盐酸,注入1000 mL 水中,摇匀。

氢氧化钠标准溶液配制与标定一、配制:将氢氧化钠配成饱和溶液,注入塑料桶中密闭放置至溶液清亮,使用前以塑料管虹吸上层清液。
浓度氢氧化钠饱和溶液注入不含CO2的水0.1mol/L量取5ml1000中摇匀0.2mol/L量取10ml1000中摇匀0.5mol/L量取26ml1000中摇匀1.0mol/L量取52ml1000中摇匀二、标定:1、原理: KHC8H4O4+NOH→KNaC8H4O4+H2O酸式酚酞碱式酚酞HIn→In-+H+(无色)(红色)酚酞为一有机弱酸,在酸性溶液中为无色,当碱色离子增加到一定浓度时,溶液即呈粉红色。
2、仪器:滴定管50ml;三角瓶250ml。
3、标定过程0.1mol/LNOH标准溶液称取0.4-0.6克;0.2mol/L称1-1.2克;0.5mol/L称取3克于105-110℃烘至恒重的苯二甲酸氢钾,称准至0.0002克,分别溶于50ml;80ml不含二氧化碳水中,加2滴1%酚酞指示剂,用配好的待标定溶液至溶液呈粉红色与标准色相同。
同时作空白试验。
4、计算:C(NaOH)=m / (V1-V2)*0.2042C(NaOH)---氢氧化钠溶液浓度 m——苯二甲酸氢钾之质量(克)V1——氢氧化钠溶液用量(毫升) V2——空白氢氧化钠溶液用量(毫升)0.2042——与1.000mol/LNOH标准溶相当的以克表示的当量苯二甲酸氢钾之质量5、注意事项:1、为使标定的浓度准确,标定后应用相应浓度盐酸对标。
2、液溶有效期2个月。
3、氢氧化钠饱和溶液之配制:于1000硬质容器中,加70毫升水,逐渐加入700克氢氧化钠。
随加随搅拌,使溶解完全冷却后移入盛氢氧化钠饱和液之试药瓶中,以胶塞密塞,静置7天以上,使含之碳酸钠沉淀完全。
取澄清之氢氧化钠饱和液少1.1.配制 C(1/2Br2)=0.1 mol/L 称取3克溴酸钾及25克溴化钾,于1000ml水中,摇均。
1.2. 标定量取35.00ml--40.00ml配置好的溴溶液,置于碘量瓶中,溶于25毫升水,加2克碘化钾及5毫升盐酸溶液(20%),摇均,于暗处放置5分钟,加150毫升水(15℃--20℃)用0.1mol/L硫代硫酸钠标准滴定液滴定,近终点时加2毫升淀粉指示液(10g/L),继续滴定至溶液蓝色消失。
标准溶液配制记录一、实验目的。
本实验旨在记录标准溶液的配制过程,以及相关实验数据,为后续实验提供准确可靠的参考依据。
二、实验原理。
标准溶液是已知浓度的溶液,通常用于分析化学中的定量分析。
在配制标准溶液时,需要根据溶质的化学性质和实验要求,选择适当的溶剂和溶质的质量,按照一定的比例配制而成。
三、实验步骤。
1. 准备实验所需的试剂和仪器设备,包括天平、容量瓶、移液管等。
2. 根据实验要求,选择合适的溶剂和溶质,并按照所需的浓度比例进行称量。
3. 将称量好的溶质溶解于适量的溶剂中,摇匀使其充分溶解。
4. 用容量瓶将溶液定容至刻度线,摇匀混合。
5. 将配制好的标准溶液转移至干净的密封瓶中,标注好溶液的名称、浓度、配制日期等信息。
四、实验数据记录。
| 溶质 | 质量/g | 溶剂 | 体积/mL | 浓度/mol/L | 配制日期 |。
|------|--------|------|---------|------------|----------|。
| NaCl | 5.85 | 水 | 1000 | 0.1 |2022/03/15|。
| KCl | 7.20 | 水 | 1000 | 0.2 |2022/03/16|。
五、实验结果分析。
通过本次实验的记录数据,我们成功配制出了两种浓度不同的标准溶液,分别为0.1mol/L的NaCl溶液和0.2mol/L的KCl溶液。
在实验过程中,我们严格按照配制步骤进行操作,确保了实验结果的准确性和可靠性。
六、实验总结。
本次实验记录了标准溶液的配制过程和相关数据,为后续实验提供了重要的参考依据。
在实验中,我们需要严格按照配制步骤进行操作,确保实验结果的准确性和可靠性。
同时,对于配制好的标准溶液,我们也需要做好标注和保存工作,以便后续实验的使用。
七、实验注意事项。
1. 在配制标准溶液时,需要准确称量溶质和溶剂,严格按照比例进行配制。
2. 配制好的标准溶液需要标注清楚名称、浓度、配制日期等信息,并保存在干净的密封瓶中。