大学化学上册作业题及答案
- 格式:doc
- 大小:265.00 KB
- 文档页数:21

《大学化学(上册)》作业题专业____________ 班别______________ 学号____________ 姓名______________基础化学部无机及分析教研室编2008 秋绪论4•正确地修约下列数据:(1)37.800至3位;(2)72.75至3位;(3)90.045至4位;(4)125.550 至4 位;5.以正确的有效位数给出下列算式的结果:(1) 50.00X 27.80 X 0.1167;(2) (2.776X 0.0050) -6.7 X 10-3+ ( 0.036 X 0.0271)3.10 21.14 5.10(3)0.00112024.16 (9.85-4.3) 5.6715.839 14.238第10章实验误差和数据处理2.重复分析一银合金试样,测得银的质量分数分别为95.67%, 95.61% , 95.71%和95.60%。
试计算:⑴均差;(2)标准差;(3)变异系数。
3.现对一种煤的含水量做了4次测定,测得水的质量分数为18.3%, 18.9 %,17.7 %和18.6%,试求在置信水平95%时的置信区间。
5.为检验一种新的分析方法的有效性,现采用一种钙的质量分数 3 (Ca)=21.20% (真实值口)的标样以新方法进行分析,若X = —(Ca)= 21.24%, s=0.12% , n=10。
试问X与口的置信水平90%和95%时,是否存在显著差异?8现有两个含铀试样的测定结果如下:试样 1 10.32%, 10.39%, 10.19%, 10.21 %试样 2 10.45%, 10.41%, 10.51%, 10.36%, 10.34%, 10.39%试问在置信水平95%时,两试样有无显著性差异?9 用Q 检验法检测下列结果: 6.02 , 7.28, 7.32, 7.02, 7.92, 7.12, 7.32, 7.22。
11某生对一含硫酸根试样做了4次测定,得到硫酸根的质量分数分别为9.35%, 9.29%, 9.38%和9.27%。

无机化学(第四版)答案第一章物质的结构1-1 在自然界中氢有三种同位素,氧也有三种同位素,问:总共有种含不同核素的水分子?由于3H太少,可以忽略不计,问:不计3H时天然水中共有多少种同位素异构水分子?1-2 天然氟是单核素(19F)元素,而天然碳有两种稳定同位素(12C和13C),在质谱仪中,每一质量数的微粒出现一个峰,氢预言在质谱仪中能出现几个相应于CF4+的峰?1-3 用质谱仪测得溴得两种天然同位素的相对原子质量和同位素丰度分别为79Br 789183占50。
54%,81Br 80。
9163占49。
46%,求溴的相对原子质量(原子量)。
1-4 铊的天然同位素203Tl和205Tl的核素质量分别为202。
97u和204。
97u,已知铊的相对原子质量(原子量)为204。
39,求铊的同位素丰度。
1-5 等质量的银制成氯化银和碘化银,测得质量比m(AgCl):m(AgBr)=1。
63810:1,又测得银和氯得相对原子质量(原子量)分别为107。
868和35。
453,求碘得相对原子质量(原子量)。
1-6 表1-1中贝采里乌斯1826年测得的铂原子量与现代测定的铂的相对原子质量(原子量)相比,有多大差别?1-7 设全球有50亿人,设每人每秒数2个金原子,需要多少年全球的人才能数完1mol金原子(1年按365天计)?1-8 试讨论,为什么有的元素的相对质量(原子量)的有效数字的位数多达9位,而有的元素的相对原子质量(原子量)的有效数字却少至3~4位?1-9 太阳系,例如地球,存在周期表所有稳定元素,而太阳却只开始发生氢燃烧,该核反应的产物只有氢,应怎样理解这个事实?1-10 中国古代哲学家认为,宇宙万物起源于一种叫“元气”的物质,“元气生阴阳,阴阳生万物”,请对比元素诞生说与这种古代哲学。
1-11 “金木水火土”是中国古代的元素论,至今仍有许多人对它们的“相生相克”深信不疑。
与化学元素论相比,它出发点最致命的错误是什么?1-12 请用计算机编一个小程序,按1.3式计算氢光谱各谱系的谱线的波长(本练习为开放式习题,并不需要所有学生都会做)。

无机化学第五版上册答案北京师范大学华中师范1、纸色谱是分配色谱中的一种,它是以滤纸为(),以纸上所含的水分为固定相的分配色谱。
()[单选题] *A固定相B吸附剂C展开剂D支持剂(正确答案)2、以橙皮苷为指标成分进行定性鉴别的中药是()[单选题] *A葛根B黄芩C槐花D陈皮(正确答案)3、以下哪种分离方法是利用分子筛的原理的()[单选题] *A吸附色谱法B萃取法C沉淀法D透析法(正确答案)4、沉淀法的分类不包括以下哪一种方法()[单选题] *A水提醇沉法B碱提酸沉法C铅盐沉淀法D结晶法(正确答案)5、下列关于香豆素的说法,不正确的是()[单选题] *A游离香豆素多具有芳香气味B分子量小的香豆素有挥发性和升华性C香豆素苷多无香味D香豆素苷多无挥发性,但有升华性(正确答案)6、从香豆素类的结构与分类看,下列属于简单香豆素类的是()[单选题] * A龙脑B七叶内酯(正确答案)C薄荷醇D西瑞香素7、中药紫草中的主要有效成分属于()[单选题] *A苯醌类B萘醌类(正确答案)C蒽醌类D菲醌类8、凡具有()的木脂素,与三氯化铁反应,呈阳性()[单选题] * A酚羟基(正确答案)B羧酸C醇羟基D氨基9、区别挥发油与油脂常用的方法是()[单选题] *A相对密度B溶解性C油迹试验(正确答案)D沸点10、有机溶剂加热提取中药成分应采用()[单选题] *A回流装置(正确答案)B蒸馏装置C萃取装置D分馏装置11、香豆素与浓度高的碱长时间加热生成的产物是()[单选题] *A脱水化合物B顺式邻羟基桂皮酸(正确答案)C反式邻羟基桂皮酸D醌式结构12、苯丙素类的基本母核是具有一个或数个()单元的天然化合物()[单选题] *AC6-C3基团(正确答案)BC6-C6基团CC5-C3基团DC8-C8基团13、当一种溶剂无法结晶时,常常使用混合溶剂,下列不是常用的混合溶剂是()[单选题] *A甲醇-水B乙酸-水C乙醚-丙酮D石油醚-水(正确答案)14、在结晶溶剂的选择过程中首先要遵循的是()[单选题] * A成分的纯度(正确答案)B相似相容原理C冷却热饱和原理D以上都不对15、阿托品的结构类型是()[单选题] *A喹啉类B异喹啉类C莨菪烷类(正确答案)D苄基异喹啉类16、提取遇热不稳定的成分宜用()[单选题] *A回流法B煎煮法C渗漉法(正确答案)D蒸馏法17、以葛根素为指标成分进行定性鉴别的中药是()[单选题] * A葛根(正确答案)B黄芩C槐花D陈皮18、中药补骨脂中的补骨脂内脂具有()[单选题] * A抗菌作用B光敏作用(正确答案)C解痉利胆作用D抗维生素样作用19、下列生物碱碱性最强的是()[单选题] * APkA=22BPkA=5(正确答案)CPkA=13DPkA=5820、检识黄酮类化合物首选()[单选题] *A盐酸-镁粉反应(正确答案)B四氢硼钠反应C硼酸显色反应D锆盐-枸橼酸反应21、具有升华性的生物碱是()[单选题] *A烟碱B咖啡因(正确答案)C槟榔碱D苦参碱22、倍半萜和二萜在化学结构上的明显区别是()[单选题] *A氮原子数不同B碳原子数不同(正确答案)C碳环数不同D硫原子数不同23、具有酚羟基或羧基的游离蒽醌类成分有一定酸性,可用的提取方法是()[单选题]* A酸溶碱沉法B碱溶酸沉法(正确答案)C水提醇沉法D醇提水沉法24、不属于木脂素类化合物的物理性质的是()[单选题] *A一般没有挥发性B有光学活性C易溶于有机溶剂D有色晶体(正确答案)25、结晶法一般是在分离纯化物质的哪个阶段常常使用的()[单选题] *A开始B中期C最后(正确答案)D以上均可26、由两个苯环通过三碳链相互连接成的具有6C-3C-6C基本骨架的一系列化合物是()[单选题] *A苷类B黄酮类(正确答案)C醌类D生物碱类27、苯丙素类化合物的生物合成途径是()[单选题] *A醋酸-丙二酸途径B丙二酸途径C莽草酸途径(正确答案)D氨基酸途径28、具有挥发性的香豆素成分是()[单选题] *A游离小分子简单香豆素(正确答案)B香豆素苷C呋喃香豆素D双香豆素29、南五味子保肝的主要效药效成分是()[单选题] *A蒽醌B香豆素C黄酮D木脂素(正确答案)30、黄酮母核具有的下列何种结构特点在碱液中不稳定()[单选题] * A邻二酚羟基(正确答案)B3-羟基C5-羟基D7-羟基。

第一章化学反应基本规律1、在标准态的规定中,下述表达不正确的是( )A、标准压力PӨ=100.00KPaB、T=298.15KC、bӨ=1.00mol·kg-1D、纯固体或纯液体处于标准压力。
2、在标准条件下,下列反应式中能表示CO2的Δf H mӨ(298.15K)的反应式为( )A、C(金刚石)+ O2(g)= CO2(g)B、C(石墨)+O2(g)= CO2(g)C、CO(g)+1/2O2(g)= CO2(g)D、CO2(g)=CO(g)+1/2O2(g)3、已知下列反应在一定温度下的热效应:4Fe2O3(s)+Fe(s)=3Fe3O4(s), Δr H mӨ=-74 kJ·mol-14Fe(s)+3O2(g)=2Fe2O3(s), Δr H mӨ=-1664kJ·mol-1则可计算出Fe3O4(s)的标准摩尔生成焓等于( )4、等压过程,高温非自发,低温自发的条件是( )5、等温条件下,某反应Δr G mӨ=10kJ·mol-1,这表示该反应在标准状态下( )A、自发进行B、非自发进行C、自发与否,需具体分析6、汽车尾气中的CO,可用加入催化剂催化其热分解的方法消除。
已知热分解反应CO(g)= C(s)+O2(g)的Δr H mӨ=110.5kJ·mol-1,Δr S mӨ=-0.089kJ·mol-1·K-1这一方法正确与否?解释其原因:7、(1)U,S,H,G均为( )(2)Δr H m>0为( )(3)Δr G m <0为( )(4)KӨ为( )8、反应的Δr H mӨ <0,温度升高时(T2>T1)则平衡常数( )当Δr H mӨ>0,温度升高时则( )9、碳燃烧反应为基元反应,其方程式为C(s)+O2 (g)→CO2 (g)则其反应速率方程式为( )A、υ=kc(C)c(CO2)B、υ=kc(O2)c(CO2)C、υ=kc(CO2)D、υ=kc(O2)10、升高温度,可增加反应速度,主要因为( )A、增加了分子总数B、增加了活化分子百分数C、降低了活化能D、促进平衡向吸热方向移动11、已测得高温时焦炭与二氧化碳反应C+CO2→2CO的活化能为167kJ·mol-1。

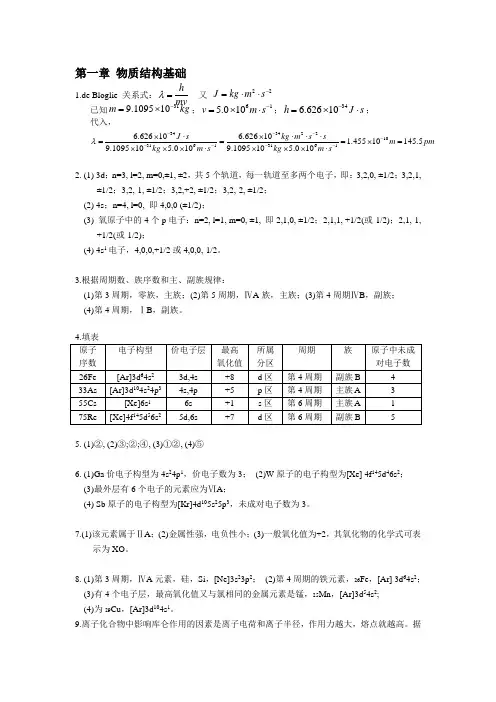
第一章 物质结构基础1.de Bloglie 关系式:hmv λ=又 22J kg m s -=⋅⋅ 已知319.109510m kg -=⨯;615.010v m s -=⨯⋅;346.62610h J s -=⨯⋅;代入,34342210316131616.62610 6.62610 1.45510145.59.109510 5.0109.109510 5.010J s kg m s sm pm kg m s kg m sλ--------⨯⋅⨯⋅⋅⋅===⨯=⨯⨯⨯⋅⨯⨯⨯⋅2. (1) 3d ;n=3, l=2, m=0,±1, ±2,共5个轨道,每一轨道至多两个电子,即:3,2,0, ±1/2;3,2,1,±1/2;3,2,-1, ±1/2;3,2,+2, ±1/2;3,2,-2, ±1/2; (2) 4s ;n=4, l=0, 即4,0,0 (±1/2);(3) 氧原子中的4个p 电子:n=2, l=1, m=0, ±1, 即2,1,0, ±1/2;2,1,1, +1/2(或-1/2);2,1,-1,+1/2(或-1/2);(4) 4s 1电子,4,0,0,+1/2或4,0,0,-1/2。
3.根据周期数、族序数和主、副族规律:(1)第3周期,零族,主族;(2)第5周期,ⅣA 族,主族;(3)第4周期ⅣB ,副族; (4)第4周期,ⅠB ,副族。
5. (1)②, (2)③;②;④, (3)①②, (4)⑤6. (1)Ga 价电子构型为4s 24p 1,价电子数为3; (2)W 原子的电子构型为[Xe] 4f 145d 46s 2; (3)最外层有6个电子的元素应为ⅥA ;(4) Sb 原子的电子构型为[Kr]4d 105s 25p 3,未成对电子数为3。
7.(1)该元素属于ⅡA ;(2)金属性强,电负性小;(3)一般氧化值为+2,其氧化物的化学式可表示为XO 。

无机化学(第四版)答案第一章物质得结构1-1在自然界中氢有三种同位素,氧也有三种同位素,问:总共有种含不同核素得水分子?由于3H太少,可以忽略不计,问:不计3H时天然水中共有多少种同位素异构水分子?1-2 天然氟就是单核素(19F)元素,而天然碳有两种稳定同位素(12C与13C),在质谱仪中,每一质量数得微粒出现一个峰,氢预言在质谱仪中能出现几个相应于CF4+得峰?1—3用质谱仪测得溴得两种天然同位素得相对原子质量与同位素丰度分别为79Br 789183占50、54%,81Br 80。
9163占49。
46%,求溴得相对原子质量(原子量)。
1-4 铊得天然同位素203Tl与205Tl得核素质量分别为202、97u与204、97u,已知铊得相对原子质量(原子量)为204。
39,求铊得同位素丰度。
1-5 等质量得银制成氯化银与碘化银,测得质量比m(AgCl):m(AgBr)=1。
63810:1,又测得银与氯得相对原子质量(原子量)分别为107。
868与35。
453,求碘得相对原子质量(原子量)、1-6表1-1中贝采里乌斯1826年测得得铂原子量与现代测定得铂得相对原子质量(原子量)相比,有多大差别?1-7 设全球有50亿人,设每人每秒数2个金原子,需要多少年全球得人才能数完1mol金原子(1年按365天计)?1-8 试讨论,为什么有得元素得相对质量(原子量)得有效数字得位数多达9位,而有得元素得相对原子质量(原子量)得有效数字却少至3~4位?1-9 太阳系,例如地球,存在周期表所有稳定元素,而太阳却只开始发生氢燃烧,该核反应得产物只有氢,应怎样理解这个事实?1—10 中国古代哲学家认为,宇宙万物起源于一种叫“元气”得物质,“元气生阴阳,阴阳生万物",请对比元素诞生说与这种古代哲学。
1—11 “金木水火土”就是中国古代得元素论,至今仍有许多人对它们得“相生相克”深信不疑。
与化学元素论相比,它出发点最致命得错误就是什么?1—12 请用计算机编一个小程序,按1、3式计算氢光谱各谱系得谱线得波长(本练习为开放式习题,并不需要所有学生都会做)。

大学化学作业大全与答案(专升本,共90题)大学化学作业大全( 共 90 题)1.(单选题 )对于某特定的酸碱体系而言,分布系数δ值()。
(本题5.0 分)A、只取决于该体系的 [H + ]或 pH 值B、只取决于该体系的总浓度сC、既要考虑体系的 [H + ] ,又要考虑该体系的 cD、只取决于该体系的离解常数学生答案: A标准答案: A解析:得分: 52.(单选题)为使反应A2+ +B 4+ =A 3+ +B 3+完全度达到99.9% ,两电对的条件电位之差至少大于()。
(本题 5.0 分)A、0.1VB、0 .12VC、0.35VD、0.18V学生答案: C标准答案: C解析:得分: 53.(单选题 )CaF2 在 pH=3 .0 时,比在 pH=4 .0 时的溶解度大。
其原因是()。
(本题5.0 分)A、盐效应B、配位效应C、酸效应D、同离子效应学生答案: C标准答案: C解析:得分: 54.(单选题 )高压氢气瓶的瓶外表颜色为()。
(本题5.0 分)A、天蓝B、黑色C、白色D、深绿学生答案: B标准答案: D解析:得分: 05.(单选题 )分析测定中的偶然误差,就统计规律来讲,以下不正确的是()。
(本题5.0 分)A、多次平行测量数据符合正态分布B、数值随机可变C、大误差出现的概率小,小误差出现的概率大D、数值相等的正、负误差出现的概率均等学生答案: B标准答案: A解析:得分: 06.(单选题 )测定水中钙硬度时,消除Mg 2+的干扰可用()。
(本题5.0 分)A、控制酸度法B、配位掩蔽法C、氧化还原掩蔽法D、沉淀掩蔽法学生答案: B标准答案: D解析:得分: 07.(单选题)标定NaOH 溶液的常用的基准物质除了邻苯二甲酸氢钾,还有()。
(本题 5.0 分)A、基准 Na 2CO 3B、草酸C、硼砂D、盐酸学生答案: C标准答案: B解析:得分: 08.(单选题 )不利于减少碘量法中误差的操作是()。

无机化学(第四版)答案第一章物质的结构1-1 在自然界中氢有三种同位素,氧也有三种同位素,问:总共有种含不同核素的水分子?由于3H太少,可以忽略不计,问:不计3H时天然水中共有多少种同位素异构水分子?1-2 天然氟是单核素(19F)元素,而天然碳有两种稳定同位素(12C和13C),在质谱仪中,每一质量数的微粒出现一个峰,氢预言在质谱仪中能出现几个相应于CF4+的峰?1-3 用质谱仪测得溴得两种天然同位素的相对原子质量和同位素丰度分别为79Br 789183占50。
54%,81Br 80。
9163占49。
46%,求溴的相对原子质量(原子量)。
1-4 铊的天然同位素203Tl和205Tl的核素质量分别为202。
97u和204。
97u,已知铊的相对原子质量(原子量)为204。
39,求铊的同位素丰度。
1-5 等质量的银制成氯化银和碘化银,测得质量比m(AgCl):m(AgBr)=1。
63810:1,又测得银和氯得相对原子质量(原子量)分别为107。
868和35。
453,求碘得相对原子质量(原子量)。
1-6 表1-1中贝采里乌斯1826年测得的铂原子量与现代测定的铂的相对原子质量(原子量)相比,有多大差别?1-7 设全球有50亿人,设每人每秒数2个金原子,需要多少年全球的人才能数完1mol金原子(1年按365天计)?1-8 试讨论,为什么有的元素的相对质量(原子量)的有效数字的位数多达9位,而有的元素的相对原子质量(原子量)的有效数字却少至3~4位?1-9 太阳系,例如地球,存在周期表所有稳定元素,而太阳却只开始发生氢燃烧,该核反应的产物只有氢,应怎样理解这个事实?1-10 中国古代哲学家认为,宇宙万物起源于一种叫“元气”的物质,“元气生阴阳,阴阳生万物”,请对比元素诞生说与这种古代哲学。
1-11 “金木水火土”是中国古代的元素论,至今仍有许多人对它们的“相生相克”深信不疑。
与化学元素论相比,它出发点最致命的错误是什么?1-12 请用计算机编一个小程序,按1.3式计算氢光谱各谱系的谱线的波长(本练习为开放式习题,并不需要所有学生都会做)。

大一化学基础试题及答案一、选择题(每题2分,共20分)1. 物质的量(摩尔)是表示物质的量的单位,其符号为:A. molB. gC. kgD. L答案:A2. 以下哪个元素的原子序数为11?A. NaB. MgC. AlD. Si答案:A3. 根据阿伏伽德罗定律,1摩尔任何气体在标准状况下的体积是:A. 22.4 LB. 22.4 mLC. 224 LD. 2.24 L答案:A4. 以下哪个化合物的化学式为H2O?A. 氢气B. 氧气C. 过氧化氢D. 水答案:D5. 以下哪个反应是氧化还原反应?A. CO2 + H2O → H2CO3B. 2H2 + O2 → 2H2OC. NaCl → Na+ + Cl-D. CH4 + 2O2 → CO2 + 2H2O答案:D6. 以下哪个元素属于过渡金属?A. NaB. FeC. ArD. He答案:B7. 以下哪个化合物是共价化合物?A. NaClB. HClC. MgOD. Fe答案:B8. 根据酸碱质子理论,以下哪个物质是酸?A. H2OB. NH3C. HClD. NaOH答案:C9. 以下哪个反应是酸碱中和反应?A. NaOH + HCl → NaCl + H2OB. Fe + H2SO4 → FeSO4 + H2C. 2Na + 2H2O → 2NaOH + H2D. CH4 + 2O2 → CO2 + 2H2O答案:A10. 以下哪个元素的电子排布为1s² 2s² 2p⁶ 3s² 3p⁶?A. OB. NaC. MgD. S答案:B二、填空题(每空1分,共20分)1. 元素周期表中,第IA族的元素具有最外层________个电子。
答案:12. 摩尔质量的单位是________。
答案:g/mol3. 根据电子排布,氖(Ne)属于________区元素。
答案:s区4. 化学反应中的能量变化通常表现为________或________。

第5章 溶液与电离平衡习题答案原子量取四位有效数字,计算过程采用“四舍六入五成双”取舍,热力学数据除题目给出外均引用自书后附录以及兰氏手册。
1. 实验室某些常用的试剂百分浓度及密度分别是:(1)浓盐酸:含HCl 37.0%,密度1.19 g ⋅cm -3;加至3位有效数字 (2)浓硫酸:含H 2SO 4 98.0%,密度1.98 g ⋅cm -3; (3)浓硝酸:含HNO 3 70.0%,密度1.42 g ⋅cm -3; (4)浓氨水:含NH 3 28.0%,密度0.900 g ⋅cm -3。
试分别计算它们的物质的量浓度。
解:(1) -33-3-131.19g cm 1000cm 37.0%12.0mol dm 36.5g mol 1.0dmn c V ⋅⨯⨯===⋅⋅⨯ (2)19.8 mol·dm -3(3)15.8 mol·dm -3 (4)14.8 mol·dm -3 2. 是非题(1) 0.10 mol .dm -3 HAc 溶液中c (H +) = 1.3⨯10-3 mol .dm -3,故0.050 mol .dm -3 HAc 溶液中c (H +) = 0.65⨯10-3 mol .dm -3;(2)向浓度均为0.10 mol .dm -3的NH 3⋅ H 2O- NH 4Cl 的缓冲溶液中,加入HCl 使c (HCl) = 0.099 mol .dm -3,则由于溶液的缓冲作用,pH 不变;(3)Na 2CO 3溶液中通入适量CO 2气体,便可得到一种缓冲溶液; (4)多元弱酸盐的水解(如Na 3PO 4),以第一步水解为主;(5)将浓度均为0.10 mol .dm -3的HAc 和NaAc 混合溶液冲稀至浓度均为0.05 mol .dm -3,则由于HAc 电离度增大,混合溶液的酸度降低; (6)在一定的温度下,改变溶液的pH ,水的离子积不变; (7)弱电解质的电离度随弱电解质浓度降低而增大;(8)NH 4Ac 为一元弱酸碱盐,水解程度很大,故其水溶液的酸碱性很大。
普通化学大学试题及答案一、选择题(每题2分,共40分)1. 以下哪种元素的原子序数为8?A. 氧B. 氮C. 氟D. 氦答案:A2. 化学反应中,能量变化通常表现为:A. 热能B. 光能C. 电能D. 机械能答案:A3. 酸碱中和反应的实质是:A. 酸碱分子的简单混合B. 酸中的氢离子与碱中的氢氧根离子结合生成水C. 酸中的氢氧根离子与碱中的氢离子结合生成水D. 酸中的氢离子与碱中的氢离子结合答案:B4. 以下哪种物质属于电解质?A. 酒精B. 蔗糖C. 氯化钠D. 醋酸答案:C5. 摩尔质量的单位是:A. 千克B. 克C. 摩尔每千克D. 千克每摩尔答案:B6. 以下哪种化合物是共价化合物?A. 氯化钠B. 硫酸铜C. 氧化铁D. 氢氧化钠答案:B7. 以下哪种元素的原子结构中,最外层电子数为6?A. 碳B. 氧C. 氟D. 氦答案:A8. 以下哪种物质是强酸?A. 醋酸B. 柠檬酸C. 硫酸D. 碳酸答案:C9. 以下哪种物质是强碱?A. 氢氧化钠B. 氢氧化钾C. 氢氧化钙D. 氢氧化铵答案:A10. 以下哪种元素的原子结构中,最外层电子数为2?A. 锂B. 钠C. 镁D. 铝答案:B11. 以下哪种物质是弱电解质?A. 氯化钠B. 醋酸钠C. 硫酸铜D. 氢氧化钠答案:B12. 以下哪种化合物是离子化合物?A. 水B. 二氧化碳C. 氯化钠D. 氨气答案:C13. 以下哪种元素的原子结构中,最外层电子数为1?A. 氢B. 锂C. 钠D. 钾答案:A14. 以下哪种物质是弱碱?A. 氢氧化钠B. 氢氧化钾C. 氨水D. 氢氧化钙答案:C15. 以下哪种元素的原子结构中,最外层电子数为3?A. 硼B. 碳C. 氮D. 氧答案:C16. 以下哪种物质是强电解质?A. 醋酸钠B. 硫酸铜C. 氢氧化钠D. 醋酸答案:C17. 以下哪种化合物是金属化合物?A. 氯化钠B. 硫酸铜C. 氧化铁D. 氢氧化钠答案:A18. 以下哪种元素的原子结构中,最外层电子数为4?A. 碳B. 硅C. 磷D. 硫答案:B19. 以下哪种物质是弱酸?A. 醋酸B. 硫酸C. 盐酸D. 碳酸答案:A20. 以下哪种元素的原子结构中,最外层电子数为5?A. 氮B. 磷C. 砷D. 锑答案:A二、填空题(每题2分,共20分)1. 元素周期表中,第IA族元素的最外层电子数为________。
大学化学习题第一章1.现有一定浓度的蔗糖溶液,在-0.25℃时结冰。
已知在298K时纯水的蒸汽压为3.130kPa,水的K f=1.86 K·kg·mol-1,则该蔗糖溶液在上述温度下的渗透压(kP a)为(C )(A)600 (B)180 (C)332 (D)-332△T f = K f×b B b B= △T f / K f =0.1344∏V=nRT ∏=cRT =0.1344×8.314×298 =333 kPa,(因浓度小可以近似认为b B=c)2. 现有一瓶硫酸溶液,其质量分数为98%,则其物质的量分数应为(C )(A)0.5 (B)0.98 (C)0.90 (D)0.80(980/98)/[20/18+ 980/98]=0.93. 现有1mol理想气体,若它的密度为d,分子摩尔质量为M,在T(K)温度下体积为V (L),则下述关系正确的是(D )(A)p V=( M/d) RT (B)pV d= RT(C)p V=( d/n) RT (D)p M/d=RT4. 理想溶液是指-------------------------------------------------------------------------------------( D )(A) 溶质对溶剂分子间作用力没有明显影响(B) 溶解过程中几乎没有热效应(C) 溶解前后溶质和溶剂的体积没有变化(D) 以上三个性质5. 有一种称“墨海”的带盖砚台,其结构如图所示,当在砚台中加入墨汁,在外圈加入清水,并盖严,经足够长的时间,砚中发生了什么变化?请写出现象并解释原因。
答案:经足够长的时间,砚中墨汁变谈,因外圈的清水蒸气压大,而砚台中加入墨汁蒸气压小,外圈的清水水分子蒸发而在墨汁中凝聚。
6. 当26.9 g 未知难挥发非电解质溶于500 g 硝基苯中, 溶液的凝固点降低了2.30 K 。
第1章 化学热力学参考答案:(一)选择题1.A 2.A 3.C 4.B 5.D 6.C 7.C 8.C 9. A 10. C 11. A 12.C (二)填空题1.40;2.等温、等容、不做非体积功,等温、等压,不做非体积功; 3.>,<,=,> 4.增大、不变 5.不变 6.3.990 kJ·mol -1(三)判断题1. ×2. ×3. ×4. ×5. √6. ×7. ×8. ×9. × 10. × (四)计算题1.解:(g)O N (l)H 2N 4242+O(l)4H (g)3N 22+(l)H N 42摩尔燃烧热为 2.解:)mol ·(kJ 28.254166.963.502)84.285(401f B r --=-⨯--⨯+=∆=∆∑HH ν)mol ·(kJ14.627211r-Θ-=∆=H Q pK 1077.3109.9824.37333mr r ⨯=⨯--=∆∆=-S T 转)mol ·(kJ 78.34357.86)15.137(36.3941f B r --=---=∆=∆∑G ν)K ·mol ·(J 9.9865.21056.1975.191216.21311B r ---=--⨯+==∆∑νNO(g)CO(g)+(g)N 21(g)CO 22+)mol ·(kJ 24.37325.90)52.110(5.3931f B r --=----=∆=∆∑H ν此反应的 是较大的负值,且)(,)(-∆-∆S H 型反应,从热力学上看,在 T 转的温度以内反应都可自发进行。
3.解:外压kPa 50e =p ,11p nRT V =,22p nRTV =,2e p p = 系统所做功:定温变化,0=∆U0=+=∆W Q U ,所以Q =1 247.1(J ) 定温过程pV =常数 ∆(pV )=0 所以 0)(=∆+∆=∆pV U H 4.解:查表知CaO(s) + SO 3(g) = CaSO 4(s)求得同理求得 因为 所以根据经验推断可知,反应可以自发进行。
化学习题(附参考答案)一、单选题(共36题,每题1分,共36分)1.爆炸品按爆炸性的大小,可分为( )项。
A、5B、6C、4D、3正确答案:A2.危险化学品名编号由五位阿拉伯数字组成,编号为43100,其数字3代表的含义是( )。
A、危险品的顺序号B、危险品的类别C、危险品的数量D、危险品的项别正确答案:D3.洗消方舱上的污水收集池是( )吨。
A、3B、1C、2D、4正确答案:A4.下列不是汽油的物理性质的是( )。
A、比水轻B、极易燃烧C、挥发性强D、不溶于水正确答案:B5.金属钠应储存于( )中。
A、汽油B、水C、柴油D、煤油正确答案:D6.氨气泄漏时用( )进行中和。
A、三合二溶液B、次氯酸钙溶液C、苏打水D、水正确答案:D7.氧化剂、有机过氧化物与( )接触会引起着火爆炸。
A、高锰酸钾B、空气C、氮气D、易燃物品正确答案:D8.对金属钠火灾扑救的错误措施为( )。
A、氯代烃灭火。
B、碳酸钠干粉C、碳酸钙干粉D、石墨粉正确答案:A9.( )遇高温易分解放出氧和热量,极易引起燃烧爆炸。
A、有机过氧化物B、催化剂C、氧化剂D、有毒品正确答案:A10.不属于物理洗消的方法是( )。
A、溶解B、加热C、吸附D、次氯酸钙正确答案:D11.盐酸灭火时注意事项正确的是( )。
A、废物流入江河或毒气,烟雾对上风方向造成公害B、战人员及时洗澡C、禁止向泄漏物直接射水D、污染水带用清水浸泡1小时正确答案:C12.金属钠是( )软金属。
A、黑色B、灰色C、黄色D、银白色正确答案:D13.高氯酸是强氧化剂,( )的发烟液体。
A、无色粘稠B、白色透明C、白色粘稠D、无色透明正确答案:D14.双氧水属于( )。
A、无机过氧化物B、有机过氧化物C、复配型过氧化物D、其它类型化物正确答案:A15.危险化学品第四类是( )。
A、有毒品B、氧化剂和有机过氧化物C、易燃固体、自燃物品和遇湿易燃物品D、爆炸品正确答案:C16.沙林的主要成分是( )。
基础化学试题及答案大一一、选择题(每题2分,共20分)1. 化学元素周期表中,氧元素的原子序数是多少?A. 6B. 8C. 16D. 182. 以下哪个不是化学元素的符号?A. FeB. AuC. CuD. Ca3. 摩尔质量的单位是:A. gB. kgC. g/molD. mol/g4. 原子的核外电子排布遵循哪个原则?A. 泡利不相容原理B. 能量最低原理C. 洪特规则D. 所有以上5. 以下哪个是强酸?A. 醋酸B. 碳酸C. 氢氧化钠D. 氢氧化钾6. 根据酸碱质子理论,以下哪个是酸?A. 硫酸钠B. 氯化钠C. 碳酸氢钠D. 氢氧化钠7. 化学键中,离子键通常存在于:A. 金属与非金属之间B. 非金属与非金属之间C. 金属与金属之间D. 非金属与金属之间8. 氧化还原反应中,氧化剂和还原剂分别发生什么变化?A. 氧化剂被氧化,还原剂被还原B. 氧化剂被还原,还原剂被氧化C. 氧化剂被还原,还原剂被氧化D. 氧化剂被氧化,还原剂被氧化9. 以下哪个是化学平衡的表达式?A. K = [A][B]/[C][D]B. K = [A]/[B]C. K = [C][D]/[A][B]D. K = [A] + [B] - [C] - [D]10. 根据勒夏特列原理,增加反应物浓度,平衡会如何移动?A. 向左移动B. 向右移动C. 不移动D. 无法确定答案:1. B2. D3. C4. D5. A6. C7. A8. B9. C10. B二、填空题(每空2分,共20分)1. 原子的核外电子排布遵循的三大规则是:______、______、______。
答案:能量最低原理、泡利不相容原理、洪特规则2. 摩尔浓度(Molarity)的定义是:______。
答案:单位体积溶液中所含溶质的摩尔数3. 化学平衡常数(K)表达式为:K = [C][D]/[A][B],其中[A]、[B]、[C]、[D]分别代表______。
《大学化学(上册)》作业题专业___________班别____________学号___________姓名____________基础化学部无机及分析教研室编2008秋绪论4.正确地修约下列数据:(1)37.800至3位;(2)72.75至3位;(3)90.045至4位;(4)125.550至4位;5.以正确的有效位数给出下列算式的结果:(1)50.00×27.80×0.1167;(2)(2.776×0.0050)-6.7×10-3+(0.036×0.0271)(3)(4)0.0011205.1021.143.10⨯⨯238.14839.155.674.3)-9.85(24.16-⨯⨯第10章实验误差和数据处理2. 重复分析一银合金试样,测得银的质量分数分别为95.67%,95.61%,95.71%和95.60%。
试计算:(1)均差;(2)标准差;(3)变异系数。
3. 现对一种煤的含水量做了4次测定,测得水的质量分数为18.3%,18.9%,17.7%和18.6%,试求在置信水平95%时的置信区间。
5. 为检验一种新的分析方法的有效性,现采用一种钙的质量分数ω(Ca)=21.20%(真实值μ)的标样以新方法进行分析,若x= (Ca)=21.24%,s=0.12%,n=10。
试问x与μ的置信水平90%和95%时,是否存在显著差异?8 现有两个含铀试样的测定结果如下:试样1 10.32%,10.39%,10.19%,10.21%试样2 10.45%,10.41%,10.51%,10.36%,10.34%,10.39%试问在置信水平95%时,两试样有无显著性差异?9 用Q检验法检测下列结果:6.02,7.28,7.32,7.02,7.92,7.12,7.32,7.22。
11 某生对一含硫酸根试样做了4次测定,得到硫酸根的质量分数分别为9.35%,9.29%,9.38%和9.27%。
试问其平均值x是多少?若已知该试样经精确测定硫酸根的质量分数为9.30%,则4次测定的绝对误差各是多少?平均值x的绝对误差和相对误差又是多少?第6章酸碱平衡和酸碱滴定法4. 从附表中查出下列各酸的pK a值,并计算它们的K a和相应的共轭碱的K b值。
(1)砷酸(H3AsO4)(2)亚磷酸(H3PO3)(3)硼酸(H3BO3)(4)邻苯二甲酸(C8H6O4)(5)铵离子(NH4+)(6)8-羟基喹啉盐(C9H8ON+)(7)乙二胺盐(C2H10N22+)(8)氨基乙酸盐(C2H6O2N+)7. 写出下列各溶液的质子条件式:(1)NH4Ac (2)H2SO4(3)NaH2PO4(4)(NH4)2HPO417. 计算下列各溶液的pH值(忽略离子强度的影响):(1)0.180 mol•L-1苯甲酸溶液(2)0.250 mol•L-1磷酸二氢钠溶液(3)0.700 mol•L-1砷酸溶液(4)0.200 mol•L-1氰化铵溶液21.为了制备pH=5.00的缓冲溶液。
某生用1.0mol/L HAc和1.0mol/L NaAc混合,如果他已用了100mL HAc溶液,问还需要多少毫升NaAc溶液?30.下列碱溶液能否用酸滴定?如果能滴定,试计算计量点时的pH值,并选择合适的指示剂(设滴定剂和被测物的浓度均为0.1000 mol/L)(1)六亚甲基四胺(CH2)6N4(2)甲胺CH3NH2(3)羟基乙胺HOCH2CH2NH2(4) 羟胺NH2OH32.下列酸溶液能否用强碱滴定?如果能滴定,试计算计量点时的pH值,并选择合适的指示剂(设滴定剂和被测物的浓度均为0.1000 mol/L)(1)氢氰酸HCN (2)氢氟酸HF(3)盐酸羟胺NH2OH.HCl (4) 次氯酸HClO33.下列酸碱溶液能否准确分步滴定或分别滴定,或准确滴定其中的一种?(1)0.1000 mol/L柠檬酸(2)0.01000 mol/L砷酸37.称取草酸试样 1.778g,用水溶解后转入250mL容量瓶中,稀释至刻度。
吸取此试液25.00mL,以0.1093mol/LNaOH标准溶液滴定,用去25.84mL,计算此草酸试样H2C2O4.2H2O 的质量分数。
38.某碱灰试样,除含有Na2CO3外,还可能含有NaOH或NaHCO3及不能与酸作用的物质。
今称取1.100g该试样溶于适量的水后,用甲基橙为指示剂需加HCl溶液(1.00ml HC l≒0.01400g CaO)31.40mL才能到达终点。
若用酚酞作指示剂时,同样质量的试样需该浓度HCl 溶液13.30mL,才能到达终点。
计算试样中各组分的质量分数。
39.用蒸馏法测定某肥料中含氮量。
称取试样0.2360g,加浓碱液蒸馏,馏出的NH3用0.1014 mol/L HCl 50.00 mL吸收,然后用0.1010mol/L NaOH滴定过量的HCl,计有去NaOH 10.70 mL。
计算该肥料中氮的质量分数。
第7章配位平衡和配位滴定9. 计算pH为11.0,游离CN-浓度为0.0100mol•L-1的溶液中,Hg(Ⅱ)-EDTA配合物的条件稳定常数。
10. 当c(NH3+NH4+)=0.2mol•L-1,pH=8.0时,Co(Ⅱ)-EDTA配合物的条件稳定常数是多少?15. 假定在pH=2.0时,用0.005mol•L-1EDTA滴定0.0100mol•L-1Fe3+。
计算在计量点时游离Fe3+的浓度。
17. 滴定25.00mL 0.0100mol•L-1 CaCO3标准溶液需20.00mL EDTA。
今用该EDTA溶液测定水硬度时,取75.00mL水样,需30.00mL EDTA溶液。
试计算该水样的硬度。
19. 现用25.00mL 0.04520mol•L-1 EDTA处理一50.00mL含Ni2+和Zn2+的溶液,使其完全反应。
过量未反应的EDTA需用12.40mL 0.01230mol•L-1 Mg2+溶液进行滴定。
然后再加入过量的2,3-二巯基丙醇从锌-EDTA配合物中置换出EDTA。
释放出的EDTA需29.20mLMg2+滴定。
试计算原试液中Ni2+和Zn2+的浓度。
第8章沉淀平衡和沉淀滴定1.写出下列被测物质的换算因数的表达式:被测物称量形式换算因数ZnCl2 ZnCl2 (NH4)2SO4 Cu2HgI4 Cu2HgI4 Cu2HgI4AgCl Zn2P2O7 NH4B(C6H5)4AgIHgOCu2. 重量法测定砷时,先将其氧化成砷酸盐,然后沉淀为Ag3AsO4,溶于HNO3,再将银沉淀为AgCl并进行称量。
写出计算原试样中As2S3质量分数的换算因数并计算其数值。
8.完成下表:AgBrAg2C2O4Ca3(PO4)2PbBr2 MgNH4PO41.22×10-4g/100ml0.296g/100ml5×10-131×10-112.5×10-1313.计算Ag2CrO4在下列溶液中的溶解度:(1)0.10 mol·L-1Na2CrO4溶液;(2)0.10mol·L-1AgNO3溶液(不考虑铬酸根的水解)。
20.试计算在pH=4.00时,CaF2的溶解度。
第9章原电池与氧化还原反应6. 写出下列原电池的电极反应式和电池反应式,并计算电池电动势。
(1)Zn|Zn2+(0.1mol·L-1)||I-(0.1 mol·L-1),I2|Pt(2)Pt|Fe2+(1 mol·L-1),Fe3+(1 mol·L-1)||Ce4+(1 mol·L-1),Ce3+(1 mol·L-1)|Pt(3)Pt|H2(pΘ)|H+(0.001 mol·L-1)||H+(1 mol·L-1)|H2(pΘ)|Pt7. 已知电对H3AsO4(aq)+2H+(aq)+2e-HAsO2(aq)+2H2O(l);EΘ(H3AsO4/HAsO2)=0.560VI2(aq) + 2e- 2 I-(aq);EΘ(I2/I-)=0.536V试计算下列反应的平衡常数:H3AsO4 + 2I- + 2H+ = HAsO2 + I2 + 2 H2O如果溶液的pH=7,反应朝什么方向进行?如果溶液中的[H+]=6 mol·L-1,反应朝什么方向进行?11. 铁棒放在0.0100 mol·L-1 FeSO4溶液中作为一个半电池,另一半电池为锰棒插在0.100mol·L-1 MnSO4溶液中组成原电池。
已知V Fe Fe E 440.0)/(2-=+θ,V Mn Mn E 182.1)/(2-=+θ。
试求(1)电池的电动势。
(2)反应的平衡常数。
12. 有下列电势图:Cu Cu Cu CuO VV V −−→−−−→−−−→−++++++518.0155.028.1(1)判断Cu +能否发生歧化反应?(2)计算电对Cu 2+/Cu 的标准电极电势。
28. 将某碳酸钙试样0.1914g 溶于盐酸,并将钙沉淀为CaC 2O 4,用稀硫酸溶解沉淀,用高锰酸钾溶液滴定需36.50mL 。
该高锰酸钾溶液35.57mL 相当于0.2383g Na 2C 2O 4。
空白测定需0.08mL 高锰酸钾溶液。
计算试样中CaO 的质量分数。
31.称取0.2683g 铬铁矿试样,用过氧化钠熔融。
破坏过量Na 2O 2,熔块用水浸取,所得溶液酸化后,加50.00mL 0.1022 mol ·L -1溶液Fe 2+ 溶液。
将Cr (VI )完全还原后,剩余的未反应的Fe 2+用0.01667 mol·L -1K 2Cr 2O 7滴定,消耗18.04mL 。
试计算试样中铬的质量分数。
32.测定软锰矿中MnO2的含量,准确称取软锰矿试样0.5261g,在酸性介质中加入0.7049g Na2C2O4。
待反应完全后,过量的草酸用0.02160mol/LKMnO4标准滴定溶液滴定,用去30.47ml。
试计算软锰矿中的MnO2的质量分数。
绪论 参考答案 4、(1)37.8 (2)72.8 (3) 90.04 (4) 125.6 5、(1)原式=162.2(2)原式=2.8×0.0050- 6.7×10-3+(0.036×0.027)=0.014- 6.7×10-3+0.00097=0.014-0.007+0.001=0.008(3)原式= (3.10×21.4×5.10)/0.00112=3.02×105(4)原式= (24.16×5.5×5.67)/1.601=(24×5.5×5.7)/1.6=4.7×102第10章 参考答案 2、解: =95.66% (1)= (0.01%+0.05%+0.05%+06%)/4=0.04%(2)S={ [(0.01%)2+(0.05%)2+(0.05%)2+(06%)2]/(4-1)}1/2=0.05% (3)C v =S/=0.052% 3、 =18.4%S= {[(0.1%)2+(0.5%)2+(0.7%)2+(0.2%)2]/(4-1)}1/2=0.5%当置信水平为95%时,由表查出,t 值为3.182,置信区间为:±t.s/n 1/2=(18.4±3.182×0.5/41/2=(18.4±0.8)%5、t=|-μ|/(s/n 1/2)=1.054当置信水平为90%和95%时,由表查出,t 值分别为1.833和2.262,都比t 计算值大,所以无显著差别。