生产工艺变更单
- 格式:xls
- 大小:18.00 KB
- 文档页数:1

工艺技术变更单工艺技术变更单变更单号:2022-001变更类型:工艺技术变更变更项目:产品制造工艺流程调整变更原因:随着市场需求的变化以及新一轮技术革新的到来,我们公司决定对产品的制造工艺流程进行调整,以提高生产效率和产品质量。
此次变更旨在优化产品制造流程,降低生产成本,并保证产品的稳定性和可靠性。
变更内容:1. 原来的工艺流程中,存在一些不必要的重复步骤,此次变更将会删除并简化这些重复步骤,从而提高生产效率。
2. 对生产设备进行升级和改造,以适应新的工艺流程要求,保证设备的稳定运行。
3. 引入新的自动化设备和技术,以代替过去的手工操作,提高产品的制造精度和一致性。
4. 修改产品测试流程,并引入更加高效、准确的测试仪器和方法,以提高产品质量检测的可靠性和准确性。
5. 调整供应链和物流管理,以适应新的工艺流程,缩短供应链的供货周期,并减少库存。
变更实施计划:1. 针对工艺流程的调整,我们将组织专门的技术团队进行详细的工艺分析和设计,并进行试验验证。
2. 对生产设备的升级和改造,将在非工作时间进行,以避免影响生产进度。
3. 引入新设备和技术,将会进行培训和技术指导,确保员工能够熟练操作和使用新设备和技术。
4. 对测试流程和仪器的调整将逐步实施,先进行小范围试点,然后逐步推广到整个生产线。
5. 调整供应链和物流管理,将与供应商和物流公司进行沟通,确保新的工艺流程能够顺利执行。
变更影响评估:1. 从生产效率和成本方面来看,此次变更能够明显提高生产效率和降低生产成本,从而提高企业竞争力。
2. 从产品质量方面来看,引入新的自动化设备和技术以及优化测试流程,将会提高产品的制造精度和一致性,减少不良品率。
3. 从供应链管理方面来看,调整供应链和物流管理,将能够缩短供货周期,减少库存和仓储成本。
变更验证:在变更实施后,我们将进行全面的考核和评估,以验证变更是否取得预期效果。
同时,将收集员工和客户的反馈意见,以了解变更是否对他们产生了积极的影响。

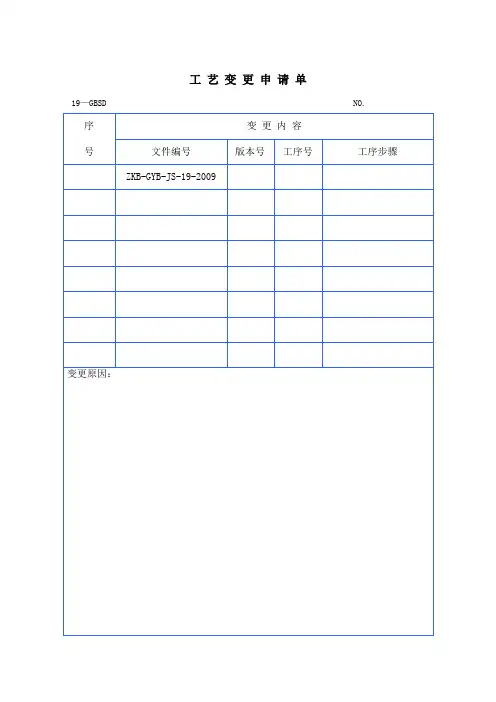

电镀工艺变更申请书尊敬的XXX公司领导:我谨代表我们部门向您提交这份电镀工艺变更申请书,希望能得到您的批准和支持。
首先,请允许我简要介绍一下电镀工艺变更的背景和原因。
目前,我司使用的电镀工艺已经有些年头,虽然在生产过程中取得了一定的成果,但也暴露出了许多问题。
比如,电镀效率低、生产成本高、废液处理困难以及对环境的影响等。
这些问题不仅限制了我们的生产效率和产品质量,也对环境造成了一定的负担。
因此,为了提高生产效率、降低成本、减少对环境的影响,我们决定对现有的电镀工艺进行变更。
接下来,我将详细介绍电镀工艺变更的具体内容和预期效果。
一、电镀工艺变更内容1. 更换电镀液:我们将采用一种新型的环保型电镀液,该电镀液具有高效、低毒、易回收等特点,能够显著提高电镀效率和产品质量。
2. 优化电镀工艺参数:通过对电镀电流、电压、时间等参数的优化,使得电镀过程更加稳定,提高产品表面的光洁度和均匀性。
3. 改进废液处理方法:采用先进的生物降解技术对废液进行处理,使其达到国家排放标准,减少对环境的影响。
二、预期效果1. 提高生产效率:新型电镀液的使用将使得电镀过程更加稳定,从而提高生产效率。
2. 降低生产成本:新型电镀液的购买成本虽然较高,但因其高效、低毒、易回收等特点,长期来看将降低生产成本。
3. 提高产品质量:电镀过程的优化将使得产品表面光洁度和均匀性得到提升,从而提高产品质量。
4. 减少对环境的影响:废液处理方法的改进将使得废液达到国家排放标准,减少对环境的影响。
最后,我们将认真贯彻执行电镀工艺变更方案,并对变更后的工艺进行持续改进和完善。
同时,我们也将密切关注电镀工艺变更对生产质量和环境的影响,确保变更方案的有效性和可行性。
希望领导能批准我们的电镀工艺变更申请,并给予支持和指导。
此致敬礼!申请人:(签名)申请日期:年月日。

第1篇申请部门: [部门名称]申请日期: [年/月/日]申请人: [申请人姓名]职务: [申请人职务]项目名称: [项目名称]一、背景说明随着我国科技水平的不断提高和市场竞争的日益激烈,[项目名称]在研发、生产过程中,为了提升产品品质、降低生产成本、提高生产效率,有必要对现有工艺进行优化和改进。
经研究,现提出以下工艺变更申请。
二、变更原因1. 技术原因:- 原有工艺在技术方面存在一定的局限性,无法满足产品性能提升的要求。
- 现有技术发展迅速,采用新技术、新材料、新工艺可以提高产品性能和附加值。
2. 成本原因:- 原有工艺生产成本较高,通过优化工艺流程,降低材料消耗和能源消耗,可以降低生产成本。
- 市场竞争激烈,降低产品售价以提升市场竞争力。
3. 效率原因:- 原有工艺生产效率较低,通过优化工艺流程,提高生产速度,满足市场需求。
4. 环保原因:- 原有工艺在生产过程中产生大量废弃物,对环境造成污染。
采用环保工艺可以减少污染,实现绿色生产。
三、变更内容1. 工艺流程变更:- [具体变更内容,如:改变原材料的选用、调整生产步骤、优化生产设备等] 2. 设备变更:- [具体变更内容,如:更换生产设备、升级设备性能等]3. 人员培训:- [具体变更内容,如:对新工艺、新设备进行培训,提高员工操作技能等] 4. 质量控制:- [具体变更内容,如:优化质量检验流程,提高产品质量等]四、变更预期效果1. 技术指标提升:- 产品性能、可靠性、稳定性等方面得到提升。
2. 成本降低:- 材料消耗、能源消耗、人工成本等得到降低。
3. 生产效率提高:- 生产周期缩短,生产效率提升。
4. 环保效益:- 减少废弃物排放,降低环境污染。
五、变更实施计划1. 前期准备:- 成立工艺变更小组,负责变更方案的制定、实施和监督。
- 对现有工艺进行评估,确定变更方向和重点。
2. 实施阶段:- 按照变更方案,逐步实施工艺、设备、人员等方面的变更。
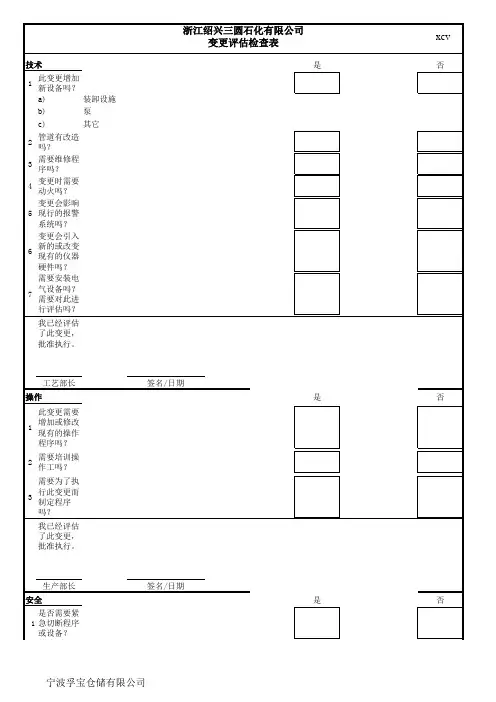

第1页/共2页生产工艺变更过程控制单编号:GYGC变更原因:提出人:提出日期:执行人:开始日期:关联产品:□ABC □DEF□其它:变更名称:变更方案:(可另附技术文档说明)前期调研:□理论分析(若有,相关分析请以附件形式提供)□已有应用实例请简要说明:□其它,请简要说明:关联岗位:□QA □PM □采购□计划调度□QC□仓储□服务□生产小组□其它:关联资料:□无□有,请按以下分类填写。
☐图纸编号:□工艺卡编号:□其它:风险值分析:风险预审:□否,直接执行测试验证□是,请完善以下预审信息会议记录编号:会议结论:□通过□不通过以上:□同意□其它,请简要说明:审核人/日期:关联岗位1()□同意变更□其他,请说明:签名:日期:关联岗位2()□同意变更□其他,请说明:签名:日期:关联岗位3()□同意变更□其他,请说明:签名:日期:关联岗位4()□同意变更□其他,请说明:签名:日期:关联岗位5()□同意变更□其他,请说明:签名:日期:关联岗位6()□同意变更□其他,请说明:签名:日期:关联岗位7()□同意变更□其他,请说明:签名:日期:关联岗位8()□同意变更□其他,请说明:签名:日期:关联岗位9()□同意变更□其他,请说明:签名:日期:关联岗位10()□同意变更□其他,请说明:签名:日期:评审结论:基于关联岗位相关意见:□同意变更□其他,请说明:审核人/日期:生产部门负责人意见:□同意变更□其他,请说明:签名:日期:上级意见:(如需)□同意变更□其他,请说明:签名:日期:变更附件汇总:□实验报告()份□会议记录()份□试样单()份□物料信息()份□成本信息()份□其他:变更结果输出:□生产工艺通知编号:□作业文件编号:□其它:第2页/共2页。
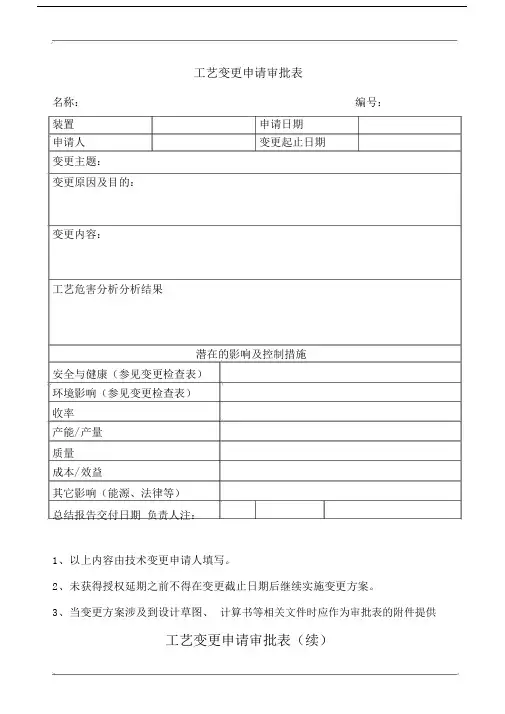
工艺变更申请审批表名称:编号:装置申请日期申请人变更起止日期变更主题:变更原因及目的:变更内容:工艺危害分析分析结果潜在的影响及控制措施安全与健康(参见变更检查表)环境影响(参见变更检查表)收率产能/ 产量质量成本/ 效益其它影响(能源、法律等)总结报告交付日期负责人注:1、以上内容由技术变更申请人填写。
2、未获得授权延期之前不得在变更截止日期后继续实施变更方案。
3、当变更方案涉及到设计草图、计算书等相关文件时应作为审批表的附件提供工艺变更申请审批表(续)变更所带来的问题陈述:变更的技术依据(预期改善的性质、实施此项变更的安全性、评审支持的实验或工艺数据等)工艺变更详细说明(包括操作程序、试验日志、关键的工艺变量值等连带变更要求)审查意见:审查成员签字 / 日期变更申请人:技术发展部:设备部:属地单位:安全环保部:变更批准人:日期:分发:变更检查表安全健康是否不适用是否存在任何可能导致安全问题的化学反应?检查化学反应矩阵模型。
是否存在任何易燃易爆化学物质或灰尘?是否存在任何有危险的原材料流流速、成分或温度条件变更?是否会因加热、冷却或精确的温度控制失控而导致安全问题?是否具有为安全操作所必需的仪表、控制、紧急制动、开关或报警?检查操作人员通道所在地并实施监控。
是否有任何出于安全考虑而必须联锁的设备?是否有任何校准与否对安全非常重要的仪表?有无会给人员及设备造成危害的腐蚀物?是否存在空气排放问题?检查通风要求。
是否存在有毒或危害性化学物品?如:石棉,放射性物质?检查通风要求。
是否可能因蒸汽、仪表气源、电力或任何其它供应的中断而导致不安全状况?阀门位置错误对于安全问题是否重要?是否要求吹扫或惰性气体保存?是否需要通风孔、安全阀、溢出、排水或冲洗连接?检查其尺寸、位置及供应商。
是否需要冷冻保护?是否存在任何压力容器?泄压需要是否受变更方案的影响?不同压力等级的容器之间是否有连接?检查泄压要求?温度是否高或低至需要通过隔离来保护人员安全?温度是否高或低至可能造成管道或设备的热膨胀?是否需要采取筑堤、围栏或其它围护措施以控制泄漏?检查尺寸。
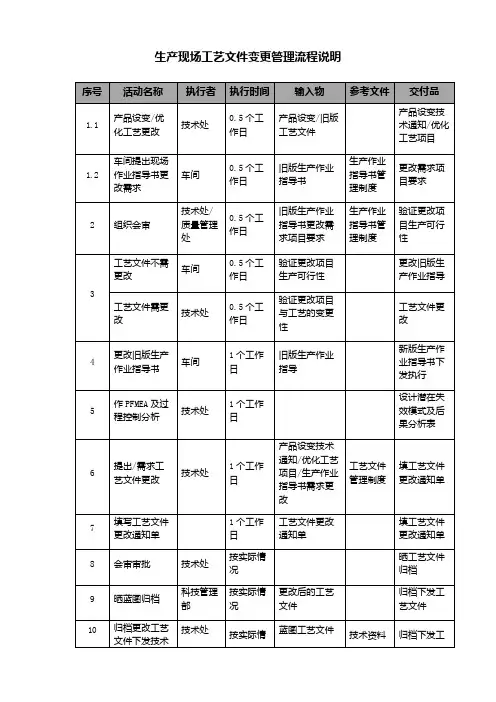

工艺更改通知单三篇
篇一:工艺更改通知单
编号:日期:
产品图号产品名称更改图样图号更改图样名称实施日期
更
改
内
容
及
说
明
更改前更改后
更改理由发送单位
部门签名日期
工修单号
生效日
期
更改内容
制
品
处
理
成
本
变
更情况
□不变□下降□上升
财务会签编制:审核:批准:
主管单位:文件编号
工艺文件名称工艺文件编号实施日期
变更内容及原因说明
变更前
变更后
原因说
明
变更申请人/日期:审核/日期:批准/日期: 告知单位:
主管单位:技术中心
工艺文件名称工艺文件编号实施日期
变更内容及原因说明
变更前
变更后
原因说明
变更等级0级 1级
变更申请人:审核:批准:
说明:
1、变动两项及以下工艺参数时为0级,变动三项及以上工艺参数时为1级。
2、0级变更由工艺支持工程师(技术员)提出,技术科(副)科长审核,技术中心主任批准。
3、1级变更由技术科(副)科长提出,技术中心主任审核,分管领导批准。
附件2 :药品生产工艺变更情况表一、不影响安全性、有效性和质■可控性的工艺变更(一)中药I类和H类变更1.I类变更:此类变更不会引起药用物质基础的改变,对药物的吸收、利用不会产生明显影响,不会引起安全性、有效性的明显改变。
如变更不含挥发性成分、热敏性成分药物的粉碎工艺(其粉碎粒度基本相同)、浓缩干燥工艺或制粒工艺(缩短受热时间或降低受热温度)等,但变更为特殊的浓缩干燥方法,如微波干燥等方法,不属于此类变更。
2.II类变更:此类变更对其药用物质基础或对药物的吸收、利用有影响,但变化不大,包括工艺过程中一些工艺参数及工艺方法的改变,如变更含挥发性成分、热敏性成分药物的涉及受热温度、受热时间的工艺操作,应进行对比研究,如药用物质变化不大,属于H类变更。
(二)化学药品I类和H类变更1.变更原料药的生产工艺I类变更:(1 )变更试剂、起始原料的来源;(2)提高试剂、起始原料、中间体的质量标准;II类变更:(3)变更起始原料、溶剂、试剂、中间体的质量标准;2.变更制剂的生产工艺I类变更:(1)增加生产过程质量控制方法或严格控制限度;(2 )片剂、胶囊、栓剂或阴道栓印记变更; (3)普通或肠溶片剂、胶囊、栓剂或阴道栓的形状、尺寸变更;II类变更:(4)变更生产设备;包括无菌制剂生产中采用相同设计及操作原理的设备替代另一种设备;非无菌制剂生产中采用设计及操作原理不同的设备替代另一种设备;改变半固体制剂生产中混合设备类型,由高速剪切机变更为低速剪切机,或相反变更。
如涉及无菌产品时,变更生产设备不应降低产品的无菌保证水平。
(5)变更制剂生产过程,包括口服固体制剂物料混合过程的混合时间及混合速度等变更,包括半固体制剂混合过程中的混合速度、混合时间、冷却速度等生产过程的变更,还包括半固体制剂水相与油相混合过程的变更。
对于无菌制剂,这种变更包括:①对采用终端灭菌工艺生产的无菌制剂,取消中间过程的滤过环节;②变更除菌过滤过程的滤过参数(包括流速、压力、时间、或体积,但滤过材料和孔径不变)等。
工艺变更联络函
尊敬的客户,
感谢您一直以来对我们产品的信任与支持。
为了更好地满足您的需求,我们在生产过程中进行了一些工艺变更,请您务必注意以下内容:
1. 原材料的变更:我们将使用更优质的原材料替换原有的材料,以提高产品的品质和使用寿命。
2. 工艺流程的变更:我们将对生产中的某些工艺环节进行改进,以提高生产效率和产品质量。
3. 外观的变更:我们对产品的外观进行了一些修改,以更好地符合客户的审美需求。
我们保证在工艺变更的过程中,仍然会秉承“质量第一,客户至上”的服务宗旨,为您提供最好的产品和服务。
如果您有任何进一步的问题或建议,请随时与我们联系,我们将尽快回复您。
再次感谢您的支持和信任。
- 1 -。
药品生产工艺变更承诺书模板本人_____(甲方:药品生产企业全称)______(以下简称甲方)和_____(乙方:药品监管部门全称)______(以下简称乙方),经双方友好协商一致,就甲方生产的以下药品的工艺变更事宜达成如下承诺:一、_____(药品通用名称)______的生产工艺变更,包括但不限于原辅料来源、生产工艺流程、设备更换等内容,将严格遵守国家药品监管部门相关规定和标准,确保生产过程符合药品生产质量管理规范。
二、甲方承诺在进行任何生产工艺变更前,将提前向乙方递交书面变更申请,并详细说明变更内容、变更原因、变更前后工艺流程以及影响分析等相关资料,接受乙方审查。
三、甲方承诺在生产工艺变更过程中,将严格按照乙方要求进行记录和资料保存,确保变更过程可追溯,便于日后复查核实。
四、如因生产工艺变更导致_____(药品通用名称)______产品质量问题或安全隐患,甲方将立即停止生产并采取有效措施进行纠正,全力配合乙方进行调查处理,并承担相应的责任。
五、本承诺书自双方签署之日起生效,有效期至_____(具体日期)______。
双方同意在生产工艺变更过程中保持密切沟通,及时解决出现的问题,并共同维护公共药品安全和市场秩序。
甲方(盖章):_________________________法定代表人(签名):_____________________日期:_________________________乙方(盖章):_________________________法定代表人(签名):_____________________日期:_________________________以上为药品生产工艺变更承诺书,双方应严格遵守承诺内容,确保药品质量和患者安全。