相图的基本知识及单元系相图
- 格式:ppt
- 大小:737.50 KB
- 文档页数:12
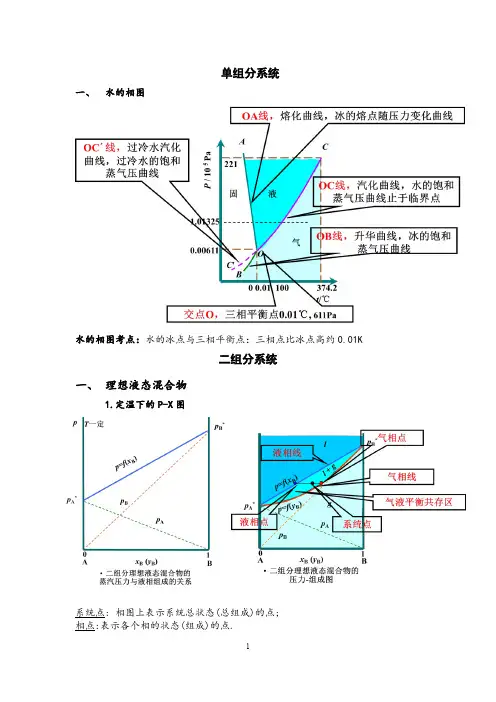
单组分系统一、水的相图水的相图考点:水的冰点与三相平衡点:三相点比冰点高约0.01K二组分系统一、理想液态混合物1.定温下的P-X图系统点: 相图上表示系统总状态(总组成)的点;相点:表示各个相的状态(组成)的点.结线:两个平衡相点的连结线.系统点总是在结线上2.定压下的T-X图泡点: 液相升温至开始起泡沸腾的温度;露点: 气相降温至开始凝结的温度.两点之间为相变温度区间, 与系统总组成有关.精馏原理:将液态混合物同时经多次部分气化和部分冷凝而使之分离的操作称为精馏。
同一层隔板上, 自下而上的有较高温度的气相与反方向的较低温度的液相相遇. 通过热交换,气相部分冷凝, 液相则部分气化.二、非理想液态混合物1.二组分真实液态混合物的4种类型的P-X图关于正偏差:若两组分分子间的吸引力小于各纯组分分子间吸引力,形成混合物后,分子就容易逸出液面而产生正偏差.若纯组分有缔合作用,在形成混合物后发生离解,因分子数增多而产生正偏差.混合时常有吸热及体积增大现象.关于负偏差:若两组分分子间的吸引力大于各纯组分分子间吸引力,形成混合物后,分子就较难逸出液面而产生负偏差.若形成混合物后分子发生缔合,因分子数减少而产生负偏差.混合时常有放热及体积缩小现象.2. 二组分真实液态混合物的4种类型的T-X图恒沸点处气相组成和液相组成相同。
此点对应的自由度数为0.一般正偏差和一般负偏差系统的温度-组成相图与理想系统的类似.3.部分互溶系统部分互溶的情况:系统会以两个饱和溶液平衡共存,这两个液层称为共轭溶液. 当混合物组成未达到两组分的相互溶解度时, 系统都以均相存在。
将具有两个液层的系统升高或降低至某个温度,两个液层的界面消失而成为一个液相,这个温度叫做最高或最低会溶温度。
4. 二组分液态完全互溶向部分互溶过渡5. 二组分液态部分互溶向完全不互溶过渡6. 完全不互溶三、二组分固-液平衡体系1.固态完全不互溶系统2.热分析法冷却曲线出现平台的原因:释放的凝固热抵消了因冷却而散失的热量出现最低点:因最初非常微细的晶体难以析出,过冷现象导致斜率变小的原因:固态Bi析出所释放的凝固热部分抵消了降温过程散失的热量低共熔温度、低共熔混合物3.溶解度法4.固态部分互熔系统5.固态完全互熔系统晶内偏析:退火:淬火:6.生成稳定化合物的系统注:若化合物数目有N种,则其相图就被看作是由(N+1)个简单低共熔点的固态不互溶系统的相图组合而成。





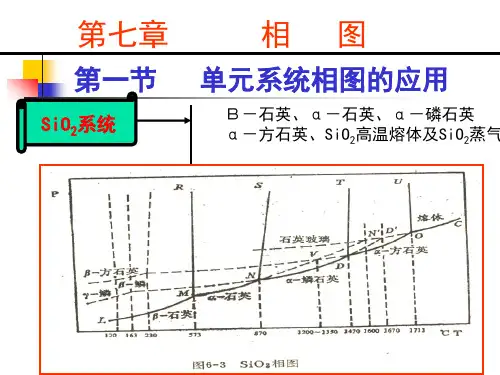

1.相律的有关概念与相律表达式(1)独立组份数C=S-R-R′。
S为物种数,R为独立化学反应计量式数目。
R′ 为同一相中独立的浓度限制条件数(包括不同物种依反应计量式比例关系及离子物种电中性条件)(2)自由度数f,系指相平衡体系中相数保持不变时,所具有独立可变的强度变量数。
(3)相律内容及其数学表达式。
相律就是揭示pVT平衡系统中自由度数、独立组份数和相数三者之间的制约关系。
表达式为:f=C-Φ+2;式中(式中 2 指T、p两强度变量)当T、p中有任一固定,则表达式为:条件自由度数f*=C-Φ+1当考虑除T、p、X B以外的其他变量或相间有某种限制时,则表达式为f=C-Φ+n;(式中n≥2)(4)相律的局限性与应用的关键性。
相律是一个定性规律,它指明特定条件下该平衡系统至多存在的相数及其相应的独立变量数,但不能指明是哪些相共存?哪些性质可作为独立变量及其它们之间的定量关系?相律对单相与复相都适用,但应用相律时,首先要考察系统是否满足相律成立的条件,并确定系统的组份数。
2.单组份系统的相图与特征(1)单组份系统相律与相图:因C=1 ,故相律表达式为f=3-Φ。
显然f最小为零,Φ最多应为 3 ,因相数最少为 1 ,故自由度数最多为 2 。
相图是用几何图形来描述多相平衡系统宏观状态与T、p、X B(组成)的关系。
在单组份相图中有单相的面、两相平衡线和三相平衡的点,自由度分别为f=2、f=1、f=0。
(2)单组份相变的特征与类型。
相变是一个连续的质的飞跃。
相平衡时物质在各相中的化学势相等,相变时某些物理性质有突变。
根据物性的不同变化有一级相变和连续相变(包括二级相变等高阶相变)之分;前者广为存在如气、液、固之间转变,其特点是物质在两相中的化学势一级导数不相等,且发生有限的突变〔即〕,此类相变平衡曲线斜率符合克拉贝龙方程。
后者如氦He(Ⅰ)与He(Ⅱ)的转变。
正常状态与超导状态的转变,其特点是化学势的一级导数在相变点连续〔即V1=V2,S1=S2〕,但化学势二级导数在相变点附近则迅速变化,出现一个极大峰如;或。

第6章单组元相图及纯晶体的凝固物质由液态转变为固态的过程称为凝固。
物质由液态转变为晶态的过程称为结晶材料的性能组织结构相种类数量尺寸形状分布C ONTENTS6.1 单元系相变的热力学及相平衡6.2纯晶体的凝固6.1单元系相变的热力学及相平衡1. 相(Phase)在一个系统中,成分、结构相同,性能一致的均匀的组成部分叫做相,不同相之间有明显的界面分开,该界面称为相界面。
注意:相在物理性能和化学性能上是均匀的。
相界面和晶界的区别。
6.1单元系相变的热力学及相平衡2. 组元(Component)组元通常是指系统中每一个可以单独分离出来,并能独立存在的化学纯物质,在一个给定的系统中,组元就是构成系统的各种化学元素或化合物。
按组元数目,将系统分为:一元系二元系三元系……化学元素:Cu, Ni, Fe 等化合物:Al 2O 3, MgO, Na 2O, SiO 2等6.1单元系相变的热力学及相平衡3. 相平衡在某一温度下,系统中各个相经过很长时间也不互相转变,处于平衡状态,这种平衡称为相平衡。
各组元在各相中的温度、压力和化学势相同。
A B热力学动态平衡6.1单元系相变的热力学及相平衡4.吉布斯相律(Gibbs Phase Rule)处于热力学平衡状态的系统中自由度与组元数和相数之间的关系定律,通常简称为相律。
f = C-P+N只考虑温度和压力对系统平衡状态的影响:f = C-P+2凝聚系统:f = C-P+1式中:f(freedom)是自由度数;C(component)是组成材料系统的独立组元数;P(phase)是平衡相的数目。
吉布斯相律的应用和局限性相律是检验、分析和使用相图的重要工具,利用它可以分析和确定系统中可能存在的相数,检验和研究相图。
注意使用相律有一些限制:(1)只适用于热力学平衡状态,各相温度相等、压力相等、化学势相等(化学平衡)。
(2)只表示体系中组元和相的数目,不能指明组元和相的类型和含量。
相图的知识点总结一、相图的基本概念1. 相:在热力学上,相是物质在宏观上具有一致的物理化学性质的部分。
常见的相包括固态、液态和气态。
在相图中,我们研究物质在不同条件下的相之间的转化关系。
2. 相变:相变是指物质从一种相转变为另一种相的过程。
例如固态到液态的熔化,液态到气态的汽化等,这些都是相变过程。
3. 相图:相图是在一定条件下,用图形方式表示物质对温度、压力、成分等条件变化而产生的相变规律的图。
常见的相图包括平衡相图、相图、反应平衡相图等。
二、相图的表示方法1. 温度-浓度相图:这种相图是根据不同成分的合金在不同温度下的相变关系进行绘制的。
通常用等温线(等温变化)和等浓度线(等浓度变化)来表示。
2. 压力-温度相图:这种相图是以压力和温度为坐标轴,描述物质在不同压力和温度条件下的相变规律。
对于气体和气体混合物的相图,常用此种表示方法。
3. 化学反应平衡相图:这种相图是表示化学反应在不同温度和压力条件下的平衡相态。
通过这种相图可以了解化学反应在不同条件下的平衡规律,对于化学工程和环境保护有着重要的意义。
三、相图的应用1. 材料设计与开发:相图在材料工程和材料科学中有着重要的应用。
通过研究合金和混合物在不同条件下的相变规律,可以设计和开发具有特定性能和特征的新材料。
2. 工艺优化:在材料的加工和制备过程中,研究相图可以帮助我们选择最合适的工艺参数,以达到最佳的加工效果和产品性能。
3. 环境保护:通过研究化学反应平衡相图,可以帮助我们了解化学反应在不同条件下的平衡态,从而有助于环境保护和资源循环利用。
四、相图的局限性尽管相图在材料研究和工程应用中具有重要的作用,但也存在一些局限性。
例如,相图可能忽略了一些非平衡相变过程,而在实际应用中许多相变过程都是非平衡过程。
此外,相图中也可能无法完全描述复杂体系的相变规律,因此在实际研究和应用中需要结合实验数据和理论模型进行分析。
总之,相图是物质科学中重要的工具,在材料研究和工程应用中具有重要的作用。