韦格纳肉芽肿诊疗指南
- 格式:doc
- 大小:40.50 KB
- 文档页数:4
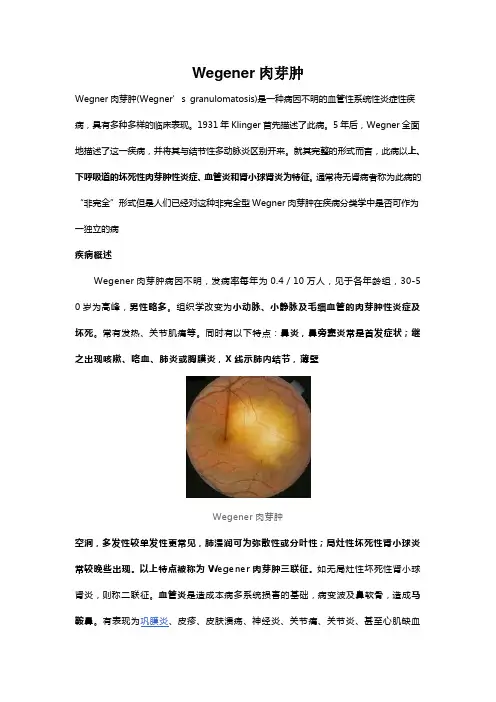
Wegener肉芽肿Wegner肉芽肿(Wegner’s granulomatosis)是一种病因不明的血管性系统性炎症性疾病,具有多种多样的临床表现。
1931年Klinger首先描述了此病。
5年后,Wegner全面地描述了这一疾病,并将其与结节性多动脉炎区别开来。
就其完整的形式而言,此病以上、下呼吸道的坏死性肉芽肿性炎症、血管炎和肾小球肾炎为特征。
通常将无肾病者称为此病的“非完全”形式但是人们已经对这种非完全型Wegner肉芽肿在疾病分类学中是否可作为一独立的病疾病概述Wegener肉芽肿病因不明,发病率每年为0.4/10万人,见于各年龄组,30-5 0岁为高峰,男性略多。
组织学改变为小动脉、小静脉及毛细血管的肉芽肿性炎症及坏死。
常有发热、关节肌痛等。
同时有以下特点:鼻炎,鼻旁窦炎常是首发症状;继之出现咳嗽、咯血、肺炎或胸膜炎,X线示肺内结节,薄壁Wegener肉芽肿空洞,多发性较单发性更常见,肺浸润可为弥散性或分叶性;局灶性坏死性肾小球炎常较晚些出现。
以上特点被称为Wegener肉芽肿三联征。
如无局灶性坏死性肾小球肾炎,则称二联征。
血管炎是造成本病多系统损害的基础,病变波及鼻软骨,造成马鞍鼻。
有表现为巩膜炎、皮疹、皮肤溃疡、神经炎、关节痛、关节炎、甚至心肌缺血者。
血C—ANCA阳性是一特征。
早期病例阳性率为50%,三联征活动期病例可达1 00%,静止期常为阴性,大多病例的滴度与病情活动程度呈平行关系。
过去死亡率很高,自从联合使用肾上腺糖皮质激素和环磷酰胺,缓解率在90%以上,4年存活率为88%。
病变局限在呼吸道者,有人主张用复方新诺明(磺胺甲基异恶唑加甲氧苄氨嘧啶)治疗。
流行病学Wegner肉芽肿属于非常见病,且易误诊,其流行病学还不十分清楚据估计美国Wegner肉芽肿的发病率接近3×10-5。
来自英国的四项研究显示该病的年发病率为0.5×10-6~8.5×10-6。



wegener肉芽肿病诊断标准(一)Wegener肉芽肿病诊断标准什么是Wegener肉芽肿病?Wegener肉芽肿病是一种罕见的血管炎性疾病,其特点是累及呼吸道和肾脏,并可伴发其他多系统症状,如关节痛、发热、出血等。
Wegener肉芽肿病的诊断标准Wegener肉芽肿病的诊断标准为美国风湿病学会(ACR)和欧洲风湿病学会(EULAR)所公认的诊断标准,主要包括以下几点:1.上、下呼吸道病变:包括持续或反复出现的鼻塞、鼻出血、鼻窦炎、中耳病变等上呼吸道病变,以及肺实质、肺间质病变等下呼吸道病变。
2.肾脏病变:出现血尿、蛋白尿、肾功能损害等肾脏病变。
3.肺部影像学改变:X线、CT、MRI等检查发现肺部广泛浸润性病变。
4.组织学检查:通过组织学检查发现具有特征性的坏死性血管炎,伴有肉芽肿、坏死和炎症细胞浸润等特点。
5.血清ANCA阳性:具有抗中性粒细胞胞浆抗体(ANCA)阳性结果。
诊断过程中应注意的问题在进行Wegener肉芽肿病的诊断过程中,需要注意以下几点:1.诊断应是全面的,需要综合考虑患者的症状、体征、实验室检查和影像学检查等因素。
2.ANCA的阳性和组织学检查是诊断的重要指标,但不是必备条件,特别是对于早期病例和轻度病例,可能出现阴性结果。
3.需要排除其他类似的疾病,如结节性多动脉炎、显微镜下多血管炎等。
结论Wegener肉芽肿病的诊断标准为根据上、下呼吸道病变、肾脏病变、肺部影像学改变、组织学检查和血清ANCA阳性等指标进行综合评估。
在进行诊断时需要注意全面性和排除其他类似疾病的可能。
病例分析一般来说,Wegener肉芽肿病的症状表现各异,但其主要表现常包括呼吸道或肺部症状、肾脏症状和全身症状等。
以下是一个病例分析:患者女性,年龄35岁,近期出现了咳嗽、咳痰和呼吸急促等呼吸道症状,同时伴有血尿、蛋白尿和乏力等肾脏症状,有体重下降、发热等全身症状。
X线检查显示肺部有广泛浸润性病变。
经过一系列实验室检查和影像学检查,发现该患者血清ANCA阳性,肾脏活检发现具有特征性的坏死性血管炎,伴有肉芽肿、坏死和炎症细胞浸润等特点。




wegener肉芽肿病诊断标准标题:Wegener肉芽肿病诊断标准详解文档正文:Wegener肉芽肿病(Wegener's Granulomatosis,WG),现称为肉芽肿性多血管炎(GPA),是一种罕见的自身免疫性疾病,主要累及上、下呼吸道和肾脏。
其诊断过程复杂且关键,需要综合临床表现、实验室检查以及组织病理学证据。
以下是Wegener肉芽肿病的主要诊断标准:1. **临床症状**:- 上呼吸道表现:鼻窦炎、鼻炎或喉炎等,可伴有鼻中隔穿孔、脓性分泌物或出血。
- 下呼吸道表现:肺部受累表现为咳嗽、咳痰、呼吸困难、胸痛及血痰等,胸部影像学可见结节、空洞或肺炎样改变。
- 肾脏受累:出现血尿、蛋白尿、肾功能异常等。
2. **实验室检查**:- 血液检查:常有贫血、血小板减少、ESR升高、CRP升高等炎症反应指标异常。
- ANCA(抗中性粒细胞胞浆抗体)检测:约90%的WG患者ANCA阳性,其中以C-ANCA(胞质型)为主,且多数与PR3-ANCA(蛋白酶3-ANCA)相关。
3. **病理学证据**:- 组织活检:通过鼻黏膜、肺、肾或其他受累器官的活检,发现典型的肉芽肿性炎症改变,即中小血管壁的坏死性肉芽肿性炎症,并且结合临床病史和实验室检查结果,可以明确诊断。
根据以上内容,通常采用以下诊断流程:- 若存在上呼吸道和下呼吸道的症状加上肾受累的表现,并且ANCA检测为C-ANCA阳性,高度怀疑WG。
- 进一步通过相应部位的组织活检获取病理学证据,证实为特征性的肉芽肿性血管炎,则可确诊为Wegener肉芽肿病。
请注意,由于WG病情进展迅速且预后严重,早期准确诊断并及时治疗至关重要。
在临床实践中,应由经验丰富的医生根据全面的评估结果做出最终诊断。



韦格氏肉芽肿诊断标准
韦格纳肉芽肿的诊断标准主要基于临床表现、组织病理检查和实验室检查等多方面的综合考虑。
根据1990年美国风湿病学会提出的分类标准,韦格纳肉芽肿的诊断需要满足以下四条中的至少两条:
1. 上呼吸道、下呼吸道或肾脏出现坏死性肉芽肿性炎症。
2. 抗中性粒细胞胞质抗体(ANCA)阳性。
3. 肾脏活检显示坏死性肾小球肾炎或坏死性新月体性肾炎。
除了上述分类标准外,还需要结合患者的临床表现和实验室检查进行综合分析。
韦格纳肉芽肿的典型临床表现包括发热、体重下降、乏力、关节痛、鼻窦炎、鼻出血、咳嗽、呼吸困难、血尿、蛋白尿等。
实验室检查方面,可以出现血沉增快、C反应蛋白升高、肾功能异常等指标异常。
需要注意的是,韦格纳肉芽肿的诊断需要排除其他可能引起类似临床表现的疾病,如结节病、过敏性肉芽肿性血管炎等。
因此,在确诊前需要进行全面的评估和鉴别诊断。
总之,韦格纳肉芽肿的诊断需要综合考虑临床表现、组织病理检查和实验室检查等多方面的信息,并进行全面的评估和鉴别诊断。
韦格内肉芽肿的病因治疗与预防韦格纳(Wegenergranulomatosis,WG)肉芽肿是一种临床表现复杂、预后不良的系统性坏死性血管炎,其特征是全呼吸道肉芽肿病变、系统性坏死性血管炎和肾小球-肾炎。
Klinger(1931)首次报告一例,解剖为"结节性多动脉炎的界限型"。
Wegner1936年报告3例,1939年报告18例,根据活检和尸检资料命名本病"鼻源性肉芽肿",它主要涉及动脉和肾脏,被命名为韦格纳肉芽肿。
抗中性粒细胞浆抗体(ANCA)发现和免疫病理学研究证明,韦格纳肉芽肿是一种自身免疫性疾病。
超过三分之二的患者类风湿因子阳性也表明,这是由自身免疫反应形成的免疫复合物引起的一系列炎症反应,激活补体介导。
ANCA与原蛋白激酶相对应-3(PR-3)和过氧化物酶,依照细胞染色的表现型前者称为C-ANCA,后者称为P-ANCA,在WG 中C-ANCA特异性高。
C-ANCA血管内皮细胞、多型核细胞CD4淋巴细胞的细胞内或细胞表面物质也可以通过TNF-a和可溶性IL-受体刺激上述细胞,进一步说明了免疫病理过程引起的血管炎。
有相当多的证据支持韦格纳肉芽肿是一种自身免疫性疾病,ANCA可能参与血管的激活和损伤。
WG与抗PR3.自身抗体具有很强的特异性关系,抗体效率与临床疾病的活动性有关,测复发。
该病对免疫抑制剂的治疗反应良好。
但也有不支持的基础。
尽管在大多数情况下WG(韦格纳肉芽肿)患者血清中可检测到抗性PR3特异抗体,但仍有少数患者ANCA阴性。
其次,在受累组织中,既没有发现自己的抗体,也没有自己的反应T细胞,没有发现抗性PR3.免疫复合物。
因此,即使提示ANCA在WG这种疾病有一定的作用,也不是最基本的作用。
该病起病缓慢,全身症状包括全身不适、疲劳、厌食、消瘦和发烧。
发烧通常与上呼吸道感染有关,特别是鼻窦继发性感染。
也可发生在无明显活性活性感染的患者中,并出现本病的原发症状。
【疾病名】韦格纳肉芽肿【英文名】Wegner granulomatosis【别名】韦格内肉芽肿;Wegener granulomatosis;韦格纳肉芽肿病;Wegener 肉芽肿;坏死性肉芽肿【ICD号】M31.3【病因和发病机制研究的进展】1.病因研究进展2.发病机制研究进展 韦格纳肉芽肿病(Wegener granulomatosis,WG)是一种特殊的全身性血管炎病变,最初可从头颈部症状开始。
Godman提出WG必须满足三个条件:上呼吸道坏死性肉芽肿病变、血管炎及肾小球肾炎(即威格纳三联征),近年增加了c-ANCA阳性。
Fienberg和Carrington先后提出局限性WG的概念,即病变局限于一个解剖学部位而未广泛累及多系统。
光镜下WG显示三种病变:坏死、肉芽肿及真正的血管炎,其他继发改变有微脓肿和纤维化。
遗憾的是头颈部活检标本常缺乏其中一项、两项、甚至全部三项典型病变。
病变中坏死很有特点,坏死带在病变组织中分布不均匀,低倍镜下呈地图样,边缘呈波状或明显锯齿状。
坏死常呈嗜碱性,并有细碎的颗粒。
坏死带常被多核巨细胞围绕。
‘肉芽肿性炎症’是对不同表现具有根本不同含义的一个名词。
一般显微镜下‘肉芽肿性炎症’是指单核组织细胞(巨噬细胞)和炎细胞对刺激的一种反应:包括感染(如分支杆菌或霉菌)、毒素因子或异物、肿瘤、不明刺激、类肉瘤病和WG。
WG的肉芽肿性炎症巨嗜细胞的聚集十分稀疏,不象类肉瘤病或结核病中巨嗜细胞聚集得那样紧密。
此外WG中多核巨细胞与急、慢性炎细胞同时存在。
WG的血管炎不同于非特异性慢性炎症,后者仅显示血管增生而缺乏真正的血管壁损伤。
WG的血管炎出现血管壁损伤,典型的是累犯中小动静脉的纤维素样坏死。
这种血管壁损伤又伴有急、慢性炎细胞浸润。
有时在血管壁出现肉芽肿性炎症。
WG的肺部病理改变与头颈部相似,显示坏死、肉芽肿性炎症与血管炎特点更为显著。
肾脏表现常为非特异性坏死性肾小球肾炎。
【诊断研究进展】1.辅助诊断检查进展(1)实验室检查进展:①一般检查:WG实验室检查出现血沉升高、血浆I gG升高,但缺乏特异性指标。
第15章韦格纳肉芽肿【概述】韦格纳肉芽肿(Wegener's granulomatosis,WG)是一种坏死性肉芽肿性血管炎,属自身免疫性疾病。
病变累及小动脉、静脉及毛细血管,偶尔累及大动脉,其病理以血管壁的炎症为特征,主要侵犯上、下呼吸道和肾脏,韦格纳肉芽肿通常以鼻黏膜和肺组织的局灶性肉芽肿性炎症为开始,继而进展为血管的弥漫性坏死性肉芽肿性炎症。
临床常表现为鼻和副鼻窦炎、肺病变和进行性肾功能衰竭。
还可累及关节、眼、皮肤,亦可侵及心脏、神经系统及耳等。
无肾脏受累者被称为局限性韦格纳肉芽肿。
该病男性略多于女性,从儿童到老年人均可发病,最近报道的年龄范围在5~91岁之间发病,但中年人多发,40~50岁是本病的高发年龄,平均年龄为41岁。
各人种均可发病,根据美国Gary S. Hoffma的研究,韦格纳肉芽肿的发病率为每30000~50000人中有一人发病,其中97%的患者是高加索人,2%为黑人,1%为其他种族。
我国发病情况尚无统计资料。
未经治疗的韦格纳肉芽肿病死率可高达90%以上,经激素和免疫抑制剂治疗后,韦格纳肉芽肿的预后明显改善。
尽管该病有类似炎性过程,但尚无独立的致病因素,病因至今不明。
【临床表现】韦格纳肉芽肿临床表现多样,可累及多系统。
典型的韦格纳肉芽肿有三联征:上呼吸道、肺和肾病变。
1.一般症状可以起病缓慢,持续一段时间,也可表现为快速进展性发病。
病初症状包括发热、疲劳、抑郁、纳差、体重下降、关节痛、盗汗、尿色改变和虚弱,其中发热最常见。
发热有时是由鼻窦的细菌感染引起。
2.上呼吸道症状大部分患者以上呼吸道病变为首发症状。
通常表现是持续性流涕,而且不断加重。
流涕可来源于鼻窦的分泌,并导致上呼吸道的阻塞和疼痛。
伴有鼻黏膜溃疡和结痂,鼻出血,唾液中带血丝。
鼻窦炎可以较轻,严重者鼻中隔穿孔,鼻骨破坏,出现鞍鼻。
咽鼓管的阻塞能引发中耳炎,导致听力丧失,而后者常是患者的第一主诉。
部分患者可因声门下狭窄出现声音嘶哑及呼吸喘鸣。
3.下呼吸道症状肺部受累是韦格纳肉芽肿基本特征之一,约50%的患者在起病时即有肺部表现,总计80%以上的患者将在整个病程中出现肺部病变。
胸闷、气短、咳嗽、咯血以及胸膜炎是最常见的症状。
大量肺泡性出血较少见,但一旦出现,则可发生呼吸困难和呼吸衰竭。
有约1/3的患者肺部影像学检查有肺内阴影,可缺乏临床症状。
查体可有叩浊、呼吸音减低以及湿啰音等体征。
因为支气管内膜受累以及疤痕形成,55%以上的患者在肺功能检测时可出现阻塞性通气功能障碍,另有30%~40%的患者可出现限制性通气功能障碍以及弥散功能障碍。
4.肾脏损害大部分病例有肾脏病变,出现蛋白尿,红、白细胞及管型尿,严重者伴有高血压和肾病综合征,终可导致肾功能衰竭,是韦格纳肉芽肿的重要死因之一。
无肾脏受累者称为局限型韦格纳肉芽肿,应警惕部分患者在起病时无肾脏病变,但随病情进展可逐渐发展至肾小球肾炎。
5.眼受累眼受累的最高比例可至50%以上,其中约15%的患者为首发症状。
韦格纳肉芽肿可累及眼的任何区域,表现为眼球突出、视神经及眼肌损伤、结膜炎、角膜溃疡、表层巩膜炎、虹膜炎、视网膜血管炎、视力障碍等。
6.皮肤黏膜多数患者有皮肤黏膜损伤,表现为下肢可触及的紫癜、多形红斑、斑疹、瘀点(斑)、丘疹、皮下结节、坏死性溃疡形成以及浅表皮肤糜烂等。
其中皮肤紫癜最为常见。
7.神经系统很少有韦格纳肉芽肿患者以神经系统病变为首发症状,但仍有约1/3的患者在病程中出现神经系统病变。
以外周神经病变最常见,多发性单神经炎是主要的病变类型,临床表现为对称性的末梢神经病变。
肌电图以及神经传导检查有助于外周神经病变的诊断。
8.关节病变关节病变在韦格纳肉芽肿中较为常见,约30%的患者发病时有关节病变,全部病程中可有约70%的患者关节受累。
多数表现为关节疼痛以及肌痛,1/3的患者可出现对称性、非对称性以及游走性关节炎(可为单关节、寡关节或多关节的肿胀和疼痛)。
9.其他韦格纳肉芽肿也可累及心脏而出现心包炎、心肌炎。
胃肠道受累时可出现腹痛、腹泻及出血;尸检时可发现脾脏受损(包括坏死、血管炎以及肉芽肿形成)。
泌尿生殖系统(不包括肾脏),如膀胱炎、睾丸炎、附睾炎等受累较少见。
【诊断要点】1.诊断及分类标准韦格纳肉芽肿的诊断时间平均为5~15个月。
国外资料报道其中40%的诊断是在不到三个月的时间里得出的,10%可长达5~15年才被诊断。
为了达到最有效的治疗,韦格纳肉芽肿早期诊断至关重要。
无症状患者可通过血清学检查ANCA(尤其是c-ANCA)以及鼻窦和肺脏的CT扫描有助于诊断。
上呼吸道、支气管内膜及肾脏活检是诊断的重要依据,病理显示肺小血管壁有中性粒细胞及单个核细胞浸润,可见巨细胞、多形核巨细胞肉芽肿,可破坏肺组织,形成空洞。
肾病理为局灶性、节段性、新月体性坏死性肾小球肾炎,免疫荧光检测无或很少免疫球蛋白及补体沉积。
当诊断困难时,有必要进行胸腔镜或开胸活检以提供诊断的病理依据。
目前韦格纳肉芽肿的诊断标准采用1990年美国风湿病学会(ACR)分类标准(见表16-1):表16-1. 1990年美国风湿病学会(ACR)韦格纳肉芽肿分类标准1.鼻或口腔炎症痛性或无痛性口腔溃疡,脓性或血性鼻腔分泌物2.胸片异常胸片示结节、固定浸润病灶或空洞3.尿沉渣异常镜下血尿(RBC>5/高倍视野)或出现红细胞管型4.病理性肉芽肿性炎性改变动脉壁或动脉周围,或血管(动脉或微动脉)外区域有中性粒细胞浸润形成肉芽肿性炎变符合2条或2条以上时可诊断为韦格纳肉芽肿,诊断的敏感性和特异性分别为88.2%和92.0%。
韦格纳肉芽肿在临床上常被误诊,为了能早期诊断,对有以下情况者应反复进行活组织检查:不明原因的发热伴有呼吸道症状;慢性鼻炎及副鼻窦炎,经检查有黏膜糜烂或肉芽组织增生;眼、口腔黏膜有溃疡、坏死或肉芽肿;肺内有可变性结节状阴影或空洞;皮肤有紫癜、结节、坏死和溃疡等。
2.鉴别诊断韦格纳肉芽肿主要与以下几种疾病鉴别:(1)显微镜下多血管炎(microscopic polyangiitis, MPA):目前认为显微镜下多血管炎为一独立的系统性血管炎。
是一种主要累及小血管的系统性坏死性血管炎,可侵犯肾脏、皮肤和肺等脏器的小动脉、微动脉、毛细血管的小静脉。
常表现为坏死性肾小球肾炎和肺毛细血管炎。
累及肾脏时出现蛋白尿、镜下血尿和红细胞管型。
抗中性粒细胞胞浆抗体(ANCA)阳性是MPA的重要诊断依据,60%~80%为髓过氧化物酶(MPO)-ANCA阳性,在荧光检测法示核周型(p-ANCA)阳性,胸部X线检查在早期可发现无特征性肺部浸润影或小泡状浸润影,中晚期可出现肺间质纤维化。
(2)变应性肉芽肿性血管炎(Churg-Strauss Syndrome):有重度哮喘;肺和肺外脏器有中小动脉、静脉炎及坏死性肉芽肿;周围血嗜酸性粒细胞增高。
韦格纳肉芽肿与CSS均可累及上呼吸道,但前者常有上呼吸道溃疡,胸片示肺内有破坏性病变如结节、空洞形成,而在CSS则不多见。
韦格纳肉芽肿病灶中很少有嗜酸性粒细胞浸润,周围血嗜酸性粒细胞增高不明显,也无哮喘发作。
(3)淋巴瘤样肉芽肿病(Lymphomatoid granulomatosis):是多形细胞浸润性血管炎和血管中心性坏死性肉芽肿病,浸润细胞为小淋巴细胞、浆细胞、组织细胞及非典型淋巴细胞,病变主要累及肺、皮肤、神经系统及肾间质,但不侵犯上呼吸道。
(4)肺出血-肾炎综合征(Goodpasture syndrome):是以肺出血和急进性肾小球肾炎为特征的综合征,抗肾小球基底膜抗体阳性,由此引致的弥漫性肺泡出血及肾小球肾炎综合征,以发热、咳嗽、咯血及肾炎为突出表现,但一般无其它血管炎征象。
本病多缺乏上呼吸道病变,肾病理可见基底膜有免疫复合物沉积。
(5)复发性多软骨炎:复发性多软骨炎是以软骨受累为主要表现,临床表现也可有鼻塌陷、听力障碍、气管狭窄,但该病一般均有耳廓受累,而无鼻窦受累,实验室检查ANCA阴性,活动期抗Ⅱ型胶原抗体阳性。
【治疗方案及原则】治疗可分为3期,即诱导缓解、维持缓解以及控制复发。
循证医学(EBM)显示糖皮质激素加环磷酰胺(CYC)联合治疗有显著疗效,特别是肾脏受累以及具有严重呼吸系统疾病的患者,应作为首选治疗方案。
目前认为未经治疗的韦格纳肉芽肿患者的预后很差,90%以上的患者在两年内死亡,死因通常是呼吸衰竭或/和肾功能衰竭。
1.糖皮质激素活动期用泼尼松1.0~1.5 mg/(kg•d)。
用4~6周,病情缓解后减量并以小剂量维持。
对严重病例如中枢神经系统血管炎、呼吸道病变伴低氧血症如肺泡出血、进行性肾功能衰竭,可采用冲击疗法:甲基泼尼松龙1.0 g/d 3天,第4天改口服泼尼松1.0~1.5mg/(kg•d),然后根据病情逐渐减量。
2.免疫抑制剂(1)环磷酰胺:通常给予口服CYC 1~3 mg/(kg•d),也可用CYC 200mg,隔日一次。
对病情平稳的患者可用1mg/(kg•d)维持。
对严重病例给予CYC 1.0g冲击治疗,每3~4周一次,同时给予每天口服CYC 100mg。
CYC是治疗本病的基本药物,可使用一年或数年,撤药后患者能长期缓解。
用药期间注意观察不良反应,如骨髓抑制、继发感染等。
循证医学显示,CYC能显著地改善韦格纳肉芽肿患者的生存期,但不能完全控制肾脏等器官损害的进展。
(2)硫唑嘌呤:为嘌呤类似药,有抗炎和免疫抑制双重作用,有时可替代CYC。
一般用量为2~2.5mg/(kg•d),总量不超过200 mg/d。
,但需根据病情及个体差异而定,用药期间应监测不良反应。
如CYC不能控制病情,可合并使用硫唑嘌呤或改用硫唑嘌呤。
(3)甲氨蝶呤(MTX):MTX一般用量为10~25mg,一周一次,口服、肌注或静注疗效相同,如CYC不能控制可合并使用之。
(4)环孢霉素:作用机理为抑制IL-2合成,抑制T淋巴细胞的激活。
优点为无骨髓抑制作用。
但免疫抑制作用也较弱。
常用剂量为3 ~ 5mg/(kg•d)。
(5)霉酚酸酯:初始用量1.5g/d,分3次口服,维持3月,维持剂量1.0g/d,分2~3次口服,维持6~9月。
(6)丙种球蛋白:静脉用丙种球蛋白(IVIG)与补体和细胞因子网络相互作用,提供抗独特型(anti-idiotypic)抗体作用于T、B细胞。
大剂量丙球还具有广谱抗病毒、细菌及中和循环性抗体的作用。
一般与激素及其他免疫抑制剂合用,剂量为300~400mg/(kg•d),连用5 ~ 7天。
3.其他治疗(1)复方新诺明片:对于病变局限于上呼吸道以及已用泼尼松和CYC控制病情者,可选用复方新诺明片进行抗感染治疗(2~6片/日),认为有良好疗效,能预防复发,延长生存时间。
在使用免疫抑制剂和激素治疗时,应注意预防卡氏肺囊虫感染所致的肺炎,约6%的韦格纳肉芽肿患者在免疫抑制治疗的过程出现卡氏肺囊虫肺炎,并可成为韦格纳肉芽肿的死亡原因。