2016年全国普通高等学校招生统一考试化学(北京卷精编版)
- 格式:pdf
- 大小:592.74 KB
- 文档页数:7

绝密★启封并使用完毕前试题类型:2016年普通高等学校招生全国统一考试理科综合能力测试(化学)注意事项:1.本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分。
2.答题前,考生务必将自己的姓名、准考证号填写在本试题相应的位置。
3.全部答案在答题卡上完成,答在本试题上无效。
4.考试结束后,将本试题和答题卡一并交回。
第Ⅰ卷(选择题共126分)本卷共21小题,每小题6分,共126分。
可能用到的相对原子质量:一、选择题:本大题共13小题,每小题6分。
在每小题给出的四个选项中,只有一项是符合题目要求的。
7.下列关于燃料的说法错误的是A.燃料燃烧产物CO2是温室气体之一B.化石燃料完全燃烧不会造成大气污染C.以液化石油气代替燃油可减少大气污染D.燃料不完全燃烧排放的CO是大气污染物之一8.下列各组中的物质均能发生就加成反应的是A.乙烯和乙醇B.苯和氯乙烯C.乙酸和溴乙烷D.丙烯和丙烷9.a、b、c、d为短周期元素,a的原子中只有1个电子,b2-和c+的电子层结构相同,d与b同族。
下列叙述错误的是A.a与其他三种元素形成的二元化合物中其化合价均为+1B.b与其他三种元素均可形成至少两种二元化合物C.c的原子半径是这些元素中最大的D.d与a形成的化合物的溶液呈弱酸性10.分子式为C4H8Cl2的有机物共有(不含立体异构)A.7种B.8种C.9种D.10种11.Mg–AgCl电池是一种以海水为电解质溶液的水激活电池。
下列叙述错误..的是A.负极反应式为Mg–2e–=Mg2+B.正极反应式为Ag++e–=AgC.电池放电时Cl–由正极向负极迁移D.负极会发生副反应Mg+2H2O=Mg(OH)2+H2↑12.某白色粉末由两种物质组成,为鉴别其成分进行如下实验:①取少量样品加入足量水仍有部分固体未溶解:再加入足量稀盐酸,有气泡产生,固体全部溶解;②取少量样品加入足量稀盐酸有气泡产生,震荡后仍有固体存在。
该白色粉末可能为A.NaHCO3、Al(OH)3B.AgCl、NaHCO3C.Na2SO3、BaCO3D.Na2CO3、CuSO413.下列实验操作能达到实验目的的是实验目的实验操作A. 制备Fe(OH)3胶体将NaOH浓溶液滴加到饱和FeCl3溶液中B. 由MgCl2溶液制备无水MgCl2将MgCl2溶液加热蒸干C. 除去Cu粉中混有的CuO 加入稀硝酸溶液,过滤、洗涤、干燥D. 比较水与乙醇中氢的活泼性分别将少量钠投入到盛有水和乙醇的烧杯中第II卷(非选择题共174分)三、非选择题:包括必考题和选考题两部分。
2016年普通高等学校招生全国统一考试
化学
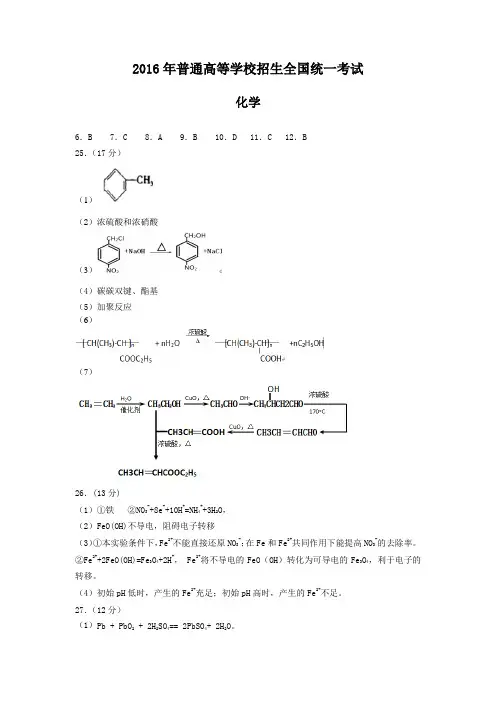
6.B 7.C 8.A 9.B 10.D 11.C 12.B
25.(17分)
(1)
(2)浓硫酸和浓硝酸
(3)
(4)碳碳双键、酯基
(5)加聚反应
(6)
(7)
26.(13分)
(1)①铁②NO3-+8e-+10H+=NH4++3H2O,
(2)FeO(OH)不导电,阻碍电子转移
(3)①本实验条件下,Fe2+不能直接还原NO3-;在Fe和Fe2+共同作用下能提高NO3-的去除率。
②Fe2++2FeO(OH)=Fe3O4+2H+, Fe2+将不导电的FeO(OH)转化为可导电的Fe3O4,利于电子的转移。
(4)初始pH低时,产生的Fe2+充足;初始pH高时,产生的Fe2+不足。
27.(12分)
(1)Pb + PbO
2 + 2H2SO4== 2PbSO4+ 2H2O。
(2)①2Fe3++Pb+SO42—==PbSO4+2Fe2+;
②取a中红色溶液少量,加入过量Pb,充分反应后,红色褪去。
(3)①A、B;②将粗PbO溶解在一定量35%NaOH溶液中,加热至110℃,充分溶解后,趁热过滤,冷却结晶,过滤得到PbO固体。
28.(16分)
(1)2Ag++SO32—Ag2SO4↓。
(2)①有红色固体生成;②a.HCl和BaCl2溶液。
b.在I-的作用下,Cu2+转化为白色沉淀CuI,SO32-转化为SO42-。
(3)①Al3+、OH-。
②a、,b、V1明显大于V2。
(4)亚硫酸盐的溶解性、氧化还原性、在水溶液中的酸碱性;两种盐溶液中阴阳离子的性质和反应条件。

2016年普通高等学校招生全国统一考试(新课标I卷)理科综合(化学部分)7.化学与生活密切相关。
下列有关说法错误的是()A、用灼烧的方法可以区分蚕丝和人造纤维B、食用油反复加热会产生稠环芳烃等有害物质C、加热能杀死流感病毒是因为蛋白质受热变性D、医用消毒酒精中乙醇的浓度为95%【答案】D【解析】A、蚕丝的主要成分为蛋白质,灼烧时会有烧焦羽毛的气味,而人造纤维由纤维素改性得到,灼烧时有刺激性气味,可由此区分二者,故A正确。
B、食用油反复加热,碳链会变成环状,产生稠环芳烃等有害物质,故B正确。
C、加热、强酸碱、重金属盐均可以使蛋白质变性,因此加热可杀死流感病毒,故C正确。
D、医用酒精中乙醇的浓度为75%,工业酒精中乙醇的浓度为95%,故D错误。
因此,本题选D。
8.设N A为阿伏加德罗常数值。
下列有关叙述正确的是()A、14 g乙烯和丙烯混合气体中的氢原子数为2N AB、1 mol N2与4 mol H2反应生成的NH3分子数为2N AC、1 mol Fe溶于过量硝酸,电子转移数为2N AD、标准状况下,2.24L CCl4含有的共价键数为0.4N A【答案】A【解析】9.下列关于有机化合物的说法正确的是()A、2-甲基丁烷也称为异丁烷B、由乙烯生成乙醇属于加成反应C、C4H9Cl有3种同分异构体D、油脂和蛋白质都属于高分子化合物【答案】B【解析】10.作能达到实验目的的是()A、用长颈漏斗分离出乙酸与乙醇反应的产物B、用向上排空气法收集铜粉与稀硝酸反应产生的NOC、配制氯化铁溶液时,将氯化铁溶解在较浓的盐酸中再加水稀释D、将Cl2与HCl混合气体通过饱和食盐水可得到纯净的Cl2【答案】C【解析】11.三室式电渗析法处理含Na2SO4废水的原理如图所示,采用惰性电极,ab、cd均为离子交换膜,在直流电场的作用下,两膜中间的Na +和SO 42–可通过离子交换膜,而两端隔室中离子被阻挡不能进入中间隔室。

2016年普通高等学校招生全国统一考试理科综合能力测试(化学)注意事项:1.本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分。
2.答题前,考生务必将自己的姓名、准考证号填写在本试题相应的位置。
3.全部答案在答题卡上完成,答在本试题上无效。
4. 考试结束后,将本试题和答题卡一并交回。
第Ⅰ卷(选择题共126分)本卷共21小题,每小题6分,共126分。
可能用到的相对原子质量:一、选择题:本大题共13小题,每小题6分。
在每小题给出的四个选项中,只有一项是符合题目要求的。
7.化学与生活密切相关,下列有关说法错误的是A.用灼烧的方法可以区分蚕丝和人造纤维B.食用油反复加热会产生稠环芳香烃等有害物质C.加热能杀死流感病毒是因为蛋白质受热变性D.医用消毒酒精中乙醇的浓度为95%8.设N A为阿伏加德罗常数值。
下列有关叙述正确的是A.14 g乙烯和丙烯混合气体中的氢原子数为2N AB.1 molN2与4 molH2反应生成的NH3分子数为2N AC.1 molFe溶于过量硝酸,电子转移数为2N AD.标准状况下,2.24 LCCl4含有的共价键数为0.4N A9.下列关于有机化合物的说法正确的是A.2-甲基丁烷也称异丁烷B.由乙烯生成乙醇属于加成反应C.C4H9Cl有3中同分异构体D.油脂和蛋白质都属于高分子化合物10.下列实验操作能达到实验目的的是 A.用长颈漏斗分离出乙酸与乙醇反应的产物 B.用向上排空气法收集铜粉与稀硝酸反应产生的NOC.配制氯化铁溶液时,将氯化铁溶解在较浓的盐酸中再加水稀释D.将Cl 2与HCl 混合气体通过饱和食盐水可得到纯净的Cl 211.三室式电渗析法处理含Na 2SO 4废水的原理如图所示,采用惰性电极,ab 、cd 均为离子交换膜,在直流电场的作用下,两膜中间的Na +和24SO -可通过离子交换膜,而两端隔室中离子被阻挡不能进入中间隔室。
下列叙述正确的是A.通电后中间隔室的24SO -离子向正极迁移,正极区溶液pH 增大 B.该法在处理含Na 2SO 4废水时可以得到NaOH 和H 2SO 4产品 C.负极反应为2H 2O –4e –=O 2+4H +,负极区溶液pH 降低 D.当电路中通过1mol 电子的电量时,会有0.5mol 的O 2生成12.298K 时,在20.0mL 0.10mol 1L -⋅氨水中滴入0.10mol 1L -⋅的盐酸,溶液的pH 与所加盐酸的体积关系如图所示。

1.根据所给的信息和标志,判断下列说法错误的是( )【答案】B【解析】试题分析:A. 麻黄碱具有平喘功能,常用于治疗气喘咳嗽,正确;B.醋酸能够与碳酸氢钠反应,降低药效,错误;C.图示标志为放射性标志,对人体伤害较大,看到有该标志的丢弃物,应远离并报警,正确;D.该标志为可回收物标志,正确;故选B。
【考点定位】考查化学史、物质的性质和用途、化学实验安全【名师点晴】本题考查了物质的性质和用途、化学实验安全等知识点。
题目比较基础,要熟悉常见的化学标志:如物品回收标志;中国节能标志;禁止放易燃物标志;节水标志;禁止吸烟标志;中国环境标志;绿色食品标志;当心火灾——易燃物质标志等。
知道常见的抗酸药及其治疗原理。
此类试题有利于提高学生的化学素养。
2.下列对氨基酸和蛋白质的描述正确的是( )A.蛋白质水解的最终产物是氨基酸B.氨基酸和蛋白质遇重金属离子均会变性C.α-氨基丙酸与α-氨基苯丙酸混合物脱水成肽,只生成2种二肽D.氨基酸溶于过量氢氧化钠溶液中生成的离子,在电场作用下向负极移动【答案】A【解析】试题分析:A.蛋白质是各种氨基酸通过缩聚反应生成的高分子化合物,水解的最终产物是氨基酸,正确;B.氨基酸不具有生物活性,遇重金属离子反应不属于变性,错误;C.α-氨基丙酸与α-氨基苯丙酸混合物脱水成肽,可以生成4种二肽(α-氨基丙酸与α-氨基苯丙酸可以生成两种、α-氨基丙酸与α-氨基丙酸可生成1种、α-氨基苯丙酸与α-氨基苯丙酸可生成1种),错误;D.氨基酸溶于过量氢氧化钠溶液中生成酸根离子,带负电荷,在电场作用下向正极移动,错误,故选A。
【考点定位】考查氨基酸和蛋白质的结构和性质【名师点晴】本题侧重对蛋白质和氨基酸的性质的考查。
解答本题要注意区分蛋白质的变性和盐析,向蛋白质溶液中加入某些浓的无机盐(如铵盐、钠盐等)溶液,可使蛋白质的溶解度降低而从溶液中析出,属于蛋白质的盐析,是物理变化;蛋白质发生盐析后,性质不改变,析出的蛋白质加水后又可重新溶解,因此,盐析是可逆的。

2016年高考北京卷理综化学试题参考解析6.我国科技创新成果斐然,下列成果中获得诺贝尔奖的是A.徐光宪建立稀土串级萃取理论B.屠呦呦发现抗疟新药青蒿素C.闵恩泽研发重油裂解催化剂D.侯德榜联合制碱法【答案】B【解析】试题分析:屠呦呦发现的抗疟疾的新药青蒿素获得了诺贝尔奖。
考点:化学发展7.下列中草药煎制步骤中,属于过滤操作的是A.冷水浸泡B.加热煎制C.箅渣取液D.灌装保存【答案】C【解析】试题分析:A、冷水浸泡属于物质的溶解,故错误;B、加热煎制属于加热,故错误;C、箅渣取液属于过滤操作,故正确;D、灌装是液体转移,故错误。
考点:物质的分离和提纯的操作8.下列食品添加剂中,其试用目的与反应速率有关的是A.抗氧化剂B.调味剂C.着色剂D.增稠剂【答案】A【解析】试题分析:A、抗氧化剂减少食品与氧气的接触,延缓氧化的反应速率,故正确;B、调味剂是为了增加食品的味道,与速率无关,故错误;C、着色剂是为了给食品添加某种颜色,与速率无关,故错误;D增稠剂是改变物质的浓度,与速率无关。
考点:食品添加剂9.在一定条件下,甲苯可生成二甲苯混合物和苯。
有关物质的沸点、熔点如下:对二甲苯邻二甲苯间二甲苯苯沸点/℃138 144 139 80熔点/℃13 25 47 6下列说法不正确的是A.该反应属于取代反应B.甲苯的沸点高于144 ℃C.用蒸馏的方法可将苯从反应所得产物中首先分离出来D.从二甲苯混合物中,用冷却结晶的方法可将对二甲苯分离出来【答案】B考点:物质的分离和提纯,有机物的反应类型10.K2Cr2O7溶液中存在平衡:Cr2O72-(橙色)+H2O 2 CrO42-(黄色)+2H+。
用K2Cr2O7溶液进行下列实验:结合实验,下列说法不正确的是A.①中溶液橙色加深,③中溶液变黄B.②中Cr2O72-被C2H5OH还原C.对比②和④可知K2Cr2O7酸性溶液氧化性强D.若向④中加入70%H2SO4溶液至过量,溶液变为橙色【答案】D【解析】试题分析:A、在平衡体系中加入酸,平衡逆向移动,重铬酸根离子浓度增大,橙色加深,加入碱,平衡正向移动,溶液变黄,故正确;B、②中重铬酸钾氧化乙醇,重铬酸钾被还原,故正确;C、②是酸性条件,④是碱性条件,酸性条件下氧化乙醇,而碱性条件不能,说明酸性条件下氧化性强,故正确;D、若向④溶液中加入70%的硫酸到过量,溶液为酸性,可以氧化乙醇,溶液变绿色,故错误。

2016年高考化学理科综合北京卷(化学部分)一、选择题1.我国科技创新成果斐然,下列成果中获得诺贝尔奖的是( )A.徐光宪建立稀土串级萃取理论B.屠呦呦发现抗疟新药青蒿素C.闵恩泽研发重油裂解催化剂D.侯德榜联合制碱法2.下列中草药煎制步骤中,属于过滤操作的是( )A.如同上图AB.如同上图BC.如同上图CD.如同上图D3.下列食品添加剂中,其试用目的与反应速率有关的是( )A.抗氧化剂B.调味剂C.着色剂D.增稠剂4. 在一定条件下,甲苯可生成二甲苯混合物和苯。
有关物质的沸点、熔点如下:下列说法不正确的是( )A.该反应属于取代反应B.甲苯的沸点高于144 ℃C.用蒸馏的方法可将苯从反应所得产物中首先分离出来D.从二甲苯混合物中,用冷却结晶的方法可将对二甲苯分离出来5. $\sub{K}{2}\sub{Cr}{2}\sub{O}{7}$溶液中存在平衡:$\sup{\sub{Cr}{2}\sub{O}{7}}{2-}(橙色)+\sub{H}{2}O\to{<-->}{2}\sup{2Cr\sub{O}{4}}{2-}(黄色)+\sup{2H}{+}$。
用$\sub{K}{2}\sub{Cr}{2}\sub{O}{7}$溶液进行下列实验:结合实验,下列说法不正确的是( )A.①中溶液橙色加深,③中溶液变黄B.②中<<\sup{\sub{Cr}{2}\sub{O}{7}}{2-}>>被<<\sub{C}{2}\sub{H}{5}OH>>还原C.对比②和④可知<<\sub{K}{2}\sub{Cr}{2}\sub{O}{7}>>酸性溶液氧化性强D.若向④中加入70%<<\sub{H}{2}\sub{SO}{4}>>溶液至过量,溶液变为橙色6. 在两份相同的< {2}\sub{H}{2}\sub{SO}{4}\sub{NaHSO}{4}$溶液,其导电能力随滴入溶液体积变化的曲线如下图所示。

2016高考北京卷化学试题解析(一)新东方在线侯宇2016年高考理科综合考试已经结束了,针对今年化学命题形势和内容,新东方在线化学老师侯宇为大家带来了详尽的分析。
总的来说今年高考的化学题,其实跟往年的思路差不多,我们都说继承和发扬,今年的北京卷的高考化学题,跟以往相比较基本上也是这个思路,继承和发扬。
继承为主,发扬为辅,基本上是以继承为主要的方面。
[真题]6.我国科技创新成果斐然,下列成果中获得诺贝尔奖的是A.徐光宪建立稀土串级萃取理论B.屠呦呦发现抗疟新药青蒿素C.闵恩泽研发重油裂解催化剂D.侯德榜联合制碱法[侯宇老师解析]主要看下面获得诺贝尔奖的,这个东西跟实际生活很相关,也是我们北京高考化学一直以来的传统,会跟生活、跟实际情况联系到一起,当然这里边的这些事可能跟我们实际生活关系都不是特别大,但很多你应该能听说过。
所以这个题就可以轻松的选出B。
[真题]7.下列中草药煎制步骤中,属于过滤操作的是[侯宇老师解析]第7题,说下列中草药煎制的过程属于过滤操作的事,第一个是浸泡,跟过滤没关系,第二个是加热,就是煮。
C选项,把渣怎么弄掉,底下拿了像滤网一样的东西,就是过滤,D选项说罐装保存,就是装瓶里面,对比下来就是C。
这也是我们做北京高考化学题的时候可以掌握的一个小策略,就是你把四个选项都看看。
当然就有可能出现一些出题人,他觉得这是生活常识,但是放到我们考生,放到我们这些孩子的眼中,可能未必是常识。
所以有一些事情,比方说第6题,我们就直接命中B选项。
但是有一些题目我们拿不准的,怎么办?四个选项都看一看,然后选出一个最优结果。
客观来说其实像第6题,我们也是在逐个选项的排查过程当中才看到B选项。
所有题目都应该这样去做。
第7题也是这样的,我们逐一选项去看,跟第6题的感觉上就是读到这儿并不是特别的确定就是D,你看D不是,那就是C。
[真题]8.下列食品添加剂中,其试用目的与反应速率有关的是A.抗氧化剂B.调味剂C.着色剂D.增稠剂[侯宇老师解析]第8题也是这样的,说下列食品添加剂当中,与反应速率相关的是哪个,如果你没有概念的话就都看到。

![[精校版]2016年全国高考试卷汇编 (word)北京卷 化学部分](https://uimg.taocdn.com/9b4cd222be1e650e52ea99b4.webp)
2016年普通高等学校招生全国统一考试(北京卷)理综化学可能用到的相对原子质量:H 1 C 12 O 16 Na 23 Al 27 S 32第一部分(选择题共42分)本部分共7小题,每小题6分,共42分。
在每小题列出的四个选项中,选出最符合题目要求的一项。
6.我国科技创新成果斐然,下列成果中获得诺贝尔奖的是( )A.徐光宪建立稀土串级萃取理论B.屠呦呦发现抗疟新药青蒿素C.闵恩泽研发重油裂解催化剂D.侯德榜联合制碱法7.下列中草药煎制步骤中,属于过滤操作的是( )8.下列食品添加剂中,其使用目的与反应速率有关的是( )A.抗氧化剂B.调味剂C.着色剂D.增稠剂9.在一定条件下,甲苯可生成二甲苯混合物和苯。
有关物质的沸点、熔点如下:下列说法不正确的是( )A.该反应属于取代反应B.甲苯的沸点高于144 ℃C.用蒸馏的方法可将苯从反应所得产物中首先分离出来D.从二甲苯混合物中,用冷却结晶的方法可将对二甲苯分离出来10.K2Cr2O7溶液中存在平衡:Cr2-(橙色)+H2O2Cr-(黄色)+2H+。
用K2Cr2O7溶液进行下列实验:结合实验, 下列说法不正确的是( )A.①中溶液橙色加深,③中溶液变黄B.②中Cr2-被C2H5OH还原C.对比②和④可知K2Cr2O7酸性溶液氧化性强D.若向④中加入70% H2SO4溶液至过量,溶液变为橙色11.在两份相同的Ba(OH)2溶液中,分别滴入物质的量浓度相等的H2SO4、NaHSO4溶液,其导电能力随滴入溶液体积变化的曲线如图所示。
下列分析不正确的是( )A.①代表滴加H2SO4溶液的变化曲线B.b点,溶液中大量存在的离子是Na+、OH-C.c点,两溶液中含有相同量的OH-D.a、d两点对应的溶液均显中性12.用石墨电极完成下列电解实验。
下列对实验现象的解释或推测不合理的是( )A.a、d处:2H2O+2e-H2↑+2OH-B.b处:2Cl--2e-Cl2↑C.c处发生了反应:Fe-2e-Fe2+D.根据实验一的原理,实验二中m处能析出铜第二部分(非选择题共58分)本部分共4小题,共58分。

2016年普通高等学校招生全国统一考试(北京卷)化学一、选择题1.我国科技创新成果斐然,下列成果中获得诺贝尔奖的是( )A.徐光宪建立稀土串级萃取理论B.屠呦呦发现抗疟新药青蒿素C.闵恩泽研发重油裂解催化剂D.侯德榜联合制碱法解析:2015年10月,屠呦呦因发现青蒿素治疗疟疾的新疗法获诺贝尔生理学或医学奖。
答案:B2.下列中草药煎制步骤中,属于过滤操作的是( )A.AB.BC.CD.D解析:A.冷水浸泡属于物质的溶解,故A错误;B.加热煎制属于加热,故B错误;C.箅渣取液将固体和液体分离,属于过滤操作,故C正确;D.灌装是液体转移,故D错误。
答案:C3.下列食品添加剂中,其试用目的与反应速率有关的是( )A.抗氧化剂B.调味剂C.着色剂D.增稠剂解析:A.抗氧化剂减少食品与氧气的接触,延缓氧化的反应速率,故A正确;B.调味剂是为了增加食品的味道,与速率无关,故B错误;C.着色剂是为了给食品添加某种颜色,与速率无关,故C错误;D.增稠剂是改变物质的浓度,与速率无关,故D错误。
答案:A下列说法不正确的是( )A.该反应属于取代反应B.甲苯的沸点高于144℃C.用蒸馏的方法可将苯从反应所得产物中首先分离出来D.从二甲苯混合物中,用冷却结晶的方法可将对二甲苯分离出来解析:A、甲苯变成二甲苯是苯环上的氢原子被甲基取代所得,属于取代反应,故A正确;B、甲苯的相对分子质量比二甲苯小,故沸点比二甲苯低,故B错误;C、苯的沸点与二甲苯的沸点相差较大,可以用蒸馏的方法分离,故C正确;D、因为对二甲苯的沸点较低,冷却后邻二甲苯与间二甲苯容易形成固体,从而将对二甲苯分离出来,所以能用冷却结晶的方法分离出来,故D正确。
答案:B5.K2Cr2O7溶液中存在平衡:Cr2O72﹣(橙色)+H2O⇌2CrO42﹣(黄色)+2H+。
用K2Cr2O7溶液进行下列实验:结合实验,下列说法不正确的是( )A.①中溶液橙色加深,③中溶液变黄B.②中Cr2O72﹣被C2H5OH还原C.对比②和④可知K2Cr2O7酸性溶液氧化性强D.若向④中加入70%H2SO4溶液至过量,溶液变为橙色解析:A.在平衡体系中加入酸,平衡逆向移动,重铬酸根离子浓度增大,橙色加深,加入碱,平衡正向移动,溶液变黄,故A正确;B.②中重铬酸钾氧化乙醇,重铬酸钾被还原,故B 正确;C.②是酸性条件,④是碱性条件,酸性条件下氧化乙醇,而碱性条件不能,说明酸性条件下氧化性强,故B正确;D.若向④溶液中加入70%的硫酸到过量,溶液为酸性,可以氧化乙醇,溶液变绿色,故D错误。
2016年普通高等学校招生全国统一考试(北京卷)化学部分答案1.C 【解析】过滤是常用的物质分离方法,适用于固液分离,C 项符合题意;A 项和B 项均为浸取,D 项为溶液的转移,A 项、B 项、D 项均不符合题意。
2.A 【解析】相对于食物,抗氧化剂可以更快地被氧气氧化,从而降低了包装袋中氧气的浓度,减缓食品被氧化的速率。
3.B 【解析】甲苯生成二甲苯和苯,可分别理解成甲苯中苯环上的氢被甲基取代、甲苯中的甲基被氢取代,A 项正确;同系物中,碳原子数越多,沸点越高,所以甲苯的沸点应低于二甲苯,即低于138 ℃,B 项错误;苯的沸点最低,可最先分离出来,C 项正确;三种二甲苯间沸点相近,熔点差异大,将温度控制在稍低于13 ℃,对二甲苯结晶析出,D 项正确。
4.D 【解析】A 项,在平衡体系中加入酸,平衡逆向移动,重铬酸根离子浓度增大,橙色加深,加入碱,平衡正向移动,溶液变黄,A 项正确;B 项,②中酸性重铬酸钾溶液氧化乙醇,重铬酸钾被还原为绿色的3Cr +,B 项正确;C 项,②是酸性条件,④是碱性条件,227K Cr O 在酸性条件下能氧化乙醇,而在碱性条件下不能,说明其在酸性条件下氧化性强,C 项正确;D 项,若向④中加入70%24H SO 溶液至过量,溶液为酸性,227K Cr O 可以氧化乙醇,溶液变为绿色,D 项错误。
5.C 【解析】向2Ba (OH)溶液中加入等物质的量浓度的24H SO 溶液,发生反应24H SO +2Ba(OH)4BaSO ↓+22H O ,当加入的24H SO 的物质的量与2Ba(OH)的物质的量相等时,溶液中的离子浓度最低,导电能力最弱,对应①中a 点,继续滴加24H SO 溶液,导电能力逐渐增强,故①代表滴加24H SO 溶液的曲线。
另一份溶液,当加入少量4NaHSO 溶液时,发生反应4NaHSO +2Ba(OH)4BaSO ↓+2H O + NaOH ,当加入的4NaHSO 的物质的量与2Ba(OH)的物质的量相等时,反应后混合液的主要溶质为NaOH ,此时对应②中b 点,B 项正确;继续滴加4NaHSO 溶液,发生反应NaOH +4NaHSO 24Na SO +2H O ,当加入的4NaHSO 的物质的量与2Ba(OH)的总物质的量之比为2:1时,发生反应24NaHSO +2Ba(OH) 4BaSO ↓+24Na SO +2H O ,溶质为24Na SO ,对应②中d 点。
一、单选题
2016年全国普通高等学校招生统一考试化学(北京卷精编版)
1. 我国科技创新成果斐然,下列成果中获得诺贝尔奖的是
A.徐光宪建立稀土串级萃取理论
B.屠呦呦发现抗疟新药青蒿素
C.闵恩泽研发重油裂解催化剂
D.侯德榜联合制碱法
2. 下列中草药煎制步骤中,属于过滤操作的是
A.冷水浸泡B.加热煎制C.箅渣取液D.灌装保存
3. 下列食品添加剂中,其使用目的与反应速率有关的是( )
A.抗氧化剂B.调味剂
C.着色剂D.增稠剂
4. 在一定条件下,甲苯可生成二甲苯混合物和苯。
有关物质的沸点、熔点如下:
对二甲苯邻二甲苯间二甲苯苯
沸点/℃138 144 139 80
熔点/℃13 −25 −47 6
下列说法不正确的是
A.该反应属于取代反应
B.甲苯的沸点高于144 ℃
C.用蒸馏的方法可将苯从反应所得产物中首先分离出来
D.从二甲苯混合物中,用冷却结晶的方法可将对二甲苯分离出来
5. K2Cr2O7溶液中存在平衡:Cr2O72-(橙色)+H2O⇌2CrO42-(黄色)+2H+。
用K2Cr2O7溶液进行下列实验:
结合实验,下列说法不正确的是()
A.①中溶液橙色加深,③中溶液变黄
B.②中Cr2O72-被C2H5OH还原
C.对比②和④可知K2Cr2O7酸性溶液氧化性强
D.若向④中加入70%H2SO4溶液至过量,溶液变为橙色
6. 在两份相同的Ba(OH)2溶液中,分别滴入物质的量浓度相等的H2SO4、NaHSO4溶液,其导电能力随滴入溶液体积变化的曲线如图所示。
下列分析的是( )
A.①代表滴加H2SO4溶液的变化曲线
B.b点,溶液中大量存在的离子是Na+、OH–
C.c点,两溶液中含有相同量的OH–
D.a、d两点对应的溶液均显中性
不正确
7. 用石墨电极完成下列电解实验
实验一实验二
装置
现象a、d处试纸变蓝;b处变红,局部褪色;c
处无明显变化
两个石墨电极附近有气泡产生;n处有
气泡产生……
下列对实验现象的解释或推测不合理的是()
A.a、d处:2H2O+2e-=H2↑+2OH-B.b处:2Cl--2e-=Cl2↑
C.c处发生了反应:Fe-2e-=Fe2+D.根据实验一的原理,实验二中m处能析出铜
二、有机推断题
8. 功能高分子P的合成路线如下:
(1)A的分子式是C7H8,其结构简式是___________________。
(2)试剂a是_______________。
(3)反应③的化学方程式:_______________。
(4)E的分子式是C6H10O2。
E中含有的官能团:_______________。
(5)反应④的反应类型是_______________。
(6)反应⑤的化学方程式:_______________。
(5)已知:2CH3CHO。
以乙烯为起始原料,选用必要的无机试剂合成E,写出合成路线(用结构简式表示有机物),用箭头表示转化关系,箭头上注明试剂和反应条件)。
_______________。
三、原理综合题
9. 用零价铁(Fe)去除水体中的硝酸盐(NO3-)已成为环境修复研究的热点之一。
(1)Fe还原水体中NO3-的反应原理如图所示。
①作负极的物质是________。
②正极的电极反应式是_________。
(2)将足量铁粉投入水体中,经24小时测定NO3—的去除率和pH,结果如下:
初始pH pH=2.5 pH=4.5
NO3—的去除率接近100% <50%
24小时pH 接近中性接近中性
铁的最终物质形态
四、工业流程题
pH=4.5时,NO 3-的去除率低。
其原因是________。
(3)实验发现:在初始pH=4.5的水体中投入足量铁粉的同时,补充一定量的Fe 2+可以明显提高NO 3-的去除率。
对Fe 2+的作用提出两种假设: Ⅰ. Fe 2+直接还原NO 3-;
Ⅱ. Fe 2+破坏FeO (OH )氧化层。
①做对比实验,结果如右图所示,可得到的结论是_______。
②同位素示踪法证实Fe 2+能与FeO (OH )反应生成Fe 3O 4。
结合该反应的离子方程式,解释加入Fe 2+提高NO 3-去除率的原因:______。
pH =4.5(其他条件相同)
(4)其他条件与(2)相同,经1小时测定NO 3-的去除率和pH ,结果如下:
初始pH
pH=2.5 pH=4.5 NO 3—的去除率
约10% 约3% 1小时pH 接近中性接近中性
与(2)中数据对比,解释(2)中初始pH 不同时,NO 3—去除率和铁的最终物质形态不同的原因:__________。
10. 以废旧铅酸电池中的含铅废料(Pb 、PbO 、PbO 2、PbSO 4及炭黑等)和H 2SO 4为原料,制备高纯PbO ,实现铅的再生利用。
其工作流程如
下:
(1)过程Ⅰ中,在Fe 2+催化下,Pb 和PbO 2反应生成PbSO 4的化学方程式是__________。
五、实验题(2)过程Ⅰ中,Fe 2+催化过程可表示为:
i :2Fe 2++ PbO 2+4H ++SO 42−
2Fe 3++PbSO 4+2H 2O ii: ……
①写出ii 的例子方程式:________________。
②下列实验方案可证实上述催化过程。
将实验方案补充完整。
a.向酸化的FeSO 4溶液中加入KSCN 溶液,溶液几乎无色,再加入少量PbO 2,溶液变红。
b.______________。
(3)PbO 溶解在NaOH 溶液中,存在平衡:PbO (s )+NaOH (aq )NaHPbO 2(aq ),其溶解度曲线如图所示。
①过程Ⅱ的目的是脱硫。
滤液1经处理后可在过程Ⅱ中重复使用,其目的是_____(选填序号)。
A.减少PbO 的损失,提高产品的产率
B.重复利用NaOH ,提高原料的利用率
C.增加Na ₂SO 4浓度,提高脱硫效率
②过程Ⅲ的目的是提纯。
结合上述溶解度曲线,简述过程Ⅲ的操作:____。
11. 以Na 2SO 3溶液和不同金属的硫酸盐溶液作为实验对象,探究盐的性质和盐溶液间反应的多样性。
实验 试剂
现象
滴管 试管
2 mL 0.2 mol·L −1 Na 2
SO 3溶液
饱和Ag 2SO 4溶液
Ⅰ.产生白色沉淀 0.2 mol·L −1 CuSO 4溶液 Ⅱ.溶液变绿,继续滴加产生棕黄色沉淀 0.1 mol·L −1 Al 2(SO 4)3溶液 Ⅲ.开始无明显变化,继
续滴加产生白色沉淀
(1)经检验,现象Ⅰ中的白色沉淀是Ag 2SO 3。
用离子方程式解释现象Ⅰ:____________。
(2)经检验,现象Ⅱ的棕黄色沉淀中不含SO 42−,含有Cu +、Cu 2+和SO 32−。
已知:Cu +Cu +Cu 2+,Cu 2+CuI↓(白色)+I 2。
①用稀硫酸证实沉淀中含有Cu +的实验现象是_____________。
②通过下列实验证实,沉淀中含有Cu 2+和SO 32−。
KI溶液洗净的棕黄色沉淀取上层清液分成两份淀粉溶液试剂1 无明显现象
白色沉淀A
a.白色沉淀A是BaSO4,试剂1是____________。
b.证实沉淀中含有Cu2+和SO32−的理由是___________。
(3)已知:Al2(SO4)3在水溶液中不存在。
经检验,现象Ⅲ的白色沉淀中无SO42−,该白色沉淀既能溶于强酸,又能溶于强碱,还可使酸性K MnO4溶液褪色。
①推测沉淀中含有亚硫酸根和________。
②对于沉淀中亚硫酸根的存在形式提出两种假设:
i.被Al(OH)3所吸附;
ii.存在于铝的碱式盐中。
对假设ii设计了对比实验,证实了假设ii成立。
a.将对比实验方案补充完整。
步骤二:_____________(按上图形式呈现)。
(4)根据实验,亚硫酸盐的性质有___________。
盐溶液间反应的多样性与__________有关。