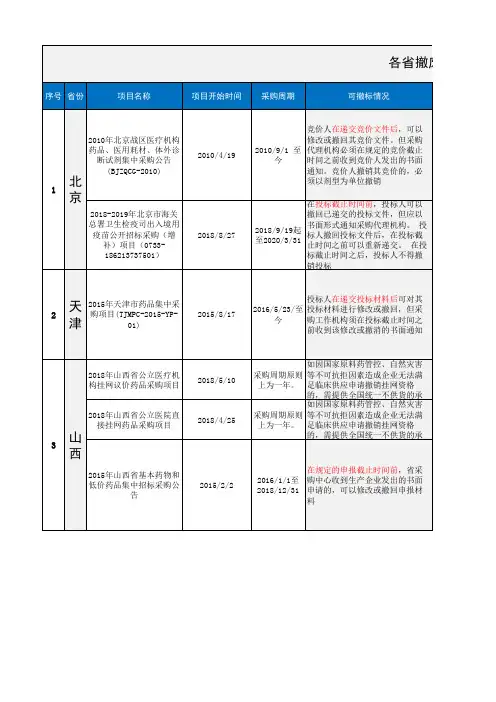
2017年度山西省第二类疫苗集中采购入围企业及价格公布
- 格式:doc
- 大小:218.50 KB
- 文档页数:10
![山西省物价局关于制定公布107种乙类化学药品最高零售价格的通知-晋价管字[2003]22号](https://uimg.taocdn.com/10188b61178884868762caaedd3383c4bb4cb44b.webp)
山西省物价局关于制定公布107种乙类化学药品最高零售价格的通知正文:---------------------------------------------------------------------------------------------------------------------------------------------------- 山西省物价局关于制定公布107种乙类化学药品最高零售价格的通知(晋价管字[2003]22号2003年1月16日)各市(地)物价局:根据《国家计委关于公布199种西药价格的通知》(计价格(2002)2822号)精神,现将列入国家基本医疗保险药品目录的107种乙类化学药品我省最高零售价格(见附表,印发给你们,请认真贯彻执行,并就有关问题通知如下:一、本通知附表中未列的剂型和规格,各生产和经营单位要按与表列代表规格品保持合理比价的原则提出意见。
于2月20日前报省物价局审定,由省物价局上报国家计委核定并统一公布价格。
在国家计委未公布价格前,可暂按省物价局制定的价格执行。
二、附表中所列GMP最高零售价是指通过国家GMP验收并取得GMP证书的生产企业执行的价格。
GMP企业名单以国家药品监督管理局发布的《药品GMP公告》为准。
进口药品按照附表中规定的GMP价格执行。
拥有产品专利权的企业,可按照附表备注的原研制药品所对应的价格执行。
三、申请单独定价的企业按规定的程序申报。
在单独定价前,须按本通知规定的价格执行。
四、凡属国家基本医疗保险目录未列剂型、且国家药品监督管理局批准为非处方药品(OTC)的,自批准之日起,该药品改由企业自主定价,原规定价格不再生效。
五、已过专利保护期与国内仿制药品差价超过规定幅度的原研制药品,本通知公布的价格为临时价格。
上述原研制药品价格将按照逐步到位的原则,经专家评审后重新核定其价格。
六、此次公布的药品均为含税价格,省内外生产和经营在我省销售的药品,凡现行销价低于本通知公布最高零售价的,继续执行原销价,高于公布最高零售价格的,要降到公布规定的最高零售价。

山西省卫生和计划生育委员会关于做好2018年公立医疗机构挂网议价药品采购工作的通知文章属性•【制定机关】山西省卫生和计划生育委员会•【公布日期】2018.05.09•【字号】晋卫药政发〔2018〕2号•【施行日期】2018.05.09•【效力等级】地方规范性文件•【时效性】现行有效•【主题分类】药政管理正文山西省卫生和计划生育委员会关于做好2018年公立医疗机构挂网议价药品采购工作的通知晋卫药政发〔2018〕2号各市卫生计生委,省药械集中采购中心,委直各医疗机构:为进一步规范全省公立医疗机构药品集中分类采购工作,以需求为导向,保障临床药品供应,促进企业公平有序竞争,降低药品虚高价格,根据国家及山西省公立医疗机构药品集中分类采购相关文件精神,结合全省实际,现就做好2018年公立医疗机构(含县级医疗集团)挂网议价药品采购工作相关事宜通知如下:一、挂网议价采购药品目录范围(一)纳入全省2018年公立医疗机构挂网议价采购药品目录包括:急(抢)救药品、妇儿专科非专利药品、通过仿制药质量疗效一致性评价药品、常用低价药品、基础输液、二类精神药品、历史采购量小的药品以及列入国家和山西省短缺药品清单内药品。
(二)公立医疗机构备案采购药品足量供应满三个月,且全省有20家以上三级公立医疗机构备案采购的药品,经企业申请后可纳入挂网议价采购药品目录。
二、集中采购平台挂网方式(一)已在山西省药械集中采购平台(以下简称为“集中采购平台”)按挂网议价采购方式挂网的药品保留挂网资格,经挂网企业重新确认后,由山西省药械集中招标采购中心(以下简称为“省药采中心”)纳入2018年挂网议价采购药品目录。
省级集中招标中标药品目录中只有国外企业生产并独家中标的药品,国内企业新批准上市的仿制药品可以申请纳入挂网议价采购目录。
(二)申请新增基础输液、历史采购量小目录内药品以及公立医疗机构备案采购足量供应满三个月且全省有20家以上三级公立医疗机构采购的药品,生产企业须提供全国三省份省级药品采购交易平台现行最低交易价格,无法提供的,暂不予以挂网。
![浙江省物价局关于公布省疾病预防控制中心二类疫苗购销备案价格的通知-浙价医[2011]225号](https://uimg.taocdn.com/1f55ba0e0a4e767f5acfa1c7aa00b52acfc79c60.webp)
浙江省物价局关于公布省疾病预防控制中心二类疫苗购销备案价格的通知正文:---------------------------------------------------------------------------------------------------------------------------------------------------- 浙江省物价局关于公布省疾病预防控制中心二类疫苗购销备案价格的通知(浙价医〔2011〕225号)各市、县(市、区)物价局:为规范疫苗价格秩序,减轻二类疫苗接种者的经济负担,根据浙江省物价局《关于加强疫苗价格管理的通知》(浙价医〔2011〕172)规定,现将2011年省疾病预防控制中心集中采购的二类疫苗购销备案价格予以公布,并就有关问题通知如下:一、2011年省疾病预防控制中心集中采购的二类疫苗购销备案价格具体详见附件1。
今后我局将根据省疾病预防控制中心二类疫苗集中采购中标情况,在浙江省物价局网站上公布省疾病预防控制中心二类疫苗集中采购购销备案价格,不再另行发文。
二、人用狂犬病疫苗全省各类接种单位备案最高零售价格详见附件2。
三、各市、县(市、区)疾病预防控制中心应及时将采购的二类疫苗购销价格以书面和电子形式向同级价格主管部门备案。
四、本通知自2011年7月1日起执行。
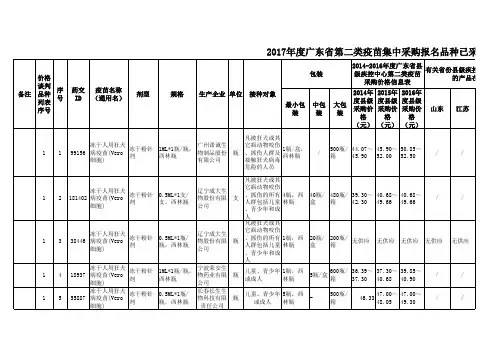
附件:1.2011年省疾病预防控制中心二类疫苗购销备案价格表2.2011年人用狂犬疫苗及狂犬病人免疫球蛋白备案最高零售价格表二○一一年六月二十九日附件12011年省疾病预防控制中心二类疫苗购销备案价格表金额:元序号疫苗名称(商品名)剂型规格计价单位生产企业(产地)购进价格销售价格1甲型肝炎灭活疫苗(孩尔来福)注射剂(儿童)250U/0.5ml/剂量/支,预填充注射器支北京科兴生物制品有限公司55.0 56.9 2甲型肝炎灭活疫苗(孩尔来福)注射剂(儿童)250U/0.5ml/剂量/瓶,西林瓶瓶北京科兴生物制品有限公司42.0 43.4 3甲型肝炎灭活疫苗(孩尔来福)注射剂(成人)500U/1.0ml/剂量/支,预填充注射器支北京科兴生物制品有限公司60.0 62.1 4甲型肝炎灭活疫苗(孩尔来福)注射剂(成人)500U/1.0ml/剂量/瓶,西林瓶瓶北京科兴生物制品有限公司45.0 46.5 5甲型肝炎灭活疫苗(维赛瑞安)注射剂(成人)1.0ml/剂量/瓶,含甲型肝炎病毒抗原640EU,西林瓶瓶中国医学科学院医学生物学研究所47.0 48.6 6甲型肝炎灭活疫苗(维赛瑞安)注射剂(儿童)0.5ml/剂量/瓶,含甲型肝炎病毒抗原320EU,西林瓶瓶中国医学科学院医学生物学研究所42.0 43.4 7甲型肝炎灭活疫苗(贺福立适)注射剂720EL.U/0.5ml/剂量/支,预填充注射器支葛兰素史克生物制品有限公司(比利时)100.0 103.5 8甲型肝炎灭活疫苗(贺福立适)注射剂720EL.U./0.5ml/剂量/瓶,西林瓶瓶葛兰素史克生物制品有限公司(比利时)70.0 72.4 9甲型肝炎灭活疫苗(爱巴苏)注射剂24IU/0.5ml/剂量/支,预填充注射器支Berna Biotech Ltd(瑞士)110.0 113.8 10冻干甲型肝炎减毒活疫苗注射剂复溶后0.5ml/剂次/瓶,含甲型肝炎减毒活病毒不低于6.5lgCCID50,西林瓶(附稀释液)瓶浙江普康生物技术股份有限公司45.0 46.5 11冻干甲型肝炎减毒活疫苗(维赛瑞吉)注射剂复溶后1.0ml/剂量/瓶,含甲型肝炎减毒活病毒不低于6.50lgCCID50,西林瓶(附稀释液)瓶中国医学科学院医学生物学研究所42.0 43.4 12万信® 冻干甲型肝炎减毒活疫苗注射剂复溶后1.0ml/剂量/瓶,含甲型肝炎减毒活病毒不低于6.50lgCCID50,西林瓶(附稀释液)瓶长春长生生物科技股份有限公司35.0 36.2 13冻干甲型肝炎减毒活疫苗(海威克)注射剂复溶后1.0ml/剂量/瓶,含甲型肝炎减毒活病毒不低于6.50lgCCID50,西林瓶(附稀释液)瓶长春生物制品研究所38.0 39.3 14甲型乙型肝炎联合疫苗(倍尔来福)注射剂(儿童)250U/5μg/0.5ml/剂量/支,预填充注射器支北京科兴生物制品有限公司75.0 77.6 15甲型乙型肝炎联合疫苗(倍尔来福)注射剂(儿童)250U/5μg/0.5ml/剂量/支,西林瓶瓶北京科兴生物制品有限公司45.0 46.5 16甲型乙型肝炎联合疫苗(倍尔来福)注射剂(成人)500U/10μg/1.0ml/剂量/瓶,预填充注射器支北京科兴生物制品有限公司80.0 82.8 17甲型乙型肝炎联合疫苗(倍尔来福)注射剂(成人)500U/10μg/1.0ml/剂量/瓶,西林瓶瓶北京科兴生物制品有限公司50.0 51.7 18甲、乙型肝炎联合疫苗(双福立适)注射剂(成人剂量)720EL.U.,20μg/1.0ml/剂量/支,预填充注射器支上海葛兰素史克生物制品有限公司150.0 155.2 19重组乙型肝炎疫苗(汉逊酵母)注射剂10μg/0.5ml/剂量/瓶,3瓶/盒/人份,安瓿人份大连汉信生物制药有限公司15.0 15.5 20重组乙型肝炎疫苗(汉逊酵母)(汉逊瑞安)注射剂10μg/0.5ml/剂量/瓶,西林瓶瓶大连汉信生物制药有限公司9.0 9.3 21重组乙型肝炎疫苗(酿酒酵母)注射剂10μg/1.0ml/剂量/安瓿支北京天坛生物制品股份有限公司12.0 12.4 22重组乙型肝炎疫苗(汉逊酵母)注射剂0.5ml/剂量/瓶,含HBsAg10μg,西林瓶瓶华兰生物疫苗有限公司14.5 15.0 23重组乙型肝炎疫苗(酿酒酵母)注射剂10μg/0.5ml/剂量/西林瓶,3瓶/人份,人份深圳康泰生物制品股份有限公司13.5 13.9 24重组乙型肝炎疫苗(酿酒酵母)注射剂10μg/0.5ml/剂量/支,3支/人份,安瓿人份深圳康泰生物制品股份有限公司12.5 12.9 25重组乙型肝炎疫苗(酿酒酵母)注射剂60μg/1.0ml/剂量/支,预填充注射器支深圳康泰生物制品股份有限公司190.0 196.6 26重组乙型肝炎疫苗(CHO细胞)注射剂10μg/0.5ml/瓶,含HBsAg10μg;3瓶/人份,西林瓶人份华北制药金坦生物技术股份有限公司18.0 18.6 27重组乙型肝炎疫苗(CHO细胞)注射剂20μg/1.0ml/瓶,西林瓶瓶华北制药金坦生物技术股份有限公司12.0 12.4 28重组乙型肝炎疫苗(酿酒酵母)(安在时)注射剂10μg/0.5ml/剂量/支,预填充注射器支葛兰素史克生物制品有限公司(比利时)41.0 42.4 29重组乙型肝炎疫苗(酿酒酵母)(安在时)注射剂20μg/1.0ml/剂量/支,预填充注射器支葛兰素史克生物制品有限公司(比利时)51.6 53.4 30重组乙型肝炎疫苗(酿酒酵母)(安在时)注射剂10μg/0.5ml/剂量/瓶,西林瓶瓶葛兰素史克生物制品有限公司(比利时)36.0 37.2 31重组乙型肝炎疫苗(酿酒酵母)(安在时)注射剂20μg/1.0ml/剂量/瓶,西林瓶瓶葛兰素史克生物制品有限公司(比利时)43.7 45.2 32重组乙型肝炎疫苗(汉逊酵母)(益可欣)注射剂10μg/0.5ml/剂量/瓶,西林瓶支Berna Biotech Korea Corp.(韩国)45.0 46.5 33重组乙型肝炎疫苗(汉逊酵母)(益可欣)注射剂20μg/1.0ml/剂量/瓶,西林瓶支Berna Biotech Korea Corp.(韩国)55.0 56.9 3423价肺炎球菌多糖菌苗(惠益康)注射剂0.5ml/剂量/瓶;含纯化的23种血清型肺炎球菌荚膜多糖各25μg,西林瓶瓶成都生物制品研究所98.0 101.4 3523价肺炎球菌多糖菌苗(纽莫法)注射剂0.5ml/剂量/瓶,西林瓶瓶默沙东制药有限公司(美国)130.0 134.5 3623价肺炎球菌多糖菌苗(优博23*)注射剂0.5ml/支,预填充注射器支赛诺菲巴斯德(法国)158.0 163.5 377价肺炎球菌结合疫苗(沛儿)注射剂0.5ml/支,预填充注射器支惠氏制药有限公司(美国)608.0 629.2 38冻干A、C群脑膜炎球菌结合疫苗冻干制剂复溶后为0.5ml/剂量/瓶,含与破伤风类毒素结合的A、C群脑膜炎球菌多糖各10μg,西林瓶(附稀释液)瓶罗益(无锡)生物制药有限公司30.0 31.0 39冻干A、C群脑膜炎球菌多糖结合疫苗(沃尔康)注射剂复溶后为0.5ml/剂量/瓶,含与破伤风类毒素结合的A、C群脑膜炎球菌多糖各10μg,西林瓶(附稀释液)瓶玉溪沃森生物技术有限公司58.0 60.0 40A+C群脑膜炎球菌多糖结合疫苗(盟纳康)注射剂(液体)0.5ml/剂量/瓶,含与破伤风类毒素结合的A、C群脑膜炎球菌多糖各10μg,西林瓶(附稀释液)瓶北京绿竹生物技术有限公司26.0 26.9 41ACYW135脑膜炎球菌多糖疫苗(御脑宁)注射剂复溶后0.5ml/剂量/瓶,西林瓶瓶浙江天元生物药业有限公司42.0 43.4 42b型流感嗜血杆菌结合疫苗(呵儿贝)注射剂0.5ml/10μg/剂量/瓶,西林瓶瓶兰州生物制品研究所45.0 46.5 43b型流感嗜血杆菌结合疫苗(邦贝克)注射剂10μg/0.5ml/剂量/瓶,西林瓶瓶玉溪沃森生物技术有限公司55.0 56.9 44b型流感嗜血杆菌结合疫苗(邦贝克)注射剂10μg/0.5ml/剂量/支,预填充注射器支玉溪沃森生物技术有限公司75.0 77.6 45b型流感嗜血杆菌结合疫苗(贺新立适)注射剂10μg/0.5ml/剂量/支,预填充注射器支葛兰素史克生物制品有限公司(比利时)80.0 82.8 46b型流感嗜血杆菌结合疫苗(贺新立适)注射剂10μg/0.5ml/剂量/瓶,西林瓶瓶葛兰素史克生物制品有限公司(比利时)68.0 70.3 47b型流感嗜血杆菌结合疫苗(安尔宝)注射剂10Ug/支+含预冲型注射器装稀释液0.5ml/支,预填充注射器支赛诺菲巴斯德(法国)75.0 77.6 48b型流感嗜血杆菌结合疫苗(维可思)注射剂10μg/0.5ml/剂量/支,预填充注射器支诺华疫苗和诊断试剂有限责任公司(意大利)85.0 87.9 49吸附无细胞百白破灭活脊髓灰质炎和b型流感嗜血杆菌(结合)联合疫苗(潘太欣)注射剂本品为两个包材包装,⑴百白破脊髓灰质炎疫苗混悬液0.5 ml;⑵b型流感嗜血杆菌结合疫苗冻干粉。

国家食品药品监督管理总局、国家卫生计生委关于进一步加强疫苗流通监管促进疫苗供应工作的通知文章属性•【制定机关】国家食品药品监督管理总局(已撤销),国家卫生和计划生育委员会(已撤销)•【公布日期】2017.08.30•【文号】食药监药化监〔2017〕76号•【施行日期】2017.08.30•【效力等级】部门规范性文件•【时效性】现行有效•【主题分类】免疫规划正文食品药品监管总局国家卫生计生委关于进一步加强疫苗流通监管促进疫苗供应工作的通知食药监药化监〔2017〕76号各省、自治区、直辖市食品药品监督管理局、卫生计生委,新疆生产建设兵团食品药品监督管理局、卫生局:为进一步贯彻落实新修订的《疫苗流通和预防接种管理条例》,规范第二类疫苗(以下称疫苗)冷链储存运输管理,解决疫苗配送过程中的实际问题,保证疫苗供应的可及性,现将有关要求通知如下:一、规范疫苗储运管理,提高疫苗配送效率(一)疫苗生产企业、疫苗配送企业、疫苗区域仓储企业储存和运输疫苗应当严格执行《药品经营质量管理规范》《疫苗储存和运输管理规范》的要求;各级疾病预防控制机构、接种单位储存和运输疫苗应当严格执行《疫苗储存和运输管理规范》《预防接种工作规范》的要求。
(二)疫苗生产企业可直接向县级疾病预防控制机构配送疫苗,也可委托具备药品冷链运输条件的企业配送。
疫苗配送可采取干线运输+区域仓储+区域配送的分段接力方式。
干线运输是指疫苗从疫苗生产企业运输至区域仓储或直接运输至县级疾病预防控制机构的运输过程;区域仓储是指疫苗从疫苗生产企业配送至县级疾病预防控制机构的过程中,发生的冷链储存活动;区域配送是指疫苗从区域仓储直接配送至县级疾病预防控制机构的过程。
(三)疫苗生产企业应当对疫苗配送企业的配送能力进行评估,严控配送企业数量。
在同一省、自治区、直辖市,同一家疫苗生产企业选取疫苗配送企业不得超过2家。
接受委托配送的企业不得再次委托。
(四)疫苗的区域仓储可使用其他疫苗生产企业的冷库、配送企业的冷库、区域仓储企业的冷库。

山西省人民政府办公厅关于印发山西省深化“放管服效”改革重点任务分工方案的通知文章属性•【制定机关】山西省人民政府办公厅•【公布日期】2017.08.22•【字号】晋政办发〔2017〕101号•【施行日期】2017.08.22•【效力等级】地方规范性文件•【时效性】现行有效•【主题分类】机关工作正文山西省人民政府办公厅关于印发山西省深化“放管服效”改革重点任务分工方案的通知晋政办发〔2017〕101号各市、县人民政府,省人民政府各委、办、厅、局:《山西省深化“放管服效”改革重点任务分工方案》已经省人民政府同意,现转发给你们,请认真贯彻执行。
山西省人民政府办公厅2017年8月22日山西省深化“放管服效”改革重点任务分工方案为贯彻落实《国务院办公厅关于印发全国深化简政放权放管结合优化服务改革电视电话会议重点任务分工方案的通知》(国办发〔2017〕57号)精神,切实把我省“放管服效”改革落到实处,结合我省实际,制定分工方案如下。
一、工作目标认真贯彻落实党中央、国务院及省委、省政府的决策部署,以“为促进就业创业降门槛、为各类市场主体减负担、为激发有效投资拓空间、为公平营商创条件、为群众办事生活增便利”为目标,以破解当前我省“放管服效”改革进程中存在的重点难点问题、全力打造全国审批最少、流程最优、体制最顺、机制最活、效率最高、服务最好的“六最”发展环境为着力点,采取有效措施,创新体制机制,充分激发市场活力和经济发展内生动力,为塑造山西美好形象、实现振兴崛起增添新的动能和活力。
二、任务分工(一)为促进就业创业降门槛。
1.大力推行“多证合一”改革,2017年10月底前在全省范围内实现“多证合一、一照一码”,对工商登记前后涉及的信息采集、记载公示和管理备查类的各种涉企证照事项,能整合的尽量整合、能简化的尽量简化、该减掉的坚决减掉。
大力推行全程电子化和电子营业执照,以市场主体办理登记“零见面”、电子营业执照“无介质”为目标,进一步优化线上服务。

2017年疫苗行业分析报告2017年11月目录一、2016年二类疫苗批签发下滑明显 (4)二、新型疫苗消费需求提升 (6)1、手足口病(EV71)疫苗 (7)2、肺炎疫苗 (8)(1)肺炎结合疫苗 (9)(2)23价肺炎多糖疫苗 (12)3、脊髓灰质炎灭活疫苗 (13)4、Hib-AC结合疫苗 (16)5、DTap-X多联疫苗 (18)6、HPV疫苗 (20)三、传统主流二类疫苗需求稳定 (22)1、狂犬疫苗 (22)2、水痘疫苗 (25)3、Hib结合疫苗 (27)4、轮状病毒疫苗 (28)本报告从批签发看新型疫苗消费的崛起,国内疫苗消费结构正逐步发生变化,18年开始国内HPV 疫苗、13价肺炎结合疫苗等新型疫苗陆续上市驱动疫苗行业快速增长。
疫苗渠道改革后,行业快速恢复。
疫苗流通改革(16年4月23日实施)后一年有余,大部分省份都进行了省级疫苗集中采购交易平台建设,并集中招标采购,疫苗行业销售快速恢复,疫苗流通新政后,疫苗产品改为高开实行一票制,部分流通渠道利润返回上游工业,智飞生物、沃森生物、康泰生物等疫苗企业收入端和利润端都有靓丽表现。
大品种陆续获批上市使行业发展迎来新契机。
一剂多防、联合疫苗的开发对传统疫苗的升级换代,是疫苗研发的趋势之一。
近几年,国内疫苗市场虽经历乙肝疫苗事件和山东疫苗事件不利影响,但多个新品种获批上市使行业发展迎来新契机。
一、新型疫苗方面:2015年开始,手足口(EV71)疫苗、宫颈癌(HPV)疫苗、13价肺炎结合疫苗陆续在国内获批上市;二、疫苗升级换代产品—多联苗:康泰生物的DTap-Hib 和智飞生物的Hib-AC 结合苗在13、14年底获批签发,上市推广销售。
18年起是,大品种收货季,预计智飞代理的HPV 疫苗18年靓丽表现,代理5价轮状病毒疫苗获批;预计沃森生物的13价肺炎结合疫苗18年获批,HPV 疫苗18年揭盲;康泰生物的23价肺炎多糖疫苗18年获批,人二倍体狂犬疫苗也有望获批,后续还有IPV 等大品种。

2018年度山西省第二类疫苗集中采购实施方案为进一步规范全省第二类疫苗的采购、配送和供应,明确部门职责,细化采购流程,根据《山西省卫生和计划生育委员会第二类疫苗集中采购管理办法(试行)》(以下简称《管理办法》)要求,结合我省实际,制定本实施方案。
第一章组织机构及职责一、基本原则按照公开、透明、公平、公正、诚实信用的原则,在省卫生计生委第二类疫苗集中采购领导组(以下简称“领导组”)统一领导下,由省疾病预防控制中心(以下简称“省疾控中心”)组织、省药械集中招标采购中心(以下简称“省药招中心”)协同,在“山西省第二类疫苗阳光采购平台”(以下简称“采购平台”)实行省级集中采购。
二、实施范围全省各级疾病预防控制机构(以下简称“疾控机构”)、预防接种单位、第二类疫苗生产企业、省药招中心及各有关单位。
三、机构及职责省疾控中心起草《2018年度山西省第二类疫苗集中采购实施方案》(以下简称《实施方案》),报省卫生计生委第二类疫苗集中— 1 —采购领导组办公室(以下简称“领导组办公室”),提请领导组审核同意。
省疾控中心审查疫苗生产企业提供的相关信息后,在采购平台上完成第二类疫苗生产企业注册,组织专家论证完成《2018年度山西省第二类疫苗集中采购品种需求目录》(以下简称《需求目录》)(见附件1)编制工作。
省药招中心负责组织专家进行价格谈判,按照实施方案和需求目录,采用谈判形式确定疫苗生产企业第二类疫苗的每个品种、规格的集中采购价格,形成《2018年度山西省第二类疫苗集中采购品种入围目录》(以下简称《入围目录》),并将该目录反馈省疾控中心进行确认后,通过采购平台公布入围目录和集中采购价格。
县级疾病控制机构负责根据辖区内接种单位申报的采购计划,通过采购平台进行本行政区域内第二类疫苗的集中采购,并供应接种单位。
接种单位负责根据预防接种工作的需要,制定第二类疫苗的采购计划,并向县级卫生计生行政部门和县级疾病预防控制机构报告。

省级非免疫规划疫苗集中采购实施方案为进一步规范非免疫规划疫苗采购管理,保障非免疫规划疫苗质量和供应,为人民群众提供安全有效、价格合理的非免疫规划疫苗,保护人民群众身体健康,根据《中华人民共和国疫苗管理法》等有关规定,结合我区实际,制定本方案。
一、基本原则按照公开、公平、公正和诚实信用原则,依托自治区公共资源交易中心实行全区集中采购。
加强非免疫规划疫苗采购全过程综合监管,切实保障非免疫规划疫苗质量和供应。
二、适用范围非免疫规划疫苗上市许可持有人、配送单位、疾病预防控制机构、接种单位以及各级卫生健康行政部门、非免疫规划疫苗集中采购机构和监管部门等适用本方案。
三、采购流程(一)发布采购公告。
自治区公共资源交易中心会同自治区疾病预防控制中心,依据本实施方案编制非免疫规划疫苗采购目录和疫苗采购文件,通过交易平台发布采购公告,并报自治区卫生健康委、自治区机关事务管理局备案。
采购公告发布以自治区药品和医疗器械集中采购网为准。
公告日期与疫苗上市许可持有人响应申请截止日期之间不少于20天。
(二)申报。
1.报名对象。
只接收疫苗上市许可持有人直接报名。
进口疫苗国内总代理视同疫苗上市许可持有人。
国外上市许可持有人或国外代理商在国内设总代理的,只接受国内总代理的报名;在国内不设总代理的,只接受一家一级代理商的报名,此一级代理商代理的区域应当包括XX辖区范围。
2.网上注册。
拟参加当次非免疫规划疫苗集中采购的疫苗上市许可持有人和产品,应通过XX壮族自治区药械集中采购平台(以下简称“自治区药械集中采购平台”)进行网上注册。
没有在规定时间内网上注册的疫苗上市许可持有人和产品不能参加当次集中采购活动。
3.申报材料。
疫苗上市许可持有人申报的材料包括纸质材料和电子图片两种形式,纸质材料和电子图片不一致的以纸质材料为准。
所有拟参加当次集中采购的疫苗上市许可持有人和产品,应当在规定的时间内将纸质材料递交到自治区公共资源交易中心,并将相关材料的电子图片上传至自治区药械集中采购平台。
山西省卫生厅关于公布第二批基本药物配送备选企业
名单的通知
文章属性
•【制定机关】山西省卫生厅
•【公布日期】2010.12.15
•【字号】
•【施行日期】2010.12.15
•【效力等级】地方规范性文件
•【时效性】现行有效
•【主题分类】药政管理
正文
山西省卫生厅关于公布第二批基本药物配送备选企业名单的
通知
各市卫生局:
根据《山西省医疗机构国家基本药物集中招标采购配送实施办法》和《山西省2010年度政府办基层医疗卫生机构配送企业遴选工作方案》,经审查,山西省晋城医药药材公司等26家药品批发企业符合基本药物配送企业备选条件,现予公布。
请各市根据基本药物配送工作需要,科学合理的确定基本药物配送企业数量。
附件:第二批基本药物配送备选企业名单
二○一○年十二月十五日附件:。
山西省物价局关于公布甘露醇等226种招标采购药品销售价格的通知文章属性•【制定机关】山西省物价局•【公布日期】2001.01.11•【字号】晋价管字[2001]第13号•【施行日期】2001.01.11•【效力等级】地方规范性文件•【时效性】现行有效•【主题分类】政府采购正文山西省物价局关于公布甘露醇等226种招标采购药品销售价格的通知(晋价管字[2001]第13号二00一年一月十一日)省卫生厅:根据国家计委、卫生部等五部委局关于印发《医疗机构药品集中招标采购试点工作若干规定的通知》精神,山西医科大学第一医院、山西医科大学第二医院、山西省肿瘤医院、山西省中医药研究院、山西省心血管研究所、山西省第二人民医院、太原市人民医院、太原市第二人民医院、太原市中心医院等九大医院联合于2000年12月开展了药品集中招标采购试点工作并取得较好的经济效益和社会效益。
第一批招标采购226个品种规格,招标价格比采购进价进口药品平均降低8-10%,国产药品平均降价达15.19%。
为进一步推进这项工作,杜绝药品采购活动中的不正之风,减轻患者医药费负担和财政支出,现将招标采购的药品零售价格公布如下:附:九家医院药品集中招标采购目录山西医科大学第一医院山西医科大学第二医院山西省肿瘤医院山西省中医药研究院山西省心血管研究所山西省第二人民医院太原市人民医院太原市第二人民医院太原市中心医院招标药品汇总表序号药品名称剂型规格供货价零售价生产厂家供货商备注129头孢唑啉钠注射剂0.5G 1.75 2.10华北制药市药品部铝盖GMP企业130头孢唑啉钠注射剂0.5G 1.65 1.98哈药总厂省新特药铝盖GMP企业131头孢曲松钠注射剂1.0G36.0043.20石家庄制药五龙口GMP企业132头孢曲松钠注射剂1.0G34.7641.71哈药集团万科达GMP企业133头孢曲松钠注射剂1.0G43.3352.00丽珠集团省药材采供站GMP企业134头孢曲松钠注射剂1.0G47.8357.40东北总厂医药五公司GMP企业135氨苄青霉素注射剂0.5G0.600.72哈药总厂省新特药GMP企业136氨苄青霉素注射剂0.5G0.660.79石家庄制药五龙口GMP企业137氨苄青霉素注射剂0.5G0.620.74山西博康省普药GMP企业138哌拉西林钠注射剂2.0G12.9615.55山西博康省普药GMP企业139哌拉西林钠注射剂2.0G12.9615.55山西同领省普药GMP企业140头孢噻肟钠注射剂1.0G14.1216.94三九集团三九慷辉GMP企业141头孢噻肟钠注射剂1.0G14.0016.80珠海联邦省普药进口药142头孢噻肟钠注射剂1.0G15.0018.00上海新亚省药材采供站GMP企业143头孢他啶钠注射剂1.0G73.4688.15哈药集团市药品部GMP企业144头孢他啶钠注射剂1.0G62.1574.58三九集团三九慷辉GMP企业145头孢他啶钠注射剂1.0G60.0072.00海南海灵省普药GMP企业146头孢哌酮钠注射剂1.0G53.6964.43珠海联邦省普药进口药147头孢哌酮钠注射剂1.0G48.6258.34哈药集团市药品部溶媒结晶粉GMP企业148头孢哌酮钠注射剂1.0G50.8761.04丽珠集团省新特药溶媒结晶粉GMP企业149头孢呋辛钠注射剂0.75G42.1550.58深圳信立泰天星生化GMP企业150头孢呋辛钠注射剂0.75G42.1550.58深圳制药厂省普药GMP企业议标品种目录序号药品名称商品名称剂型规格供货价零售价生产厂家供货商备注151头孢哌酮钠先锋必注射剂 1.0G76.8092.16大连辉瑞省普药进口药152头孢哌酮钠\舒巴坦舒普深注射剂 1.0G111.90134.28大连辉瑞省普药进口药153氟康唑大扶康注射剂0.2*50ML212.31254.77大连辉瑞省新特药进口药154氟康唑大扶康注射剂0.4*100ML418.68502.42大连辉瑞省新特药进口药155氟康唑大扶康胶囊50MG*7S192.00 230.40大连辉瑞省新特药进口药156阿奇霉素希舒美片剂0.25*6S106.4 127.68大连辉瑞省普药进口药157头孢呋辛钠西力欣注射剂0.75G47.0056.40英国葛兰素省新特药进口药158头孢呋辛钠西力欣片剂0.25*12S62.5075.00英国葛兰素省新特药进口药159头孢他啶钠复达欣注射剂 1.0G118.00 141.60英国葛兰素省新特药进口药160辛伐他汀舒降之片剂20MG*7S49.70 59.64杭州默沙东省新特药进口药161非诺贝特力平之片剂100MG*25S69.00 82.80法国省新特药进口药162双氯灭痛扶它林片剂25MG*30S26.4031.68北京诺华省新特药进口药163双氯灭痛扶它林乳剂20G22.0026.40北京诺华省新特药进口药164头孢曲松钠罗氏芬注射剂 1.0G127.88 153.46上海罗氏省普药进口药165奥美拉唑洛赛克胶囊20MG*14S184.00 220.80阿斯特拉省普药进口药166布洛芬缓释片芬必得胶囊300MG*20S13.45 16.14中美史克省普药进口药167多潘立酮片吗叮啉片剂10MG*30S13.8216.58西安杨森省普药进口药168头孢他啶钠凯复定注射剂 1.0G120.00144.00美国礼来省普药进口药169头孢呋辛钠力复乐注射剂0.75G48.00 57.60美国礼来省普药进口药170血脂康胶囊0.3*12S14.40 17.28北大维信省新特药GMP企业171青毒素注射剂80万IU0.450.54华药集团省普药GMP企业172青毒素注射剂160万IU0.80 0.96华药集团省普药GMP企业173青毒素注射剂400万IU 2.00 2.40华药集团省普药GMP企业174环磷酰胺注射剂0.2G*5支15.00 18.00上海华联省新特药GMP企业175环磷酰胺注射剂0.2G 4.225.06江苏恒瑞市药品部GMP企业176脂肪乳注射液20%100ML46.69 56.03华瑞制药省普药进口药177脂肪乳注射液30%100ML67.10 80.52华瑞制药省普药进口药178脂肪乳注射液20%250ML85.27 102.32华瑞制药省普药进口药179脂肪乳注射液30%250ML131.62 157.94华瑞制药省普药进口药180脂肪乳注射液10%500ML86.11 103.33华瑞制药省普药进口药18118种氨基酸凡命注射液7%250ML25.30 30.36华瑞制药省普药进口药18218种氨基酸乐凡命注射液8.5%250ML36.6043.92华瑞制药省普药进口药183恩丹西酮注射剂2ML*4MG64.00 76.80山东齐鲁远东药业GMP企业184恩丹西酮注射剂4ML*8MG107.00 128.40山东齐鲁远东药业GMP企业185左旋氧氟沙星粉针剂0.1G51.66 61.99山西同领省普药GMP企业186人血白蛋白注射剂10G272.00 326.40上海莱士上海莱士GMP企业187重组人白介素2德路生注射液50万IU176.40 211.68北京四环省普药GMP企业188重组人白介素2德路生注射液100万IU239.40 287.28北京四环省普药GMP企业189左旋氧氟沙星可乐必妥片剂100MG*10S46.69 56.03日本第一制药省普药进口药190罗红霉素赛乐林胶囊150MG*12S51.04 61.25香港联邦省普药进口药191羟氨苄西林阿莫西林胶囊0.25G*20S18.40 22.08贝克诺顿省普药进口药192羟氨苄西林阿莫仙胶囊0.25G*24S21.74 26.09香港联邦省普药进口药193羟氨苄西林阿莫灵胶囊0.25G*24S23.50 28.20香港澳美省医药供销进口药194羟氨青霉素安必仙胶囊0.25G*24S21.60 25.92香港联邦省普药进口药195氨苄\舒巴坦强力安必仙注射剂0.75G16.6319.96香港联邦省普药进口药196氨苄\舒巴坦强力安必仙注射剂 1.5G47.6857.22香港联邦省普药进口药197氨苄\舒巴坦优力新注射液0.75G40.0548.06美国辉瑞省新特药进口药198头孢噻肟钠凯福隆注射液 1.0G70.00 84.00赫司特省新特药进口药199头孢哌酮钠头孢必注射剂 1.0G70.00 84.00塞普路斯省普药进口药200氧哌嗪\舒巴坦特灭注射液 1.5G52.80 63.36湘北威尔曼省新特药GMP企业201氨苄西林钠注射剂0.5G0.660.79山东齐鲁远东药业GMP企业邀标品种目录序号药品名称剂型规格供应价零售价生产厂家供货商备注202眼明注射剂1G*10支*2ML12.0014.40天津生化药厂省普药GMP企业203泛影葡胺注射剂60%*100ML60.0072.00上海信谊市药品部GMP企业204泛影葡胺注射剂76%*20ML*5支55.0066.00上海信谊市药品部GMP企业205辅酶A注射剂100U*10支 3.30 3.96天津生化药厂省普药GMP企业206辅酶A注射剂100U*10支 2.80 3.36上海第一生化市药品部GMP企业207白蛋白注射剂10G225.00270.00安徽大安安徽大安GMP企业208聚肌胞注射剂2MG*10支 3.60 4.32天津生化药厂省普药GMP企业209ATP注射剂20MG*10支 3.30 3.96上海第一生化市药品部GMP企业210ATP注射剂20MG*50支124.20149.04日本省普药进口药211硝苯地平控释片(伲福达)片剂20MG*30S21.137525.37青岛黄海北城公司GMP企业212皮炎宁酊酊剂20ML 2.30 2.76沈阳红旗省普药GMP企业213利福平胶囊0.15G*100S20.0024.00沈阳红旗省普药GMP企业214利福平片剂0.15G*100S12.0014.40浙江新昌市药品部GMP企业215吡嗪酰胺片剂0.25G*100S17.0020.40沈阳红旗省普药GMP企业216吡嗪酰胺胶囊0.25G*100S28.0033.60沈阳红旗省普药GMP企业217丙戊酸钠片剂0.2G*100S15.0018.00江苏恒瑞省普药GMP企业218重组人白介素2(欧耐特)粉针20万IU104.00124.80北京瑞得合通北京瑞得合通GMP企业219重组人白介素2(欧耐特)粉针50万IU164.00196.80北京瑞得合通北京瑞得合通GMP企业220重组人白介素2(欧耐特)粉针100万IU325.00390.00北京瑞得合通北京瑞得合通GMP企业22118种氨基酸注射剂250ML15.0018.00广州侨光省普药GMP企业222VB12注射剂0.5MG*10支 2.44 2.93上海第一生化省普药GMP企业223甘露醇注射剂250ML 3.50 4.20山东华鲁卫材进出口GMP企业224甘露醇注射剂250ML 3.50 4.20青岛国风市药品部GMP企业225氟康唑注射剂0.2G*100ML160.50192.60上海信谊市药品部GMP企业226胃肠舒胶囊0.4G*20S19.3023.16西安生化厂医药中成药GMP企业。
2016年4月23日重新修订的《疫苗流通和预防接种管理条例》(以下简称新条例)改变了所有疫苗生产企业二类疫苗的销售渠道,二类疫苗销售变成了'一票制“模式。
以下是本站分享的,希望能帮助到大家!疫苗生产企业二类疫苗销售实行“一票制”后的改变“一票制”后二类疫苗迎来了“救命”政策!2月7日,国务院办公厅印发《国务院办公厅关于进一步加强疫苗流通和预防接种管理工作的意见》(下称《意见》),明确提出“疫苗生产企业可采取‘干线运输+区域仓储+区域配送’的分段接力方式配送疫苗,干线运输可委托专业冷链运输企业,区域仓储和区域配送可委托具备冷链储运条件的配送企业。
各省(区、市)人民政府要结合本地区实际研究采取有效措施,确保偏远地区疫苗及时配送”。
与此同时,包括“组织开展第二类疫苗的评价、遴选,提出第二类疫苗使用品目”、“加快推进疫苗追溯信息系统建设,采取信息化手段,加强疫苗生产、流通和使用全过程追溯管理”、“支持新型疫苗特别是多联多价疫苗的研发和产业化”和“建立疫苗纳入或退出国家免疫规划”、“逐步推动将安全、有效、财政可负担的第二类疫苗纳入国家免疫规划”等重要变革性内容逐一被公布。
在二类疫苗市场几乎历经近一年的“冰冻期”后,《意见》开始解封全国百亿市场二类苗。
疫苗“一票制”“在2016年开始疫苗‘一票制‘后,这个政策可以说是为之前的政策打了补丁。
”昨日,有长期观察疫苗市场的业内人士向赛柏蓝表示。
公开资料显示,2016年,案值7亿元的山东非法经营疫苗事件曝光,轰动了国内外,也引起了世卫组织的高度关注。
当年4月,“国务院关于修改《疫苗流通和预防接种管理条例》的决定”公布,其核心修改内容为二类疫苗批发企业不能再经营疫苗,要求接种单位做到“票、账、货、款”一致;强化疫苗全程冷链储存、运输管理制度,并建立全程追溯系统;针对违法行为加大处罚及问责力度。
这个随后被业内称为疫苗“一票制”的政策带来的影响却远超出了最初的预期。
附件:
山西省2016-2017年度集中采购目录及采购限额标准
一、政府集中采购目录
以下项目应当委托政府集中采购机构组织实施采购活动。
注1:带★产品单次或批量采购30万元以下(市县20万元以下)实行协议供货
管理,但单件产品单价超过30万元(含汽车类)不受30万元限额限制。
市县可根据管理实际对实行协议供货和定点采购管理的品目进行适当增减。
注2:目录中未实行协议供货、定点采购的品目单次采购10万元以下(市县5
万元以下)由采购人自行采购。
二、部门集中采购目录
部门集中采购项目是指部门或系统有特殊要求的,需要由部门或系统统一配置的货物、工程和服务项目,可以委托代理机构采购,也可自行依照法定程序组织采购,其中自行采取招标方式组织采购的,采购人应当具备法律规定的条件。
三、政府采购限额标准
集中采购目录之外,达到以下限额标准的项目由采购人分散采购,按照法定采购方式和程序进行:
货物类:采购预算超过10万元的各类货物;
工程类:采购预算超过10万元的各类工程;
服务类:采购预算超过10万元的各类服务。
四、公开招标数额标准
货物、服务采购项目预算金额达到100万元及以上的(市县80万元以上的),应采用公开招标采购方式。
公开招标数额标准之上符合其他采购方式法定情形的,经财政部门批准可以采用非公开招标采购方式。
政府采购工程公开招标数额标准按照国务院及本省有关规定执行。