电子天平,奥豪斯CP114,分析天平,量程:110g,读数精度:0.0001g
- 格式:docx
- 大小:534.76 KB
- 文档页数:2

银纳米线的溶剂热法制备及表征刘裕堃;曹峰;胡超;秦天柱;赵博为;何桂美;王娟【摘要】以硝酸银为银源、聚乙烯吡咯烷酮(K-30)为模板剂和包覆剂、葡萄糖为还原剂、乙二醇为溶剂,采用溶剂热法成功制备出银纳米线.采用X-射线衍射(XRD)、扫描电子显微镜(SEM)、紫外可见吸收光谱(UV-Vis)、热重(TG)等手段对银纳米线进行了表征.结果表明,在反应温度为160 ℃、反应时间为4 h、聚乙烯吡咯烷酮(K-30)与硝酸银物质的量比为5的条件下,制备出直径100~150 nm、长度10~20μm的银纳米线.XRD物相分析表明,产物为结晶度较高、具有面心立方结构的纯银纳米线.%Using silver nitrate as a silver source,poly-vinylpyrrolidone(K-30)as a template and a covered agent,glucose as a reducing agent,and ethylene glycol as a solvent,we prepared silver nanowires by a solvothermal method.We characterized the silver nanowires by X-ray diffraction(XRD),scanning electron microscope(SEM),ultraviolet-visible absorption spectrum(UV-Vis) and thermogravimetry(TG).Results show that we can prepare silver nanowires with diameter of 100~150 nm,and length of 10~20 μm under the conditions as follows:reaction temperature of160 ℃,reaction time of 4 h,and molar ratio of poly-vinylpyrrolidone(K-30) and silver nitrate of 5.XRD phase analysis shows that the prepared silver nanowires have a high degree of crystallization and face-centered cubic structure.【期刊名称】《化学与生物工程》【年(卷),期】2017(034)007【总页数】4页(P35-37,42)【关键词】银纳米线;溶剂热法;聚乙烯吡咯烷酮【作者】刘裕堃;曹峰;胡超;秦天柱;赵博为;何桂美;王娟【作者单位】湖北大学化学化工学院,湖北武汉430062;湖北大学化学化工学院,湖北武汉430062;湖北大学化学化工学院,湖北武汉430062;湖北大学化学化工学院,湖北武汉430062;湖北大学化学化工学院,湖北武汉430062;湖北大学化学化工学院,湖北武汉430062;湖北大学化学化工学院,湖北武汉430062【正文语种】中文【中图分类】TQ131.22纳米银是一种同时具有高比表面积和表面活性、强杀菌性能、优良导电性和稳定物理化学性质的金属银单质,已逐渐发展成为一种高效的功能材料,被广泛应用于催化材料[1]、低温超导材料[2]、生物传感材料[3-4]和无机抗菌材料等领域。

CP114电子天平操作规程
1.调水平:使用前检查电子天平是否水平,如气泡偏移,调节红色水平调节
钮,使气泡位于水平仪的中心,接通电源;
2.开机:按一下“”键开启电源,仪器自检,屏幕显示【0.0000】后,预热60
分钟;
3.标准:按住“打印/校准”键直到屏幕显示【CAL】。
标准砝码值【200.0000】
在屏幕上闪烁,把100g的标准砝码放在秤盘上,此时显示屏闪动【bosy】。
当显示【clearpad】时,移走砝码,显示【done】,校准完成;
4.去皮:将空容器放在天平盘上,稳定后显示容器质量,按“去皮”或“置零”
键,显示“0.0000”,此时可以加样进行称量;
5.称量:将待称量物品放在空容器里,当显示屏左侧的稳定状态探测符【*】
出现,即可读取称量结果;按“去皮”或“置零”键,
6.关机:按住“Off”键不放,直到显示屏出现【OFF】,松开按键。
7.称量完毕,取出称量物品,关好天平门,并认真填写仪器使用记录。
8.注意事项
8.1保持天平清洁,防止灰尘进入天平内部,称量结束后用天平刷清理干净
8.2保持天平水平,称量腐蚀性物品时须放入具盖容器中称量。
8.3经常检查天平室的防潮硅胶,发现变成红色,应及时更换。
8.4严禁称量超出天平称量范围的物品(包括容器重量)
8.5每天下班前须关闭电源开关。
8.6仪器长期不用时,应将仪器,及配件装入原包装箱内,放置于阴凉干燥处。

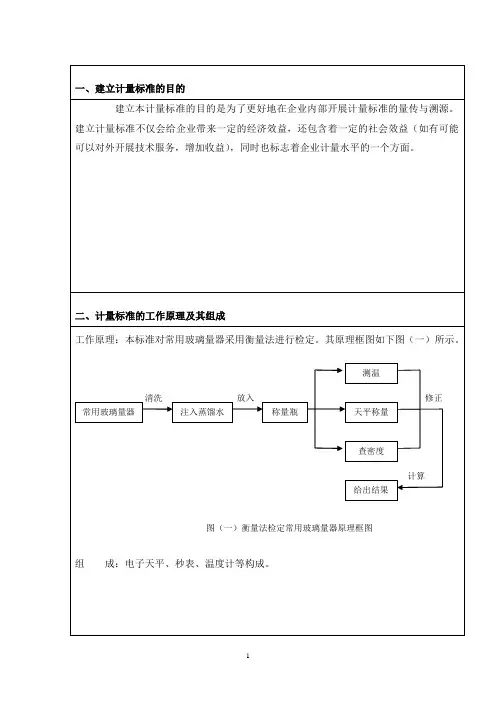
计量标准技术报告计量标准名称电子天平检定装置计量标准负责人建标单位名称(公章)填写日期目录一、建立计量标准的目的 (2)二、计量标准的工作原理及其组成................................... .. (2)三、计量标准器及主要配套设备................ .. (3)四、计量标准的主要技术指标 (4)五、环境条件 (4)六、计量标准的量值溯源和传递框图.............................. (5)七、计量标准的测量重复性试验................................... . (6)八、计量标准的稳定性考核 (7)九、检定或校准结果的测量不确定度评定 (8)十、检定或校准结果的验证 (15)十一、结论 (16)十二、附加说明 (16)12356七、计量标准的重复性试验取200g 的电子天平,编号为:D ,测量时环境温度为20℃,在本装置正常工作条件下,在其200g 测量点上等精度重复测量10次,测量结果如下:序号 测量值x i (g ) u i=x i -x (mg)u i2 (mg)1 200.0001 0.08 0.00642 200.0000 0.02 0.00043 200.0000 0.02 0.0004 4 200.0000 0.02 0.00045 200.0000 0.02 0.00046 200.0000 0.02 0.00047 200.0000 0.02 0.00048 200.0000 0.02 0.00049 200.0000 0.02 0.0004 10200.0001 0.080.0064x200.00002==-=∑∑==-91101212i ini xi Un xs 0.03(mg )结论:1. 经过评定200g 电子天平测量结果的不确定度U 95= 0.12mg2. 在重复性条件下,对200g 电子天平重复测量10次,其重复性误差为s=0.03mg3. 由于s=0.03mg <1/3U 95= 0.04mg计量标准的重复性考核合格,该计量标准重复性可靠满足JJG1033-2008计量标准考核规范的要求。

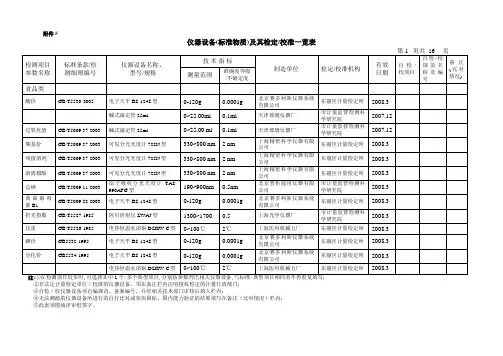
仪器设备(标准物质)及其检定/校准一览表②非法定计量检定单位/校准的仪器设备,须在备注栏内注明授权检定的计量行政部门;③自检/校仪器设备须自编规范、备案编号,并经相关技术部门审核后填入栏内;④无法溯源的仪器设备所进行的自行比对或参加国际、国内能力验证的结果填写在备注(比对情况)栏内;⑤此表须现场评审组签字。
仪器设备(标准物质)及其检定/校准一览表注:①在检测项目较多时,可选择其中1个/多个典型项目,分别按参数列出相关仪器设备,与标准/典型项目相同者不再重复填写;②非法定计量检定单位/校准的仪器设备,须在备注栏内注明授权检定的计量行政部门;③自检/校仪器设备须自编规范、备案编号,并经相关技术部门审核后填入栏内;④无法溯源的仪器设备所进行的自行比对或参加国际、国内能力验证的结果填写在备注(比对情况)栏内;⑤此表须现场评审组签字。
仪器设备(标准物质)及其检定/校准一览表②非法定计量检定单位/校准的仪器设备,须在备注栏内注明授权检定的计量行政部门;③自检/校仪器设备须自编规范、备案编号,并经相关技术部门审核后填入栏内;④无法溯源的仪器设备所进行的自行比对或参加国际、国内能力验证的结果填写在备注(比对情况)栏内;⑤此表须现场评审组签字。
仪器设备(标准物质)及其检定/校准一览表②非法定计量检定单位/校准的仪器设备,须在备注栏内注明授权检定的计量行政部门;③自检/校仪器设备须自编规范、备案编号,并经相关技术部门审核后填入栏内;④无法溯源的仪器设备所进行的自行比对或参加国际、国内能力验证的结果填写在备注(比对情况)栏内;⑤此表须现场评审组签字。
仪器设备(标准物质)及其检定/校准一览表注:①在检测项目较多时,可选择其中1个/多个典型项目,分别按参数列出相关仪器设备,与标准/典型项目相同者不再重复填写;②非法定计量检定单位/校准的仪器设备,须在备注栏内注明授权检定的计量行政部门;③自检/校仪器设备须自编规范、备案编号,并经相关技术部门审核后填入栏内;④无法溯源的仪器设备所进行的自行比对或参加国际、国内能力验证的结果填写在备注(比对情况)栏内;⑤此表须现场评审组签字。

1.0目的定期进行内部校准,确保电子天平在使用时符合允许误差。
2.0校准周期每6个月校准一次。
3.0仪器3.1电子天平3.1.1型号CP224S3.1.1.1Max(最大称量):220g3.1.1.2d(实际分度值):0.1mg3.1.2型号TP4KS3.1.2.1Max(最大称量):4000g3.1.2.2d(实际分度值):0.1g3.2标准砝码(已校准):1mg~200g、2kg4.0校准项目及允许误差4.1型号CP224S4.1.1天平鉴别力:e=10d(e=1mg),免检。
4.1.2天平最大允许误差:称量范围允许误差0~50000e ±0.5e(±0.5mg)>50000e~200000e ±1.0e(±1.0mg)>200000e ±1.5e(±1.5mg)4.1.3天平四角误差(试验载荷=100g):±1.0e(±1.0mg)。
4.2型号TP4KS4.2.1天平鉴别力:e=10d(e=1g),免检。
4.2.2天平最大允许误差:称量范围允许误差0~500e ±0.5e(±0.5g)>500e~2000e ±1.0e(±1.0g)>2000e ±1.5e(±1.5g)4.2.3天平四角误差(试验载荷=2000g):±1.0e(±1.0g)。
5.0 步骤5.1 校准前确保电子天平通电预热至少30分钟。
5.2 将电子天平调至水平位置。
5.3进行天平最大允许误差校准。
5.3.1 将天平调至零点。
5.3.2 从步骤4.0的每一称量范围中任意选取一个重量。
5.3.3 根据选好的重量,从标准砝码中选择对应重量的标准砝码。
5.3.4 将砝码放到称量盘上,待读数稳定后,将该读数记录下来。
5.3.5 重复上述步骤操作三次,计算平均值。

电子天平的校准方法沈阳龙腾ESJ200 ESJ180 ESJ120 ESJ60系列内校步骤:①将天平调至水平状态②天平预热40分钟③使天平空载并稳定地显示零位④按天平的“CAL”健,天平显示“CAL in”⑤等待几秒天平显示“CAL………”⑥稍后天平显示“CALdn”⑦此时应轻缓地将天平右侧的校准砝码搬下,使天平内部校准砝码加至天平的称量系统上⑧天平显示“CAL………”⑨稍后天平显示“CAL UP”⑩此时应轻缓地将天平右侧的校准砝码搬上,使天平内部校准砝码脱离天平的称量系统⑾稍后天平显示“CAL………”⑿等后天平显示“CAL END”⒀等后天平显示零位,表明天平完成一次内部校准。
注:如果校正过程中显示“CALno”,说明校准有错误或环境问题,应排除故障关机后重新开机进行校准。
沈阳龙腾FR系列内校步骤:①将天平调至水平状态②天平预热40分钟③使天平空载并稳定地显示零位④按天平的“CAL”触摸健⑤天平显示“CAL O”⑥稍后天平显示“CALF”⑦天平显示零位,此时表示天平完成校准。
沈阳龙腾JD系列外校步骤:①将天平调至水平状态②天平预热40分钟③清洁称盘使天平空稳定地显示零位④按住天平的“CAL”健,同时迅速按打印键天平显示校准砝码的重量值(用“MODE”和“PRINT” 键可以调整校准砝码值)⑤天平显示“CAL O”⑥稍后天平显示“CALF”在天平称盘上加放已显示质量值的标准砝码,按“TARE”或“RE -ZERO”键⑦天平显示“CALEND”时取下砝码⑧稍后天平显示零位,校准结束沈阳龙腾ES-1000 ES-2000 ES-5000系列外校步骤:以ES-2000为例①将天平调至水平状态②天平预热40分钟③清洁称盘使天平空稳定地显示零位④按住天平的“CAL”健,⑤天平显示“CAL 0.00g”⑥加放2000g标准砝码(全量值砝码)⑦天平显示“2000.00”⑧按天平的“CAL”健,⑨天平显示“CALEND”天平显示全量值⑩稍后天平显示零位,取下标准砝码,校准结束注:如果校正中显示“CALno”,说明天平不能校准,查看显示值与砝码实际值是否相差较大,如果是,则可调整天平微调电位器,使显示值与实际值接近,再使用校准键重新校准,方法如下:①取下天平右侧全量电位器塑料帽②将天平清零稳定后,把全量砝码放在称盘上③根据显示值与实际值的差值,用小螺丝刀调整全量电位器,若显示值小于砝码值,顺时针旋电位器,直到显示值与砝码值接近。
JM 系列电子天平JM Series Electronic Balance 使用说书Operation Lnstruction上海光正医疗仪器有限公司Shanghai Guang Zheng Medical Instrument Co., Ltd 包装附件天平主机1台秤盘1个电源线1根说明书、合格证、保修卡1份标准砝码(限d=10mg, d=1mg) 1个⊙计数及称重切换一、将容器置于秤盘上(不需要可不放),待显示稳定后按一下<去皮键>去除容器皮重。
二、按住<计数键>不放直到闪烁显示×××,松开按键。
×××代表计数。
反复按<单位键>您可在10、20、30、40、50、100、150、200中选择您需要的计件数。
此时您也可以一直按住<去皮键>不放从而退出计数状态,回到称量状态。
三、在容器中放入您选择计数目的物件,(如您选择的计数件数是30,则放入30个物件即可)按<计数键>,显示“------”等待状态,稍候天平显示所放物件件数,就可进行技术操作。
四、如果欲读取计数物件的重量,可按一下<计数键>进行物件计数和称重切换操作。
五、如果平均单个物件的重量小于两倍的天平最小读数值则闪烁显示错误信息“Erro_2”,这时可按<去皮键>退出,或经过一段时间自动退出,回到称量状态。
⊙打开包装请检查若有损坏或缺件及时和我厂联系。
⊙错误信息一、上横线﹉﹉超载,被称物超出称量范围。
若此错误发生在量程范围内,可能是天平校准不正确。
请重新校准天平。
二、下横线﹍﹍指示被示称量偏负,请重新校准天平。
三、Erro_2平均单个物件的重量太小,增加物件数量,然后再换算。
四、读数偏大:先对天平进行校准,之后还不准确则再重复上述过程1-3次,若还不准确,进行多点校准,若还不准确,天平需要进行维修。
山药中多糖的含量测定方法学研究徐广忠;刘亚豪;周军;丁志远【摘要】目的:建立山药中多糖含量的测定方法,测定并比较不同产地山药中多糖的含量.方法:采用紫外-可见分光光度法测定山药中多糖的含量,苯酚-硫酸法显色,显色条件:苯酚浓度:5%;苯酚用量:1mL;硫酸用量:7mL;温度:40℃;时间:15min;测定波长:490nm.结果:葡萄糖浓度在10.07~100.7μg/ml范围内呈良好线性关系,r=0.9995,重复性RSD=1.1%(n=6),平均回收率98.5%,RSD=1.2%(n=6).结论:本法简便、准确、重复性好,适用于山药中多糖的含量测定,且测得不同产地的山药中多糖的含量存在较大差异.【期刊名称】《黑龙江科技信息》【年(卷),期】2017(000)034【总页数】3页(P3-5)【关键词】山药;多糖;紫外-可见分光光度法【作者】徐广忠;刘亚豪;周军;丁志远【作者单位】亳州职业技术学院,安徽亳州 236800;安徽亳州浙皖中药饮片股份有限公司,安徽亳州 236800;安徽亳州浙皖中药饮片股份有限公司,安徽亳州 236800;安徽亳州浙皖中药饮片股份有限公司,安徽亳州 236800;安徽广美药业股份有限公司,安徽亳州 236800【正文语种】中文山药为薯蓣科植物薯蓣的干燥根茎,广泛分布于我国大部分地区,具有很高的营养价值和药用价值,是常用的药食两用植物。
食用山药主要分布在南方地区,而药用山药主要分布在北方地区,尤以怀山药为代表,其药用价值较高 [1]。
山药性甘,平,归脾、肺、肾经。
具有补脾养胃,生津益肺,补肾涩精的功效,用于脾虚食少,久泻不止,肺虚喘咳,肾虚遗精,带下,尿频,虚热消渴等[2]。
山药中含有多糖、尿囊素、糖蛋白、皂苷、蛋白质、氨基酸、淀粉和脂肪等多种成分,其中多糖是山药的主要活性成分,具有降低血糖、调节免疫、抗氧化、抗衰老、抗肿瘤等多种药理作用[3-5]。
然而药典及各地方药品标准中,尚未将山药中多糖含量作为质量控制项目。
序号量具名称规格/型号制造商校准依据允许误差1压力表0-1.0MPa SMCJJG52-2013 2.5级测量上限的90%-100% 允许误差降低一级。
(有 1.0、1.6、2.5、4.0等级)23压力表0-1.6MPa青岛工业仪表研究所JJG52-2013 2.5级测量上限的90%-100% 允许误差降低一级。
(有 1.0、1.6、2.5、4.0等级)24数显绝缘电阻表MS5201MASTECHJJG1005-2005JJG315-1983JJG(航天)35-1999JJG724-1991绝缘电阻:200M Ω/250V ±3%、200M Ω/500V ±3%、0-1000M Ω/1000V ±3%、1000-2000M Ω/1000V ±5%直流电压:1000V ±0.8%交流电压:700V ±1.2%电阻:200Ω±1.2%25绝缘电阻测试仪CS2676CX 南京长盛仪器JJG1005-2005输出电压(DC )精度:±(2%+3‰FS )电阻精度:300V-1000V:R <1000M Ω ±2% R <10G Ω ±3% R <100G Ω ±5%100V-300V:R <1000M Ω ±3% R <10G Ω ±5% R <100G Ω ±7%30.0V-99.9V:R <1000M Ω ±3% R <10G Ω ±5% R <100G Ω ±7%1.0V-9.99V:R <100M Ω ±5% R <1G Ω ±7%26数字万用表MS8261MASTECH JJF1587-2016直流电压:量程200mV-200V ±(0.5%读数+1字)量程1000V ±(0.8%读数+2字)交流电压:量程2V-200V ±(0.8%读数+3字)量程750V ±(1.2%读数+3字)电阻:量程200Ω ±(0.8%+3字)量程2k Ω-2M Ω ±(0.8%+1字)量程20M Ω ±(1.0%读数+2字)量程200M Ω ±(5.0%读数+10字)直流电流:量程2mA ±(0.8读数+1字)量程20mA-200mA ±(1.5%读数+1字)量程10A ±(2.0%读数+5字)交流电流:量程2mA ±(1.0读数+3字)量程200mA ±(1.8%读数+3字)量程10A ±(3.0%读数+7字)计量器具允许误差序号量具名称规格/型号制造商校准依据允许误差计量器具允许误差27数字万用表87V FLUKE JJG315-1983JJG598-89JJG(航天)34-1999JJG(航天)35-1999JJG724-1991直流电压:±(0.05%+1)交流电压:±(0.7%+2)直流电流:±(0.2%+2)交流电流:±(1.0%+2)电阻:±(0.2%+1)29干湿球温度计-10-50℃上海华辰JJG205-2005温度示值误差不超过± 2.0℃湿度允许误差:±5%RH(40%RH-70RH 20℃)±7%RH(40%RH以下或70RH以上 20℃)30温湿度表TH-101B美德时JJG205-2005温度示值误差不超过± 2.0℃湿度允许误差:±5%RH(40%RH-70RH 20℃)±7%RH(40%RH以下或70RH以上 20℃)31数显温度指示调节仪E5CN欧姆龙JJG617-1996±2.0℃42扭矩扳手 4.5-30N·mENDURA JJG707-2014示值误差:±3% 44扭矩扳手5-25N·mSATA JJG707-2014示值误差:±3%45红外测温仪ST25Raytek JJG856-2015证书:100℃±3℃200℃±3℃300℃±6℃400℃±8℃500℃±10℃无锡市计量测试院说明书-18-23℃±2℃23-510℃读数的±1%或±1℃46针式数字测温仪TP101JJG874-2007±1℃76密度计1.200~1.300g/cm3JJG42-2011浮计示值的最大允许误差,除分度值为0.5kg/m3的石油密度计为±0.6个分度值外,其他均不能大于±1个分度值79电子天平ARRV70上海奥豪斯JJG1036-2008准确度等级:II级,最大称量:410/100g,检定分度值:0.1/0.01g最大允许误差 I级 II级 III级 IIII级±0.5e 0≤m≤5*104 0≤m≤5*103 0≤m≤5*102 0≤m≤50±1.0e 5*104<m≤2*105 5*103<m≤2*104 5*102<m≤2*103 50<m≤2*102±1.5e 2*105<m 2*104<m≤1*105 2*103<m≤1*104 2*102<m≤1*103序号量具名称规格/型号制造商校准依据允许误差计量器具允许误差80架盘天平HC-TP11-20上海精科天平JJG156-2016JJG99-2006最大称量:2000g,分度值:2g最大允许误差:载荷m(以检定分度值e表示)最大允许误差0≤m≤500 ±0.5e500<m≤2000 ±1.0e注:天平使用中检查的最大允许误差应是首次检定时最大允许误差的2倍。
超声波辅助提取茶叶总黄酮及抗氧化活性分析吕名秀;高玉梅;董雪茹;强黎明;李玲玲【摘要】采用超声波辅助法探讨了铁观音茶叶中总黄酮的最佳提取工艺条件,并测定了铁观音茶叶总黄酮清除羟基自由基的能力.结果表明,超声波功率400 W,料液比1∶30 g·mL-1,浸提时间30 min,乙醇浓度50%为超声波辅助提取铁观音茶叶总黄酮的最佳工艺条件,总黄酮提取率为4.74%;抗氧化实验表明随着铁观音茶叶总黄酮浓度的增大,其对羟基自由基的清除能力增大,当浓度达到0.80 g/L,清除率为65.14%,与BHT相比具有较强的抗氧化能力.%Flavonoids from Tieguanyin tea were extracted by ultrasonic method, and their antioxidant activity was determined.The results showed that the optimum extraction conditions are ultrasonic power of 400 W, material to liquid r atio of 1∶30 g·mL-1, extracting time of 30 min, ethanol concentration of 50%, and the extraction yield of tea flavonoids is 4.74%.With the increasing concentration of tea flavonoids, their antioxidant activity became greater.When the concentration of tea flavonoids reaches 0.80 g/L, clearance rate of free radical is 65.14%.The antioxidant capacity of tea flavonoids is stronger than butylated hydroxytoluene (BHT).【期刊名称】《化学研究》【年(卷),期】2017(028)002【总页数】6页(P213-218)【关键词】茶叶;总黄酮;超声波;抗氧化活性【作者】吕名秀;高玉梅;董雪茹;强黎明;李玲玲【作者单位】河南工程学院材料与化学工程学院,河南郑州 450007;河南工程学院材料与化学工程学院,河南郑州 450007;河南工程学院材料与化学工程学院,河南郑州 450007;河南工程学院材料与化学工程学院,河南郑州 450007;河南工程学院材料与化学工程学院,河南郑州 450007【正文语种】中文【中图分类】TS201.1茶叶是重要的世界性作物之一,广泛分布于亚洲、远东、拉美和大洋洲等地[1]. 它是世界上仅次于水的第二大饮品. 据FAO-IGG统计,2015年全球茶叶产量达到528.5万吨. 2010年以来,中国茶叶产量持续增长,2015年已达到227.8万吨,稳居世界第一产茶国的地位[2-3]. 茶叶中所含的成分很多,将近500种. 人们熟知的几种重要成分有茶多酚、黄酮类化合物、维生素C、咖啡碱、蛋白质等[4]. 另外,茶叶中还含有许多人体必需的微量元素,如钙、铁、锌、镁、碘、氟、锰、钼、硒、锗等[5-6].许多文献报道,茶叶具有良好的抗氧化能力[7],能抑制活性氧的形成,有效清除自由基[8],这与其含有多种抗氧化物有关,如黄酮、儿茶素、茶黄素、没食子酸等[9]. 黄酮有很多的药理作用,已被广泛的应用于医学的临床治疗[10-13]. 黄酮具有降血压、防止动脉硬化、降血脂、清热解毒、抗氧化、强化细胞膜、活化细胞等功效[7]. 随着患有肿瘤疾病人数的增多,现代医学对黄酮的需求越来越大. 茶叶在全球分布广泛,且茶叶中总黄酮含量较高[14]. 另外,市场上使用的食品抗氧化剂大多是通过化学实验合成品(如 BHT),存在食品安全性问题. 而天然抗氧化剂具有安全、无毒等优点[15].以茶叶为原料,从茶叶中提取黄酮,既可满足于当代医学上、食品添加剂及化妆品对黄酮的需求,又使得茶叶得到广泛的开发利用,因此探索提取茶叶黄酮的工艺研究具有良好的经济效益和社会效益. 目前,超声波提取法在天然产物中有效成分的提取上表现出较强的优势:提取速度快、提取效率高、节约溶剂、低温进行(40~60 ℃)、操作简单易行、提取料液杂质少等[16-18],与传统提取法相比,超声波提取法是一种实现快速、高效、环保、节能的现代新技术. 本研究将通过单因素实验和正交试验,确定超声波辅助法提取铁观音茶叶总黄酮的最佳工艺条件,同时对茶叶总黄酮进行抗氧化活性分析,为茶叶的综合开发利用提供理论依据.1.1 材料与仪器铁观音茶叶购于福建省安溪县宝隆茶业有限公司;芦丁标准品购于南京苏朗医药科技开发有限公司;无水乙醇、亚硝酸钠、硝酸铝、氢氧化钠、三羟甲基氨基甲烷(Tris)、邻二氮菲、七水合硫酸亚铁、2,6-二叔丁基-4-甲基苯酚(BHT)、盐酸、双氧水等均为分析纯试剂.XH-300 UL电脑微波超声波紫外光组合催化合成仪,北京祥鹄科技发展有限公司;CP 114型电子天平,奥豪斯仪器(上海)有限公司;UV-3600紫外可见近红外分光光度计,日本Shimadzu公司;DK-8 AX恒温水浴槽,上海精密仪器仪表有限公司.1.2 实验方法1.2.1 原料处理首先要把铁观音茶叶粉碎,通过恒温干燥箱干燥至恒重,封口密封,在干燥处保存. 粉碎过40目筛、烘干至恒重,密封,在干燥处保存备用.1.2.2 芦丁标准曲线的绘制将芦丁标准品在120℃下恒温烘干,精密称取纯度为98%的芦丁标准品10.30 mg,置于10 mL容量瓶中,用60%乙醇溶解,然后用70%乙醇定容至刻度线,摇匀,得到芦丁标准溶液[15-16],浓度1.009 4 g/L.精密吸取芦丁标准溶液0.00、0.10、0.20、0.30、0.40、0.50、0.60 mL,分别置于10 mL容量瓶中,加60%的乙醇至2.0 mL;加入5%的NaNO2溶液0.4 mL,摇匀放置6 min;然后加入10%的Al(NO3)3溶液0.4 mL,摇匀再放置6 min;再加4.0 mL 5%的NaOH溶液;用70%的乙醇定容,摇晃均匀后等待10 min;最后在波长510 nm处测溶液的吸光度A(见图1). 重复3次,算其平均值.1.2.3 茶叶提取物的制备称取干燥的茶叶粉末2.00 g,加入60 mL 70%的乙醇于60 ℃水浴锅中回流提取1 h,抽滤. 滤液定容至100 mL,摇匀备用.1.2.4 提取茶叶总黄酮的单因素试验分别考察了超声波功率,浸提时间,乙醇的体积分数,料液比和温度等五个因素对超声波辅助法从茶叶中提取总黄酮的最佳工艺,每组试验重复3次,取平均值作图.1.2.5 提取茶叶总黄酮的正交试验通过比较每个因素对实验结果的影响,选取乙醇浓度、超声波功率、浸提时间及料液比四个因素为考察因素,以茶叶总黄酮提取率为考察指标,设计四因素三水平正交实验. 根据正交试验结果得出茶叶总黄酮提取率最大的工艺条件并进行验证试验[19-20],每个试验重复3次,取平均值.1.3 总黄酮提取率的计算方法测定提取液的吸光度[21-22],具体方法同1.2.2. 根据芦丁标准曲线计算茶叶总黄酮的质量浓度ρ,每组试验重复3次,取平均值,计算茶叶总黄酮的提取率.1.4 铁观音茶叶总黄酮对·OH的清除能力测定在10 mL容量瓶中依次加入7.5 mmol/L邻二氮菲溶液1.0 mL,50.0 mmol/L Tris-HCl (pH=7.4)溶液2.0 mL,7.5 mmol/L FeSO4 溶液1.0 mL,混匀后,再分别加入铁观音茶叶总黄酮浓度为0.2、0.4、0.6、0.8、1.0、1.2 g/L的溶液1.0 mL,0.1%的双氧水1.0 mL,用蒸馏水定容,混合均匀后,置于37 ℃的水浴中保温1 h,在510 nm处测得Ai,当用蒸馏水替代试样得到A1,用蒸馏水替代H2O2和试样得到A0,可排除样品本身的影响,BHT作对照,Tris-HCl溶液作空白溶液,计算得到自由基清除率[23]. 每组试验重复3次,取平均值作图.2.1 单因素试验结果2.1.1 超声波功率对茶叶总黄酮提取的影响在200~500 W范围内,改变超声波功率,测定茶叶总黄酮的提取率,结果见图2. 茶叶总黄酮的提取率随着超声波功率的增大呈现先升后降的趋势,350 W时茶叶总黄酮提取率最高,推测可能是因为超声波功率太大,能量太高,使部分总黄酮结构遭到破坏,这样就导致检测到的总黄酮含量减少. 因此,试验选择350 W作为提取茶叶总黄酮的超声波功率.2.1.2 浸提时间对茶叶总黄酮提取的影响由图3可以看出:延长浸提时间,茶叶总黄酮的提取率呈现先增加后减小的趋势,浸提时间为30 min时,茶叶总黄酮提取率最高. 30 min前茶叶总黄酮的提取率随时间延长而增大;30 min之后,茶叶总黄酮的提取率随时间的延长反而下降,这可能是因为时间太长,会使茶叶细胞内其他杂质进入提取液,增大传质阻力,影响茶叶总黄酮的溶出. 因此,超声波辅助下,茶叶总黄酮的最佳浸提时间为30 min. 2.1.3 乙醇浓度对茶叶总黄酮提取的影响由图4可以得出:随着乙醇浓度的增大,茶叶总黄酮的提取率呈现先升后降的趋势,乙醇浓度为50%时,茶叶总黄酮提取效果最好. 当乙醇浓度大于50%时,茶叶总黄酮的提取率下降,这可能是乙醇浓度过大,茶叶中一些易溶于乙醇的脂溶性物质、色素等副产物溶出,从而减少了茶叶总黄酮的溶出量,测量结果偏低. 因次,选择50%乙醇为提取茶叶总黄酮的溶剂.2.1.4 料液比对茶叶总黄酮提取的影响由图5可以得出:增加溶剂的体积,茶叶总黄酮的提取率呈现先升后降的趋势,料液比为1∶20 g·mL-1时,茶叶总黄酮的提取率最大. 但随着溶剂体积继续增大,茶叶总黄酮的提取率减小,这也许是由于随着乙醇用量的增大,许多易溶于乙醇的其他物质大量溶出,干扰了茶叶总黄酮的溶出,从而使茶叶总黄酮的提取率降低. 因此提取茶叶总黄酮的最适合的料液比是1∶20 g·mL-1.2.1.5 温度对茶叶总黄酮提取的影响由图6可得:升高温度,在35 ℃之前,茶叶总黄酮的提取率随温度升高而迅速升高,在35 ℃之后茶叶总黄酮的提取率升高的较为缓慢,从节约能量和满足实验条件的方面来说,选择温度35 ℃恰到好处,既能满足实验所需要到的温度又减少耗能使提取茶叶总黄酮的量最多又节约了成本.2.2 正交试验结果分析为获得茶叶总黄酮最优的提取工艺,在单因素试验基础上,选择乙醇浓度、超声波功率、浸提时间及料液比作为考察因素,以总黄酮提取率为考察指标,按照L9(34)正交表进行正交试验,因素水平表如表1所示,正交试验结果与数据分析见表2.正交实验结果说明,不同的因素对提取率的影响是:乙醇浓度 > 超声波功率 > 料液比 > 浸提时间. 根据结果可知,超声波辅助法提取茶叶总黄酮最佳条件是:A2B3D3C2,即乙醇浓度为50%,超声波功率为400 W,浸提时间为30 min,茶叶与乙醇的料液比为1∶30 g·mL-1.2.3 验证实验为确定优化提取工艺的稳定性,在该工艺条件下进行3组平行实验,测得铁观音茶叶总黄酮的提取率分别为4.72%,4.74%,4.75%,平均为4.74%,此条件为铁观音茶叶总黄酮的最佳提取工艺.2.4 清除·OH自由基能力以BHT作为对照,测定了茶叶总黄酮清除羟基自由基能力,结果如图7所示. 茶叶总黄酮对·OH自由基的清除能力随着总黄酮浓度的增加而增大,当浓度达到0.8 g/L后,清除率为65.14%,说明茶叶总黄酮能够清除·OH自由基,且在测定浓度范围内茶叶总黄酮清除·OH自由基能力强于BHT.采用超声波辅助法提取茶叶中的总黄酮具有良好的效果. 单因素试验和正交试验结果显示各因素对茶叶黄铜提取率的影响顺序为:乙醇浓度>超声波功率>料液比>浸提时间. 通过验证试验可知超声波辅助法提取茶叶总黄酮的最优条件为:乙醇浓度50%,超声波功率400 W,浸提时间30 min,料液比为1∶30 g·mL-1,在此条件下,茶叶总黄酮的提取率可达4.74%. 茶叶总黄酮和BHT对·OH自由基的清除能力均随着浓度增大而变强. 茶叶总黄酮能够清除·OH,且比BHT对·OH的清除能力强.【相关文献】[1] 吴东碧. 安溪茶叶综合利用现状及其对策研究[D]. 北京: 中国农业科学院, 2009: 1-2.WU D B. The study on the comprehensive utilization of Anxi tea and its strategy [D]. Beijing: Chinese Academy of Agricultural Sciences, 2009: 1-2.[2] 王庆, 于英杰, 李佳禾, 等. 经济新常态下中国茶产业改革发展建议[J]. 中国茶叶加工, 2016(3): 5-12.WANG Q, YU Y J, LI J H, et al. Proposals on reform and development of Chinese tea industry under new economic normal [J]. China Tea Processing, 2016(3): 5-12.[3] 李佳禾. 2015中国茶产业消费报告[J]. 茶世界, 2015(12): 29-37.LI J H. Tea industry consumption report of China in 2015 [J]. Tea World, 2015(12): 29-37.[4] 陆晨, 张士康, 朱科学, 等. 碱提酸沉法提取茶叶蛋白质的研究[J]. 现代食品科技, 2011, 27(6): 673-677.LU C, ZHANG S K, ZHU K X, et al. Extraction of tea protein using alkali extraction-acid precipitation method [J]. Modern Food Science and Technology, 2011, 27(6): 673-677. [5] 宛晓春, 李大祥, 张正竹, 等. 茶叶生物化学研究进展[J]. 茶叶科学, 2015, 35(1): 1-10.WAN X C, LI D X, ZHANG Z Z, et al. Research advance on tea biochemistry [J]. Journal of Tea Science, 2015, 35(1): 1-10.[6] 李娟, 活泼, 杨海燕. 茶叶功效成分研究进展[J]. 浙江科技学院学报, 2005, 17(4): 285-289.LI J, HUO P, YANG H Y, et al. Research advances in functional compositions of tea [J]. Journal of Zhejiang University of Science and Technology, 2005, 17(4): 285-289.[7] KANWAR J, TASKEEN M, MOHAMMAD I, et al. Recent advances on tea polyphenols [J]. Frontiers in Bioscience (Elite Edition), 2012, 4: 111-131.[8] 侯冬岩, 回瑞华, 刘晓媛, 等. 绿茶、红茶和乌龙茶抗氧化性能的比较[J]. 食品科学, 2006, 27(3): 90-93.HOU D Y, HUI R H, LIU X Y, et al. Comparison of the antioxidation effects of green tea, black tea and wulong tea [J]. Food Science, 2006, 27(3): 90-93.[9] 杨青, 郭彩清, 油继辉, 等. 黄酮类物质的生理功能及应用发展动态[J]. 贵州农业科学, 2007, 35(2): 143-146.YANG Q, GUO C Q, YOU J H, et al. Physiological function of the flavonoids and it s application [J]. Guizhou Agricultural Sciences, 2007, 35(2): 143-146.[10] 黄河胜, 马传庚, 陈志武. 黄酮类化合物药理作用研究进展[J]. 中国中药杂志, 2000, 25(10): 582-589.HUANG H S, MA C G, CHEN Z W. Advances in research of pharmacological effects of flavonoid compounds [J]. China Journal of Chinese Materia Medica, 2000, 25(10): 582-589.[11] 王基云, 姚瑶, 肖旭. 沙枣花黄酮成分含量测定及其药理作用的初步研究[J]. 时珍国医国药, 2010, 21(4): 812-814.WANG J Y, YAO Y, XIAO X. Determine the contents of total flavonoids in elaeagnus angustifolia blossoms and the preliminary research of the pharmacological effects [J]. Lishizhen Medicine and Materia Medica Research, 2010, 21(4): 812-814.[12] 李冬生, 陈朝银, 赵声兰, 等. 黄酮类化合物改善记忆的机制研究[J]. 食品工业科技, 2014(10): 360-365.LI D S, CHEN Z Y, ZHAO S L, et al. Study on mechanisms of flavonoids improving memory [J]. Science and Technology of Food Industry, 2014(10): 360-365.[13] 唐传核. 植物功能性的食品[M]. 北京: 化学工业出版社, 2004: 324-372.TANG C H. Plant functional food [M]. Beijing: Chemical Industry Press, 2004: 324-372. [14] KIM E K, LEE S J, MOON S H, et al. Free radical scavenging activity and comparative proteomic analysis of anti-oxidative protein against H2O2-induced oxidative stress in neuronal cells [J]. Food Chemistry, 2009, 117(2): 232-240.[15] 宋秋华, 张磊, 梁飞, 等. 黄酮类化合物提取和纯化工艺研究进展[J]. 山西化工, 2007, 27(4): 24-27.SONG Q H, ZHANG L, LIANG F, et al. Progress in research of the extracting and purifying technology of flavoniods [J]. Shanxi Chemical Industry, 2007, 27(4): 24-27.[16] 王顺新, 牟德华, 王小伟. 超声波辅助提取人参果叶黄酮工艺研究[J]. 食品工业, 2016, 37(5):68-70.WANG S X, MOU D H, WANG X W. Study on extraction of flavonoids from solanum muricatum leaf by ultrasonic [J]. Food Industry, 2016, 37(5): 68-70.[17] 杜若源, 谢晶, 王婷, 等. 超声波辅助提取银杏叶中总黄酮的工艺优化[J]. 食品与机械, 2015, 1(1): 1-3.DU R Y, XIE J, WANG T, et al. Optimizationon extracting technology of total flavonoids from Ginkgo biloba leaves by ultrasonic-assisted method [J]. Food and Machinery, 2015, 1(1): 1-3.[18] 许瑞波, 周洪英, 陈林. 地瓜叶总黄酮的超声辅助提取及生物活性研究[J]. 食品科学, 2013, (14): 141-146.XU R B, ZHOU H Y, CHEN L. Ultrasonic-assisted extraction and bioactivity of flavonoids from ipomoea batatas lam leaves [J]. Food Science, 2013, (14): 141-146.[19] 韩雅慧, 顾赛麒, 陶宁萍, 等. 甘草总黄酮提取工艺及总抗氧化活性研究[J]. 食品工业科技, 2012, 33(2): 239-242.HAN Y H, GU S Q, TAO N P, et al. Study on the extraction conditions and total antioxidant capacity of licoflavone from two kinds of liquorice samples [J]. Science and Technology of Food Industry, 2012, 33(2): 239-242.[20] SIRIPORN O, CHADARAT D, SONGYOT A, et al. Comparison of antioxidant capacities and cytotoxicities of certain fruit peels [J]. Food Chemistry, 2007, 103(3): 839-846.[21] GAVIN N M, DURAKO M J. Localization and antioxidant capacity of flavonoids from intertidal and subtidal halophila johnsonii and halophila decipiens [J]. Aquatic Botany, 2011, 95(3): 242-247.[22] 李娇娟, 龚建良, 周尽花. 油茶叶总黄酮的提取及抗氧化活性研究[J]. 食品研究与开发, 2008,29(12): 93-96.LI J J, GONG J L, ZHOU J H. Research on extraction and antioxidant activities of the total flavonoids from Camellia oleifera Abel leaves [J]. Food Research and Development, 2008, 29(12): 93-96.[23] 周金伟, 陈雪, 易有金, 等. 不同类型茶叶体外抗氧化能力的比较分析[J].中国食品学报, 2014, 14(8): 262-267.ZHOU J W, CHEN X, YI Y J, et al. Comparative analysis on capacities of different types of fermented teas in vitro [J]. Journal of Chinese Institute of Food Science and Technology, 2014, 14(8): 262-267.。
关于奥豪斯奥豪斯总部设在美国新泽西州帕西帕尼,是全球领先的称重产品、实验室设备和分析仪器制造商,符合并超越实验室、工业、教育、食品等多个行业的称重及测量需求。
作为通过ISO 9001:2015认证的制造商,奥豪斯公司与产品具有精准、可靠、价格合理的特性,同时拥有行业领先的全球客户服务体系。
奥豪斯公司 OHAUS Corporation上海市徐汇区桂平路 680 号33 幢 7 楼电话:4008 217 188传真:(021)64859748O H A U S .c o m生产管理体系通过 ISO 9001:2015 认证。
80776553 20200218 © 版权所有 奥豪斯公司实验室工业食品教育零售美国奥豪斯价值之旅天平和工业衡器分析仪器实验室设备灵感源于务实目录品牌故事2奥豪斯价值之旅4信任6智能8创新10承诺12产品应用14实验室16工业18教育20食品22零售24详情请访问从定义称量行业标准的“哈佛之旅”天平,到突破性的Explorer 分析天平和精密天平,奥豪斯秉承创新之理念。
1907年,Gustav Ohaus 和父亲Karl Ohaus 在新泽西州纽瓦克市创办了一家小型天平维修工厂。
随后,他们将OHAUS 注册为商标,开始制造天平和工业衡器。
随着业务发展,奥豪斯因产品精准、可靠、耐用享有盛誉。
2创新之路百年经典全球化运营以质量、精准和价值为代名词的奥豪斯,已将业务扩展至更广发的专业产品市场,如分析仪器和实验室设备等。
产品丰富在深耕美国本土市场的同时,奥豪斯的分支机构也逐步遍及六大洲,建立了广泛的经销商网络,以快速响应世界各地的客户需求。
随着数字化的发展和专业技术研发,奥豪斯产品始终能符合并超越市场需求。
奥豪斯价值之旅奥豪斯自创立一个多世纪以来,一直是精准和可靠的代名词。
奥豪斯精密天平和工业衡器、实验室设备和分析仪器等,专为满足不同行业持续发展的需求而设计。
“灵感源于务实”的理念,已深入奥豪斯所有产品和服务,能为客户提供实实在在的价值,帮助客户提高质量和准确性。