第一节 肥皂的性质及去污原理2
- 格式:ppt
- 大小:291.00 KB
- 文档页数:54

肥皂的制备班级:精细化学品生产技术30903班组员:李晔王浩亮李海艳指导老师:***一、肥皂的概述1.1 肥皂的定义肥皂从广义上讲,是油脂、腊、松香或脂肪酸与有机或无机碱进行皂化或中和所得的产物。
而油脂、蜡、松香与碱所以能发生作用,实质上是脂肪酸与碱作用,因而肥皂是脂肪酸盐:ROOM,式中R代表烃基,M为金属离子或有机碱类。
只有碳数在8~22的脂肪酸碱金属盐才具有洗涤作用,因此肥皂是至少含有8个碳原子的脂肪酸或混合脂肪酸的碱性盐类(无机的或有机的总称)。
8个碳原子数以下的脂肪酸及其碱金属盐在水溶解度太大,且表面活性差;大于22个碳原子的脂肪酸盐类难溶于水,两者均不适宜做肥皂1.2 肥皂的去污原理肥皂分子结构可以分成二个部分。
一端是带电荷呈极性的COO-(亲水部位) ,另一端为非极性的碳链(亲油部位)。
肥皂能破坏水的表面张力,当肥皂分子进入水中时,具有极性的亲水部位,会破坏水分子间的吸引力而使水的表面张力降低,使水分子乎均地分配在待清洗的衣物或皮肤表面。
肥皂的亲油部位,深入油污,而亲水部位溶于水中,此结合物经搅动后形成较小的油滴,其表面布满肥皂的亲水部位,而不会重新聚在一起成大油污。
此过程(又称乳化)重复多次,则所有油污均会变成非常微小的油滴溶于水中,可被轻易地冲洗干净。
不仅是肥皂,任何洗涤剂的去污都是由于下列几种用途:1、润湿作用。
即使得纺织品或其他固态物质能被水所润湿,为此要求任何洗涤剂都是表面活性剂,能降低水的表面张力,使水分子易于渗透到织物组织中去。
2、乳化力。
污物被肥皂或洗涤剂分子包围后,易于分散到液体中去形成乳状液,因此,也要求洗涤剂能降低水的表面张力。
3、分散作用或胶溶作用。
这就要求洗涤剂分子是分散剂,把油渍、污物变成发散的胶体溶液,其中主要靠洗涤剂分子和水形成的双电层的吸附引力。
4、保护作用。
保护胶体粒子不发生聚沉作用。
5、去污作用。
防止污垢重新沉积在织物上的能力。
6、泡沫力。
起泡是洗涤过程中很普遍的现象,但并不是洗涤剂中表面活性物质的主要性质。

肥皂去污的科学原理是什么肥皂去污的科学原理是什么肥皂是人类使用最广泛的清洁剂之一,它具有卓越的去污能力,能够有效地清洗衣物、餐具、地板等各种物品。
那么,肥皂去污的科学原理是什么呢?肥皂的主要成分是一种称为表面活性剂的化合物,它可以使水和油相互溶解。
表面活性剂分为阳离子和阴离子两种,而肥皂属于阳离子表面活性剂。
阳离子表面活性剂分子具有一个带正电荷的氮或氧原子,这使得他们能够与带负电荷的油脂分子吸引并结合。
肥皂分子由长链烷基和一个带正电荷的极性头部组成。
烷基部分是有机化合物的非极性疏水部分,而极性头部带有正电荷,可以与水中的阴离子相互作用。
这种特殊结构使得肥皂在清洁过程中发挥着重要的作用。
肥皂的去污原理主要包括润湿、分散、乳化、浸透和乳液混合等过程。
首先,在润湿过程中,肥皂分子与水形成复合体,将油污包覆在水中。
然后,肥皂分子的疏水部分与油污分子中的疏水部分相互作用,将油污颗粒分散在水中。
此时,肥皂分子在水中形成胶束结构,其中水分子包围着含油分子。
接下来,肥皂分子的疏水部分与油污分子的疏水部分形成乳化剂,通过降低油脂的表面张力使其分解成小颗粒。
乳化过程中,肥皂分子能够将油污分子封装在其疏水尾部形成的胶团中,将其分散在水中。
同时,肥皂还能通过浸透作用改善去污效果。
肥皂分子可以渗透到油污的内部,与油污分子相互作用,将其与物体表面分离开来。
这种浸透作用可以使油污更容易被水洗走。
最后,乳液混合过程是肥皂的最后一步,它将油污微粒与水混合在一起形成乳状液体。
在这个过程中,肥皂的表面活性剂作用将油污微粒分散在水中,使其变得可溶于水,便于冲洗。
肥皂去污的科学原理是基于表面活性剂的作用机制。
通过肥皂分子与水和油相互作用,将油脂分子分散在水中,然后再通过浸透和乳化作用将油污与物体表面分离。
最终,通过乳液混合作用使油污微粒分散在水中,实现去污的目的。
总结起来,肥皂去污的科学原理是由表面活性剂进行的一系列作用过程,包括润湿、分散、乳化、浸透和乳液混合等步骤。

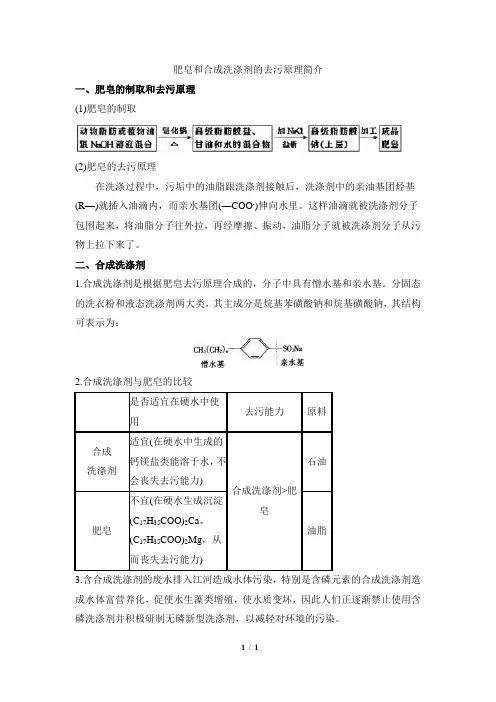
肥皂和合成洗涤剂的去污原理简介
一、肥皂的制取和去污原理
(1)肥皂的制取
(2)肥皂的去污原理
在洗涤过程中,污垢中的油脂跟洗涤剂接触后,洗涤剂中的亲油基团烃基(R—)就插入油滴内,而亲水基团(—COO-)伸向水里。
这样油滴就被洗涤剂分子包围起来,将油脂分子往外拉,再经摩擦、振动,油脂分子就被洗涤剂分子从污物上拉下来了。
二、合成洗涤剂
1.合成洗涤剂是根据肥皂去污原理合成的,分子中具有憎水基和亲水基。
分固态的洗衣粉和液态洗涤剂两大类,其主成分是烷基苯磺酸钠和烷基磺酸钠,其结构可表示为:
2.合成洗涤剂与肥皂的比较
是否适宜在硬水中使
用
去污能力原料
合成洗涤剂适宜(在硬水中生成的
钙镁盐类能溶于水,不
会丧失去污能力)
合成洗涤剂>肥
皂
石油
肥皂不宜(在硬水生成沉淀
(C17H35COO)2Ca、
(C17H35COO)2Mg,从
而丧失去污能力)
油脂
3.含合成洗涤剂的废水排入江河造成水体污染,特别是含磷元素的合成洗涤剂造成水体富营养化,促使水生藻类增殖,使水质变坏,因此人们正逐渐禁止使用含磷洗涤剂并积极研制无磷新型洗涤剂,以减轻对环境的污染。
1/ 1。

肥皂去污的科学原理是什么有很多的人都会用肥皂洗衣服,因为用肥皂洗衣服可以去除污渍。
下面为您精心推荐了肥皂去污的科学原理,希望对您有所帮助。
肥皂去污的原理肥皂是高级脂肪酸的钠盐,它的分子可分为两部分:一部分是极性的羧基,它易溶于水,是亲水而憎油的,叫做亲水基;另一部分是非极性的烃基,它不溶于水而溶于油,是亲油而憎水的,叫做憎水基。
例如:当肥皂溶于水时,在水面上,肥皂分子中亲水的羧基部分倾向于进入水分子中,而憎水的烃基部分则被排斥在水的外面,形成定向排列的肥皂分子。
这种高级脂肪酸盐层的存在,削弱了水表面上水分子与水分子之间的引力,所以肥皂可以强烈地降低水的表面张力,因而是一种表面活性剂。
当肥皂在水中的浓度较低时,肥皂分子是以单分子形式存在的,这些分子聚集在水的表面,即亲水基团进入水中,憎水基团被排斥在水的外面。
当水中肥皂的浓度逐渐增大时,水的表面上聚集的肥皂分子逐渐增多而形成单分子层。
继续增大肥皂的浓度时,由于水的表面已被占满,水溶液内部的肥皂分子中憎水的烃基开始彼此靠范德华力聚集在一起,而亲水的`羧基包裹在外面,形成胶体大小的聚集粒子,称为胶束。
肥皂的胶束呈球形,如图12-2。
形成胶束的最低浓度称为临界胶束浓度。
达到临界胶束浓度时,水的表面已被占满,水的表面张力降至最低。
超过了临界胶束浓度,再增大水中肥皂的浓度,只能增加溶液中胶束的数量。
在洗涤衣物时,肥皂分子中憎水的烃基部分就溶解进入油污内,而亲水的羧基部分则伸在油污外面的水中,油污被肥皂分子包围形成稳定的乳浊液。
通过机械搓揉和水的冲刷,油污等污物就脱离附着物分散成更小的乳浊液滴进入水中,随水漂洗而离去。
这就是肥皂的洗涤原理,如图12-3所示。
在临界胶束浓度前后,去污能力与肥皂的浓度有很大的关系:低于临界胶束浓度,去污能力随肥皂的浓度的下降而急剧下降;超过临界胶束浓度,去污能力几乎不能随肥皂的浓度而改变。
其他的洗涤剂也是如此。
肥皂虽然具有优良的洗涤作用,但也还有一些缺点。

![[课外阅读]肥皂的成分种类和去污原理](https://uimg.taocdn.com/adda4e123c1ec5da51e27011.webp)
[课外阅读]肥皂的成分种类和去污原理成分主要成分都是硬脂酸钠,其分子式是C17H35COONa(也可以写成RCOONa,由氢氧化钠和碱合油脂发生反应产生)。
如果在里面加进香料和染料,就做成既有颜色,又有香味的香皂了;如果往里面加点药物(如硼酸或石碳酸),它就变成药皂了。
种类肥皂的用途很广,除了大家熟悉的用来洗衣服之外,还广泛地用于纺织工业。
通常以高级脂肪酸的钠盐用得最多,一般叫做硬肥皂;其钾盐叫做软肥皂,多用于洗发刮脸等。
其铵盐则常用来做雪花膏。
根据肥皂的成分,从脂肪酸部分来考虑,饱和度大的脂肪酸所制得的肥皂比较硬;反之,不饱和度较大的脂肪酸所制得的肥皂比较软。
肥皂的主要原料是熔点较高的油脂。
从碳链长短来考虑,一般说来,脂肪酸的碳链太短,所做成的肥皂在水中溶解度太大;碳链太长,则溶解度太小。
因此,只有C10~C20的脂肪酸钾盐或钠盐才适于做肥皂,实际上,肥皂中含C16~C18脂肪酸的钠盐为最多。
肥皂中通常还含有大量的水。
在成品中加入香料、染料及其他填充剂后,即得各种肥皂。
普通使用的黄色洗衣皂,一般掺有松香,松香是以钠盐的形式而加入的,其目的是增加肥皂的溶解度和多起泡沫,并且作为填充剂也比较便宜。
白色洗衣皂则加入碳酸钠和水玻璃(有含量可达12%),一般洗衣皂的成分中约含30%的水分。
如果,把白色洗衣皂干燥后切成薄片,即得皂片,用以洗高级织物。
在肥皂中加入适量的苯酚和甲酚的混合物(防腐,杀菌)或硼酸即得药皂。
香皂需要比较高级的原料,例如,用牛油或棕榈油与椰子油混用,制得的肥皂,弄碎,干燥至含水量约为10~15%,再加入香料、染料后,压制成型即得。
液体的钾肥皂常用作洗发水等,通常是以椰子油为原料制得的。
肥皂,通常分为硬皂、软皂和过脂皂3种。
如果在肥皂中加入某些药物,那就成为药皂了,如硫磺皂、檀香皂等。
硬皂即常说的“臭肥皂”,它含碱量高,去油去污能力强,但对皮肤也有较大的刺激性,反复使用时可使皮肤很快发生干燥、粗糙、脱皮等现象。
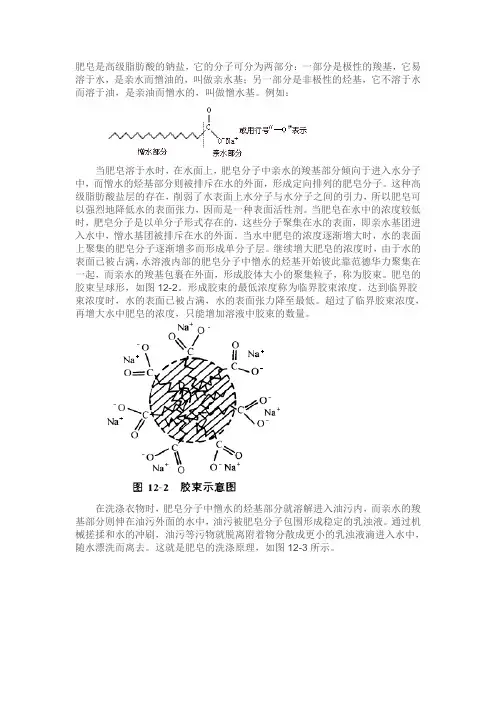
肥皂是高级脂肪酸的钠盐,它的分子可分为两部分:一部分是极性的羧基,它易溶于水,是亲水而憎油的,叫做亲水基;另一部分是非极性的烃基,它不溶于水而溶于油,是亲油而憎水的,叫做憎水基。
例如:当肥皂溶于水时,在水面上,肥皂分子中亲水的羧基部分倾向于进入水分子中,而憎水的烃基部分则被排斥在水的外面,形成定向排列的肥皂分子。
这种高级脂肪酸盐层的存在,削弱了水表面上水分子与水分子之间的引力,所以肥皂可以强烈地降低水的表面张力,因而是一种表面活性剂。
当肥皂在水中的浓度较低时,肥皂分子是以单分子形式存在的,这些分子聚集在水的表面,即亲水基团进入水中,憎水基团被排斥在水的外面。
当水中肥皂的浓度逐渐增大时,水的表面上聚集的肥皂分子逐渐增多而形成单分子层。
继续增大肥皂的浓度时,由于水的表面已被占满,水溶液内部的肥皂分子中憎水的烃基开始彼此靠范德华力聚集在一起,而亲水的羧基包裹在外面,形成胶体大小的聚集粒子,称为胶束。
肥皂的胶束呈球形,如图12-2。
形成胶束的最低浓度称为临界胶束浓度。
达到临界胶束浓度时,水的表面已被占满,水的表面张力降至最低。
超过了临界胶束浓度,再增大水中肥皂的浓度,只能增加溶液中胶束的数量。
在洗涤衣物时,肥皂分子中憎水的烃基部分就溶解进入油污内,而亲水的羧基部分则伸在油污外面的水中,油污被肥皂分子包围形成稳定的乳浊液。
通过机械搓揉和水的冲刷,油污等污物就脱离附着物分散成更小的乳浊液滴进入水中,随水漂洗而离去。
这就是肥皂的洗涤原理,如图12-3所示。
在临界胶束浓度前后,去污能力与肥皂的浓度有很大的关系:低于临界胶束浓度,去污能力随肥皂的浓度的下降而急剧下降;超过临界胶束浓度,去污能力几乎不能随肥皂的浓度而改变。
其他的洗涤剂也是如此。
肥皂虽然具有优良的洗涤作用,但也还有一些缺点。
例如,肥皂不宜在酸性或硬水中使用,因在酸性水中能形成难溶于水的脂肪酸,而在硬水中能生成不溶于水的脂肪酸钙盐和镁盐。
这样不仅浪费肥皂,而且去污能力也大大降低。

肥皂去污原理及注意事项
肥皂的去污原理是利用其表面活性剂的特性。
肥皂分子中含有一个亲水的极性头和一个疏水的非极性尾部。
在水中,肥皂分子形成胶束结构,头部朝向水分子,尾部聚集在一起。
当肥皂与油污或脏物接触时,尾部会吸附在油脂表面,而头部则与水结合。
这样,肥皂将油脂包裹在胶束中,使其悬浮在水中,并通过机械搅拌使其分散和溶解。
随后,肥皂和水一起冲洗,将含有污垢的肥皂从物体表面带走,达到清洁的效果。
注意事项:
1. 不可过度使用肥皂,因为过多的肥皂可能会残留在物体表面,难以清洗干净,可能会导致油脂堆积或刺激皮肤。
2. 在使用肥皂清洁某些特殊材料或物体时,要先测试其对肥皂的耐受性,以免造成损伤。
3. 清洗后要彻底冲洗,以确保肥皂残留物完全冲洗干净,避免留下污渍。
4. 即使使用肥皂清洗,也要避免使用过于粗糙的刷子或磨擦物体的方法,以免划伤或损坏物体表面。
5. 对于特别油腻或顽固的污渍,可以使用刷子或清洁剂配合肥皂清洗,但要注意使用时的安全和适当的配比。
6. 定期清洗肥皂容器和清洁工具,以免细菌或污垢滋生。


肥皂的制作及其原理一、实验目的:肥皂是必不可少的日常生活用品,肥皂到底是什么?如何制取肥皂?通过本实验即得到解决。
二、实验原理:油脂的主要成分是高级脂肪酸的甘油酯,油脂在碱性条件下水解生成肥皂的主要成分——高级脂肪酸的钠盐。
如:这种反应类型称之为皂化。
如果往里面加点药物(如硼酸或石炭酸),它就变成药皂了;肥皂包括洗衣皂、香皂、金属皂、液体皂,肥皂中除含高级脂肪酸盐外,还含有松香、水玻璃(硅酸钠)、香料、染料等填充剂。
过程:经皂化、盐析、过滤、洗涤、整理成型后,称为皂基,再继续加工而成为不同商品形式的肥皂。
三、制造过程和方法1、实验仪器:烧杯、量筒、蒸发皿、玻璃棒、酒精灯、铁圈、铁架台、火柴。
2、实验药品:植物油或动物油、乙醇、40%氢氧化钠溶液、氯化钠饱和溶液、蒸馏水。
3、实验步骤:A、在一干燥的蒸发皿中加入6g植物油、5ml乙醇和10ml 40%氢氧化钠溶液。
B、在搅拌下,给蒸发皿中的液体微微加热,加热过程中加入乙醇与水混合液(1:1),直到混合物变稠。
C、继续加热,直到把一滴混合物加到水中时,在液体表面不再形成油滴为止。
D、把盛有混合物的蒸发皿放在冷水中冷却,然后加入150ml氯化钠饱和溶液,充分搅拌。
这一步分离方法叫做盐析。
E、向其中加入1-2滴香料,用定性滤纸滤出固态物质,弃去含有甘油的溶液,把固态物质挤干,并把它压制成型,晾干,即制成肥皂。
4、制作过程中应注意的事项(1)油脂不易溶于碱水,加入乙醇为的是增加油脂在碱液中的溶解度,乙醇的高挥发性将水分快速带出,加快皂化反应速度。
(2)加热用小火。
(3)皂化反应时,不能让蒸发皿里的混合液蒸干或溅到外面。
四、去污原理肥皂分子结构可以分成二个部分。
一端是带电荷呈极性的—COO—(亲水部位) ,另一端为非极性的碳链R—(亲油部位)。
肥皂能破坏水的表面张力,当肥皂分子进入水中时,具有极性的亲水部位,会破坏水分子间的吸引力而使水的表面张力降低,使水分子平均地分配在待清洗的衣物或皮肤表面。
肥皂去污原因探究学校:青岛智荣中学北校班级:九年级三班学生姓名:孙茗指导老师:赵业肥皂去污原因探究【摘要】肥皂的分子结构一端是带电荷呈极性的亲水基,另一端是非极性的憎水基。
憎水基具有亲油的特性,在水与油污的界面上,深入油污,与油脂分子结合在一起,使油脂乳化,让油脂溶于肥皂水中。
亲水基具有亲水的特性,会破坏水分子间的吸引力而使水的表面张力降低,伸在油滴外面,插入水中。
油污形成非常微小的油污颗粒后被许多亲水基包围着分散并悬浮于水中形成乳浊液,经过重复多次摩擦振动,油污就会被轻易地冲洗干净。
【关键词】肥皂起源发展形成去污原理影响因素去污比较肥皂是大家每天都用的一种洗涤用品,它能很快把我们衣服上的脏东西带走、把我们的手洗的干干净净,真是太神奇了!为什么肥皂有如此大的功效呢?带着这样的疑问,我查阅了大量的资料,以期用化学知识解开自己心中的迷惑。
一、肥皂的起源传说肥皂是在罗马一个叫SAPO的山下河流里洗衣服的女人们发现的。
这些女人发现,若是在某个特定的时间、特定的地点洗衣服,会洗的比平时更加干净。
究其原因,这是由于在山丘上神殿燃烧祭品处,当地人把羊作为祭品放在灶台上烧烤来举行仪式,烧烤时流出来的油脂又滴落到下面燃烧过的草木灰上,油脂和草木灰的混合物跟雨水一起流入了河中,形成了液体肥皂。
所以肥皂的名字SOAP 的由来就是源自这个山丘SAPO的名字。
流入河流的羊脂和草木灰(碱性),其实就是制成肥皂的两种基本物质。
还有一个传说肥皂的发明者是地中海东岸的腓尼基人。
在公元前7世纪古埃及的一个皇宫里,一个腓尼基厨师不小心把一罐食用油打翻在地,他非常害怕,赶快趁别人还没发现时用灶炉里的草木灰撒在上面,然后再把这些混合浸透了油脂的草木灰用手捧出去扔掉了。
望着自己满手的油腻,他想:这么脏的手,不知道要洗到什么时候才能洗干净啊?他一边犹豫着一边把手放到了水中。
奇迹出现了:他只是轻轻地搓了几下,那满手的油腻就很容易地洗掉了,甚至连原来一直难以洗掉的老污垢也随之被洗掉了。
肥皂和合成洗涤剂1.制肥皂的流程注意当用NaOH溶液反应时,最终得到的是钠肥皂,又称硬肥皂;当用KOH溶液反应时,最终得到的是钾肥皂,又称软肥皂。
2.肥皂的去污原理肥皂的主要成分是高级脂肪酸钠盐。
从结构上看,它的分子可以分为两部分,一部分是极性的—COONa(或—COO-),易溶于水,是亲水基;另一部分是非极性的烃基—R,易溶于油,不溶于水,是憎水基。
其去污原理如图4-1-1所示,在水分子和外力作用下完成去污。
图4-1-13.肥皂和合成洗涤剂去污能力比较合成洗涤剂是根据肥皂的去污原理合成的分子中具有亲水基和憎水基的物质,其结构如图4-1-2所示。
图4-1-2合成洗涤剂分为固态的洗衣粉和液态的洗涤剂等。
其主要成分是烷基苯磺酸钠或烷基磺酸钠等。
(1)肥皂和合成洗涤剂去污的相同点二者都存在亲水基、憎水基两部分,分别位于分子的两端。
在洗涤时,亲水基溶于水中,憎水基则插入油污中,在水和外力作用下完成去污过程。
(2)肥皂和合成洗涤剂去污的不同点①合成洗涤剂具有去污能力强、原料廉价易得(主要原料是石油)、不受水质的影响等优点,并且适合洗衣机使用。
②制造肥皂的主要原料是油脂,原料相对合成洗涤剂的原料——石油来说比较昂贵。
且肥皂不适合在硬水中使用,硬水中含有较多的Ca2+、Mg2+,肥皂中的高级脂肪酸根离子容易结合水中的Ca2+、Mg2+而生成沉淀,使去污能力降低,如2C17H35COO-+Ca2+→(C17H35COO)Ca↓。
2名师提醒盐析在肥皂制备过程中加入食盐细粒的目的是发生盐析,这样可降低高级脂肪酸钠在水中的溶解度,使其析出。
而盐析是一个可逆的物理过程,即盐析后得到的高级脂肪酸钠在水中能重新溶解。
典例详析例1下列关于皂化反应的说法错误的是A.油脂经皂化反应后,生成的高级脂肪酸钠、甘油和水形成混合液B.加入食盐可以使高级脂肪酸钠析出,这一过程叫盐析C.向皂化反应后的混合溶液中加入食盐并搅拌,静置一段时间,溶液分成上下两层,下层是高级脂肪酸钠D.皂化反应后的混合溶液中加入食盐,可以通过过滤的方法分离提纯解析◆油脂在碱性溶液的作用下发生的水解反应,叫皂化反应,生成的高级脂肪酸钠、甘油都溶于水,故能形成混合液,A项正确;加食盐细粒可降低高级脂肪酸钠在水中的溶解度而使其析出,这一过程叫做盐析,B项正确;盐析后,上层是密度较小的高级脂肪酸钠,下层是甘油和食盐的混合液,C项错误;加入食盐后,高级脂肪酸钠析出,可用过滤的方法分离提纯,D项正确。
肥皂去污的作用原理是
肥皂去污的作用原理是通过其含有的表面活性剂分子,使油脂和污垢的颗粒悬浮在水中,从而实现去除的效果。
肥皂主要包含有两种类型的分子:亲水性和疏水性部分。
亲水性部分可以与水分子相互作用,而疏水性部分则可以与油脂和污垢相互作用。
当将肥皂与水混合时,肥皂分子会在水中形成一个薄薄的膜,使亲水性部分与水分子相连,而疏水性部分则朝向水外。
当涉及到油脂或污垢时,肥皂的疏水性部分会与其分子相互作用,使其成为一个胶状物质。
这使得油脂和污垢的颗粒能够从表面上解离,并悬浮在水中。
此外,肥皂的表面活性剂分子能够降低液体表面的表面张力,使水分子更容易进入油脂和污垢之间的间隙。
这加速了肥皂与污垢的接触并去除。
化学初三上鲁教版-肥皂去污的秘密
衣服脏了,一般只要浸在水里,擦点肥皂搓搓,然后用清水洗一洗就干净了。
为什么用水和肥皂就可以去污呢?
因为普通的肥皂,它的主要成分是高级脂肪酸的钠盐和钾盐。
这些盐的分子,一部分能溶于水,叫“亲水基”;另一部分却不溶于水,而溶于油,叫“亲油基”。
当肥皂分子与油污分子相遇的时候,肥皂的亲水基溶于水,而亲油基那么溶于油中,肥皂分子因为既有亲水又有亲油的两重性,所以就能使原来互不相溶的油和水联系起来。
油污等物被肥皂分子和水分子包围后,它们与衣服纤维间的附着力减小,一经搓洗,肥皂液就渗入不等量的空气,生成了大量泡沫。
泡沫表面好像有一层紧张的薄膜,它既扩增了肥皂液的表面积,又使肥皂液更具有收缩力,通常把这种液面的收缩力叫做表面张力。
在表面张力的作用下,衣服所沾有的油污灰尘等微粒,就容易脱离衣物,随水而去,这就是肥皂能去污的秘密。