微生物菌种使用记录
- 格式:doc
- 大小:30.00 KB
- 文档页数:1

微生物实验用菌种管理规程(ISO13485-2016/YYT0287-2017)1.0目的规范微生物学检定用菌种的管理,最大限度降低变异率,确保菌种的溯源性与稳定性,从而确保微生物学检验结果的准确可靠。
2.0适用范围适用于微生物实验用菌种管理,包括菌种的申购、传代、使用及销毁等。
3.0引用/参考文件ChP2015实用药品微生物检验检测技术指南4.0职责质量控制实验室负责菌种的申购、传代、使用、销毁等工作,QA负责监控和参与OOS调查。
5.0程序5.1术语和定义5.1.1标准菌株由中国药品生物制品检定所医学微生物菌种保藏管理中心或者其他经认可的机构提供的冷冻干燥菌。
5.1.2传代菌株用标准菌种制备的采用特定保存方法长期固定保存的菌种,用于传代及制备工作用菌种,3代后的传代菌株在需要时可以作为工作菌株使用。
5.1.3工作菌株用标准菌种或传代用菌种接种至普通琼脂斜面培养后,作为日常工作使用的菌种。
5.1.4菌种的代将菌种接种至一新鲜培养基上或培养基内,每萌发一次即称为一代,从菌种保藏中心获得的冷冻干燥菌种为第0代。
5.2菌种来源5.2.1标准菌株由中国药品生物制品检定所医学菌种保藏中心(CMCC)或者其他经认可的机构提供的冷冻干燥菌种。
5.2.2质量控制实验室涉及到的菌种种类、代码、保存方法及保存条件如下。
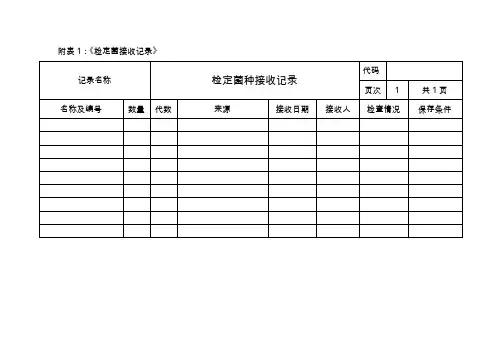
菌种名称菌种代码保存方法保存温度保存期限TSA斜面2~8℃1个月金黄色葡萄球菌CMCC(B)26003冷冻干燥管-20℃1年TSA斜面2~8℃1个月铜绿假单胞菌CMCC(B)10104冷冻干燥管-20℃1年TSA斜面2~8℃1个月枯草芽孢杆菌CMCC(B)63501冷冻干燥管-20℃1年SDA斜面2~8℃3个月白色念珠菌CMCC(F)98001冷冻干燥管-20℃1年SDA斜面2~8℃3个月黑曲霉菌CMCC(F)98003冷冻干燥管-20℃1年TSA斜面2~8℃1个月生孢梭菌CMCC(B)64941冷冻干燥管-20℃1年5.3菌种的申购、验收、保存5.3.1菌种的申购5.3.1.1微生物室QC依据菌种的库存及菌种的使用情况,提出采购申请,申请需明确菌种的名称,标准编号以及申购数量等信息。
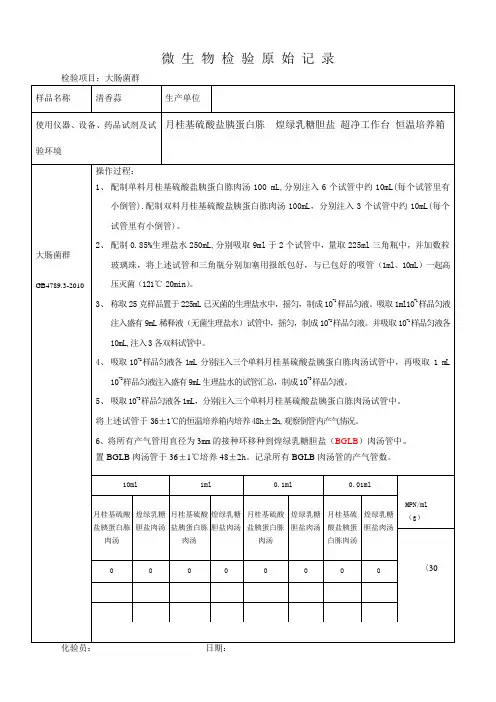
微生物检验原始记录检验项目:大肠菌群样品名称清香蒜生产单位使用仪器、设备、药品试剂及试验环境月桂基硫酸盐胰蛋白胨煌绿乳糖胆盐超净工作台恒温培养箱大肠菌群GB4789.3-2010操作过程:1、配制单料月桂基硫酸盐胰蛋白胨肉汤100 mL,分别注入6个试管中约10mL(每个试管里有小倒管).配制双料月桂基硫酸盐胰蛋白胨肉汤100mL,分别注入3个试管中约10mL(每个试管里有小倒管)。
2、配制0.85%生理盐水250mL,分别吸取9ml于2个试管中,量取225ml三角瓶中,并加数粒玻璃珠,将上述试管和三角瓶分别加塞用报纸包好,与已包好的吸管(1ml、10mL)一起高压灭菌(121℃ 20min)。
3、称取25克样品置于225mL已灭菌的生理盐水中,摇匀,制成10-1样品匀液。
吸取1ml10-1样品匀液注入盛有9mL稀释液(无菌生理盐水)试管中,摇匀,制成10-2样品匀液。
并吸取10-1样品匀液各10mL,注入3各双料试管中。
4、吸取10-2样品匀液各1mL分别注入三个单料月桂基硫酸盐胰蛋白胨肉汤试管中,再吸取1 mL10-2样品匀液注入盛有9mL生理盐水的试管汇总,制成10-3样品匀液。
5、吸取10-3样品匀液各1mL,分别注入三个单料月桂基硫酸盐胰蛋白胨肉汤试管中。
将上述试管于36±1℃的恒温培养箱内培养48h±2h,观察倒管内产气情况。
6、将所有产气管用直径为3mm的接种环移种到煌绿乳糖胆盐(BGLB)肉汤管中。
置BGLB肉汤管于36±1℃培养48±2h。
记录所有BGLB肉汤管的产气管数。
10ml 1ml 0.1ml 0.01ml月桂基硫酸盐胰蛋白胨肉汤煌绿乳糖胆盐肉汤月桂基硫酸盐胰蛋白胨肉汤煌绿乳糖胆盐肉汤月桂基硫酸盐胰蛋白胨肉汤煌绿乳糖胆盐肉汤月桂基硫酸盐胰蛋白胨肉汤煌绿乳糖胆盐肉汤MPN/ml(g)〈300 0 0 0 0 0 0 0化验员:日期:。
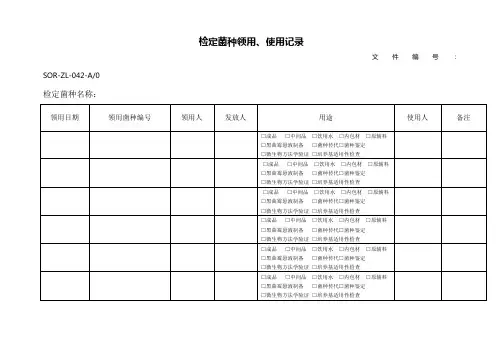


检定菌灭活记录范文菌灭活是指通过使用物理或化学手段,成功地消灭细菌的过程。
检定菌灭活记录是指记录菌灭活的过程和结果,以确保菌灭活操作的有效性和可靠性。
以下是一份1200字以上的检定菌灭活记录样本:实验目的:本实验旨在检定菌灭活操作的有效性,以确保在实际应用中能够成功地灭活细菌。
实验材料:1.菌株:使用大肠杆菌作为实验对象。
2.配制好的菌液:使用LB培养基培养得到的大肠杆菌菌液。
3.菌灭活剂:使用酒精和紫外线作为菌灭活剂。
实验步骤:1.菌株培养:将大肠杆菌菌株接种到含有LB培养基的琼脂平板上,进行培养,使菌株生长至指定密度。
2.菌液配制:从琼脂平板上挑取菌落,转移到含有LB培养基的离心管中,经培养,使菌株生长至指定浓度。
在此过程中,严格控制培养条件,确保菌株的生长状态一致性。
3.菌液分装:将培养好的菌液分装到多个离心管中,使每个离心管中的菌液量保持一致。
4.菌灭活剂处理:a.酒精处理:将一部分分装好的菌液加入含有70%酒精的离心管中,轻轻摇匀。
b.紫外线处理:将另一部分分装好的菌液暴露于紫外线灯下,暴露时间为10分钟。
c.对照组:将剩余的菌液分装到离心管中,作为对照组。
5.菌液培养:将各组的菌液分别接种到含有LB培养基的琼脂平板上,进行培养,培养时间为24小时。
6.菌落计数:计算各组菌落的数量,以评估菌灭活效果。
实验结果:在菌液培养后,对照组的琼脂平板上出现了大量的菌落,菌落数较多。
而经过酒精处理的菌液所培养的琼脂平板上,菌落数量明显减少。
经紫外线处理的菌液所培养的琼脂平板上,几乎没有菌落生长。
讨论与结论:通过本实验的菌灭活操作,成功地使用酒精和紫外线灭活了大肠杆菌。
酒精处理能够有效地减少菌落的数量,但并不能完全灭活细菌。
而紫外线处理的菌液几乎没有出现菌落生长,表明紫外线对细菌有较好的灭活效果。
因此,在实际应用中,可以根据灭菌要求选择合适的菌灭活剂和操作方式,以确保菌液的安全性。
总结:菌灭活操作是一项重要的实验步骤,能够有效地减少菌落的数量,确保实验或应用中的细菌的安全性。
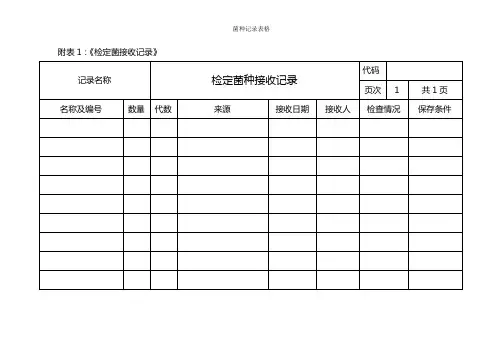
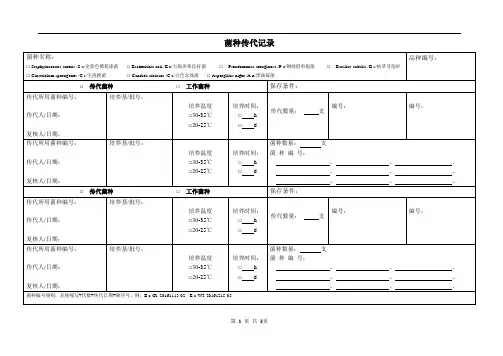

沉香化滞丸微生物限度方法学验证及报告1、供试品检品名称:沉香化滞丸规格:6g/袋×10袋/盒产品批号:1304230 1304240 1304210生产单位:河南爱民药业集团股份有限公司检验依据:《中国药典》2010年版一部2、微生物限度验证所用菌种大肠埃希菌〔CMCC(B)44102〕枯草芽孢杆菌〔CMCC(B)63501〕白色念球菌〔CMCC(F) 98001〕金黄色葡萄球菌〔CMCC(B)26003〕3、方法:《中国药典》2010年版一部微生物限度检查中薄膜过滤法验证(附录XⅢC)3.1菌液制备(1) 取经37℃培养18~24h,金黄色葡萄球菌、大肠埃希菌、枯草杆菌的营养肉汤培养物1ml+9ml0.9%盐水,10倍稀释至10-5~10-7,细菌数约为50~100cfu/ml,做活菌计数备用。
(2) 经25 ℃培养18~24小时的白色念珠菌霉菌液体培养物1ml +9ml0.9%盐水10倍稀释至10-5~10-7,菌数约为50~100cfu/ml,做活菌计数备用。
3.2结果见表1、表2表1 细菌计数结果菌种大肠埃希菌(10-7)金黄色葡萄球菌(10-6)枯草芽孢杆菌(10-5)计数(CFU)72 76 85 91 76 78均值(CFU)74 88 77表2 霉菌计数结果菌种白色念球菌(10-5)计数(CFU)69 71均值(CFU)704、供试液的制备4.1取供试品10g,置研钵中研细,慢慢加入45℃PH7.0无菌氯化钠-蛋白胨缓冲液至100ml,边加边搅拌,作为1:10的供试液,分别人工污染上述四种代表试验菌株。
5、回收率测定:5.1试验组取1ml 1:10供试液,分别加入含菌数为50~100cfu的试验菌1ml,分别注入平皿中,立即倾入营养琼脂培养基(细菌)与玫瑰红钠培养基(霉菌),细菌:33℃培养72小时,霉菌、酵母菌:26℃培养120小时。
5.2菌液组取含菌数为50~100cfu的试验菌各1ml,分别注入平皿中,立即倾入营养琼脂培养基(细菌)与玫瑰红钠培养基(霉菌),细菌:33℃培养72小时,霉菌、酵母菌:26℃培养120小时。

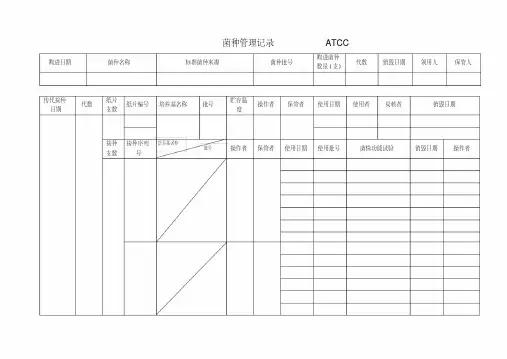
菌种记录及管理
【原创版】
目录
1.菌种记录的重要性
2.菌种管理的方法
3.菌种记录和管理的实际应用
正文
菌种记录及管理对于微生物学研究和应用具有重要意义。
无论是在实验室研究还是在工业生产中,对菌种的准确记录和管理都是保证实验结果和产品质量的关键环节。
首先,菌种记录的重要性体现在以下几个方面:
1.保证实验结果的可重复性:科研工作中,一个重要的要求就是实验结果的可重复性。
详尽的菌种记录可以帮助研究者准确地重复实验过程,避免因为菌种差异导致的实验结果的差异。
2.便于菌种的筛选和优化:对于微生物的筛选和优化,需要对不同菌种进行详细的比较和分析。
详尽的菌种记录可以提供丰富的菌种信息,方便研究者进行菌种筛选和优化。
3.有助于菌种的保存和管理:对于一些具有重要研究价值或者应用前景的菌种,需要进行长期保存。
详尽的菌种记录可以帮助研究者更好地了解菌种的特性,进行有效的保存和管理。
然后,菌种管理的方法主要包括以下几个方面:
1.建立菌种库:对于实验室或企业来说,可以建立专门的菌种库,对菌种进行集中保存和管理。
2.采用信息化管理:通过建立数据库,将菌种的信息进行电子化管理,既方便查询,也便于统计分析。
3.定期检查和更新:对于保存的菌种,需要定期进行检查和更新,以保证菌种的活性和纯度。
最后,菌种记录和管理的实际应用主要体现在以下几个方面:
1.在科研工作中,通过详尽的菌种记录和管理,可以提高实验效率,保证实验结果的可靠性。
2.在工业生产中,通过菌种记录和管理,可以保证产品的质量,提高生产的效率。
微生物检验原始记录受理编号检()号第页/共页检验依据GB15979—2002 《一次性使用卫生用品卫生标准》一、实验器材1. 试验菌株名称:金黄色葡萄球菌,菌株号:ATCC6538,培养代数代,琼脂斜面培养基培养,培养条件:2. 试剂及培养基配制、灭菌见《试剂及培养基配制记录C》:第1次;第2次;第3次。
3.二级生物安全柜:编号C 。
4.恒温水浴箱:编号。
5. 恒温培养箱:编号。
6.秒表:编号7.样品名称:。
有效成份:,含量:,批号:。
二、方法1. 操作步骤:按GB15979—2002 附录C4溶出性抗(抑)菌产品抑菌性能试验方法操作程序进行. 受理编号:检()号第页/共页2. 实验条件三、结果1. 第1次试验对金黄色葡萄球菌的抑菌效果作用时间接种稀释倍数平皿生长菌数菌药管菌数抑菌率(min)(cfu/皿)(cfu/mL)(%) 251020阳性对照:接种稀释倍数:平皿生长菌数: cfu/皿菌液浓度: cfu/mL。
阴性对照:阴性对照:菌生长。
2. 第2次试验对金黄色葡萄球菌的抑菌效果作用时间接种稀释倍数平皿生长菌数菌药管菌数抑菌率(min)(cfu/皿)(cfu/mL)(%) 251020阳性对照:接种稀释倍数:平皿生长菌数: cfu/皿菌液浓度: cfu/mL。
阴性对照:阴性对照:菌生长。
3. 第3次试验对金黄色葡萄球菌的抑菌效果作用时间接种稀释倍数平皿生长菌数菌药管菌数抑菌率(min)(cfu/皿)(cfu/mL)(%) 251020阳性对照:接种稀释倍数:平皿生长菌数: cfu/皿菌液浓度: cfu/mL。
阴性对照:阴性对照:菌生长。
4. 结果处理: 三次试验平均结果对金黄色葡萄球菌的抑菌效果作用时间 菌药管菌数 抑菌率 (min ) (cfu/mL ) (%) 251020阳性对照:菌液浓度: cfu/mL 。
阴性对照: 菌生长。
5.计算公式:(1)接种稀释倍数=(V1/V2)×A/B= (5.0/0.5)×A/0.5=20A式中V1为接种管(PBS4.5mL+菌药混合液0.5mL )液体体积;V2为接种管中菌药混合液体积(0.5mL );A 为接种前中和管液体稀释倍数;B 接种样液体积(0.5mL )。
菌种证实记录怎么写范文菌种证实记录怎么写范文1. 引言菌种证实记录是在微生物学领域中非常重要的一项工作,它记录了对某种菌株的鉴定和确认过程。
这个过程涉及到多个步骤和技术,同时需要遵循严格的实验室规范和标准。
本文将从深度和广度两个方面,对菌种证实记录的撰写范文进行全面评估,并为读者提供有价值的信息。
2. 菌种证实记录的深度探讨2.1 背景介绍菌种证实记录的第一步是对所研究的菌株进行背景介绍。
在这一部分,需要提供菌株的命名、来源、保存地点以及相关的参考文献。
还要对菌株的特征进行描述,包括形态学特征、生理特性和生化特性等。
这些信息将为后续的鉴定和确认提供基础。
2.2 鉴定方法接下来,菌种证实记录应该详细描述使用的鉴定方法。
常用的鉴定方法包括形态学观察、生理特性测试、16S rRNA基因测序等。
在描述过程中,应该注明每个步骤的操作流程和所使用的试剂、仪器设备等。
还需要提供相应的实验数据和结果分析,以便读者对鉴定过程有全面的了解。
2.3 验证和确认在鉴定完成后,需要对菌株进行验证和确认。
这一步骤主要通过进一步的实验和分析,以确保菌株的准确性和可靠性。
在证实记录中,应该记录验证实验的设计、方法和结果,以及对结果进行的解释和分析。
如果使用了其他鉴定方法或参考菌株进行比较分析,也需要进行描述和讨论。
3. 菌种证实记录的广度探讨3.1 研究意义对菌种进行证实记录的目的是为了确保研究的可靠性和科学性。
通过对菌株的鉴定和确认,可以减少结果的误差和偏差,同时也有助于促进学术交流和科技进步。
在菌种证实记录中,应该强调研究的意义和价值,以及对相关领域的贡献。
3.2 实验可行性和可重复性菌种证实记录应该详细描述实验的可行性和可重复性,以确保其他实验室或研究者可以重现和验证实验结果。
在这一部分,需要提供实验操作的详细步骤和条件,同时注明可能遇到的问题和解决方法。
还可以讨论实验的局限性和改进方向,以推动该领域的进一步研究。
4. 个人观点和理解菌种证实记录是微生物学领域中非常重要的一项工作,对于保证实验结果的准确性和可靠性起着关键作用。