临床试验立项送审材料清单【模板】
- 格式:docx
- 大小:21.66 KB
- 文档页数:3
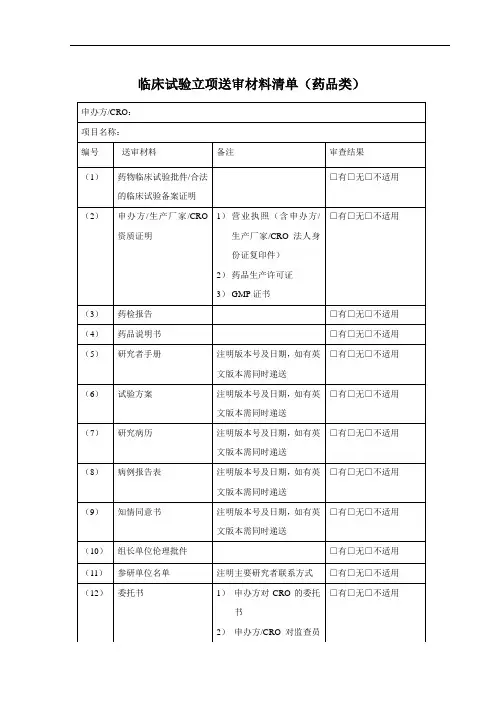

临床实验项目送审文件清单一、初始审查(.最新文件下载:请前往伦理委员会资料公共邮箱:,密码:(因后期可能的调整,实时以伦理办公室告知为准)。
或登陆萍乡市人民医院官方网站:。
公共邮箱有模板的请用医院模板,无模板的请用公司模板。
.送审文件需按清单顺序装订成册(注意:份伦理存档完整版资料装订成册后(建议:塑料蛇夹)使用适宜大小蓝色塑料档案盒(推荐:“高尚牌”大中号盒)装好。
份主审委员审查完整版资料及其他简装版资料使用文件夹、抽杆夹等都可),不接受未装订在一起的零散资料。
完整电子版资料同步发至伦理邮箱()。
. 申办方重要资料(伦理递交信及医院提供模板的申请报告等除外)首页需盖申办方或被授权的公司公章,研究方案、知情同意书还需加盖骑缝章)。
、初始审查申请·药物临床实验序号文件名机构项目形式审查综合意见表初始审查申请(主要研究者签名并注明日期)(客观填写主要研究者承担在研项目数)主要研究者简历(注意信息更新,签名和日期)研究人员职责分工表(附所有研究者的最新(近年)培训证书复印件)研究经济利益声明(主要研究者)伦理递交信和交接清单(所有资料的版本号及日期必须标明)国家食品药品监督管理总局临床实验批件或药品注册批件组长单位伦理批件其他伦理委员会对申请研究项目的重要决定临床研究方案(签字盖章并注明版本号版本日期(含本院主要研究者签字,其他相关人员签名))向受试者提供的知情同意书(①注明版本号版本日期;②涉及研究单位相关内容置换为萍乡市人民医院内容)(为最新知情同意书主版本)(联系方式中伦理信息填写模板:伦理联系人:童老师,伦理委员会联系电话:)。
其他需提供给受试者的材料(如用于招募受试者的广告(注明版本号版本日期)、招募方式说明、受试者日记卡和其他问卷表等)保险合同研究者手册、药品说明书(实验药、对照药、基础用药、辅助用药、合并用药等药品)研究病历和或病例报告表()申办者资质证明(营业执照、药品生产许可证、证书等,均加盖红印章))申办者委托的委托书及三证,委托书(均加盖红印章);简历、培训证书及身份证复印件。

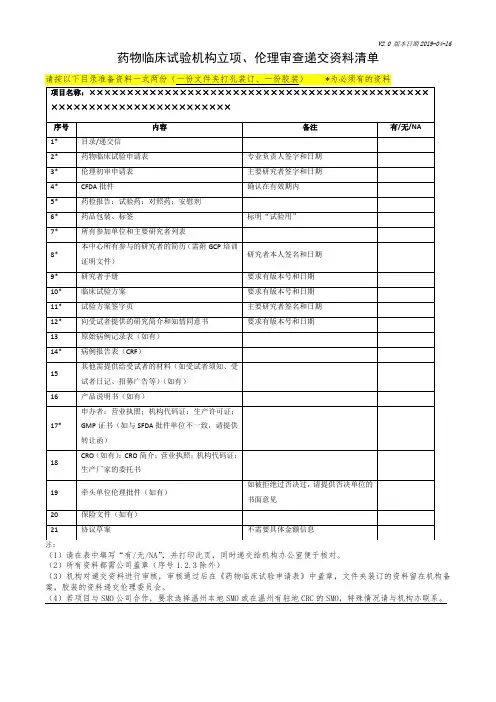
药物临床试验机构立项提交资料清单一、注意事项:1.机构立项资料递交信仅收取一份原件。
2.立项材料整体的第一页及每一部分的首页均要盖章,整体盖骑缝章。
如项目是CRO承担的,CRO的章也可以,但注明盖申办方原章的除外,不接受盖章后的彩色打印件。
3.《立项申请表》、《临床试验信息表》及《药物临床试验专业方案审核意见表及质量承诺书》在提交立项资料时一并递交,仅收取各一份原件由提交人盖章,此三份文件请勿列在立项资料目录中。
4.如递交立项资料目录中没有列出的文件,也需在文件上盖章,2页及2页以上的文件需盖齐缝章。
5.文件资料请用黑色、厚壳、双孔快劳夹装订,文件夹侧标使用统一的模板(应包含:院内项目编号、方案编号、项目名称、申办方名称、研究专业、主要研究者、批件号),模板参见附件1。
6.文件夹第一页均为《文件目录》,每项文件中间用带数字标识的隔页纸分隔。
7.请按立项申请表文件目录所列文件顺序排列各项文件,如提交《立项资料目录》中未列出的文件,请在立项申请表目录中补充完整。
文件夹中不包括的文件无需列入目录。
8.文件多的项目请准备多个“机构文件夹”,编号“①,②,③……”。
9.请在接待日,由负责项目监查的CRA将文件夹递交到机构办公室。
10.递交纸版文件资料的之前请发送一份填写完整的电子版立项文件至到机构办邮箱:(******)),立项及之后的内次备案资料均要求电子版资料内容与纸质版保持一致。
11.如立项时已有CRC的项目,请准备SMO公司资质证明、CRC中文版个人简历(并包括该CRC在我院所负责的所有项目名称、承担专业、项目院内编号、CRC 的联系电话和邮箱)至机构备案登记。
12.如在项目进行过程中更换监查员,请及时通知机构办,并递交人员变更通知函、新任监查员委托书/函、新任监查员GCP培训证书进行备案登记。


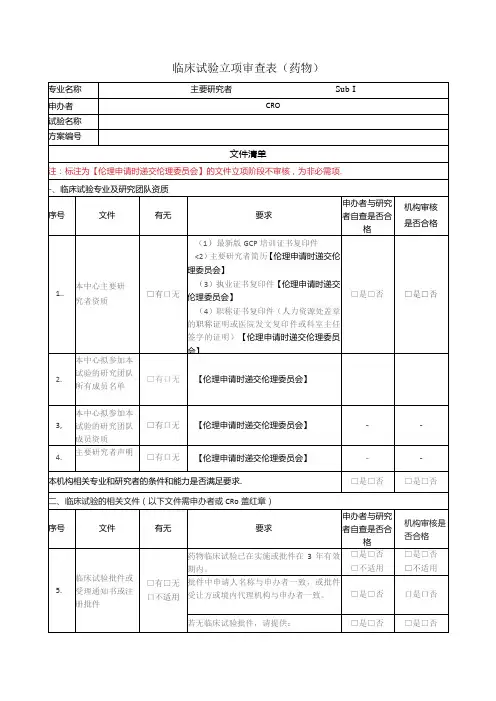

临床研究项目审批材料清单以下是临床研究项目审批材料清单的内容:
一、申请表格
1.项目申请表
2.研究计划书
二、研究团队相关材料
1.研究团队成员名单及简历
2.单位授权委托书(如适用)
3.研究团队相关资格证书复印件
三、研究协议相关材料
1.合作研究协议书
2.试验执行机构委托书(如适用)
四、研究用药材料
1.药品生产批件复印件及药物说明书
2.产品信息、药物生产工艺及质量标准文件
五、数据管理与分析材料
1.数据管理操作流程及数据管理方案
2.相关数据管理软件及工具介绍
3.数据安全与保密措施说明
六、伦理审批材料
1.伦理委员会批件复印件及研究伦理概述
2.被试者知情同意书及知情同意书模板
3.受试者退出首先同意书及退出同意书模板
七、招募材料
1.受试者招募启示及招募广告材料
2.受试者筛选、入组、排除标准及程序介绍
八、研究用具材料
1.研究用具清单及购置渠道证明
2.研究用具操作手册及标准化流程介绍
九、预算及资金管理材料
1.研究经费预算及使用计划
2.项目经费拨付与支持机构证明
十、其他附件
1.研究相关的文献资料、参考资料及证明文件
2.研究中出现的不良事件、事故和其他重大变化情况的报告
以上是临床研究项目审批材料清单的内容。
根据具体项目的需求,可能会有一些细微的变化,但总的来说,这个清单提供了一个全面和具体的指导,帮助项目研究者准备齐全的审批所需材料,确保临床研究项目的顺利进行。

26 申办方/CRO营业执照□是□否
27 申办方对CRO的委托书或协议(如有)□是□否
28 申办方/CRO对CRA的委托书□是□否
□是□否29 CRA的派遣函、身份证复印件、学历证书、个人简历、GCP证
书等
30 无需办理“人类遗传资源审批申请书”承诺书(如适用)□是□否
31 方案讨论会的会议纪要□是□否31 其他与立项审查相关的材料□是□否
□是□否32 提供给受试者的文件,如调查问卷病、受试者日记卡等(如
适用)
备注:
1、以上所有材料需加盖红章,一式两份;装订要求:每一小
项放在一份文件保护袋中,再按照目录顺序要求放入三孔
文件夹中,用索引纸分开(参考如下:齐心TC530AB 文
件夹A4打孔夹背宽40mm 1.5寸3孔O型档案夹,蓝
色天猫
+%BF%D7+o%D0%CD%BC%D0+%C6%EB%D0%C4 。
3孔O
型夹齐心蓝色)。
2、将电子档或扫描件发邮箱:.。

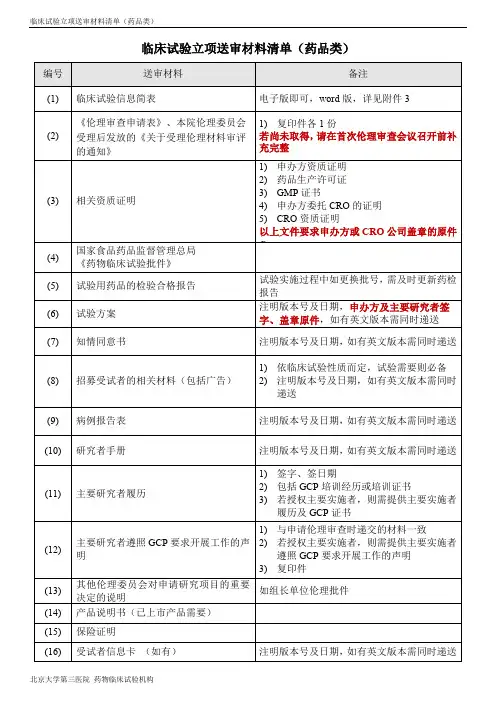
临床试验立项递交资料清单(一)药物临床试验1. 递交文件目录(含所递交文件的清单,注明所用提交文件的版本号或日期)2. 临床试验评估表和立项申请表(下载区);3. 临床试验项目委托书;4. 国家食品药品监督管理总局(CFDA)药物临床试验批件;5. 组长单位伦理委员会批件(除本中心为组长单位免提供);6. 其他伦理委员会的批件或对申请研究项目的重要决定的说明,应提供以前否定结论的理由(如有请提供);7. 临床试验方案及其修正案(注明版本号及日期,外文资料的中文版,方案封面:各试验中心PI签名及日期);8. 知情同意书(注明版本号及日期,外文资料的中文版);9. 病例报告表(注明版本号及日期);10. 研究病历(注明版本号及日期);11. 研究者手册;12. 试验药物质检报告(必须加盖药品生产厂家红章);13.临床前实验室资料;14.试验用药品标签;15. 研究者履历表及相关文件(PI签名及日期);16. 申办方的资质证明(营业执照、生产许可证、GMP证书,税务登记证,组织机构代码证等复印件);17.CRO及SMO公司资质证明(如有);18. 监查员和CRC的法人委托书,身份证复印件,学历证明、GCP 培训证书及个人研究简历;19. 其他试验相关文件提供资料(如受试者须知、受试者日记卡、研究问卷表、招募广告、保险声明等)。
备注:1、以上所有材料需加盖红章,一式两份;装订要求:每一小项放在一份文件保护袋中,再按照目录顺序要求放入三孔文件夹中,用索引纸分开(参考如下:齐心TC530AB 文件夹A4打孔夹背宽40mm 1.5寸3孔O型档案夹,蓝色天猫+%BF%D7+o%D0%CD%BC%D0+%C6%EB%D0%C4 。
3孔O型夹齐心蓝色)。
2、将电子档或扫描件发邮箱:.。
医疗器械临床试验初始审查伦理送审文件清单
1.医疗器械临床试验立项申请表
2.伦理审查申请表、初次审查意见表(研究者PI签字)
3.研究者PI履历(含GCP最新培训证书复印件,首次承担项目的同时递交医师资格证、执业证复印件)
4.研究成员名单及分工表(研究者PI签字确认)
5.NMPA批件,如果适用(2014年6月起高风险器械适用)
6.申办者的资质证明(营业执照,医疗器械生产许可证等)
7.CRO、SMO的资质证明和委托书
8.国家指定检测机构出具的检验报告
9.自测报告
10.产品的注册产品标准或相应的国家、行业标准
11.临床试验方案和修订版(注明版本号和日期,申办者和研究者PI双方签字)
12.知情同意书及其更新件(注明版本号和日期),包含受试者补偿信息,如补偿方式、数额和计划
13.招募受试者的方式和信息,如广告和宣传册等(注明版本号和日期)14.病例报告表(CRF)(注明版本号和日期)
15.原始病历或研究病历等(注明版本号和日期),如果有
16.研究者手册(注明版本号和日期)
17.现有的安全性资料
18.动物试验报告(首次用于植入人体的医疗器械)
19.申办者资料真实性声明
20.保险证明
21.其他需要审查的资料,如患者日记、患者卡片等受试者相关资料。