药品批发企业GSP认证现场检查项目和检查办法
- 格式:doc
- 大小:142.50 KB
- 文档页数:9
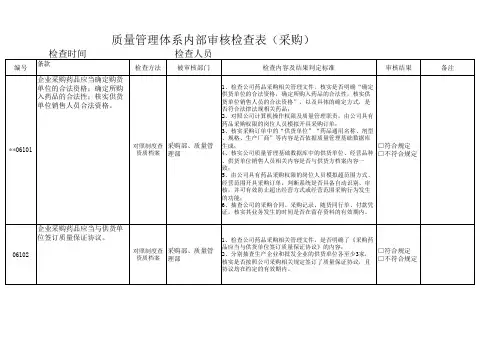
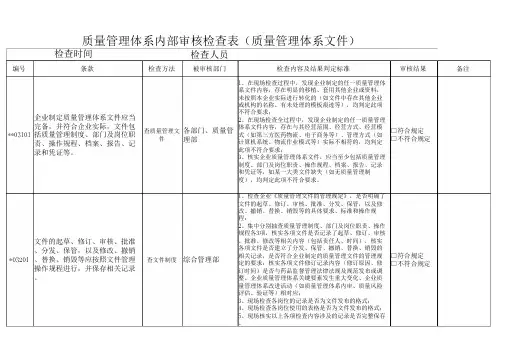
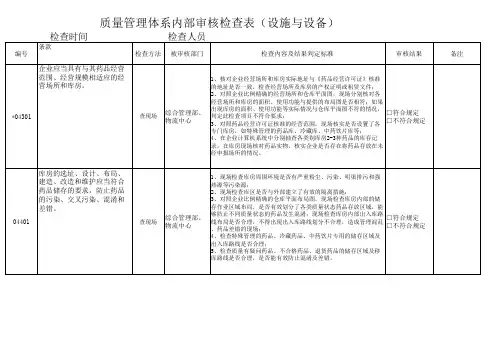
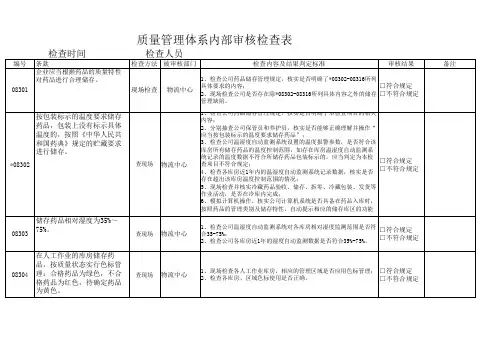
质量管理体系内部审核检查表(质量管理体系文件)检查时间编号条款检查方法检查人员被审核部门检查内容及结果判定标准审核结果备注1、在现场检查过程中,发现企业制定的任一质量管理体系文件内容,存在明显的移植、套用其他企业或资料,未按照本企业实际进行转化的(如文件中存在其他企业或机构的名称、有未处理的模板痕迹等),均判定此项不符合要求;2、在现场检查全过程中,发现企业制定的任一质量管理体系文件内容,存在与其经营范围、经营方式、经营模□符合规定式(如第三方医药物流、电子商务等)、管理方式(如□不符合规定计算机系统、物流作业模式等)实际不相符的,均判定此项不符合要求;3、核实企业质量管理体系文件,应当至少包括质量管理制度、部门及岗位职责、操作规程、档案、报告、记录和凭证等,如某一大类文件缺失(如无质量管理制度),均判定此项不符合要求。
1、检查企业《质量管理文件的管理规定》,是否明确了文件的起草、修订、审核、批准、分发、保管,以及修改、撤销、替换、销毁等的具体要求、标准和操作规程;2、集中分别抽查质量管理制度、部门及岗位职责、操作规程各3项,核实各项文件是否记录了起草、修订、审核、批准、修改等相关内容(包括责任人、时间),核实各项文件是否建立了分发、保管、撤销、替换、销毁的相关记录,是否符合企业制定的质量管理文件的管理规□符合规定定的要求:核实各项文件修订记录内容(修订原因、修□不符合规定订时间)是否与药品监督管理法律法规及规范发布或调整、企业质量管理体系关键要素发生重大变化、企业质量管理体系改进活动(如质量管理体系内审、质量风险评估、验证等)相对应;3、现场检查各岗位的记录是否为文件发布的格式;4、现场检查各岗位使用的表格是否为文件发布的格式;5、现场核实以上各项检查内容涉及的记录是否完整保存。
企业制定质量管理体系文件应当完备,并符合企业实际,文件包**03101括质量管理制度、部门及岗位职责、操作规程、档案、报告、记录和凭证等。
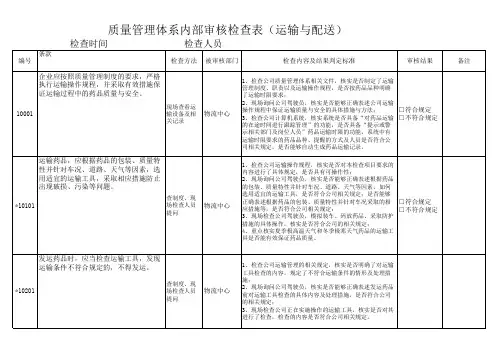
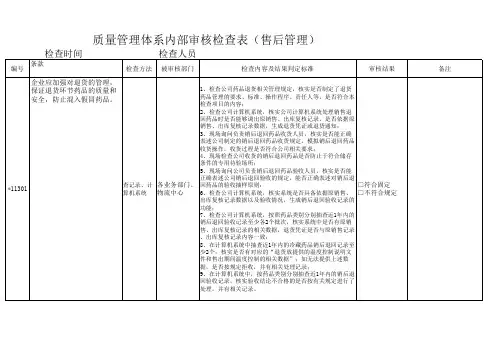

新版GSP认证检查评定标准及检查项目分第一篇:新版GSP认证检查评定标准及检查项目分GSP认证检查项目分析及实施指导新版GSP认证检查评定标准及检查项目分析第一节新版GSP认证现场检查项目分析一、药品批发企业及零售连锁企业(一)管理职责条款检查项目分析 1.经营方式:主要有批发经营、零售连锁经营、零售企业 0401 批发经营主要有下列三种:1)批发企业:法人批发企业2)非法人批发企业:一般为法人批发企业的分公司 3)非法人批发(配送)企业 2.经营范围:饮片药品中药材生化药品化学原料药抗生素中成药生物制品中药放射性化学药制剂诊断药品特殊管理药品注:√为零售企业不能经营的范围。
1.企业质量领导组织机构图 0501 质量领导组织质量管理机构进货储存销售运输其它2.质量领导组织:类似于立法机构;质量管理机构:类似于执法机构;其它:类似于监督对象;质量领导组织以主要负责人为首,由各部门负责人组成,广泛代表,整体体现,确保制度管理有效,可行,GSP认证检查项目分析及实施指导符合企业实际。
明确了企业质量领导组织的主要职责。
此条款中一些术语为采用 0502 ISO9000 质量管理体系的标准术语:质量:一般固有特征满足需要的程度。
质量管理体系:在质量方面指挥和控制组织的管理体系。
质量方针:由组织的最高管理者正式发布的总的质量宗旨和方向。
企业领导人:为法人或授权的总经理。
1.质量管理机构下设: 0601 1)质量管理组 0611 2)质量验收组不隶属于其他部门:3)药品检验室:不做要求,企业自主决定是否设置。
2.质量管理机构职能0602—内部监督职能0603—起草,提交质量领导小组审定通过,质管监督执行 0604—审批(首营企业和首营品种)0608—所有工作在质量监督下进行 0609—裁决权体现 0610—信息管理0611—教育和培训养护人员:技术水平、工作内容、强度0701 药品养护人员必须为专职,不得兼职。
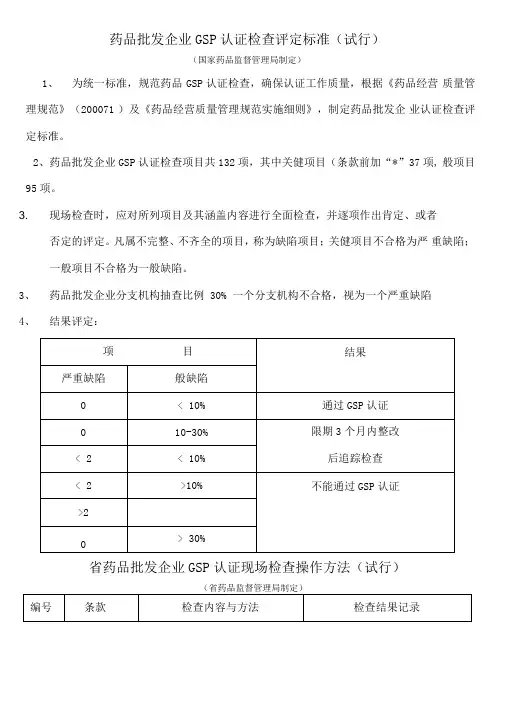
药品批发企业GSP认证检查评定标准(试行)(国家药品监督管理局制定)1、为统一标准,规范药品GSP认证检查,确保认证工作质量,根据《药品经营质量管理规范》(200071 )及《药品经营质量管理规范实施细则》,制定药品批发企业认证检查评定标准。
2、药品批发企业GSP认证检查项目共132项,其中关健项目(条款前加“*”37项, 般项目95项。
3. 现场检查时,应对所列项目及其涵盖内容进行全面检查,并逐项作出肯定、或者否定的评定。
凡属不完整、不齐全的项目,称为缺陷项目;关健项目不合格为严重缺陷;一般项目不合格为一般缺陷。
3、药品批发企业分支机构抽查比例 30% 一个分支机构不合格,视为一个严重缺陷4、结果评定:省药品批发企业GSP认证现场检查操作方法(试行)(省药品监督管理局制定)0 5口叫合士口 纟 条53告的 定 规 合 符 有 应•</ 口 否 □‘ 是 册注 品 口 进芯规 合 符 不 品、 O药少预口;应P#应质印口书口品有进件于 节件单原 进告进制应品印材复文货构 纟报;物品制复药药少准供机和验件生制物口件批原理少检印性液生件 进批上盖管。
证品复防血纟批进纟材以加量章O种5中装包 有 否 是包 有 应 片 饮 药 OO口否□‘ 是量是芯规 合 符 否 是 识 标 装 包 件 每每•</ 志标 的 格 合 量•</ 口 否 口,是产各品是装2>产各 品 明 标 材期日 货 发O种规合各品是装品饮 文K 实沖药泌准伽搴咖中灯批产期管和W明生『I材在标。
各生施药戌应号与条本5品杳检E)z(\库 品记标 收 验 样 抽 箱 开 有 否 是有否是品-5 3•</ 口 否 口,是品按否 是 定 判a,方样 抽O种是员 收 验否口是O口095好做 应 品 药 收 验否 是 录、1•</口否口,是•</ 范规 整 完品单货 供 载 记 应是录2O个货到 駐 数整完 否 是 容 内 录 记 收 验剂 各 品 期 日台一合 三否口是准 LL ft 规 刑4 且•</ 口生、 号 LL ft 、 号 文 有项缺#:品个几有如►HU贝否名品 □> 期 日 货 到 、量数号LL ft、型剂□>。

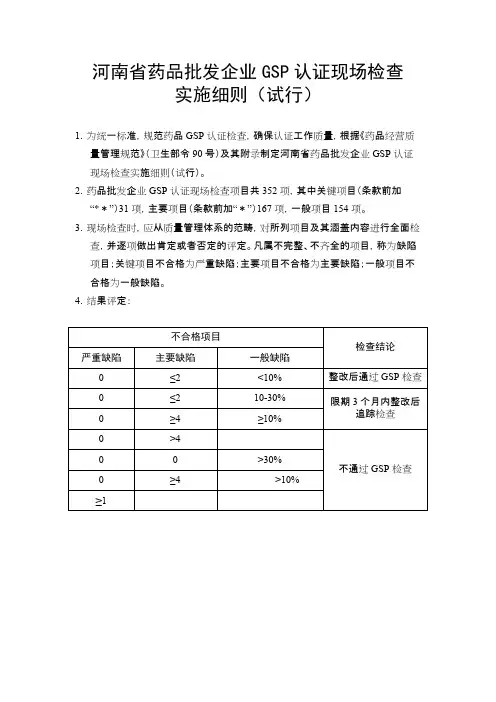
河南省药品批发企业GSP认证现场检查实施细则(试行)1.为统一标准,规范药品GSP认证检查,确保认证工作质量,根据《药品经营质量管理规范》(卫生部令90号)及其附录制定河南省药品批发企业GSP认证现场检查实施细则(试行)。
2.药品批发企业GSP认证现场检查项目共352项,其中关键项目(条款前加“**”)31项,主要项目(条款前加“*”)167项,一般项目154项。
3.现场检查时,应从质量管理体系的范畴,对所列项目及其涵盖内容进行全面检查,并逐项做出肯定或者否定的评定。
凡属不完整、不齐全的项目,称为缺陷项目;关键项目不合格为严重缺陷;主要项目不合格为主要缺陷;一般项目不合格为一般缺陷。
4.结果评定:不合格项目严重缺陷主要缺陷一般缺陷检查结论0≤2<10%整改后通过GSP检查0≤210-30% 0≥4≥10%限期3个月内整改后追踪检查0>400>30%0≥4>10%≥1不通过GSP检查药品批发企业GSP认证现场检查项目序号项目号检查内容1**00401企业应按依法批准的经营方式和经营范围从事药品经营活动,并应坚持诚实守信、依法经营,禁止任何虚假欺骗行为。
2**00501企业应当依据有关法律法规及《药品经营质量管理规范》(以下简称《规范》)的要求建立质量管理体系。
300502企业应当确定质量方针。
400503制定质量体系管理文件,开展质量策划、质量控制、质量保证、质量改进、质量风险管理等活动。
500601质量方针文件应明确企业总的质量目标和要求,并贯彻到药品经营活动的全过程。
6*00701企业所建立的质量管理体系应与其经营范围和经营规模相适应,包括组织机构、人员、设施设备、质量管理体系文件及相应的计算机系统等。
7*00801企业应当定期以及在质量管理体系关键要素发生重大变化时,组织开展内审。
800901企业应当对内审的情况进行分析,依据分析结论制定相应的质量管理体系改进措施,不断提高质量控制水平,保证质量管理体系持续有效运行。

药品批发企业换发和变更《药品经营许可证》《药品经营质量管理规范认证证书》现场检查项目 序号条款 检查内容 评定细则 1 **00401 药品经营企业应按依法批准的内容从事药品经营活动。
1、检查药品经营许可证、营业执照、其他文件所载项目是否与实际情况相符。
2、不得有挂靠、过票等行为。
3、检查药品实际经营活动(发票、账本、记录、在库药品) 2 **00402 药品经营企业应当坚持诚实守信,禁止任何虚假、欺骗行为。
1、企业有无不诚实守信的行为(如谎报资料、仓库、人员资质)。
2、不得有法律、法规等规定应进行处罚的虚假行为。
3*00501 企业应当依据有关法律法规及本规范的要求建立质量管理体系。
1、查建立的质量管理组织机构、员工花名册。
2、查质量管理组织机构框架图。
3、查企业质量 4 00502 企业应当制定质量管理体系文件,开展质量策划、质量控制、质量保证、质量改进和质量风险管理等活动。
1、查企业制定的质量管理体系文件。
2、质量策划、质量控制、质量保证、质量改进和质量风险管理等活动应在质量体系过程中体现出来。
5 00601 企业应当确定质量方针,制定的质量方针文件应当明确企业总的质量目标和要求,并贯彻到药品经营活动的全过程。
1、查企业正式的质量方针文件,文件内容中应明确企业总的质量目标和要求。
2、查企业制定的相关职能和部门质量目标、岗位质量目标等;质量目标应是定量、具体、可操作。
3、查企业人员均应知晓和理解质量方针。
4、查质量方针培训记录,质量目标的检查、评价记录等。
6 00701企业质量管理体系应当与其经营范围和规模相适应,质量管理体系应当包括组织机构、人员、设施设备、质量管理体系文件及相应的计算机系统等。
1、查是否按00501项建立了质量体系。
2、查企业的质量管理体系文件应与企业的经营范围和规模相适应,设置的机构、库房、设施设备、配备的人员、制定的制度规程与记录、计算机系统等应符合本规范及其他法规文件的规定并与企业经营范围和规模相适应。
药品批发企业GSP认证现场检查项目和检查方法1.质量管理体系:检查药品批发企业是否建立了合格的质量管理体系,包括质量方针、质量目标、质量手册和程序文件等,以及是否制定了相关的质量管理制度和标准。
检查方法:查阅质量管理手册、产地检验报告、进货验收记录等相关文件,与现场实际情况进行核对。
2.贮存条件及设备设施:检查药品批发企业的仓库贮存条件和设备设施是否符合药品贮存的要求,包括温湿度控制、通风状况、仓库面积、货架结构等。
检查方法:现场实地考察仓库贮存条件和设备设施,检查温湿度记录、通风系统运行情况以及货架的建设质量等。
3.药品库存管理:检查药品批发企业的库存管理情况,包括苯、丙基(吲哚基)甲酸酯类药品的核对、日常库存清点、药品到期日的监控和处理等。
检查方法:查阅库存记录、药品存放区域的标注情况以及库房内药品的摆放情况。
4.药品储运:检查药品批发企业的储运管理情况,包括药品入库、运输和出库的流程和记录,以及储运容器的清洁、封存和标识等。
检查方法:查阅储运记录、储运容器清洁记录以及收货和发货单据等。
5.药品回收处理:检查药品批发企业的药品回收处理情况,包括过期、残次和变质药品的处理程序和记录。
检查方法:查阅药品回收处理记录、设施和设备使用情况记录等。
6.药品投诉处理:检查药品批发企业的药品投诉处理情况,包括投诉的收集、记录、处理和追溯。
检查方法:查阅药品投诉记录、处理流程和追溯程序等。
7.员工培训:检查药品批发企业的员工培训情况,包括培训计划、培训内容和培训记录等。
检查方法:查阅培训计划和培训记录,与现场员工进行互动,了解培训的实施情况。
以上是药品批发企业GSP认证现场检查项目和检查方法的一些要点,具体的检查内容和方法还会根据不同的药品批发企业的特点和实际情况进行调整和补充。
药品批发企业GSP认证现场检查项目和检查方法GSP(药品经营质量管理规范)认证是指药品批发企业按照国家和地方相关规定,对药品经营质量管理的合规性进行评估和认证的过程。
现场检查是GSP认证的重要环节之一,通过对企业现场设施、操作流程以及文档管理等方面的检查,评估企业的GSP执行情况。
下面是药品批发企业GSP认证现场检查的项目和检查方法的详细介绍:1.设施管理:现场检查项目包括仓库面积和环境、货架及存储设备、温湿度控制设备等。
检查方法主要包括现场实地考察和设施文件查验,评估企业的仓储设施是否能够满足药品质量管理的要求。
检查人员应通过查阅企业的设备清单、保养计划、温湿度记录等文件,了解企业的设备管理情况。
2.药品采购与验收:现场检查项目包括采购流程、采购记录和验收过程。
检查方法主要包括现场实地考察和文件查验,评估企业的采购和验收管理情况。
检查人员应通过查阅企业的采购记录、交货单、验收记录等文件,了解企业的采购和验收管理流程是否合规。
3.药品存储与配送:现场检查项目包括药品存储条件、保质期管理和配送流程。
检查方法主要包括现场实地考察和文件查验,评估企业的存储和配送管理情况。
检查人员应通过查阅企业的温湿度记录、库存管理记录、配送单等文件,了解企业的存储和配送管理流程是否符合GSP的要求。
4.质量管理体系:现场检查项目包括质量管理文件、内部培训和不良品管理。
检查方法主要包括文件查验和员工访谈,评估企业的质量管理体系是否完善有效。
检查人员应通过查阅企业的质量手册、工作指导书、培训记录等文件,了解企业的质量管理体系是否符合GSP的要求。
5.药品追溯体系:现场检查项目包括药品追溯系统的建立和使用情况。
检查方法主要包括文件查验和系统演示,评估企业的药品追溯体系是否健全。
检查人员应通过查阅企业的追溯文件和记录,以及对追溯系统的操作演示,了解企业的追溯体系是否符合GSP的要求。
在现场检查过程中,检查人员应按照相关的检查项目和方法,有针对性地查阅企业的文件和记录,实地考察企业的设施和操作流程,并对企业的合规性进行评估。