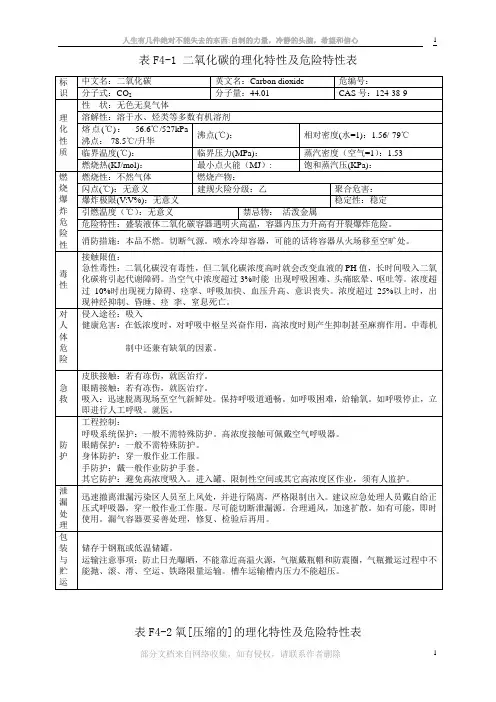
CO2密度对照表
- 格式:xls
- 大小:30.51 KB
- 文档页数:4

co2液体密度
二氧化碳(CO2)液体是一种常见的工业气体,它在许多应用中都有重要的作用。
CO2液体密度是了解其物理特性的关键指标之一。
在标准大气压下(101.325 kPa),CO2的液态密度约为1.98 g/mL。
这意味着每升CO2液体重约为1.98千克。
当温度降低时,CO2液体密度也会增加。
例如,在-20℃时,CO2的液态密度约为1.196 g/mL。
CO2液体密度的变化对其在许多应用中的使用和储存都有影响。
例如,当CO2用于制冷和冷冻时,需要确保其密度足够高以保持较低的温度。
另一方面,如果CO2液体密度过高,可能会导致在储存和运输过程中出现安全问题。
因此,在使用CO2液体时,必须考虑其密度和温度的相互作用。
总之,CO2液体密度是了解CO2物理特性的重要指标之一。
它对CO2在许多应用中的使用和储存都有重要的影响。
- 1 -。

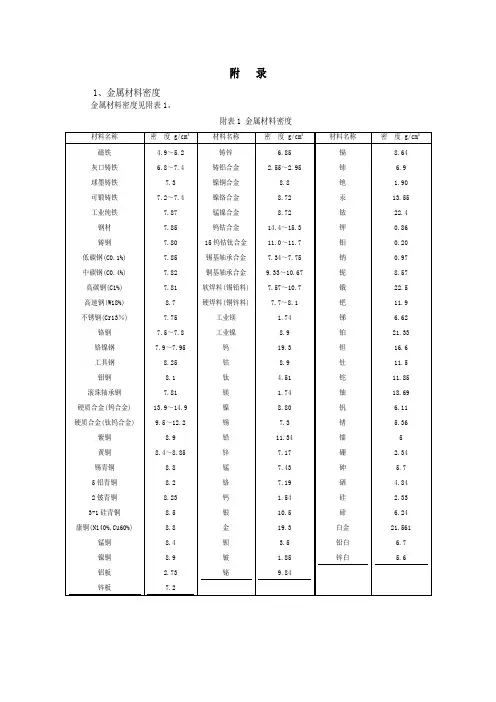
附录1、金属材料密度金属材料密度见附表1。
附表1 金属材料密度2、非金属材料密度非金属材料密度见附表2。
附表2 非金属材料密度3、气体密度气体密度见附表3。
附表3 气体密度注:表中的ρ是干燥气体在0℃和1.01325×10Pa(760mmHg)压力下的密度。
气体对空气的相对密度是假定两者在相同的压力和温度条件下的密度之比。
4、固体线胀系数固体线胀系数见附表4.附表4 固体线胀系数(100℃以下)网筛的目不是法定计量单位,网筛的目与孔直径的米数的换算关系是:1目孔的直径=1.52392 ×10-2mn 2式中:n -为每英寸的目数; m -长度的单位米。
例如,200目网筛的孔的直径尺寸为:200×1.52392 ×10-2m =0.000076196m =0.076196mm ≈0.08mm20025、装配扭矩装配时,应将在同一分组组别内的内、外螺纹进行装配。
螺纹最终的装配扭矩应满足表1要求。
在保证表1规定的扭矩前提下,螺纹可不按分组进行装配。
表1 螺纹装配扭矩值N/m6、旋合长度 GB/T 1181-1998所规定的螺纹公差仅适用于旋合长度符合表2规定的过盈配合螺纹。
对旋合长度过长或过短的过盈配合螺纹,为满足GB/T 1181-1998规定的装配扭矩要求,需适当地调整螺纹公差。
本表摘自GB/T 1181-1998。
7、摩擦系数(见表3)螺纹牙侧表面间的摩擦系数受材料、表面粗糙度、润滑剂、热处理、表面涂镀、螺纹加工精度(各种形位误差)、螺纹规格等因素影响。
必要时,用户可利用计算公式,对特定条件下的过盈配合螺纹摩擦系数进行验证(已知总过盈量和装配扭矩,求摩擦系数)和调整。

二氧化碳和水的密度摘要:一、二氧化碳与水的密度概述二、二氧化碳与水的密度比较三、实际应用:二氧化碳在水中的溶解与应用四、总结与建议正文:在我们的生活中,二氧化碳和水这两种物质无处不在,它们的密度特性也颇具特点。
接下来,我们将探讨二氧化碳和水的密度,以及其在实际应用中的重要性。
首先,让我们了解一下二氧化碳和水的密度概述。
二氧化碳(CO2)是一种无色、无味、不可燃的气体,在标准大气压下,其密度约为1.98 kg/m。
水(H2O)则是一种透明、无味的液体,密度约为1000 kg/m。
可以看出,二氧化碳的密度远小于水。
其次,我们来比较一下二氧化碳和水的密度。
在常温常压下,二氧化碳的密度是水的密度的一半左右。
这是因为二氧化碳分子质量较小,间隔较大,而水分子质量较大,间隔较小。
因此,在相同体积的情况下,二氧化碳的质量要小于水。
在实际应用中,二氧化碳在水中的溶解与应用非常广泛。
二氧化碳能溶于水,生成碳酸,这是生活中常见的饮料如碳酸饮料、啤酒等的主要成分。
此外,二氧化碳还在工业领域中有广泛应用,如制冷、灭火、制造化学品等。
综上所述,二氧化碳和水的密度差异较大,这使得二氧化碳在水中有广泛的应用。
了解二氧化碳和水的密度,可以帮助我们更好地理解生活中的一些现象,也能为我们的日常生活带来便利。
在日常生活中,我们要善于观察和思考,发现物质之间的相互作用和规律,为我们的生活增添色彩。
最后,给大家提出一些建议。
在日常生活中,我们要节约用水,保护环境,减少二氧化碳的排放。
通过低碳生活,我们可以为地球环境的可持续发展做出贡献。


不同温度co2密度对照表温度(°C)|CO2密度(kg/m³):--: | :--:-50 | 1.687-40 | 1.751-30 | 1.817-20 | 1.885-10 | 1.9560 | 2.0305 | 2.08510 | 2.14020 | 2.25930 | 2.37140 | 2.47850 | 2.57760 | 2.66870 | 2.75080 | 2.82490 | 2.890100 | 2.949CO2密度随着温度的变化有规律可循。
CO2是一种重要的温室气体,其分布以及储存容量与温度的变化是对大气环境的一个重要衡量标准。
根据统计数据,CO2在-50°C气温条件下的密度大约为1.687 kg/m³,随着温度的上升, CO2的密度也会随之变化。
在温度为-40°C时CO2的密度大约为1.751 kg/m³;在温度为-30°C时CO2的密度大约为1.817kg/m³。
当温度降至-20°C时,CO2密度又略有上升,达到1.885 kg/m³。
接着,温度继续提高至十度时,CO2密度已经上升到1.956 kg/m³。
随后,即使温度进一步上升至20°C,CO2的密度也仅为2.259 kg/m³,比上一步的1.956 kg/m³还要少。
在此之后,随着温度进一步提高,CO2的密度也在不断增加,最终在温度为100°C时达到2.949 kg/m³,在此温度条件下CO2的密度已经增加了两倍多。
以上就是CO2密度随着温度变化情况的表示,从上表可以看出,当温度在-50°C及-40°C之间时,CO2的密度变化较为剧烈,而当温度进入20°C以上时,CO2的密度则大大增加。
总之,CO2在不同温度气温条件下的密度大小变化有规律可循,该变化趋势也告诉我们大气环境的状态是如何而受温度变化的影响。

二氧化碳常温密度简介二氧化碳(CO2)是一种无色、无臭的气体,由一个碳原子和两个氧原子组成。
它是地球上最常见的化学元素之一,也是大气层中最重要的温室气体之一。
二氧化碳在常温下存在于三种形态:固态、液态和气态。
物理性质固态二氧化碳固态二氧化碳又称为干冰,是一种在常温下直接从气态转变为固态的物质。
它的密度较高,约为1.56 g/cm³。
固态二氧化碳可以在低于零摄氏度(-78.5℃)的条件下稳定存在,并且会随着温度升高而逐渐转变为气体。
液态二氧化碳液态二氧化碳是通过将二氧化碳压缩到足够高的压力下使其液化得到的。
在常温下,液态二氧化碳具有较高的密度,约为1.98 g/cm³。
液态二氧化碳具有较低的沸点(-78.5℃),因此在大气压力下会迅速蒸发转变为气态。
气态二氧化碳气态二氧化碳是最常见的形态,也是我们通常所说的二氧化碳。
在常温下,二氧化碳以气体形式存在,具有较低的密度,约为1.98 kg/m³。
它是一种无色、无臭的气体,在大气中以分子形式存在。
密度与温度关系二氧化碳的密度与温度密切相关。
一般来说,随着温度升高,二氧化碳的密度会减小;反之,随着温度降低,二氧化碳的密度会增加。
这是因为温度变化会影响分子之间的相互作用力。
在常温下(25℃),二氧化碳的密度约为1.98 kg/m³。
当温度升高到50℃时,密度会降低到约为1.84 kg/m³;而当温度降低到0℃时,密度会增加到约为2.13kg/m³。
可以看出,在常温范围内,随着温度变化,二氧化碳的密度变化不大。
应用领域温室气体二氧化碳是地球上最重要的温室气体之一。
它具有良好的吸热性能,可以吸收地球表面辐射出的红外线辐射,阻止部分热量逸散到太空中,从而维持地球温暖。
然而,由于人类活动导致大量二氧化碳的排放,造成了全球变暖和气候变化等环境问题。
饮料工业二氧化碳在饮料工业中被广泛应用。
在饮料中加入二氧化碳可以增加饮料的口感和口感,并产生起泡效果。

二氧化碳(CO2)相关物理性质
[概要]:
二氧化碳(CO2)相关物理性质
英文名称CARBON DIOXIDE
又名碳酸气
二氧化碳在常温常压下为无色而略带刺鼻气味和微酸味的气体。
17世纪初,比利时化学家J.B.Van. Helmont(1577~1644)在检测木炭燃烧和发酵过程的副产气时,发现CO2是一种与其他气体不同的气体。
1757年,J.Black第一个应用定量的方法研究这种气体,由于它是固定在石灰石中的,所以定名他为“固定空气”。
此后,H.Cavendish和J.Priestley分别研究了“固定空气”的性质。
1773年,voisier把碳放在氧气中加热,得到被它称为“碳酸”的CO2气体,测出质量组成为23.5~28.9%,杨71.1~76。
5%。
1823年,M.Faraday发现。
加压可以使CO2气体液化。
1835年,M.Thilorier制得固态CO2(干冰)。
1884年,在德国建成第一家生产液态CO2的工厂。
在自然界,CO2时最丰富的化学物质之一,为大气的一部分,也包含在某些天然气或油田伴生气中何以碳酸盐形成的矿石中。
大气里含CO2位0.03~0.04%(体积),总量约2.75×1012t,主要由含碳物质燃烧和动物的新陈代谢产生。
在国民经济各部门,CO2有着十分广泛的用途。
工业CO2主要是从合成氨、氢气生产过程中的原料气、发酵气、石灰窑气、酸中和气、乙烯氧化副反应气和烟道气等气体中提取和回收,其纯度不低于99.5%(体积)。
一、分子特性[1-3]见表1
表1。

co2常温下密度二氧化碳(CO2)是一种常见的化学物质,在常温下以气态形式存在。
它是一种无色、无味、无臭的气体,通常被用作工业生产、食品加工、医疗用途以及温室气体的研究等领域。
在这篇文章中,我们将讨论CO2在常温下的密度以及影响密度的因素。
首先,让我们了解一下二氧化碳在常温下的密度是多少。
在标准大气压(1大气压)下,CO2的密度约为1.98千克/立方米。
这意味着在常温下,每立方米的空间中大约有1.98千克的CO2气体。
CO2的密度受到几个因素的影响,其中包括温度、压力和纯度。
首先是温度,当温度升高时,CO2分子的平均动能增加,分子之间的作用力减弱,密度会相应减小。
相反,当温度降低时,CO2分子的平均动能减小,分子之间的作用力增强,密度会相应增加。
其次是压力,压力是指单位面积上的力的作用,通常以大气压(atm)或帕斯卡(Pa)为单位。
在高压下,气体分子会更加密集,导致密度增加;而在低压下,气体分子会更加稀疏,密度减小。
因此,压力的增加会导致CO2的密度增加,压力的减小会导致密度减小。
最后是纯度,纯度是指气体中的CO2分子所占的比例。
如果气体中的其他成分(如氧气、氮气等)增加,CO2的密度会相应减小。
因此,保持CO2气体的纯度对于准确测量其密度是非常重要的。
总的来说,CO2在常温下的密度约为1.98千克/立方米,但这个数值会受到温度、压力和纯度的影响。
了解CO2的密度对于工业生产、环境保护以及气体研究等领域都具有重要意义,因此我们需要对其密度的测量和影响因素有所了解。
希望本文能为您提供有关CO2常温下密度的相关信息。
co2的气体密度CO2的气体密度CO2,即二氧化碳,是一种由碳和氧元素组成的化合物。
它是一种无色、无味并且不可燃的气体。
CO2在自然界中广泛存在,是地球上最重要的温室气体之一。
它的气体密度是多少,这是一个关于CO2的重要问题。
气体密度是指单位体积气体的质量。
对于CO2来说,它的气体密度取决于温度、压力和纯度等因素。
一般情况下,CO2的气体密度约为1.98 kg/m³。
这意味着在标准大气压下,1立方米的CO2气体约重1.98千克。
CO2的气体密度与温度、压力有密切关系。
随着温度的升高,CO2分子的平均动能增加,分子之间的相互作用减弱,气体密度会降低。
相反,随着温度的降低,CO2分子的平均动能减小,分子之间的相互作用增强,气体密度会增加。
在常温常压下,CO2的气体密度约为1.98 kg/m³。
这意味着CO2气体比空气更重,因此可以以气体形式存在于大气中。
在自然界中,CO2以不同形式存在,包括大气中的CO2气体、地下的CO2水合物以及生物体内的CO2。
CO2的气体密度还受到压力的影响。
当压力增加时,CO2分子之间的相互作用增强,气体密度也会增加。
相反,当压力减小时,CO2分子之间的相互作用减弱,气体密度会降低。
除了温度和压力,CO2的气体密度还受到纯度的影响。
纯度越高,CO2分子之间的相互作用越强,气体密度也会增加。
相反,纯度越低,CO2分子之间的相互作用越弱,气体密度会降低。
CO2的气体密度对于许多领域具有重要意义。
在工业上,CO2被广泛用于制冷剂、灭火剂、化学反应中的原料等。
在大气科学中,CO2的气体密度及其变化对研究气候变化和全球变暖等问题具有重要意义。
总结起来,CO2的气体密度约为 1.98 kg/m³。
它受到温度、压力和纯度等因素的影响。
了解CO2的气体密度对于深入理解CO2在自然界中的行为和应用具有重要意义。
希望通过本文的介绍,读者对CO2的气体密度有更深入的了解。
二氧化碳密度表
随着全球气候变化问题日益突出,人们对于二氧化碳(CO2)的关注度也越来越高。
二氧化碳是一种无色、无味的气体,广泛存在于地球大气中。
它是温室气体之一,能够吸收地球表面辐射的一部分并导致大气温度上升,从而引发全球变暖的问题。
二氧化碳的密度是指在特定条件下,单位体积内所含二氧化碳的质量。
一般来说,二氧化碳的密度随着温度和压力的变化而变化。
下面是二氧化碳在不同温度和压力下的密度表:
温度(℃) 压力(atm) 密度(kg/m)
-50 1 1.98
-25 1 1.84
0 1 1.80
25 1 1.84
50 1 1.98
从上表可以看出,二氧化碳的密度受温度的影响较大。
随着温度的升高,二氧化碳的密度逐渐增加。
当温度下降至-50℃时,二氧化碳的密度最大为1.98 kg/m。
而当温度升高至50℃时,二氧化碳的密度同样达到了1.98 kg/m。
此外,二氧化碳的密度还受压力的影响。
一般情况下,二氧化碳的密度随着压力的增加而增加。
在上表中,我们可以看到在1 atm的压力下,二氧化碳的密度在不同温度下变化较小。
了解二氧化碳的密度对于深入研究全球气候变化、开展相关环境保护工作以及工业生产中的气体处理等方面起着重要作用。
通过对二氧化碳的密度变化规律的研究,人们可以更好地掌握气候变化的特征,并寻求相应的应对措施。
需要注意的是,二氧化碳的密度表中所列数值是在特定条件下测量得到的,并可能因实际环境条件的差异而有所变化。
因此,在具体应用中应注意结合实际情况进行计算和判断。