离子符号与化合价
- 格式:docx
- 大小:10.08 KB
- 文档页数:2


离子与化合价的异同离子和化合价是化学教学中的一大重点,也是难点。
在化学教学中,由于离子符号和元素化合价的标法非常相似,学生在学习时容易混淆。
为了使学生能正确书写离子符号和标出元素化合价,现将离子和化合价的异同总结如下:一、相同点离子所带的电荷数与元素化合价在数值上是相等的,离子所带的电荷的正负与元素化合价的正负相一致。
在离子化合物中,元素化合价的数值就是这种元素的一个原子得失电子的数目,化合价的正负与离子所带电荷的正负相一致。
如在氯化纳中,1个纳原子失去1个电子,钠离子带1个单位的正电荷,纳的化合价即为+1价,1个氯原子得到1个电子,氯离子带1个单位的负电荷,氯的化合价即为-1价;在氯化镁中,1个镁原子失去2个电子,镁离子带2个单位的正电荷,镁的化合价就是+2价,而1个氯原子得到1个电子,氯离子带1个单位的负电荷,氯的化合价就是-1价。
在共价化合物中,元素化合价的数值就是这种元素的一个原子与其它元素的原子形成共用电子对的数目。
化合价的正负由电子对的偏移来决定,电子对偏向哪种原子,哪种原子就显负价,偏离哪种原子,哪种原子就显正价。
如在氯化氢中,氯原子和氢原子共用一对电子,电子对偏向氯原子,则氯离子带1个单位的负电荷,氯元素的化合价就是-1价,电子对偏离氢原子,则氢离子带1个单位的正电荷,氢元素的化合价就是+1价。
二、不同点离子是指带电的原子或原子团,而化合价是指一种元素一定数目的原子和其它元素一定数目的原子相化合的性质,在书写离子符号和标元素化合价时,有许多不同之处:(1)离子带的电荷数与元素化合价所标的位置不一样:写离子符号时,离子所带的电荷数应标在元素符号的右上角,如Ba2+、O2- 而元素化合在元素符号的正上方,如、。
(2)数值与“+”、“-”的前后顺序不一样:在写离子符号时,数值在前,符号“+”、“-”在后,而标元素化合价时,符号“+”、“-”在前,数值在后。
(3)有关“1”是否省略的问题:在离子符号的书写中,若原子带1个单位的电荷,则在书写离子符号时,则只标出“+”、“-”,“1”省略不写,如纳离子Na+、Cl-;而在标元素化合价时,“1”则不能省略,如纳无素的化合价是+1价,则写为,氯元素的化合价是-1价,则写为。

铵根离子的符号和化合价【摘要】铵根离子是一种带正电荷的化学离子,在化学反应中起着重要作用。
它的符号是NH4+,化合价为+1。
铵根离子由氮原子和四个氢原子组成,具有很强的亲电性,可以与许多物质发生反应。
在生活中,铵根离子常用于肥料和清洁剂中。
其结构简单紧凑,具有稳定性。
物理性质上,铵根离子易溶于水,且具有一定的导电性。
通过对铵根离子的研究可以更深入地理解其作用机制,未来的研究将有望发现更多其在化学和生物领域的应用。
对铵根离子的认识与理解有助于拓展其在不同领域的应用,为相关领域的发展贡献新的可能性。
【关键词】铵根离子,符号,化合价,组成,性质,化学反应,应用,生活,结构,特点,物理性质,认识,理解,研究,展望1. 引言1.1 铵根离子的符号和化合价铵根离子是一种由氮原子和氢原子组成的多原子离子,其符号为NH4+。
在化合价方面,铵根离子氮原子上的价电子数为5,氢原子上的价电子数为1,因此铵根离子的总价电子数为5+4*1=9。
根据电子亏损原则,氮原子在铵根离子中会失去一个电子,形成+1的正电荷,而氢原子每个都会失去一个电子,也会形成正电荷,因此铵根离子的总电荷为+1。
对于化合价来说,铵根离子中氮原子的化合价为+3,而每个氢原子的化合价为+1。
铵根离子中氮原子与每个氢原子形成离子键,使得铵根离子整体呈现+1的电荷。
铵根离子在化学反应中起着重要作用,可以参与多种离子反应和有机反应。
在生活中,铵根离子也存在于许多化合物中,如铵盐、氨基酸等。
在结构上,铵根离子呈现出特殊的分子结构,具有一定的稳定性。
在物理性质上,铵根离子通常是固体或液体,具有一定的熔点和沸点。
通过对铵根离子的符号、化合价等方面的认识,我们可以更好地理解它在化学和生活中的应用和作用,为未来对铵根离子的研究提供更多的可能性。
2. 正文2.1 铵根离子的组成和性质铵根离子是由一个氮原子和若干个氢原子组成的离子。
它的化学式为NH4+,其中氮原子带正电荷,四个氢原子带负电荷。


离子符号、化合价例1、用化学符号表示:①3个硫原子②氖气③氧气④2个铁离子⑤n个水分子⑥5个氯分子⑦3个二氧化硫分子⑧5个氢氧根离子。
精析:本题要从元素符号、化学式及符号中所含数字所具有的含义出发,逐条回答。
答案:①3S ②Ne ③O2④2Fe3+⑤nH2O ⑥5Cl2 ⑦3SO2⑧5OH例2、下列关于化合价的说法中,正确的是A、H2中H的化合价为+1价B、H2O中氧元素的化合价为-2价C、一种元素只有一种化合价D、非金属元素在跟其它元素化合时,一定显负价精析:选项A中H2是氢气单质,氢元素没有跟其它元素化合,因此化合价应为零价。
至于B选项,H2O是氢元素与氧元素形成的化合物,在水中,氢显+1价,氧显-2价;C选项中一种元素只有一种化合价的说法不正确。
尽管有些元素只有一种化合价,但是有不少元素是有几种化合价的,如Fe就有+2、+3价。
D选项,当非金属元素跟金属元素化合时就显负价,但非金属元素与非金属元素化合时,可能显正价也可能显负价。
如硫在跟氢化合时,生成的硫化氢H2S中就显负价,而硫在跟氧化合时,生成的二氧化硫中显+4价,生成三氧化硫时显+6价。
答案:B例3、下列几种物质按氯元素化合价规律排列为KCl、、HClO、KClO3、HClO4,则空格内的物质是A、NaClB、NaClOC、Cl2D、HClO3精析:本题是根据化合物中化合价代数和为零............求出未知元素的化合价的具体应用,因此根据K的化合价是+1、H为+1、O为-2价分别求出这些化学式中氯元素的化合价,然后找出化合价的排列规律答案:C例4、改正下列错误的化学式:(1)氧化镁Mg 2O 2 (2)氢氧化铁Fe (HO )3 (3)氯气Cl(4)氩气Ar 2 (5)硫化钾KS 2(6)碳酸钠NaCO 3 (7)硫酸铵SO 4(NH 4)2(8)氢氧化铜CuOH 2精析:常见的化学式书写错误有:①元素符号排列错误:如(2)3)HO (Fe 、(7)SO 4(NH 4)2,正确顺序应该是正价在前,负价在后。


离子和化合价的区别和联系
一、区别:
概念不同:
1、离子:带电的原子或原子团
2、化合价:元素在形成化合物时变现出来的一种性质(化合价是指一种元素一定数目的原子和其它元素一定数目的原子相化合的性质)
书写不同:
1、离子符号:离子所带的电荷数应标在元素符号的右上角,如Ba2+、O2-而元素化合在元素符号的正上方
2、数值与“+”、“-”的前后顺序不一样:在写离子符号时,数值在前,符号“+”、“-”在后,而标元素化合价时,符号“+”、“-”在前,数值在后。
3、有关“1”是否省略的问题:在离子符号的书写中“1”省
略不写,而在标元素化合价时,“1”则不能省略。
Cl -
二、联系:(个人经验)+3
1、数字相同、正负号相同Al 3+ Al
2、根源都是源于电子的得失。
1、前二十个元素的元素符号(原子的序数=质子数=核电荷数=核外电子数)
2、钠质子数11。

常用化合价离子符如今,互联网已成为我们生活、工作、学习的主流,同时也是多元素化与复杂化的变化和发展进程。
同时,互联网日益重要的一个重要作用,就是它可以将各类不同的原子和化合物组成大量不同的化学公式。
化合物的离子符号是互联网呈现的一种可视化的媒介,是整个化学实验所涉及的知识的可以表达的基础,它可以很及时的表达出物质之间的连接和结构,反映出物质之间的相互关系。
常用的化学离子符号有:氢离子⊕H⁺,氧离子⊖O^{2-},氯离子⊖Cl^{1-},钙离子⊕Ca^{2+},铁离子⊖Fe^{3+},锂离子⊖Li{1-},硒离子⊕Se^{2-},硫离子⊕S^{2-},锌离子⊖Zn^{2+},镁离子⊕Mg^{2+},亚硫酸根⊖HSO_4^{-},氨离子⊖NH_4^{+},硝酸根⊖NO_3^{-},氯化钠⊖NaCl,氯化铵⊕NH_4Cl,氢氧化钠⊖NaOH,氢氧化铵⊖NH_4OH等。
互联网采用可视化中的离子符号,它可以让人们很清楚地了解不同原子和离子之间的关系,以快速、准确地准备和指示各种实验和物质之间的关系。
同时离子符号可以让学生更容易理解化学原理,在解决实际问题上有多元性和准确性的视角。
另外,离子符号可以帮助学生更好的进行实验。
离子符号的运用可以一定程度上降低实验过程的风险,它们可以让学生在新的技术下明白不同物质之间的关系,以及不同技术的含义,有助于整体的开拓实验的路径,发现新的机会与丰富的经验。
因此,我们可以说,互联网中的离子符号,可以帮助我们更深入理解和应用化学,为化学实验和实际应用提供更加有效的方法。
同时,互联网非常方便,可以把离子符号及整个学科的知识充分表达出来,从而让人们快速获取各种知识,帮助未来的生活、工作和学习。

常见离子符号(识记)Na+(钠离子)Cl-(氯离子)Mg2+(镁离子)Ca2+(钙离子)O2-(氧离子)H+(氢离子)OH-(氢氧根离子)SO42-(硫酸根离子)CO32-(碳酸根离子)NO3-(硝酸根离子)NH4+(铵根离子)K+(钾离子)Fe2+(亚铁离子)Fe3+(铁离子)Al3+(铝离子)Cu2+(铜离子)常见离子符号(识记)Na+(钠离子)Cl-(氯离子)Mg2+(镁离子)Ca2+(钙离子)O2-(氧离子)H+(氢离子)OH-(氢氧根离子)SO42-(硫酸根离子)CO32-(碳酸根离子)NO3-(硝酸根离子)NH4+(铵根离子)K+(钾离子)Fe2+(亚铁离子)Fe3+(铁离子)Al3+(铝离子)Cu2+(铜离子)常见离子符号(识记)Na+(钠离子)Cl-(氯离子)Mg2+(镁离子)Ca2+(钙离子)O2-(氧离子)H+(氢离子)OH-(氢氧根离子)SO42-(硫酸根离子)CO32-(碳酸根离子)NO3-(硝酸根离子)NH4+(铵根离子)K+(钾离子)Fe2+(亚铁离子)Fe3+(铁离子)Al3+(铝离子)Cu2+(铜离子)常见离子符号(识记)Na+(钠离子)Cl-(氯离子)Mg2+(镁离子)Ca2+(钙离子)O2-(氧离子)H+(氢离子)OH-(氢氧根离子)SO42-(硫酸根离子)CO32-(碳酸根离子)NO3-(硝酸根离子)NH4+(铵根离子)K+(钾离子)Fe2+(亚铁离子)Fe3+(铁离子)Al3+(铝离子)Cu2+(铜离子)常见离子符号(识记)Na+(钠离子)Cl-(氯离子)Mg2+(镁离子)Ca2+(钙离子)O2-(氧离子)H+(氢离子)OH-(氢氧根离子)SO42-(硫酸根离子)CO32-(碳酸根离子)NO3-(硝酸根离子)NH4+(铵根离子)K+(钾离子)Fe2+(亚铁离子)Fe3+(铁离子)Al3+(铝离子)Cu2+(铜离子)常见化合价口诀常见化合价口诀一价氢氯钾钠银;二价氧钙钡镁锌,一价氢氯钾钠银;二价氧钙钡镁锌,三铝四硅五氮磷;二三铁,二四碳,三铝四硅五氮磷;二三铁,二四碳,二四六硫都齐全;铜汞二价最常见。
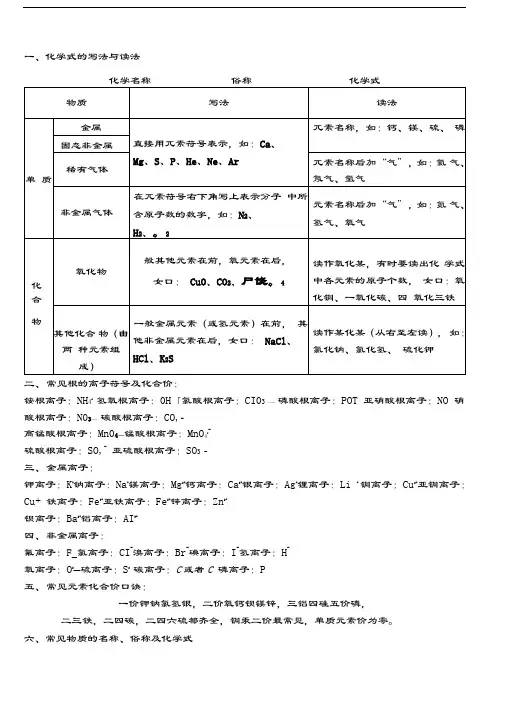
一、化学式的写法与读法
化学名称俗称化学式
二、常见根的离子符号及化合价:
铵根离子:NH4+氢氧根离子:0H「氯酸根离子:CI03 —磷酸根离子:POT 亚硝酸根离子:NO 硝酸根离子:N03—碳酸根离子:CO,-
高锰酸根离子:Mn04―锰酸根离子:MnO42-
硫酸根离子:SO,-亚硫酸根离子:SO3 -
三、金属离子:
钾离子:K+钠离子:Na+镁离子:Mg2+钙离子:Ca2+银离子:Ag+锂离子:Li + 铜离子:Cu2+亚铜离子:Cu+ 铁离子:Fe3+亚铁离子:Fe2+锌离子:Zn2+
钡离子:Ba2+铝离子:AI3+
四、非金属离子:
氟离子:F_氯离子:CI-溴离子:Br-碘离子:I-氢离子:H-
氧离子:O2—硫离子:S2碳离子:C或者C磷离子:P
五、常见元素化合价口诀:
一价钾钠氯氢银,二价氧钙钡镁锌,三铝四硅五价磷,
二三铁,二四碳,二四六硫都齐全,铜汞二价最常见,单质元素价为零。
六、常见物质的名称、俗称及化学式。

氢氧根的离子符号和化合价
《氢氧根的离子符号和化合价》
氢氧根离子的符号为OH-,其中氢原子的化合价为+1,氧原子的化合价为-2。
因此,氢氧根离子的化合价为-1。
氢氧根离子是一种非常重要的离子,它在许多化学反应和生物过程中都起着重要作用。
例如,在水中,氢氧根离子可以与金属离子形成盐,促进溶解和离子交换。
在生物体内,氢氧根离子也参与了许多重要的生物化学过程,如细胞代谢和酸碱平衡调节。
通过了解氢氧根离子的离子符号和化合价,我们可以更好地理解它在化学和生物学中的作用,为我们的学习和生活提供更多的知识基础。
常见阳离子:
氢离子——H+钠离子——Na+镁离子——Mg2+铝离子——Al3+钾离子——K+钙离子——Ca2+银离子——Ag+钡离子——Ba2+锌离子——Zn2+铜离子——Cu2+汞离子——Hg2+
铁离子——Fe3+亚铁离子——Fe2+
铵根离子——NH
4
+
常见阴离子:
氯离子——Cl-硫离子——S2-氧离子——O2-氟离子——F-
氢氧根离子——OH-硫酸根离子——SO
42-硝酸根离子——NO
3
-
碳酸根离子——CO
32-碳酸氢根离子——HCO
3
-
磷酸根离子——PO
43-亚硫酸根离子——SO
3
2—
高锰酸根离子——MnO
4-锰酸根离子——MnO
4
2-
氯酸根离子——ClO3-
化合价口诀:(括号中为负价)
一价氢(氯)钾钠银,
二价(氧)钙钡镁锌,
三铝四硅五价磷,
二三铁、二四碳,
(二)四六硫都齐全,
氮有负三和正五,
铜汞二价最常见,
莫忘单质价为零。
默写(第1遍):
氢离子铝离子钾离子银离子钡离子锌离子铜离子铁离子亚铁离子镁离子氯离子钠离子硫离子钙离子氧离子氟离子汞离子铵根离子氢氧根离子硝酸根离子碳酸根离子碳
酸氢根离子硫酸根离子磷酸根离子高锰酸根离子锰酸根离子亚硫酸根离子氯酸根离子
默写(第2遍):
氢离子铝离子钾离子银离子钡离子锌离子铜离子铁离子亚铁离子镁离子氯离子钠离子硫离子钙离子氧离子氟离子汞离子铵根离子氢氧根离子硝酸根离子碳酸根离子碳酸氢根离子硫酸根离子磷酸根离子高锰酸根离子锰酸根离子亚硫酸根离子氯酸根离子
默写(第3遍):
氢离子铝离子钾离子银离子钡离子锌离子铜离子铁离子亚铁离子镁离子氯离子钠离子硫离子钙离子氧离子氟离子汞离子铵根离子氢氧根离子硝酸根离子碳酸根离子碳酸氢根离子硫酸根离子磷酸根离子高锰酸根离子锰酸根离子亚硫酸根离子氯酸根离子
默写(第4遍):
氢离子铝离子钾离子银离子钡离子锌离子铜离子铁离子亚铁离子镁离子氯离子钠离子硫离子钙离子氧离子氟离子汞离子铵根离子氢氧根离子硝酸根离子碳酸根离子碳酸氢根离子硫酸根离子磷酸根离子高锰酸根离子锰酸根离子亚硫酸根离子氯酸根离子。