同系物及同分异构体知识规律总结
- 格式:doc
- 大小:36.50 KB
- 文档页数:4

一.同系物1.定义:通式相同,结构相似,在分子组成上相差一个或若干个“CH2”原子团的有机物。
2.判断要领:(1)结构相似,对有官能团的有机物来说,必须官能团的种类和数目都相同,例如:满足通式C n H2n+2O的饱和一元醇CH3OH, CH3 CH2OH,CH3 CH2 CH2OH互为同系物,但是CH3 CH2OH和乙二醇,丙三醇不是同系物,因为虽然它们的官能团相同都是羟基,但是羟基的数目不同,同样道理,CH3CH2Br和CH3—CHBr—CH2Br 不是同系物,CH3CH2Br和CH3CH2CL也不是同系物。
(2)同系物在分子组成上相差一个或若干个“CH2”原子团,那么同系物之间不存在同分异构体,同分异构体不可能是同系物。
3.同系物规律:(1)同系物随着碳原子数的增加,相对分子质量逐渐增大,分子间作用力逐渐增大,物质的熔沸点逐渐升高。
(2)同系物的化学性质一般相似。
( 3 )碳原子数不同的烷烃一定属于互为同系物的关系。
因为其没有类别异构例一下列各对物质,互为同系物的是()A. CH—CH===CH2和B.—OH和—CH2OH3C.CHCOOCH3和CH3 CH2COOCH3D.CH3CH2Br和CH3—CHBr—CH2Br3E.CH===CH2和环丁烷 F.戊烷和十七烷2例二下列说法中,正确的是()A.烯烃和烷烃的命名方法B.同系物之间各元素的质量分数一定相同C.不同碳原子数的烷烃一定属于互为同系物的关系D.具有相同分子通式的不同有机物一定属于同系物二.同分异构体1.定义.:具有相同的分子式,但具有不同结构的化合物,中学阶段主要研究有机物的同分异构体。
2.互为同分异构体的必备条件有二:①化合物分子式相同②化合物结构不同(如碳链骨架不同,官能团的位置不同,官能团的种类不同)3. 中学阶段要求掌握的异构方式有三种,即碳链异构,位置不同,官能团异构又叫类别异构)4.有机物还有立体异构。
常见的立体异构现象有顺反异构和对映异构,顺-2-丁烯和反-2-丁烯是顺反异构体。
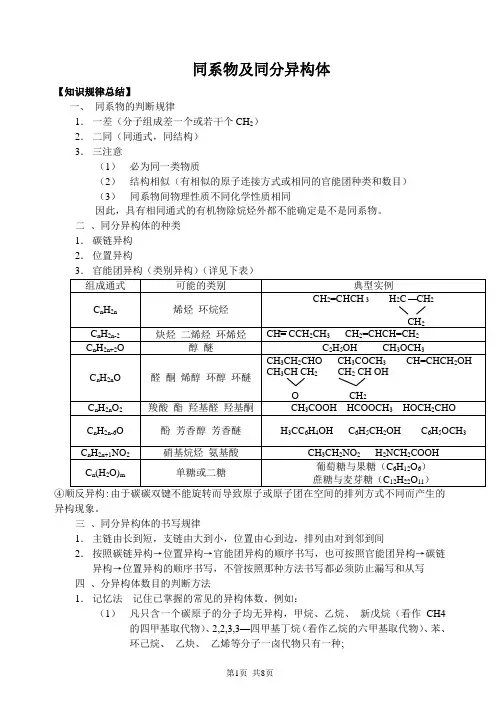
同系物及同分异构体【知识规律总结】一、同系物的判断规律1.一差(分子组成差一个或若干个CH2)2.二同(同通式,同结构)3.三注意(1)必为同一类物质(2)结构相似(有相似的原子连接方式或相同的官能团种类和数目)(3)同系物间物理性质不同化学性质相同因此,具有相同通式的有机物除烷烃外都不能确定是不是同系物。
二、同分异构体的种类1.碳链异构2.位置异构异构现象。
三、同分异构体的书写规律1.主链由长到短,支链由大到小,位置由心到边,排列由对到邻到间2.按照碳链异构→位置异构→官能团异构的顺序书写,也可按照官能团异构→碳链异构→位置异构的顺序书写,不管按照那种方法书写都必须防止漏写和从写四、分异构体数目的判断方法1.记忆法记住已掌握的常见的异构体数。
例如:(1)凡只含一个碳原子的分子均无异构,甲烷、乙烷、新戊烷(看作CH4的四甲基取代物)、2,2,3,3—四甲基丁烷(看作乙烷的六甲基取代物)、苯、环己烷、乙炔、乙烯等分子一卤代物只有一种;(2) 丁烷、丁炔、丙基、丙醇有2种; (3) 戊烷、丁烯、戊炔有3种; (4) 丁基、苯的同系物C 8H 10有4种; (5) 己烷、C 7H 8O (含苯环)有5种; (6) 戊基、苯的同系物C 9H 12有8种;2. 基元法这里的一元取代基X ,可以是原子,如卤原子,也可以是原子团,如-OH 、-CHO 、-COOH 、HCOO-等。
因此,已知丁基-C 4H 9有四种,则可断定丁醇、戊醛、戊酸以及甲酸丁酯都有4种异构体。
分子式为C 11H 16的一烷基取代苯的同分异体共有 ____ 种{说明}常可根据某些烃存在的一元取代物数目,反推原烃分子结构式。
如含碳原数少于10的烷烃中,其中一卤代物不存在异构体的有 4 种。
又如,已知烯烃C 6H 12的一氯代物只有一种,则可断定该烯烃的分子结构为3. 替元法 例如:C 6H 4Cl 2624H 替代Cl);[练已知A 的结构为A 的n 溴代物与m 溴代物的异构体数目相同,则n 和m 必满足关系式 ______4. 对称法(又称等效氢法) 判断方法如下:(1) 同一C 原子上的氢原子是等效(2) 同一C 原子所连甲基上的氢原子是等效氯(3) 处于镜面对称位置上的氢原子是等效 5.定一移一例:一氯蒽有 种同分异构体,二氯蒽有 种同分异构体。


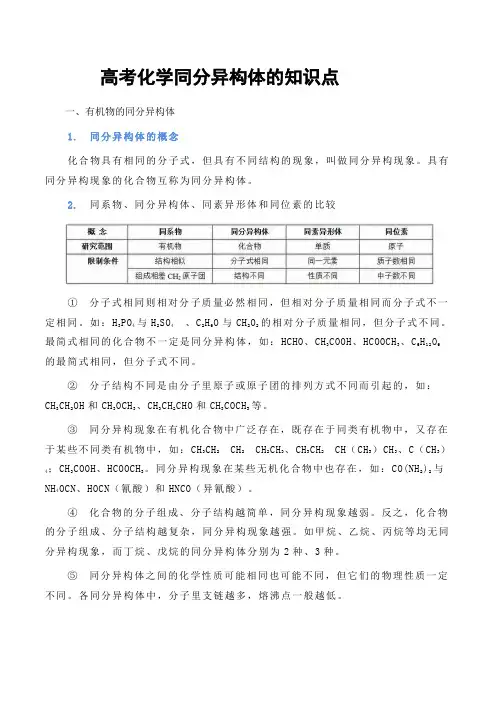
高考化学同分异构体的知识点一、有机物的同分异构体1. 同分异构体的概念化合物具有相同的分子式,但具有不同结构的现象,叫做同分异构现象。
具有同分异构现象的化合物互称为同分异构体。
2. 同系物、同分异构体、同素异形体和同位素的比较①分子式相同则相对分子质量必然相同,但相对分子质量相同而分子式不一定相同。
如:H3PO4与H2SO4、C2H6O与CH2O2的相对分子质量相同,但分子式不同。
最简式相同的化合物不一定是同分异构体,如:HCHO、CH3COOH、HCOOCH3、C6H12O6的最简式相同,但分子式不同。
②分子结构不同是由分子里原子或原子团的排列方式不同而引起的,如:CH3CH2OH和CH3OCH3、CH3CH2CHO和CH3COCH3等。
③同分异构现象在有机化合物中广泛存在,既存在于同类有机物中,又存在于某些不同类有机物中,如:CH3CH2CH2CH2CH3、CH3CH2CH(CH3)CH3、C(CH3)4;CH3COOH、HCOOCH3。
同分异构现象在某些无机化合物中也存在,如:CO(NH2)2与NH4OCN、HOCN(氰酸)和HNCO(异氰酸)。
④化合物的分子组成、分子结构越简单,同分异构现象越弱。
反之,化合物的分子组成、分子结构越复杂,同分异构现象越强。
如甲烷、乙烷、丙烷等均无同分异构现象,而丁烷、戊烷的同分异构体分别为2种、3种。
⑤同分异构体之间的化学性质可能相同也可能不同,但它们的物理性质一定不同。
各同分异构体中,分子里支链越多,熔沸点一般越低。
二. 同分异构体的类型绝大多数有机物普遍存在同分异构现象,高中阶段的同分异构现象主要有4种情况。
即碳链异构、官能团位置异构、官能团类别异构和顺反异构。
1. 碳链异构碳链异构是指由于碳原子的连接次序不同引起的异构,如,正丁烷与异丁烷。
由于烷烃分子中没有官能团,所以烷烃不存在官能团位置异构和官能团类别异构,而只有碳链异构。
再如,CH3CH2CH2CH2CHO(戊醛)与(CH3)2CHCH2CHO(2-甲基丁醛)也属于碳链异构。

专题复习同分异构体和同系物考点一、同系物:知识点:1、定义:2、同系物的判断规律3、同位素:(1)定义:(2)同位素的性质典型例题:例1:下列各物质互为同系物的是()A.OH CH2OH和B.CH3CH2OH和CH3OCH3 C.CH3一CH=CH2和CH3 CH2 CH3 D.CH3CH2OH和CH3OH 例2、下列各组物质中,一定互为同系物的是()A、分子式为CH2O2和C3H6O2的物质B、分子式为CH2O和结构简式为CH3CHO的物质C、分子式为CH4O和C2H6O的物质D、苯酚和苯甲醇(C6H5CH2OH)强化训练:1、下列各组中物质一定互为同系物的是()A.C3H4与C5H8B.C3H6与C5H10C.C3H8与C5H12D.C3H7Cl与C5H10Cl22、下列各组物质中,互为同系物的是()A.CH3CH2CH2CH3和 CH3CH=CHCH3 B.甲苯和苯乙烯C.CH≡CCH2CH3和CH2=CHCH2CH3 D.CH2=CHCH3和CH2=CHCH2CH33、下列各物质中, 互为同系物的一组是()①C2H5COOH ②C6H5—COOH ③硬脂酸④油酸⑤丙烯酸⑥CH3CH2CHOA.①③ B.③⑤ C.④⑥ D.⑤⑥4、下列化学用语表达正确的是()A.F-的结构示意图为 B.乙醇的分子式为 C2H5OHC.钙离子的电子式 Ca2+ D.纯碱的化学式为 NaOH5、下列各组物质的分类正确的是()A.同位素:1H、D+、T2B.电解质:H2O、CH3COOH、NH4HCO3C.强电解质:HF CaCO3 NaHCO3D.同系物:OH OHCH3CH3CH2OH考点二、同分异构体的种类知识点:1、同分异构体的概念。
2、同分异构体的类型:(1)碳链异构:例1:熟练地写出分子式为C4H10、C5H12、C6H14、C7H16的所有同分异构体的结构简式:(2)基的异构(写出符合—C3H7、—C4H9、—C5H11的异构)(3)位置异构:例2:分析满足下列条件的同分异构体的结构简式:①分子式为C5H10,能使溴水反应褪色同分异构体的结构简式有种(不考虑顺反异构)②分子式为C5H12O的醇类且能氧化成醛同分异构体的结构简式有种③写出符合C5H10O属于醛的同分异构体的结构简式有种④写出符合C5H10O2属于羧酸的同分异构体的结构简式有种⑤写出符合C4H8O2属于酯的同分异构体的结构简式有种(类别异构现象举例书写结构简式①单烯烃与②炔烃与③饱和一元醇与④芳香醇与⑤饱和一元醛与⑥饱和一元羧酸与⑦氨基酸与(5)顺反异构例3:已知和互为同分异构体(称作“顺反异构体”),则化学式为C3H5Cl的链状的同分异构体共有()A、3种B、4种C、5种D、63、苯环上同分异构的问题:例4:(1)写出符合分子式为C9H12且含有苯环的所有同分异构体的结构简式:(2)苯环上的三个氢原子被—OH、—Cl、—Br取代时,能生成同分异构体的数目是()A、10种B、9种C、6种D、3种(3)苯环上的三个氢原子被—OH、—OH、—Cl取代时,能生成同分异构体的数目是()A、10种B、9种C、6种D、3种(4)苯环上的三个氢原子被三个—OH取代时,能生成同分异构体的数目是()A、10种B、9种C、6种D、3种例5:邻甲基苯甲酸 有多种同分异构体,其中属于酯类且结构中含有苯环的同分异构体有 ( ) A 、6种 B 、5种 C 、4种 D 、3种4、有限制条件的同分异构:例6:写出符合分子是C 4H 8O 2符合下列条件的同分异构体的结构简式:(1)能与碳酸氢钠溶液反应(2)能水解的物质(3)能水解且能发生银镜反应(4)能与钠反应且能发生银镜反应例7、写出符合分子式C 7H 8O 含有苯环且符合下列条件的同分异构体的结构简式:(1) 能与氢氧化钠溶液反应且能使氯化铁溶液显紫色(2) 能与钠反应但是不能与氢氧化钠溶液反应(3)既不能与钠反应又不能与氢氧化钠溶液反应强化训练:1、写出符合分子式C 5H 12O 属于醇并满足下列条件:(1)可以催化氧化成醛的结构简式:(2)不可以催化氧化:(3)可以催出氧化成酮(4)不能消去2、写出符合分子是C 8H 8O 2含有苯环且符合下列条件的同分异构体的结构简式(1)能与碳酸氢钠溶液反应(2)能水解(3)能水解且能发生银镜反应(4)不能水解但是可以发生银镜反应且该物质遇氯化铁溶液显紫色COOH CH 3OH ︱CHCOOH 3、对苯二甲酸的结构简式为: ,符合下列条件的同分异构体有: 种。


同系物同分异构体(一)、同系物:结构相似,组成上相差一个或若干个“CH2”原子团的物质。
1、同系物的判断规律(1)一差(分子组成至少相差一个CH2原子团)(2)一同(具有相同的通式)(3)二相似(结构相似,化学性质相似)2、注意事项(1)同系物必须是同类有机物(2)结构相似指具有相似的原子连接方式,相同的官能团类别和官能团数目。
(3)具有相同通式的有机物除烷烃外,不能以通式相同的作为确定是不是同系物的充分条件。
(4)同分异构体之间不是同系物关系。
(5)同系物的物理性质具有规律性的变化;同系物的化学性质相似,这是我们学习和掌握有机物性质的依据。
(二)、同分异构体:具有相同分子式而分子结构不同的物质1、同分异构体的种类(1)碳架异构(指碳原子之间连接成不同的链状或环状结构而造成的异构)。
(2)位置异构(指官能团或取代基在碳架上的位置不同而造成的异构)。
(3)类别异构(指有机物分子中的官能团不同或有机物类别不同而造成的异构,也叫官能团异构)。
2、几类同分异构体(1)C n H2n:(n≥3)烯烃和环烷烃;(2)C n H2n-2:(n≥3)二烯烃和炔烃;(3)C n H2n+2O:(n≥2)饱和一元醇和饱和一元醚;(4)C n H2n O:(n≥2)饱和一元醛、烯醇和环氧烷;(n≥3)饱和一元酮;(5)C n H2n O2:(n≥2)饱和一元羧酸、饱和一元羧酸饱一元醇酯;(6)C n H2n+1O2N:(n≥2)氨基酸、硝基化合物和亚硝酸酯;(7)C n H2n-6O:(n≥7)酚、芳香醇和芳香醚。
3、几种特殊的同分异构体(1)C8H8:苯乙烯和立方烷;(2)C8H10:乙苯和邻二甲苯、间二甲苯、对二甲苯;(3)C6H12O6:葡萄糖和果糖;(4)C11H22O11:蔗糖和麦芽糖;(5)CH4ON2:尿素[CO(NH2)2]和氰酸铵[NH4CNO]4、同分异构体书写规律(1)烷烃(只可能存在碳链异构),书写时应注意全而不重。

1、同系物:结构相似,分子组成相差一个或若干个CH2原子的物质CH4和CH2H6
2、同分异构体:化合物具有相同的分子式,但具有不同结构(这个需要结构式)
*一个是物质不同*一个是结构不同
A同系物就是结构相似,分子式相差一个或多个CH2 的物质,在有机物中存在,如烷烃
B同分异构体就是化学式一致,但是结构式排布不一致的两种物质
C同位素就是在一种元素中存在着质子相同,中子数不同的数种核素(上面的“水和重水”的说法是不对的),如氢元素中的氕、氘、氚
D同素异型体就是构成的元素相同,但由于原子排列不同,形成不同性质的物质,如O2 和O3。
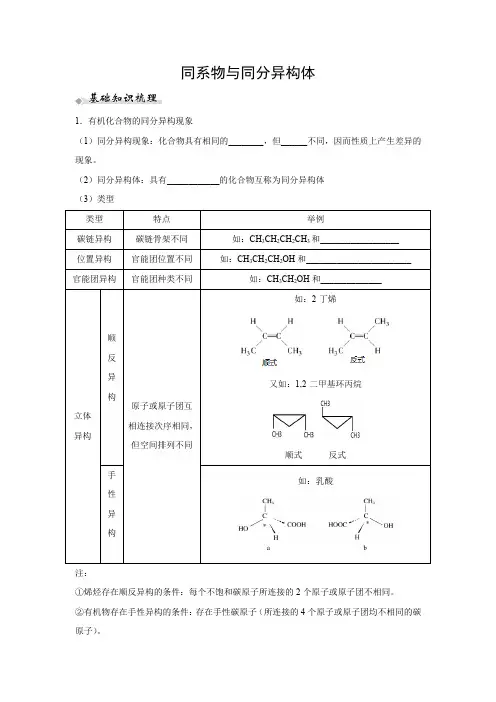
同系物与同分异构体1.有机化合物的同分异构现象(1)同分异构现象:化合物具有相同的________,但______不同,因而性质上产生差异的现象。
(2)同分异构体:具有____________的化合物互称为同分异构体(3)类型 类型特点 举例碳链异构碳链骨架不同 如:CH 3CH 2CH 2CH 3和__________________ 位置异构官能团位置不同 如:CH 3CH 2CH 2OH 和________________________ 官能团异构 官能团种类不同 如:CH 3CH 2OH 和______________立体异构顺反异构原子或原子团互相连接次序相同,但空间排列不同如:2-丁烯又如:1,2-二甲基环丙烷 顺式 反式手性异构如:乳酸 注:①烯烃存在顺反异构的条件:每个不饱和碳原子所连接的2个原子或原子团不相同。
②有机物存在手性异构的条件:存在手性碳原子(所连接的4个原子或原子团均不相同的碳原子)。
③手性异构又称对映异构或旋光异构。
2.同系物概念→结构____,分子组成上相差一个或若干个____结构→官能团种类、数目均相同、具有相同的通式、属于同类物质性质→ → 物理性质:随碳原子数的增加发生规律性变化→ 化学性质:性质相似应用体验判断正误(1)同分异构是同一物质的不同存在形式()(2)含5个碳原子的有机物,每个分子中最多可形成4个C-C单键()(3)同系物一定符合相同的通式,符合同一通式的一定是同系物()(4)和属于同系物()(5) C2H6和C3H8、C2H4和C3H6两组物质都互为同系物()(6)甲苯和邻二甲苯是同系物( )(7)乙醇和乙醚是同分异构体()(8)苯和环己烷的二氯代物都只有3种( )1、明晰同系物的概念(1)结构相似必是同类别、同数目的官能团,碳碳连接方式相同。
如乙醇和丙三醇则因官能团数目不同而不是同系物。
(2)同系物必有相同的通式,但通式相同的不一定为同系物。
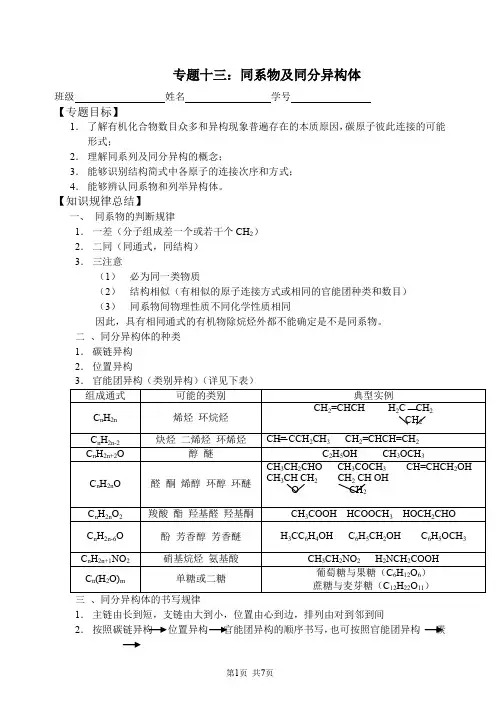
专题十三:同系物及同分异构体班级姓名学号【专题目标】1.了解有机化合物数目众多和异构现象普遍存在的本质原因,碳原子彼此连接的可能形式;2.理解同系列及同分异构的概念;3.能够识别结构简式中各原子的连接次序和方式;4.能够辨认同系物和列举异构体。
【知识规律总结】一、同系物的判断规律1.一差(分子组成差一个或若干个CH2)2.二同(同通式,同结构)3.三注意(1)必为同一类物质(2)结构相似(有相似的原子连接方式或相同的官能团种类和数目)(3)同系物间物理性质不同化学性质相同因此,具有相同通式的有机物除烷烃外都不能确定是不是同系物。
二、同分异构体的种类1.碳链异构2.位置异构三、同分异构体的书写规律1.主链由长到短,支链由大到小,位置由心到边,排列由对到邻到间2.按照碳链异构位置异构官能团异构的顺序书写,也可按照官能团异构碳链异构位置异构的顺序书写,不管按照那种方法书写都必须防止漏写和从写四、分异构体数目的判断方法1.记忆法记住已掌握的常见的异构体数。
例如:(1)凡只含一个碳原子的分子均无异构,甲烷、乙烷、新戊烷(看作CH4的四甲基取代物)、2,2,3,3—四甲基丁烷(看作乙烷的六甲基取代物)、苯、环己烷、乙炔、乙烯等分子一卤代物只有一种;(2)丁烷、丁炔、丙基、丙醇有2种;(3)戊烷、丁烯、戊炔有3种;(4)丁基C8H10有4种;(5)己烷、C7H8O(含苯环)有5种;(6)戊基、C9H12有8种;2.基元法例如:丁基有4种,丁醇、丁醛都有4种;3.替元法例如:C6H4Cl2有3种,C6H2Cl4有3种(将H替代Cl);4.对称法(又称等效氢法)判断方法如下:(1)同一C 原子上的氢原子是等效(2)同一C 原子所连甲基上的氢原子是等效氯(3)处于镜面对称位置上的氢原子是等效【经典题型】题型一:确定异构体的数目例1 某烃的一种同分异构只能生成1种一氯代物,该烃的分子式可以是()A.C3H8B.C4H10C.C5H12D.C6H14解析:分析C3H8、C4H10、、C6H14各种结构,生成的一氯代物不只1种。
专题1 同系物和同分异构体【知识要点】1.同系列、同系物分子结构相似,组成上相差若干个某原子或原子团的一系列化合物,称为同系列。
可表示为AnW B,A、B为任意一种基团(或氢原子),W为2价的某原子或有机基团,又成为该同系列的系差。
同系列的性质往往呈现规律性的变化。
同系列化合物中,若分子组成上相差一个或若干个CH2的一系列有机化合物,称为同系物。
例如:甲烷(CH4)、乙烷(C2H6)、丙烷(C3H8)、……等一系列的分子属于烷烃同系列,甲烷(CH4)、乙烷(C2H6)、丙烷(C3H8)等互称为同系物。
同系物一定属同类物质,具有相似的组成和结构(官能团的种类和个数均相同),相似的性质,相同的通式。
例如,烷烃的组成通式为C n H2n+2(n≥1),烯烃的组成通式为C n H2n (n≥2)。
同系物的几点补充:(1) 必须是符合同一通式同一类物质,化学式一定不同,而且符合同一通式的并不一定就是同系物。
(2) 结构相似,是结构特点相似,并不是完全相同。
如异丁烷与正戊烷,前者有支链,后者没有。
(3) 结构相似,但性质却有时相差较大,如:甲苯与苯。
(4) 官能团一定要相同,并且官能团数目也要相同。
2.同分异构现象、同分异构体化合物具有相同的化学式,但是具有不同结构的现象,叫做同分异构现象;具有相同化学式而结构不同的化合物互称为同分异构体。
例如:丁烷C4H10有两种结构,这就是同分异构现象,这两种化合物互称同分异构体。
CH3CH2CH2CH3CH3CH CH3CH3同分异构体的几点补充:(1) 结构不同,分子量相同,元素百分含量相同(或最简式相同)的有机物一定有相同的分子式,一定是同分异构体。
如:乙酸CH3COOH和甲酸甲酯HCOOCH3。
(2) 同分异构体不一定属于同类物质,性质不一定相似。
如:乙酸和甲酸甲酯、乙醇CH3CH2OH和甲醚CH3OCH3。
(3) 分子量相同的有机物不一定有相同的分子式。
如:甲酸HCOOH和乙醇CH3CH2OH、乙酸CH3COOH和丙醇CH3CH2CH2OH、壬烷C9H20和萘C10H8等。
注:尊敬的各位读者,本文是笔者教育资料系列文章的一篇,由于时间关系,如有相关问题,望各位雅正。
希望本文能对有需要的朋友有所帮助。
如果您需要其它类型的教育资料,可以关注笔者知识店铺。
由于部分内容来源网络,如有部分内容侵权请联系笔者。
§1同系物同分异构体专题[复习要点]1.有机化合物种类繁多的原因。
2.有机化合物的命名。
3.同系物的判断规律:两同、一差、两注意4.同分异构体(1)含义(2)种类——碳链异构、官能团位置异构、物类异构[方法指导]1.同分异构体的书写试题特点:限制一定条件,在限定的范围内书写或补写几种同分异构体解题思路:首先明确限定范围,然后在所限定范围内按官能团异构——碳链异构——位置异构的顺序书写或补写,也可通过分析已知的几个同分异构体的结构特点找出规律补写所缺的种类。
例1、已知某有机物分子中含有2个—CH3,1个—CH2—,2个—CH—,2个—OH,该有机物可能有,分别写出它们的结构简式。
例2、液晶是一种新型材料,A和胺B:CH3O CH=N)3CH3醛A :CH3O CHO 胺B:CH3NH2(1)对位上有—C4H9的苯胺可能有4CH3 (CH2)3NH2 ,(CH3)2CH CH2NH2, , 。
(2)醛6种,它们COOCH3OOCCH3,HCOO CH3,HCOO3,2.判断是否同分异构体试题特点:给出几种有机物的结构简式,分析每组物质的结构特点,判断是否为同分异构体。
解题思路:先看分子式相同,再看结构不同。
注意考虑:a.原子或原子团连接顺序 b.原子的空间排列形状c.辨别是否为同一种物质。
例3、下列物质为同分异构体的一组是()F ClA.Cl—C—Cl ,Cl—C—F B.CH3CH2NO2,H2N—CH2—COOHF FCH3C.[ CH—CH2 ] n , [ CH—CH] n D.CH3CH2C(CH3)2CH2CH3 , CH3CH2—C—CH3 C2H5CH3 CH3C2H5例4、已知乙烯分子平面构型,1,2—二氯乙烯有两种不同的空间结构(如下图所示),下列物质能形成上述空间异构体的是()Cl H Cl ClA . 1,1—二氯乙烯B . 丙烯C=C C=CC . 2—丁烯D . 1—丁烯H Cl H H3.同分异构体种类的确定试题特点:一是已知有机物结构确定取代产物的同分异构体种类,二是已知某物质某种取代物异构体数来确定其另一种取代物种数解题方法:一数分析有机物结构特点,确定不同位置H原子种数再确定取代产物数目,二是找出取代物H原子数与取代基团关系,不必写出异构体例5、(1)萘)分子中的两个氢原子分别被溴取代,所形成化合物的数目有种。
中职化学同分异构体与同系物的概念解析摘要:在中职化学教学中,同分异构体和同系物的概念是有机化学中较难理解并较易混淆的一组概念,给学生系统学习有机化学带来了困惑,也是中职化学教学过程中的重点和难点。
本文通过对同分异构体和同系物的概念剖析,教会学生准确把握这组概念,促进学生构建自己的知识体系,使学生增强学习有机化学的兴趣。
关键词:同分异构体构造异构同系物一、同分异构体的概念同分异构体是指分子组成上相同,但结构不同的化合物。
如C2H4和CO具有相同的相对分子质量,但分子式截然不同,不属于同分异构体。
C2H2和C6H6的最简式相同,但在组成原子数量上不同即分子式不同,不属于同分异构体。
再比如多糖化合物:淀粉[n]、纤维素[n]以及糖原[n],三者之�g通式相同,但当n值不同时,分子式就不同,也不是同分异构体关系。
除上述对基本概念的解析外,还需明确同分异构体的存在大多数是有机物之间,在无机物之间也可以存在这样的关系,但有机物与无机物之间一般不存在同分异构体的关系。
如无机物中的雷酸银AgONC和氰酸银AgCNO ;雷酸HONC和氰酸HOCN以及异氰酸HNCO 都是互为同分异构体的关系。
同分异构体的现象很多,一般可分为构造异构和立体异构两大类。
其中构造异构分为碳链异构,位置异构,类别异构;立体异构又分为顺反异构、光学异构、对映异构、构象异构等。
在中职医学、药学或卫生学校的教材、教参中一般其中涉及的同分异构现象主要是构造异构,下面就重点解释构造异构的知识体系。
1.碳链异构指结构中碳原子的排列顺序不同而产生的同分异构现象,具有同分异构现象的物质称为同分异构体。
这里介绍一种常见且有效的书写碳链异构的方法为“逐级减碳法”,书写步骤如下:首先根据分子式写出主链最长的直链结构式,没有分支;然后写出主链上少一个碳原子的直链式结构,把余下的一个碳原子当做取代基加在主链的碳原子上,并依次变动取代基的位置;再写出主链少两个碳原子的直链式结构,把剩余的两个碳作为支链加在主链的碳原子上;依次递减,递减过程中注意主链肯定是最长的碳链,不能因为主链碳原子的递减、支链的增多而本末倒置。
有机物单元复习 同分异构体、同系物一. 本周教学内容有机物单元复习 同分异构体、同系物 二. 教学要求1. 有机物同分异构体,同系物的判断。
2. 同分异构体的书写,数目的确定。
三. 知识分析1. 同系物和同系列结构上相似,组成上相差一个或若干个2CH原子团的有机物,按碳原子数递增的顺序所排成的系列叫同系列。
同系列中的各有机物互称同系物。
说明:(1)同系物的一些物理性质,随分子中碳原子数的递增而呈现出规律性的变化。
(2)由于同系物具有相似的结构,所以它们在化学性质上也相应地表现出某种相似性。
2. 同分异构现象和同分异构化合物具有相同的分子式,但具有不同结构的现象,叫做同分异构现象。
具有同分异构现象的化合物叫做同分异构体。
同分异构现象是有机物种类繁多的重要原因。
在高中阶段,同分异构中的“分子结构不同”主要有三种类型: (1)碳链异构:由分子内碳原子的排列顺序不同所引起的。
(2)位置异构:由官能团在碳链上的位置不同或取代基在苯环上的位置不同引起的异构。
(3)类别(跨类)异构:不同系列的物质之间,即官能团不同引起的异构。
这部分内容几乎年年考,考查内容有: ① 同系列和同分异构体数目的确定。
② 列举同分异构体的结构。
③ 判断几种结构是否相同。
④ 学会变通。
随着科学技术的飞速发展,分子生物技术的日臻成熟,新材料、新药物不断被发现和合成,要求人们对其结构和性质有一定的了解。
可以预见这部分知识仍将是新高考中“x ”的一个热点。
【典型例题】[例1] 式量100的烃,主链中含5个碳原子的可能结构有5种。
试写出它们的结构简式,并用系统命名法命名。
解析:由已知烃的式量确定分子式是解此类题的突破口,其确定方法有如下2种: 解法1:通式法:设烃分子式为xn n H C +2(2=x ,0,2-, 4-)则x n +=14100 14/)100(x n -=讨论:2=x 时,7=n 为167H C 0≤x 时,n 值均不合理 解法2:商余法用式量除以12(C 的原子量),所得商为烃所含碳原子的最大数目,而余数就是H 原子的最小数目。
同系物及同分异构体知识规律总结
一、同系物的判断规律
1.一差(分子组成差若干个CH2)
2.两同(同通式,同结构)
3.三注意
(1)必为同一类物质;
(2)结构相似(即有相似的原子连接方式或相同的官能团种类
和数目);
(3)同系物间物理性不同化学性相似。
因此,具有相同通式的有机物除烷烃外都不能确定是不是同系物。
二、同分异构体的种类
1.碳链异构
2.位置异构
3.官能团异构(类别异构)
常见的类别异构(详写下表)
常见的类别异构
与
与CH2=CHCH=CH CH3COOH、HCOOCH3与
CH3CH2—NO
三、同分异构体的书写规律
1.主链由长到短,支链由整到散,位置由心到边,排列由对到邻到间。
2.按照碳链异构→位置异构→官能团异构的顺序书写,也可按官能团异构→碳链异构→位置异构顺序书写,不管按哪种方法书写都必须防止漏写和重写。
四、同分异构体数目的判断方法
1.记忆法记住已掌握的常见的异构体数。
例如:
(1)凡只含一个碳原子的分子均无异构;甲烷、乙烷、新戊烷(看作CH4的四甲基取代物),2,2,3,3-四甲基丁烷(看作乙烷的六甲基取代物)、苯、环己烷、C2H2、C2H4等分子的一卤代物只有一种;
(2)丁烷、丁炔、丙基、丙醇有2种;
(3)戊烷、丁烯有3种;
(4)丁基、C8H10(芳烃)有4种;
(5)己烷、C7H8O(含苯环)有5种;
2.基元法例如:丁基有4种,丁醇、丁醛都有4种
3.替代法例如:二氯苯C6H4Cl2有3种,四氯苯也为3种(将H 替代Cl);又如:CH4的一氯代物只有一种,新戊烷C(CH3)4的一氯代物也只有一种。
4.对称法(又称等效氢法)等效氢法的判断可按下列有三点进行:(1)同一碳原子上的氢原子是等效的;
(2)同一碳原子所连甲基上的氢原子是等效的;
(3)处于镜面对称位置上的氢原子是等效的(相当于平面成像时,物与像的关系)。