癫痫动物模型的制备
- 格式:ppt
- 大小:864.00 KB
- 文档页数:15
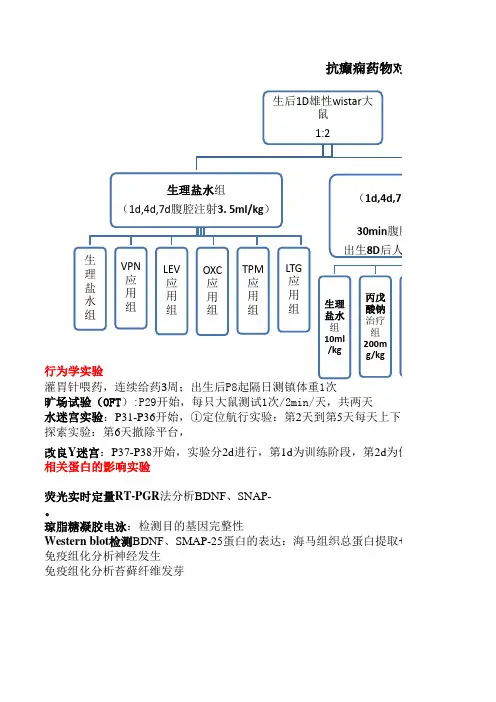
抗癫痫药物对新
水迷宫实验:P31-P36开始,①定位航行实验:第2天到第5天每天上下午各2次;②空间探索实验:第6天撤除平台,
旷场试验(OFT ):P29开始,每只大鼠测试1次/2min/天,共两天
灌胃针喂药,连续给药3周;出生后P8起隔日测镇体重1次
改良Y 迷宫:P37-P38开始,实验分2d 进行,第1d 为训练阶段,第2d 为保持阶段,每天相关蛋白的影响实验免疫组化分析苔藓纤维发芽
収出整脑用冰冷的生理盐水洗净大脑表面血液,有滤纸快速吸干后称重脑农而血液,川滤纸快逨吸r_/ri立即称iR
标本制备:分离出一侧海马,用于检测mRNA表达;另一侧海马取出后用于检测蛋白表达。
琼脂糖凝胶电泳:检测目的基因完整性
Western blot 检测BDNF 、SMAP-25蛋白的表达:海马组织总蛋白提取+蛋白浓度测定免疫组化分析神经发生
荧光实时定量RT-PGR 法分析BDNF 、SNAP-
物对新生大鼠行为及神经影响的癫痫模
两天
每天上下午各2次;②空间
,第2d为保持阶段,每天
有滤纸快速吸干后称重
马取出后用于检测蛋白表达
蛋白提取+蛋白浓度测定。


PTZ小鼠癫痫模型简介PTZ小鼠癫痫模型是一种常用于研究癫痫发作机制和药物疗效的实验动物模型。
该模型通过给小鼠注射有效剂量的低剂量苯妥英钠(pentylenetetrazol,PTZ)来诱发癫痫样发作。
PTZ是一种广泛应用的化合物,它可通过抑制穿透性氯通道和抑制γ-氨基丁酸(GABA)能系统来诱发癫痫样发作。
在PTZ小鼠癫痫模型中,PTZ通过快速注射进入体内,迅速扩散到中枢神经系统,引起癫痫样发作,包括强直性发作和癫痫惊厥。
操作步骤1.实验前准备–准备PTZ溶液:将PTZ粉末溶解在生理盐水中,制备成适当浓度的溶液。
–准备小鼠:根据实验设计,选择适当品系和年龄的小鼠,确保其健康状况和性别一致。
–实验环境准备:保持实验室的温度、湿度和光照等环境条件稳定。
2.注射PTZ溶液–将小鼠固定在适当的注射台上,确保固定牢固且不会对小鼠造成不适。
–使用细长的注射针,将事先准备好的PTZ溶液缓慢注射到小鼠腹部或尾静脉中。
–注意观察小鼠在注射过程中的反应,确保注射过程安全无误。
3.观察癫痫发作–在PTZ注射后,观察小鼠的行为反应,并记录下发作的持续时间和严重程度。
–持续记录小鼠的神经活动,例如脑电图(EEG),以评估癫痫发作的特征和模式。
–进行图像记录,如摄像或动作捕捉系统,以获得更全面的癫痫发作行为信息。
4.实验结束–在实验完成后,将小鼠转移到适当的饲养环境中,继续观察其恢复情况。
–对于需要进行多次实验的小鼠,应给予适当的间隔时间,以充分恢复其生理状态和行为表现。
数据分析PTZ小鼠癫痫模型的数据分析通常包括以下几个方面:1.行为观察分析:对小鼠的癫痫发作行为进行定性和定量分析,包括发作持续时间、发作阈值、发作次数等指标。
2.神经活动分析:对小鼠在癫痫发作过程中的脑电图(EEG)进行分析,包括评估发作时的电活动频率、振幅变化等指标。
3.药物干预研究:通过给予不同剂量或类型的抗癫痫药物,评估其对PTZ小鼠癫痫模型的影响,包括发作阈值的改变、发作次数的减少等指标。

中山大学研究生学刊(自然科学、医学版)第32卷第2期JOURNAL OF THE GRADUATES VOL.32ɴ22011SUN YAT-SEN UNIVERSITY(NATURAL SCIENCES、MEDICINE)2011癫痫动物模型的研究进展*汤丽鹏(中山大学中山医学院,广东广州510080)【内容提要】癫痫是一种以大脑局部病灶突发性的异常高频放电并向周围组织扩散为特征的大脑功能障碍,同时可伴随短暂的运动、感觉、意识及自主神经功能异常。
在研究癫痫病理生理改变及筛选抗癫痫药物时,所选择的癫痫模型起到十分重要的作用。
癫痫的疾病模型可大致分为体外模型和整体模型。
前者包括神经元模型和脑片模型;而后者可根据诱发癫痫的时程、遗传背景及药物抵抗性等特点,又可分为急性癫痫模型、慢性癫痫模型、遗传性癫痫模型和抵抗性癫痫模型。
本综述将对不同的癫痫模型的特点进行介绍,及对这些癫痫模型各自所代表的不同人类癫痫类型进行阐述,最后对这些癫痫模型进行比较。
【关键词】癫痫;脑片;急性癫痫模型;点燃癫痫模型;遗传性癫痫模型;药物抵抗性癫痫模型前言癫痫是一种以大脑局部病灶突发性的异常高频放电并向周围组织扩散为特征的大脑功能障碍,可伴有明显脑电图改变,及可能伴随着短暂性的运动、感觉、意识及自主神经功能异常。
据WHO2005年公布的流行病学调查结果显示:世界上有5千万的癫痫患者,且其平均每年发病率为0.5ɢ-1ɢ,可见癫痫是十分常见的神经系统疾病之一。
癫痫模型在癫痫的病理生理研究和抗癫痫药物的研究中发挥着重要的作用。
癫痫模型可分为体外模型和整体模型。
前者包括神经元模型和脑片模型,主要用于抗癫痫药物的筛选,还能有效的探讨抗癫痫药物的量效关系。
而后者通常包括急性癫痫模型、慢性癫痫模型、遗传性癫痫模型和抵抗性癫痫模型。
而这些整体模型又各自代表着不同的人类癫痫发作类型。
下面将简单介绍癫痫体内和整体模型。
*收稿日期:2010-05-08作者简介:汤丽鹏,女,1987年生,广东广州人,中山大学中山医学院2010级药理学专业博士研究生,主要研究方向药物抗癫痫的机制及其研究,电子邮箱:443082052@癫痫动物模型的研究进展1体外模型癫痫的体内模型的类型较少,且其操作相对较为简单。


癫痫电点燃整体动物模型研究进展癫痫是神经系统常见疾病之一,癫痫研究常用动物模型模拟人类癫痫发作以研究癫痫的发生发展病理机制及病理改变机制。
目前癫痫动物模型种类繁多,本文主要就电点燃整体动物模型的研究进展进行综述。
标签:癫痫;电点燃;整体动物模型癫痫是第三大最常见的慢性脑部疾病,其特点是脑部有持续存在的痫性反复发作的易感性,以及由于这种疾病引起的情感和认知功能障碍[1-2]。
世界卫生组织(WHO)指出,全球活动性癫痫的平均患病率为8.2%,全世界有5000万[3],我国有900万左右的癫痫患者,而且还以每年新发40~60万例的速度递增。
目前尽管有很多种类的抗癫痫西药应用于临床,抗癫痫西药以其能迅速控制癫痫发作,但仍然有1/3的癫痫患者对癫痫药物耐药。
在开发抗癫痫药物时,相关实验必需利用动物模型。
癫痫动物模型可分为离体模型和整体模型。
离体模型主要包括神经元模型和脑片模型,目前主要用于抗癫痫药物的筛选和其量效关系的研究。
整体模型主要包括化学点燃模型和电点燃模型。
本文将主要简单介绍整体电点燃模型。
整体动物模型症状分级标准:Racines癫痫行为分级:0级,正常状态;I 级,湿狗样颤动,面部肌肉痉挛及抽动(包括眨眼、动须、节律性咀嚼等);Ⅱ级,I级基础上加颈部肌肉痉挛(如节律性点头);Ⅲ级,Ⅱ级基础上加前肢痉挛;IV级,站立并伴有双侧前肢痉挛;V级,IV级的基础上加身体向后倒下、失去平衡、四肢抽动、持续站立、倾倒。
其中I、Ⅱ、Ⅲ级属于部分发作,Ⅳ和V级属于大发作。
判断癫痫动物模型是否符合人类癫痫的标准为一下两条[4]:动物模型发作行为和生物电发放与人类癫痫一致,如无发作症状则脑电图须显示有癫痫样放电即生物电异常发放。
1 最大电休克模型(maximal electroshock model,MES model)MES模型是目前使用最多的模型之一,常常用于模拟人类强直阵挛大发作,并能用于抗强直-阵挛癫痫大发作的药物筛选。


癫痫实验动物模型 The manuscript was revised on the evening of 2021癫痫是大脑神经元突发性异常高频放电,导致短暂的大脑功能障碍的一种神经系统慢性疾病。
癫痫具有自发性和反复性等特点,由于异常放电的神经元在大脑的部位不同,而有多种多样的表现。
新型抗癫痫药都是通过动物模型验证后应用于临床的。
首次推出最大电休克模型(Maximal Electroshock Seizure,MES)一.利用药物制备癫痫模型(药物建模)注射药物,通过破坏脑部神经递质释放的平衡,阻断兴奋性氨基酸的循环通路,诱发癫痫发生。
1.注射合成红藻氨酸制备大鼠癫痫模型红藻氨酸(kainic acid,KA)是海藻的提取物,可作用于脊椎动物中枢神经系统的谷氨酸受体,可直接兴奋神经元,又可增强钠离子的通透性而使神经细胞去极化,诱发癫痫发生。
KA的人工合成品即合成红藻氨酸(synthetical kainic acid,SKA),腹腔注射。
发作阶段性明显,行为学表现规律、稳定,死亡率低,适宜大规模建模。
2.注射氯化锂---匹罗卡品致大鼠癫痫模型近年来一直被认为是研究颞叶癫痫的理想模型。
3.穿刺注射海人酸杏仁核点燃大鼠癫痫模型4.急性氯化铁癫痫模型5.青霉素点燃模型6.戊四唑点燃模型类似人类失神癫痫特征,7.戊四氮(PTZ)诱导的急、慢性癫痫8.杏仁核点刺激点燃模型电极植入,给予连续电刺激。
9.经眼电刺激大鼠癫痫模型二.利用手术制备癫痫模型(手术建模)主要用于模拟外伤后癫痫,机制可能与各神经元细胞之间的突触间连接有关。
外伤后癫痫(posttraumatic epilepsy,PTE)是继发于外伤性颅脑损伤(traumatic brain injury,TBI)的癫痫形式,是常见的最为严重的后遗症。
制作PTE模型要求在体,而非脑片或细胞培养。

氯化锂2匹罗卡品致大鼠急性癫痫模型Ξ高旭光,冯体良,王 军(北京大学人民医院神经内科,北京 100044)摘要:目的 建立氯化锂2匹罗卡品化学诱导的大鼠急性癫痫模型。
方法 雄性Wistar大鼠55只,随机分为生理盐水对照组、地西泮组和致痫组。
氯化锂腹腔注射后10~10h后给予匹罗卡品。
结果 生理盐水对照组大鼠均为0级发作,地西泮组中8只大鼠为0级发作,2只出现Ⅰ级发作;致痫组均达到Ⅲ级以上的痫性发作,其中Ⅲ级2只(2/35),Ⅳ级3只(3/35),Ⅴ级30只(30/35)。
致痫组大鼠在匹罗卡品腹注射后10~90min内全部出现急性痫性发作。
结论 氯化锂2匹罗卡品诱导的大鼠急性癫痫模型具有制作方便、致痫成功率高和动物死亡率低等特点,具有同人类癫痫持续状态和颞叶癫痫相似的行为和脑电图改变。
关键词:氯化锂2匹罗卡品;癫痫持续状态;大鼠;急性癫痫模型中图法分类号:R74211 文献标识码:A 文章编号:1009-881X(2003)04-0308-02Lithium2pilocarpine induced rat model of acute epilepsyG AO Xu2guang,FENG Ti2liang,WANG Jun(neurologic department of Peking University People’s H ospital,Beijing100044)Abstract:Objective T o establish the lithium2pilocarpine induced rat m odel of acute epilepsy.Methods 55Wis2 tar male rats were divided into the m ormal saline control group,diazepam group and seizure2induced group randomly.Pilo2 carpine was injected intraperitoneally(ip)after the10~18hours of the lithium chloride ip.R esults No seizure was found in the normal saline control group,and8rats were stage0attack,2rats were stageⅠin diazepam group.In seizure2induced group,all was above stageⅢ,2rats were stageⅢ(2/35),stageⅣin3rats(3/35),stageⅤin30rats (30/35).All of the seizure2induced rats has presented acute epileptic attack after pilocarpine intraperitoneal injection within10~90minutes.Conclusion Lithium2pilocarpine2induced rats m odel of acute epilepsy was characterized easy building,with high success ful rate and lower m ortality of the animal;This m odel has mimic features of human status epilepticus and tem poral epilepsy in seizure behavior and electroencephalographic findings.K ey w ords:Lithium2pilocarpine;status epilepticus;rat;acute epileptic m odel 氯化锂2匹罗卡品大鼠癫痫模型是H onchar等于1983年首次报道,该模型使匹罗卡品的用量减少,降低了因匹罗卡品毒副作用所造成的动物死亡率。

6 Hz角膜点燃癫痫动物模型的研究进展高青;曾贵荣;欧阳冬生【摘要】耐药性癫痫是临床上癫痫防治的重大难题.癫痫动物模型是研究癫痫发病机制及筛选抗癫痫药物和探究药物作用机制的有力工具,6 Hz角膜点燃癫痫模型是一种优良的耐药性癫痫动物模型,被美国NIH推荐用于评价新药对抗耐药性癫痫的筛选工具.然而,迄今国内外未见6 Hz点燃癫痫动物模型的系统报道,现从该模型的发展历史、制作方法、症状表现、致病机制和应用现状等方面进行综述,以期提供一种探究耐药性癫痫发病机制和筛选耐药性癫痫治疗药物的有力工具和标准模型.【期刊名称】《中国实验动物学报》【年(卷),期】2019(027)003【总页数】6页(P393-398)【关键词】癫痫;6Hz;点燃;动物模型【作者】高青;曾贵荣;欧阳冬生【作者单位】中南大学湘雅医院临床药理研究所,长沙 410008;中南大学临床药理研究所,遗传药理学湖南省重点实验室,长沙 410078;北京协和医学院药用植物研究所,北京 100193;湖南省药物安全评价研究中心/新药药效与安全评价湖南省重点实验室,长沙 410331;中南大学湘雅医院临床药理研究所,长沙 410008;中南大学临床药理研究所,遗传药理学湖南省重点实验室,长沙 410078;复杂基质样本生物分析湖南省重点实验室,长沙 410000【正文语种】中文【中图分类】Q95-33癫痫(epilepsy,EP)是全球最常见的神经系统疾病之一,由多种病因引起,以脑神经元过度放电导致反复性、发作性和短暂性的中枢神经系统功能失常为特征[1]。
耐药性癫痫是临床上癫痫防治的重大难题,虽然近些年来已有不少抗癫痫药物(antiepileptic drugs,AEDs)面世,但仍有20%~30%的患者对AEDs治疗反应差,癫痫发作难以控制,且通常伴随多种严重并发症的发生[2]。
癫痫动物模型是研究致痫机制和筛选AEDs的重要手段,Openchowski等[3]于1883年首次采用冷冻大脑组织制作脑内致痫灶,成为癫痫模型制备的开端。

癫痫的动物模型一、简介癫痫症是最常见的神经系统疾病之一,其患病率在一般人口中每1000人约有5人。
根据世界卫生组织的定义,癫痫症是由先天或后天不同因素所引起的慢性脑疾病,其特征是反复性惊厥发作,伴随不同的临床和脑电图的表现。
因此,癫痫症(epilepsy)是一反复发作的临床症候群,而因一过性异常的一次脑细胞放电所引起的神经系统功能失常称为惊厥(Seizure),惊厥是临床的行为活动,一次惊厥发作不一定表示有癫痫症。
目前,国内所用的癫痫分类方法是以国际抗癫痫联盟(ILAE)1981年和1985年的分类法。
但为了兼顾临床和实验室研究,本章所讨论的癫痫现象主要根据1981年的分类,此分类法主要以临床表现及EEG为依据将癫痫分为:全身性和部分性癫痫。
迄今研究人类癫痫的发病机理仍主要依靠动物实验,癫痫产生机制的探讨及最新进展亦多直接或间接来于动物模型研究。
目前已有数十种动物模型应用于癫痫研究,选择适宜的实验模型取决于所需解决的问题、所需的癫痫类型,与临床发作的一致性以及是否简单可靠。
因此,选择适当、有价值的癫痫动物模型是有效研究癫痫机制及治疗的捷径。
现已发展并建立了类似临床癫痫类型的多种癫痫模型(表I),包括整体与离体、脑片与细胞模型,为探讨癫痫形成的机制及观察药物治疗疗效提供了有利的工具。
然而,如何合理、适当地应用这些动物模型是我们进行研究时首先应当考虑的,否则既浪费时间、精力与钱财,又不能得到可靠的结果。
以下分别介绍各种类型癫痫动物模型的利与弊。
表I:癫痫的动物模型1. 急性简单部分性 3. 复杂部分性 6. 脑组织表面致惊剂卡因酸海马脑片青霉素Tetanus toxin 原代分离细胞培养荷包牡丹碱点燃人类神经组织印防已毒 4. 全身强直-阵挛7. 癫痫持续状态士的宁遗传性胆碱能药物光敏狒狒急性电刺激听源性惊厥小鼠去除GABA Totterer 和E1 小鼠新皮层脑片遗传性癫痫易感大鼠2. 慢性简单部分性蒙古沙土鼠皮层埋置金属最大电休克氢氧化铝化学致惊剂钴代谢性derangements钨铁 5. 全身性失神冷冻损伤神经节苷脂抗体注射静脉注射致痫剂二、急性简单部分性癫痫模型这类模型是一组急性皮层损伤所致的惊厥放电。
神经系统疾病动物模型的具体步骤及方法人类疾病的发展十分复杂,以人本身作为实验对象来深入探讨疾病发生机制,推动医药学的发展之过程缓慢,临床积累的经验不仅在时间和空间上都存在局限性,而且许多实验在道义上和方法上也受到限制。
而借助于动物模型的间接研究,可以有意识地改变那些在自然条件下不可能或不易排除的因素,以便更准确地观察模型的实验结果,并与人类疾病进行比较研究,有助于更方便、更有效地认识人类疾病的发生、发展规律,研究防治措施。
人类疾病动物模型(animal model of human disease)是指各种医学科学研究中建立的具有人类疾病模拟表现的动物。
动物模型主要用于实验生理学、实验病理学和实验治疗学研究。
神经疾病动物模型的复制,是用人为的方法,使动物在一定的致病因素(物理、化学、生物)作用下,造成动物神经组织、器官或全身一定程度的损害,出现某些类似人类神经疾病的功能、代谢、形态结构方面的变化或各种疾病,通过这种手段来研究人类疾病的发生、发展规律,为研究人类神经系统疾病的预防、治疗提供理论依据。
根据神经系统的解剖,可将神经疾病动物模型分为周围神经系统疾病动物模型和中枢神经系统疾病动物模型。
根据致病因素可分为外伤动物模型、代谢障碍动物模型、发育异常动物模型、遗传代谢障碍动物模型、精神障碍动物模型及其他动物模型等。
另外,根据发病部位,除按周围或中枢神经系统大范围的分类以外,还可按具体的部位分为不同的模型。
一、周围神经疾病动物模型周围神经损伤虽然仅占全部创伤的1.5%~4.0%,但其可引起严重的肢体功能障碍,主要以运动障碍、感觉障碍和营养障碍为主,有较高的致残率。
周围神经损伤部位及程度不同,所产生的临床症状也不尽相同。
因周围神经解剖和功能上的特殊性,选择适当的实验动物与模型建立方法,对周围神经损伤修复研究有着深远的影响。
根据神经损伤的类型,主要分为卡压伤、牵拉伤及离断伤等。
卡压伤为周围神经行经某部骨纤维管。
癫痫发作模型的标准
癫痫发作模型的标准通常包括以下几个方面:
1. 发作行为:模型中的动物应该表现出与人类癫痫患者类似的癫痫发作行为,例如肢体抽搐、失禁、意识丧失等。
这些行为可以通过观察动物的行为表现或电生理记录来确定。
2. 癫痫发作特征:模型应该具有与特定类型的癫痫发作相关的电生理特征,例如癫痫放电、脑电图异常等。
这些特征可以通过使用电极记录动物的脑电图来确定。
3. 阈值和易感性:模型中的动物应该对于触发癫痫发作的刺激具有一定的阈值和易感性。
这意味着只有在特定条件下,例如应用特定药物或刺激,动物才会表现出癫痫发作。
阈值和易感性可以通过调整刺激强度或药物剂量来确定。
4. 可逆性:模型中的癫痫发作应该是可逆的,即在停止刺激或处理后,动物应该能够恢复到正常状态。
这可以通过观察动物在发作后的恢复行为或电生理记录来确定。
综上所述,癫痫发作模型的标准包括发作行为、癫痫发作特征、阈值和易感性以及可逆性。
这些标准可以帮助研究人员确定和评估癫痫发作模型的有效性和可靠性。
海人藻酸建立内侧颞叶癫痫小鼠模型的研究叶祖亮;苗育静;刘全磊;魏鹏虎;朱权【期刊名称】《中国实验动物学报》【年(卷),期】2024(32)5【摘要】目的本研究采用立体定向手术在一侧海马注射海人藻酸(kainic acid, KA),建立内侧颞叶癫痫(medial temporal lobe epilepsy, MTLE)慢性模型,通过行为学、电生理学和病理学验证其有效性。
方法取健康的C57BL/6野生型雄鼠22只,随机分成对照组(n=6)和实验组即KA注射组(n=16)。
对照组和实验组分别在海马CA3区进行微量注射生理盐水和KA,1周后再次进行立体定向手术,植入脑电记录电极。
植入术后1周开始记录小鼠脑电活动,统计癫痫发作次数和持续时间。
通过对小鼠的观察与记录,分别从行为学、电生理学和病理学方面验证慢性癫痫模型。
结果本实验对22只C57BL/6野生型雄鼠进行实验,对照组均无癫痫发作,而实验组存活的小鼠均出现癫痫发作。
成模的小鼠在行为学上发生了凝视、咀嚼、头面部肌肉抽搐、肢体痉挛等慢性癫痫自发发作行为,有2只小鼠因手术死亡、4只小鼠在急性发作期死亡、10只小鼠模型成功建立;脑电图呈内侧颞叶癫痫样脑电图改变;在病理组织学方面,经免疫荧光染色发现:CA3区神经元丢失,星形胶质细胞大量增生,符合海马硬化特征性的病理改变。
结论通过使用KA单侧、单次颅内注射构建的模型具有耗时、易操作、易成型等多项优势,该模型展现出与人类MTLE相似的脑电图、行为与神经病理改变,有助于研究治疗颞叶癫痫的药物,是癫痫外科手术预后判断的理想动物模型。
【总页数】8页(P648-655)【作者】叶祖亮;苗育静;刘全磊;魏鹏虎;朱权【作者单位】山西医科大学第一临床医学院;山西医科大学第一医院神经外科;首都医科大学宣武医院神经外科【正文语种】中文【中图分类】Q95-33【相关文献】1.构建海人酸诱导的内侧颞叶癫痫小鼠模型AAT/增强子结合蛋白同源蛋白与钙联蛋白在内侧颞叶癫痫模型小鼠海马中的表达3.生长相关蛋白-43在内侧颞叶癫痫小鼠模型海马中的表达4.锂-匹罗卡品致颞叶癫痫小鼠模型的建立及苔藓纤维出芽的实验研究5.维拉帕米对慢性颞叶内侧癫痫模型大鼠抗癫痫药物分布的影响因版权原因,仅展示原文概要,查看原文内容请购买。