(完整版)原子物理学复习资料
- 格式:doc
- 大小:361.51 KB
- 文档页数:15

原子物理学总复习指导名词解释:光谱,氢原子线系,类氢离子,电离电势,激发电势,原子空间取向量子化,原子实极化,轨道贯穿,有效电荷数,电子自旋,磁矩,旋磁比,拉莫尔进动,拉莫尔频率,朗德g因子,电子态,原子态,塞曼效应,电子组态,LS耦合,jj耦合,泡利原理,同科电子,元素周期表,壳层,原子基态,洪特定则,朗德间隔定则数据记忆:电子电量,质量,普朗克常量,玻尔半径,氢原子基态能量,里德堡常量,hc,ħc,玻尔磁子,拉莫尔进动频率著名实验的内容、现象及解释:α粒子散射实验,夫兰克—赫兹实验,施特恩—盖拉赫实验,碱金属光谱的精细结构,塞曼效应,反常塞曼效应,康普顿效应理论解释:(汤姆逊原子模型的不合理性),卢瑟福核式模型的建立、意义及不足,玻尔氢原子光谱理论的建立、意义及不足,元素周期表计算公式:氢原子光谱线系,玻尔理论能级公式、波数公式,角动量表达式及量子数取值(l,s,j),LS耦合原子态,朗德间隔定则,g因子,塞曼效应,原子基态谱线跃迁图:氢原子谱线跃迁、类氢原子谱线跃迁,碱金属原子能级跃,精细结构,塞曼效应;电子态及组态、原子态表示,选择定则,1.同位素:一些元素在元素周期表中处于同一地位,有相同原子序数,这些元素别称为同位素。
2.类氢离子:原子核外只有一个电子的离子,这类离子与氢原子类似,叫类氢离子。
3.电离电势:把电子在电场中加速,如使它与原子碰撞刚足以使原子电离,则加速时跨过的电势差称为电离电势。
4.激发电势:将初速很小的自由电子通过电场加速后与处于基态的某种原子进行碰撞,当电场电压升到一定值时,发生非弹性碰撞,加速电子的动能转变成原子内部的运动能量,使原子从基态激发到第一激发态,电场这一定值的电压称为该种原子的第一激发电势5. 原子空间取向量子化:在磁场或电场中原子的电子轨道只能取一定的几个方向,不能任意取向,一般的说,在磁场或电场中,原子的角动量的取向也是量子化的。
6. 原子实极化:当价电子在它外边运动时,好像是处在一个单位正电荷的库伦场中,当由于价电子的电场的作用,原子实中带正电的原子核和带负电的电子的中心会发生微小的相对位移,于是负电的中心不再在原子核上,形成一个电偶极子,这就是原子实的极化。

原子物理复习资料一、原子的结构原子是由位于中心的原子核和核外电子组成的。
原子核带正电荷,电子带负电荷,它们之间的静电引力使得电子围绕原子核做高速运动。
原子核由质子和中子组成,质子带正电,中子不带电。
原子的质子数决定了它的元素种类,而质子数和中子数共同决定了原子的质量数。
电子在原子核外分层排布,离核越近的电子能量越低,越稳定;离核越远的电子能量越高,越不稳定。
二、原子的能级和跃迁原子中的电子只能处于一系列不连续的能量状态,这些能量状态称为能级。
处于基态的原子是最稳定的,当原子吸收一定能量的光子或与其他粒子发生碰撞时,电子会从低能级跃迁到高能级;反之,电子会从高能级跃迁到低能级,同时释放出光子。
跃迁过程中吸收或释放的光子能量等于两个能级的能量差,即$h\nu = E_{m} E_{n}$,其中$h$ 是普朗克常量,$\nu$ 是光子的频率,$E_{m}$和$E_{n}$分别是高能级和低能级的能量。
三、氢原子的能级结构对于氢原子,其能级公式为$E_{n} =\frac{136}{n^2} \text{eV}$,其中$n$ 是量子数,$n = 1, 2, 3, \cdots$。
当$n = 1$ 时,对应的能级为基态,能量为$-136 \text{eV}$;当$n = 2$ 时,对应的能级为第一激发态,能量为$-34 \text{eV}$;以此类推。
氢原子从高能级向低能级跃迁时,可以发出一系列不同频率的光子,形成线状光谱。
四、光电效应当光照射到金属表面时,金属中的电子会吸收光子的能量,如果吸收的能量足够大,电子就能从金属表面逸出,这种现象称为光电效应。
光电效应的实验规律:1、存在饱和电流,光电流的强度与入射光的强度成正比。
2、存在遏止电压,与入射光的频率有关,而与入射光的强度无关。
3、存在截止频率(红限),当入射光的频率低于截止频率时,无论光强多大,都不会产生光电效应。
爱因斯坦提出了光子说,成功解释了光电效应。

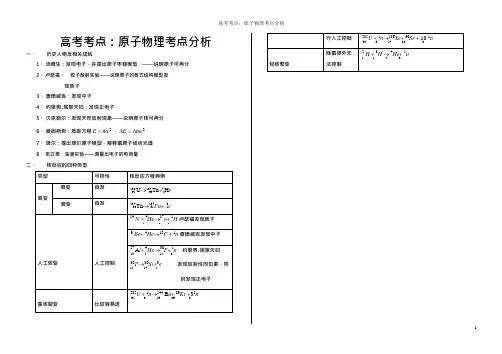
高考考点:原子物理考点分析一、历史人物及相关成就1、汤姆生:发现电子,并提出原子枣糕模型——说明原子可再分2、卢瑟福:粒子散射实验——说明原子的核式结构模型发现质子3、查德威克:发现中子4、约里奥.居里夫妇:发现正电子5、贝克勒尔:发现天然放射现象——说明原子核可再分6、爱因斯坦:质能方程E =mc2,∆E =∆mc27、玻尔:提出玻尔原子模型,解释氢原子线状光谱8、密立根:油滴实验——测量出电子的电荷量二、核反应的四种类型类型可控性核反应方程典例衰变衰变自发238 U→234 Th+4 H e92 90 2衰变自发234 Th→234Pa+0e90 91 -114N +4He→17o+1H 卢瑟福发现质子7 2 8 19Be+4He→12C +1n 查德威克发现中子4 2 6 0人工转变人工控制27A l +4He→30P+1n 约里奥.居里夫妇13 2 15 030P→30Si+0e 发现放射性同位素,同15 14 1时发现正电子重核裂变比较容易进235U +1n→144 B a+89Kr +31n92 0 56 36 0行人工控制235U +1n→136Xe+90Sr + 10 1n92 0 54 38 0轻核聚变除氢弹外无法控制2H +3H →4He+1n1 12 0提醒:1、核反应过程一般都是不可逆的,所以核反应方程只能用单箭头表示反应方向,不能用等号连接。
2、核反应的生成物一定要以实验事实为基础,不能凭空只依据两个守恒定律杜撰出生成物来写出核反应方程3、核反应遵循质量数守恒而不是质量守恒,遵循电荷数守恒射线( 4He)2 射线( 0e)1射线提醒:1、半衰期:表示原子衰变一半所用时间2、半衰期由原子核内部本身的因素据顶,跟原子所处的物理状态(如压强、温度)或化学状态(如单质、化合物)无关3、半衰期是大量原子核衰变时的统计规律,个别原子核经多长时间衰变无法预测,对个别或极少n1 数原子核,无半衰期而言。



原子物理学总复习指导名词解释:光谱,氢原子线系,类氢离子,电离电势,激发电势,原子空间取向量子化,原子实极化,轨道贯穿,有效电荷数,电子自旋,磁矩,旋磁比,拉莫尔进动,拉莫尔频率,朗德g因子,电子态,原子态,塞曼效应,电子组态,LS耦合,jj 耦合,泡利原理,同科电子,元素周期表,壳层,原子基态,洪特定则,朗德间隔定则数据记忆:电子电量,质量,普朗克常量,玻尔半径,氢原子基态能量,里德堡常量,hc,?c,玻尔磁子,拉莫尔进动频率著名实验的内容、现象及解释:a粒子散射实验,夫兰克一赫兹实验,施特恩一盖拉赫实验,碱金属光谱的精细结构,塞曼效应,反常塞曼效应,康普顿效应理论解释:(汤姆逊原子模型的不合理性),卢瑟福核式模型的建立、意义及不足,玻尔氢原子光谱理论的建立、意义及不足,元素周期表计算公式:氢原子光谱线系,玻尔理论能级公式、波数公式,角动量表达式及量子数取值(I,S, j ),LS耦合原子态,朗德间隔定则,g因子,塞曼效应,原子基态谱线跃迁图:氢原子谱线跃迁、类氢原子谱线跃迁,碱金属原子能级跃,精细结构,塞曼效应;电子态及组态、原子态表示,选择定则,1. 同位素:一些元素在元素周期表中处于同一地位,有相同原子序数,这些元素别称为同位素。
2. 类氢离子:原子核外只有一个电子的离子,这类离子与氢原子类似,叫类氢离子3. 电离电势:把电子在电场中加速,如使它与原子碰撞刚足以使原子电离,则加速时跨过的电势差称为电离电势。
4. 激发电势:将初速很小的自由电子通过电场加速后与处于基态的某种原子进行碰撞,当电场电压升到一定值时,发生非弹性碰撞,加速电子的动能转变成原子内部的运动能量,使原子从基态激发到第一激发态,电场这一定值的电压称为该种原子的第一激发电5. 原子空间取向量子化:在磁场或电场中原子的电子轨道只能取一定的几个方向,不能任意取向,一般的说,在磁场或电场中,原子的角动量的取向也是量子化的。
6. 原子实极化:当价电子在它外边运动时,好像是处在一个单位正电荷的库伦场中,当 由于价电子的电场的作用,原子实中带正电的原子核和带负电的电子的中心会发生微小 的相对位移,于是负电的中心不再在原子核上,形成一个电偶极子,这就是原子实的极 化。

第一章 原子的基本状况一、学习要点1.原子的质量和大小,R ~ 10-10 m , N o =×1023/mol2.原子核式结构模型 (1)汤姆孙原子模型(2)α粒子散射实验:装置、结果、分析 (3)原子的核式结构模型 (4)α粒子散射理论: 库仑散射理论公式:(5)原子核大小的估计 (会推导): 散射角θ:),2sin11(Z 241220θπε+⋅=Mv e r mα粒子正入射:2024Z 4Mv e r m πε= ,m r ~10-15-10-14 m二、基本练习1.选择(1)原子半径的数量级是: A .10-10cm; C. 10-10m(2)原子核式结构模型的提出是根据α粒子散射实验中: A.绝大多数α粒子散射角接近180︒ B.α粒子只偏2︒~3︒ C.以小角散射为主也存在大角散射 D.以大角散射为主也存在小()(X)Au AA g M N ==12-27C 1u 1.6605410kg12==⨯的质量22012c 42v Ze b tgM θπε=角散射(3)用相同能量的α粒子束和质子束分别与金箔正碰,测量金原子核半径的上限. 问用质子束所得结果是用α粒子束所得结果的几倍 A. 1/4 B . 1/2 C . 1 D. 24一强度为I 的α粒子束垂直射向一金箔,并为该金箔所散射。
若θ=90°对应的瞄准距离为b ,则这种能量的α粒子与金核可能达到的最短距离为:A. b ; B . 2b ; C. 4b ; D. 。
2.简答题(1)简述卢瑟福原子有核模型的要点.(2)简述α粒子散射实验. α粒子大角散射的结果说明了什么 3.褚书课本P 20-21:(1).(2).(3);第二章 原子的能级和辐射 一、学习要点:1.氢原子光谱:线状谱、4个线系(记住名称、顺序)、广义巴尔末公式)11(~22nmR -=ν、光谱项()2n R n T =、并合原则:)()(~n T m T -=ν2.玻尔氢原子理论:(1)玻尔三条基本假设的实验基础和内容(记熟)(2)圆轨道理论(会推导):氢原子中假设原子核静止,电子绕核作匀速率圆周运动02200202220A 529,04,Z Z 4≈===e m a n a n e m r e e n πεπε;13714,Z Z 40202≈===c e n c n e c e n πεααπευ; ()n hcT n hc R n e m E e n --=-=∞2222422Z 2Z )41(πε,n =1.……(3)实验验证:(a )氢原子4个线系的形成)11(Z ~,)4(222232042n m R ch e m R e -==∞∞νπεπ (会推导)非量子化轨道跃迁)(212n E E mv h -+=∞ν (b )夫-赫实验:装置、.结果及分析;原子的电离电势、激发电势 3.类氢离子(+++Li ,He ,正电子偶素.-μ原子等)(1) He +光谱:毕克林系的发现、波数公式、与氢原子巴耳末系的异同等 (2)理论处理(会推导):计及原子核的运动,电子和原子核绕共同质心作匀速率圆周运动ee m M m M +⋅=μ, 正负电荷中心之距Ze n r n 22204μπε =.能量224222Z )41(ne E n μπε-=,里德伯常数变化Mm R R eA +=∞11重氢(氘)的发现 4.椭圆轨道理论索末菲量子化条件q q n h n pdq ,⎰=为整数a nn b n e m a n e m E n p e n ϕϕϕπεπε==-==,Z 4,2Z )41(,222022422,n n n ,,3,2,1;,3,2,1 ==ϕn 一定,n E 一定,长半轴一定,有n 个短半轴,有n 个椭圆轨道(状态),即n E 为n 度简并。

《原子物理学》复习参考答案一、选择题1、C2、B3、A4、D5、A6、B7、C8、C9、B10、C二、填空题1、结构;性质2、kg-27.1106792123、核式定态结构模型4、800015、电磁辐射(不论在可见区或在可见区以外)的波长成分和强度成分6、线状光谱;带状光谱;连续光谱7、-13.68、(1)原子只能较长久地停留在一些稳定状态(简称定态);(2)原子从一个定态跃迁到另一个定态而发射或吸收辐射时,辐射的频率是一定的。
9、夫兰克-赫兹10、⎰⋯⋯==).3,2,1(n nh pdq11、0.04112、1.2413、原子实的极化;轨道在原子实中的贯穿14、1,0,1±=∆±=∆j l15、316、317、电子的轨道运动;电子的自旋运动18、单层;三层19、J S X 12+20、13S ;01S21、l s m m l n ,,,22、抗磁性;顺磁性;铁磁性23、单层;三层24、电子在靶上被减速25、0.012426、分子的电子运动状态和电子能级;构成分子的诸原子之间的振动和振动能级;分子的转动和转动能级27、中微子28、质子;中子;电子;光子29、万有引力作用;弱相互作用;电磁相互作用;强相互作用三、简答题1、答:玻尔理论中的普遍规律的内容:(1)原子只能较长久地停留在一些稳定状态(简称定态);(2)原子从一个定态跃迁到另一个定态而发射或吸收辐射时,辐射的频率是一定的。
2、答:泡利不相容原理:在费米子体系中不允许有两个或两个以上的费米子处在同一个量子态。
3、答:一部分是波长连续变化的,称为连续谱,另一部分是具有各别波长的线状谱,称为标识谱。
4、答:原子核自发地放射 射线的现象称为放射性衰变。
四、计算题1、fm E Ze Z b C e eV MeV E Z Z E Ze Z b b ZeZ E MV E b Ze Z MV k k k k k 4.371074.32120cot 1060.110121085.84)1060.1(9012cot 24'1085.8,1060.1120,1010.1901'2cot 24''242cot 2'42cot 14-19-612-19-021-12-019-60220222021-=⨯=︒⨯⨯⨯⨯⨯⨯⨯⨯⨯⨯⨯=•=∴•••⨯=⨯=︒=⨯====•=∴=∴==米米伏秒安,,已知且公式:解:根据其他粒子散射πθπεεθθπεπεθπεθ2、nm cm R R R R R R R R R R n nR n R D H DH H D D H DH 1786.010786.1100967758.10970742.1100967758.1-0970742.1536100970742.1100967758.1536)11(53653631-21131-211)1-211~8551-51-5222222=⨯=⨯⨯⨯⨯=∆∴⨯=⨯=-⨯=-=∆∴-=∆==∴====-)()(厘米,厘米已知且)(谱线,则巴耳末线系的第一条光)(得:(公式:线膨胀波长可由里德伯解:巴耳末系第一条谱λλλλλλλλν 3、eVU eV J h nmch h eV U eV J h nmc h ch h 18.511.307.211.31097.4104001031062620.640007.207.21031.3106001031062620.66001031062620.619-9-834-119-9-834-81-1-34-11-=+=∴=⨯=⨯⨯⨯⨯=∴===∴=⨯=⨯⨯⨯⨯=∴=•⨯=•••⨯==∞∞∞∞∞∞该原子的电离电势为:且又该原子第一激发电势,秒米,米伏秒安已知νλλνυλλνΘΘ 4、122123212121211,2,33212121232123211,223,21252125212,325,2123,25,2121,2,0.1,2,3212200,1;221,2,0);()。

高三物理复习资料 原子物理基础知识一、黑体和黑体辐射1.热辐射现象: 任何物体在 任何 温度下都要发射 各种 波长的电磁波,并且其辐射能量的大小及辐射能量按波长的分布都与 温度 有关,所以称为热辐射。
2.黑体:物体具有 辐射 能量的本领,又有吸收外界辐射来的能量的本领。
绝对黑体(简称“黑体”)是指能够完全吸收入射的各种(填“各种”或“部分”)波长电磁波而不发生反射的物体,而黑体辐射电磁波的强度按波长的分布只与黑体的 温度 有关。
3.实验规律:(1)随着温度的升高,黑体的辐射强度都有增加;(2)随着温度的升高,辐射强度的极大值向 波长较短 方向移动。
二、、光电效应现象 1、光电效应:光电效应:物体在光 包括 不可见光的照射下发射电子的现象称为光电效应。
2、光电效应的研究结论:① 任何 金属,都有一个极限频率,入射光的频率必须 大于 这个极限频率,才能产生光电效应; 低于 这个频率的光不能产生光电效应。
②光电子的最大初动能与入射光的强度 无关 ,只随着入射光频率的增大而 增大 。
③入射光照到金属上时,光电子的发射几乎是瞬时的,一般不超过10-9s ;④当入射光的频率大于极限频率时,入射光的强度越强,单位时间内发射的电子数 越多 。
3、光电效应的应用:光电管:光电管的阴极表面敷有 碱 金属,对电子的束缚能力比较弱,在光的照射下容易发射电子,阴极发出的电子被阳极收集,在回路中形成电流,称为 光电流 。
注意:①光电管两极加上正向电压,可以增强光电流。
②光电流的大小跟入射光的强度和正向电压有关,与入射光的频率无关。
入射光的强度越大,光电流越大。
③遏止电压U 0。
回路中的光电流随着反向电压的增加而减小,当反向电压U 0满足:02max 21eU mv ,光电流将会减小到零,所以遏止电压与入射光的 频率 有关。
4、波动理论无法解释的现象:①不论入射光的频率多少,只要光强足够大,总可以使电子获得足够多的能量,从而产生光电效应,实际上如果光的频率小于金属的极限频率,无论光强多大,都不能产生光电效应。

原子物理学复习题# 原子物理学复习题## 一、基本概念1. 原子模型的发展:- 描述汤姆森模型、卢瑟福模型和玻尔模型的主要特点。
2. 量子数:- 解释主量子数、角动量量子数和磁量子数的概念及其物理意义。
3. 波函数和概率密度:- 描述波函数在量子力学中的作用以及如何通过波函数计算电子在原子内的概率密度分布。
4. 泡利不相容原理:- 阐述泡利不相容原理的内容及其对原子结构的影响。
## 二、原子光谱1. 发射光谱与吸收光谱:- 区分发射光谱和吸收光谱,并解释它们在原子物理学中的应用。
2. 巴尔末系和莱曼系:- 描述氢原子光谱的巴尔末系和莱曼系,并解释它们如何与能级跃迁相关。
3. 精细结构和超精细结构:- 解释原子光谱中的精细结构和超精细结构现象及其原因。
## 三、原子核物理1. 核力的性质:- 描述核力的短程、饱和性和交换对称性等特性。
2. 核衰变类型:- 列举并解释α衰变、β衰变和γ衰变的特点。
3. 核反应:- 描述核反应的一般过程,包括核裂变和核聚变。
## 四、量子力学基础1. 海森堡不确定性原理:- 阐述海森堡不确定性原理的内容及其在量子力学中的重要性。
2. 薛定谔方程:- 解释薛定谔方程的形式和物理意义。
3. 量子态的叠加原理:- 描述量子态叠加原理及其在量子计算中的应用。
## 五、原子结构与化学键1. 电子排布与元素周期表:- 描述电子在原子中的排布规律以及元素周期表的结构。
2. 离子键、共价键和金属键:- 区分离子键、共价键和金属键,并解释它们在物质结构中的作用。
3. 分子轨道理论:- 简述分子轨道理论的基本原理及其在化学中的应用。
## 六、实验方法1. 光谱分析:- 描述光谱分析在原子物理学中的应用,包括发射光谱和吸收光谱分析。
2. 粒子加速器:- 解释粒子加速器的工作原理及其在高能物理实验中的重要性。
3. 核磁共振(NMR):- 描述核磁共振的原理和它在化学和医学中的应用。
## 七、原子物理学的应用1. 半导体物理学:- 简述半导体物理学的基本原理及其在电子器件中的应用。
原子物理学复习总结提纲I.引言
A.原子物理学概述
B.原子结构的发现历程
II.原子结构
A.原子的基本组成
B.原子的大小和质量
C.原子核的结构
1.质子和中子
2.原子核的稳定性和不稳定性
D.原子壳层结构
1.电子的概念和特性
2.原子层能级
3.壳层填充规则
III.原子光谱
A.光的性质和特性
B.原子光谱的产生机制
C.原子发射光谱
1.电子激发
2.原子的激发态和基态
3.能级跃迁和发射光谱
D.原子吸收光谱
1.光的吸收和衰减
2.能级跃迁和吸收光谱IV.原子核物理学
A.原子核的性质和特性
B.原子核的稳定性和放射性
1.放射性的概念和分类
2.放射性衰变的过程和特征
C.核反应和核能
1.核反应的概念和条件
2.核能及其应用
V.原子物理学的应用
A.核技术与核工程
1.核裂变与核聚变
2.核电站和核燃料循环
B.医学影像学和放射治疗
1.X射线和CT扫描
2.放射治疗的原理和应用
C.等离子体物理学
1.等离子体的概念和性质
2.等离子体的应用和研究VI.总结
A.原子物理学的重要性和意义
B.原子物理学的发展前景
C.总结复习要点。
第一章 原子的基本状况一、学习要点1.原子的质量和大小,R ~ 10-10 m , N o =6.022×1023/mol2.原子核式结构模型 (1)汤姆孙原子模型(2)α粒子散射实验:装置、结果、分析 (3)原子的核式结构模型 (4)α粒子散射理论: 库仑散射理论公式:(5)原子核大小的估计 (会推导): 散射角θ:),2sin11(Z 241220θπε+⋅=Mv e r mα粒子正入射:2024Z 4Mv e r m πε=,m r ~10-15-10-14 m二、基本练习1.选择(1)原子半径的数量级是:A .10-10cm; B.10-8m C. 10-10m D.10-13m (2)原子核式结构模型的提出是根据α粒子散射实验中:A.绝大多数α粒子散射角接近180︒B.α粒子只偏2︒~3︒C.以小角散射为主也存在大角散射D.以大角散射为主也()(X)Au AA g M N ==12-27C 1u 1.6605410kg12==⨯的质量22012c 42v Ze b tgM θπε=存在小角散射(3)用相同能量的α粒子束和质子束分别与金箔正碰,测量金原子核半径的上限. 问用质子束所得结果是用α粒子束所得结果的几倍?A. 1/4 B . 1/2 C . 1 D. 2 4一强度为I 的α粒子束垂直射向一金箔,并为该金箔所散射。
若θ=90°对应的瞄准距离为b ,则这种能量的α粒子与金核可能达到的最短距离为:A. b ; B . 2b ; C. 4b ; D. 0.5b 。
2.简答题(1)简述卢瑟福原子有核模型的要点.(2)简述α粒子散射实验. α粒子大角散射的结果说明了什么? 3.褚书课本P 20-21:(1).(2).(3);第二章 原子的能级和辐射一、学习要点:1.氢原子光谱:线状谱、4个线系(记住名称、顺序)、广义巴尔末公式)11(~22nmR -=ν、光谱项()2nR n T =、并合原则:)()(~n T m T -=ν2.玻尔氢原子理论:(1)玻尔三条基本假设的实验基础和内容(记熟)(2)圆轨道理论(会推导):氢原子中假设原子核静止,电子绕核作匀速率圆周运动02200202220A529,04,Z Z 4≈===e m a n a n e m r e e n πεπε;13714,Z Z 40202≈===c e n c n e c e n πεααπευ;()n hcT n hc R n e m E e n --=-=∞2222422Z 2Z )41(πε,n =1.2.3……(3)实验验证:(a )氢原子4个线系的形成)11(Z ~,)4(222232042n m R ch e m R e -==∞∞νπεπ (会推导)非量子化轨道跃迁)(212n E E mv h -+=∞ν (b )夫-赫实验:装置、.结果及分析;原子的电离电势、激发电势3.类氢离子(+++Li ,He ,正电子偶素.-μ原子等)(1) He +光谱:毕克林系的发现、波数公式、与氢原子巴耳末系的异同等(2)理论处理(会推导):计及原子核的运动,电子和原子核绕共同质心作匀速率圆周运动ee m M m M +⋅=μ, 正负电荷中心之距Ze n r n 22204μπε =.能量224222Z )41(n e E n μπε-=,里德伯常数变化Mm R R eA +=∞11重氢(氘)的发现 4.椭圆轨道理论索末菲量子化条件q q n h n pdq ,⎰=为整数a nn b n e m a n e m E n p e n ϕϕϕπεπε==-==,Z 4,2Z )41(,222022422,n n n ,,3,2,1;,3,2,1 ==ϕn 一定,n E 一定,长半轴一定,有n 个短半轴,有n 个椭圆轨道(状态),即n E 为n 度简并。
原子物理学(褚圣麟编著高等教育出版社)第一章 原子的基本状况1、α粒子散射实验结论p9:卢瑟福的α粒子散射实验观察到,绝大多数电子只有2~3度的偏转,有1/8000的α粒子偏转大于90°,其中有接近180°的。
2、卢瑟福散射公式p13:22224014sin 2Ze d Ωd Mv σθπε⎛⎫⎛⎫= ⎪ ⎪⎝⎭⎝⎭,d σ是立体角d Ω内每个原子的散射截面 dnd Ntnσ=;N 为薄膜中单位体积中原子的个数;t 为薄膜厚度;有n 个α粒子射到薄膜上,其中d n 个落在d Ω中第二章 原子的能级和辐射1、光谱的分类p23:(1)线装光谱:是原子所发的; (2)带状光谱:是分子所发的;(3)连续光谱:固体加热所发的,原子和分子在某些情况下也会发连续光谱。
2、波数p243、谱线系p25(m < n , m = 1,2,3…),表示第m 条谱线到第n 条谱线的能量差;对于氢原子,Z = 1。
R 是里德伯常数,它由11/e R R m M∞=+确定,其中M 是原子核质量,m e 是绕核旋转的电子的质量.对于氢原子,R H = 1.09677576×107 m -1。
m = 1时的谱线系称为赖曼系;m = 2时的谱线系称为巴耳末系; m = 3时的谱线系称为帕邢系; m = 4时的谱线系称为布喇开系; m = 5时的谱线系称为普丰特系。
4、原子的能量p29:2hcRE n=-5、氢原子半径p3021n r a Z =,2012244h a meπεπ=.对于氢原子,a 1 = 0.529166×10-10m.6、氢原子能级p31212Z E E n =,2412202(4)me E hππε=-.对于氢原子,E 1 = -13.59 eV . 7、折合质量p39若不满足m << M ,则计算时的质量m 需要使用折合质量MmM mμ=+.8、电离电势(ionizing potential )p46在赖曼系中取n = ∞求得,则电离电势为.9、激发电势(excitation potential )p42原子由第m 条谱线激发到第n 条谱激发电势为.10、两个实验p42 p55:(1)夫兰克—赫兹实验证明原子能级的存在(2)史特恩—盖拉赫实验证明原子空间取向的量子化第三章 量子力学初步1、光子的能量p78E h ν=2、德布罗意(de Broglie )波长p79h pλ=3、不确定性原理(Uncertainty principle )p82/2p x ∆∆≥, /2E t ∆∆≥4、薛定谔方程(Schrodinger equation )p89定态薛定谔方程(time-independent Schrodinger equation ):5、球坐标下的薛定谔方程p1046、波函数必须满足的三个条件:有限;连续;单值(唯一) 7、五个量子数主量子数n = 1, 2, 3 ···角量子数l = 0, 1, 2 ··· (n - 1)角量子数在z 轴的分量(磁量子数)m l = 0, ±1, ±2, ··· ±l 自旋量子数s = 1/2自旋量子数在z 轴的分量m s = ±1/2第四章 碱金属原子和电子自旋1、四种线系2、锂(Li)3、钠(Na)4、碱金属的光谱项表达式*22(Δ)R RT n n ==- 5、原子实的极化和轨道贯穿使电子的能级偏低,其中轨道贯穿影响较大。
原子物理学总复习大纲第一章 原子模型 纲要1.原子的大小和质量原子的线度r 约在10-10米数量级.原子的质量使用原子质量单位u,1u 为1个碳原子12C 质量的1/12,1u=1.6605402×10-27千克.2.卢瑟福核式结构几种结构模型:汤姆逊枣糕模型(西瓜模型)、长冈半太郎土星模型、卢瑟福核式结构模型。
卢瑟福核式结构模型:原子是由原子核和核外电子组成的,原子核带正电荷Ze ,几乎集中了原子的全部质量,核外电子在核的库存仑场中绕核运动.与实验结果符合最好。
原子核的线度r 为10-14~10-15米的数量级.3.α粒子散射理论(验证模型的理论) 偏转角与瞄准距离的关系:22θcot a b = 或 ctg θ/2=4πεоMv ²/(2Ze ²)b卢瑟福散射公式: 原子核半径大小的估算公式:)2(12θcsc +=a r m或 )21(1241220θπεsi n +=Mv Ze r m 第二章玻尔模型 纲 要1.里德伯(J.R.Rydberg)方程:(1)氢、类氢离子的里德伯方程的波数表示形式⎥⎦⎤⎢⎣⎡-=≡22111n m R H λν~ ⎥⎦⎤⎢⎣⎡-=≡22111n m R Z A λν~ (2)里德伯方程的光谱项表示形式ν~=T (m)-T (n),(3)氢、类氢离子里德伯方程的能量表示形式 []2211n m hcR Z c h h A -==λν 2n Rhc Z E n -= eV Rhc 613.=2. 里德伯公式对应的轨道跃迁、能级跃迁两种形象表示21)441()(422210θπεθσsin E e Z Z c =3.其他一些相关量 (1)氢、类氢原子的里德伯常量M m R R A +=∞11(2)能级间跃迁两能级能量差E 和波长、波数的关系E n m K e V 241.=λ nmKeV E 2411.~==λν(3)氢原子、类氢原子轨道半径公式 n a r n 1= a 1=0.053nm(4)氢原子电子速度公式n c V n α= α=1/1374.一些相关思想(1) 普朗克为了解释黑体辐射实验,引入了能量交换量子化的假说:E =h ν:普朗克常量h 的物理意义是:h 是能量量子化的量度,即能量分立性的量度。
原 子 物 理一、卢瑟福的原子模型——核式构造1.1897年,_________发现了电子.他还提出了原子的______________模型.2.物理学家________用___粒子轰击金箔的实验叫__________________。
3.实验结果: 绝大局部α粒子穿过金箔后________;少数α粒子发生了较大的偏转; 极少数的α粒子甚至被____.4.实验的启示:绝大多数α粒子直线穿过,说明原子部存在很大的空隙; 少数α粒子较大偏转,说明原子部集中存在着对α粒子有斥力的正电荷;极个别α粒子反弹,说明个别粒子正对着质量比α粒子大很多的物体运动时,受到该物体很大的斥力作用. 5.原子的核式构造:卢瑟福依据α粒子散射实验的结果,提出了原子的核式构造:在原子中心有一个很小的核,叫________, 原子的全部正电荷和几乎全部质量都集中在原子核里,带负电的电子在核外空间绕核旋转.例1:在α粒子散射实验中,卢瑟福用α粒子轰击金箔,以下四个选项中哪一项属于实验得到的正确结果: A.α粒子穿过金箔时都不改变运动方向 B.极少数α粒子穿过金箔时有较大的偏转,有的甚至被反弹 C.绝大多数α粒子穿过金箔时有较大的偏转 D.α粒子穿过金箔时都有较大的偏转. 例2:根据α粒子散射实验,卢瑟福提出了原子的核式构造模型。
如图1-1所示表示了原子核式构造模型的α粒子散射图景。
图中实线表示α粒子的运动轨迹。
其中一个α粒子在从a 运动到b 、再运动到c 的过程中〔α粒子在b 点时距原子核最近〕,以下判断正确的选项是〔 〕 A .α粒子的动能先增大后减小B .α粒子的电势能先增大后减小C .α粒子的加速度先变小后变大D .电场力对α粒子先做正功后做负功 二 玻尔的原子模型 能级1.玻尔提出假说的背景——原子的核式构造学说与经典物理学的矛盾:⑴按经典物理学理论,核外电子绕核运动时,要不断地辐射电磁波,电子能量减小,其轨道半径将不断减小,最终落于原子核上,即核式构造将是不稳定的,而事实上是稳定的.⑵电子绕核运动时辐射出的电磁波的频率应等于电子绕核运动的频率,由于电子轨道半径不断减小,发射出的电磁波的频率应是连续变化的,而事实上,原子辐射的电磁波的频率只是某些特定值。
原子物理学总复习指导名词解释:光谱,氢原子线系,类氢离子,电离电势,激发电势,原子空间取向量子化,原子实极化,轨道贯穿,有效电荷数,电子自旋,磁矩,旋磁比,拉莫尔进动,拉莫尔频率,朗德g因子,电子态,原子态,塞曼效应,电子组态,LS耦合,jj耦合,泡利原理,同科电子,元素周期表,壳层,原子基态,洪特定则,朗德间隔定则数据记忆:电子电量,质量,普朗克常量,玻尔半径,氢原子基态能量,里德堡常量,hc,ħc,玻尔磁子,精细结构常数,拉莫尔进动频率著名实验的内容、现象及解释:α粒子散射实验,光电效应实验,夫兰克—赫兹实验,施特恩—盖拉赫实验,碱金属光谱的精细结构,塞曼效应,反常塞曼效应,理论解释:(汤姆逊原子模型的不合理性),卢瑟福核式模型的建立、意义及不足,玻尔氢原子光谱理论的建立、意义及不足,元素周期表计算公式:氢原子光谱线系,玻尔理论能级公式、波数公式,角动量表达式及量子数取值(l,s,j),LS耦合原子态,jj耦合原子态,朗德间隔定则,g因子,塞曼效应,原子基态谱线跃迁图:精细结构,塞曼效应;电子态及组态、原子态表示,选择定则,1.同位素:一些元素在元素周期表中处于同一地位,有相同原子序数,这些元素别称为同位素。
2.类氢离子:原子核外只有一个电子的离子,这类离子与氢原子类似,叫类氢离子。
3. 电离电势:把电子在电场中加速,如使它与原子碰撞刚足以使原子电离,则加速时跨过的电势差称为电离电势。
4.激发电势:将初速很小的自由电子通过电场加速后与处于基态的某种原子进行碰撞,当电场电压升到一定值时,发生非弹性碰撞,加速电子的动能转变成原子内部的运动能量,使原子从基态激发到第一激发态,电场这一定值的电压称为该种原子的第一激发电势 5. 原子空间取向量子化:在磁场或电场中原子的电子轨道只能取一定的几个方向,不能任意取向,一般的说,在磁场或电场中,原子的角动量的取向也是量子化的。
6.原子实极化:当价电子在它外边运动时,好像是处在一个单位正电荷的库伦场中,当由于价电子的电场的作用,原子实中带正电的原子核和带负电的电子的中心会发生微小的相对位移,于是负电的中心不再在原子核上,形成一个电偶极子,这就是原子实的极化。
7. 轨道贯穿:当电子处在原子实外边那部分轨道时,原子实对它的有效电荷数Z 是1,当电子处在穿入原子实那部分轨道时,对它起作用的有效电荷数Z 就要大于1。
8. 有效电荷数:9.电子自旋:电子既有某种方式的转动而电子是带负电的,因而它也具有磁矩,这个磁矩的方向同上述角动量的方向相反。
从电子的观点,带正电的原子实是绕着电子运动的,电子会感受到一个磁场的存在,电子既感受到这个磁场,它的自旋取向就要量子化。
(电子内禀运动或电子内禀运动量子数的简称) 10. 磁矩:11. 旋磁比:粒子磁动量和角动量的比值。
12. 拉莫尔进动:是指电子、原子核和原子的磁矩在外部磁场作用下的进动。
13. 拉莫尔频率:f=4ππmveB,式中e 和m 分别为电子的电荷和质量,μ为导磁率,v 为电子的速度。
该频率被称为拉莫尔频率14. 朗德g 因子: 磁矩j p me2gj=μ 对于单个电子:)1(2)1()1()1(1++++-++=j j s s l l j j g对于LS 耦合:式子中的L ,S ,J 是各电子耦合后的数值15. 塞曼效应:当光源放在足够强的磁场中,所发出光谱的谱线会分裂成几条,而且每条谱线的光是偏振的。
16. 电子组态:价电子可以处在各种状态,合称电子组态。
17. 泡利原理:不能有两个电子处在同一状态。
18. 同科电子:n *和l 二量子数相同的电子称为同科电子。
19. 壳层:20. 原子基态:原子的能量最低状态。
21. 洪特定则:只适合于LS 耦合,从同一电子组态形成的级中,(1)那重数最高的亦即S 值最大的能级位置最低。
(2)重数相同即具有相同S 值的能级中,那具有最大L 值的位置最低。
22. 朗德间隔定则:在一个多重能级的结构中,能级的二相邻间隔同有关的二J 值中较大那一值成正比。
数据记忆:电子电量1.602×10-19C质量:9.11×10-31kg普朗克常量:6.63×10-34J·s玻尔半径:==22014em a e ηπε 5.29×10-11m氢原子基态能量:E=-13.6ev 里德堡常量:17100974.1-∞⨯=m R 17100968.1-⨯=m R Hhc ħc (π2h =η)玻尔磁子:m s v m e⋅⋅⨯==-290B101654.12eημμ精细结构常数::3-02107.2972⨯==hce a ε拉莫尔进动频率: f=4ππmveB ,式中e 和m 分别为电子的电荷和质量,μ为导磁率,v 为电子的速度。
该频率被称为拉莫尔频率。
理论解释:1,(汤姆逊原子模型的不合理性),卢瑟福核式模型的建立、意义及不足?在α散射试验中,平均只有2-3度的偏转,但有1/8000的α粒子偏转大于90度,其中有接近180度的。
模型:原子有带正电的原子核和带负电的电子组成,带正电部分很小,电子在带正电部分外边。
实验现象解释:α粒子接近原子时,它受电子的作用引起的运动改变还是不大(库伦力不大),α粒子进入原子区域,它还在正电体以外,整个正电体对它起作用,因此受库伦力是2024Ze 2r πε因为正电部分很小,所以r 很小,故受的力很大,因此可能产生大角散射。
2,玻尔氢原子光谱理论的建立、意义及不足?条件:电子只能处于一些分立的轨道,它只能在这些轨道上绕核转动,且不产生电磁辐射。
推导过程:库仑力提供向心力:2222041r mv r Ze =πε (1)势能=k-rZe 2041πε (w=⎰∞=rr Ze dr r Ze 202204141πεπε库仑力做负功故势能增)故能量rZe r Ze mv 2414121E 20202πεπε-=-= (2)根据轨道量子化条件:πφ2hnmur P == (3)联立(1)(3)消去v 得,......3,2,14422220==n mZeh n r 其中ππε (4)令2220144me h a ππε=则Zn a r 21= (5)把(4)式代入(2)式有E=........321n )4(me 22220222,,,其中=-hn Z πεπ 氢原子光谱:● 光谱是线状的,谱线有一定位置。
● 谱线间有一定的关系 ● 每一条谱线的波数都可以表达为两光谱项之差,为整数。
其中氢的光谱项是n nR ),()(2Hn T m T -=-ν1,2En R hc-= 能级计算公式:R 为里德伯常数17100974.1-∞⨯=m R 17100968.1-⨯=m R H2,量子化通则:........3,2,1n nh pdq ⎰==,3,电子椭圆轨道半径:长半轴Za n a12= 短半轴Za nn b1φ=;0,.......,3,2,1;........,321n n r ---==n n n n n n r ,,,表示径量子数,表示角量子数,φφ4,史特恩---盖拉赫实验;其中磁力F的夹角。
是磁矩与磁场方向之间,磁感应强度变化的陡度是沿磁场方向的量,是磁矩在磁场方向的分;其中βμβμμdzBdz dB dz dB zd cos F z ==βμμcos )(21)(21)(2121S 2222vL dz dB m v L dz dB m v L m F at z ====5,(1)电子的角动量=轨道角动量+自旋角动量;j 2s l s l j hjP P P P P s l s l j -=+==-+=或其中或π(2)但是较为准确的角动量计算公式为:;,2)1(,2)1(,2)1(s l j s l j hj j P h s s P h l l P j s l -=+=+=+=+=或其中故πππ 单电子辐射跃迁的选择定则:1,0,1±=∆±=∆j l6,课后习题中两个问题的解释:主线系最长波长是电子从第一激发态向激发态跃迁产生的,辅线系系限波长是电子从无穷远处像第一激发态跃迁产生的。
7,碱金属原子的光谱项可以表达为:22*)(T ∆-==n R n R它与氢原子光谱项的差别在于有效量子数不是整数,而是主量子数减去一个数值∆ 8,(1)LS 耦合:,称为三重态值,相当于有三个能级,共有三个,,时有,对于一个单一态;那就是一个能级,称为时,显然对于,,其中其中;或故或而J 1L L 1L J 1S L J 0S ;S -L .........,1-S L S L J ,2)1(;,,.........1,L ,2)1(P 10S s S 2)1(2121212121+-====++=+=--++=+==-=+=+=πππhJ J P l l l l l l hL L s s S s hS S P J L S (2)jj 耦合..........,1j j j j J J ,21)J(J P p .21,212121J j j hp p j s s l s l j j j j --++=+==+-=,,只能有如下数值:合成原子的总角动量:电子的再和另一个,每个电子的值,也就是有两个故每个电子有两个而或π9,原子磁矩的计算: (1)磁矩j p m e2gj=μ 对于单个电子:)1(2)1()1()1(1++++-++=j j s s l l j j g(2)记。
耦合过于复杂,可以不。
是各电子耦合后的数值,其中耦合是原子的总角动量。
,的原子,对两个或两个以上电子jj S J J S S L L J J g LS P megJ J ,,L )1(2)1()1()1(1P 2J J ++++-++==μ 10,外磁场对原子的作用:原子受磁场作用的附加能量:为波尔磁子。
磁场强度,因子,是朗德,,,如下数值:称为磁量子数,只能取其中B B g ,..........1J J M 4M E μμπg J B Mg B mhegB --==∆11,塞曼效应的理论解释:[][]2'11221122'1114L 4111λλλλλλλππλλλ∆-=-=∆=-=-=-=∆)(相差不大时和对于为洛伦兹单位。
其中)(‘mcBeLg M g M mc Be g M g M发生,只有下列情况的跃迁塞曼跃迁也有跃迁定则:1,除外)。
时,线(当,产生0M 0M 0J 0M12=→==∆=∆π2,线。
,产生σ1M ±=∆原子物理复习资料一、选择题1.德布罗意假设可归结为下列关系式:( A ) A .E=h υ, p =λh; B.E=ωη,P=κη; C. E=h υ ,p =λη; D. E=ωη ,p=λη2.夫兰克—赫兹实验的结果表明:( B )A 电子自旋的存在;B 原子能量量子化C 原子具有磁性;D 原子角动量量子化3为了证实德布罗意假设,戴维孙—革末于1927年在镍单晶体上做了电子衍射实验从而证明了:B A.电子的波动性和粒子性 B.电子的波动性 C.电子的粒子性 D.所有粒子具有二项性 4.若镁原子处于基态,它的电子组态应为:( C ) A .2s2s B.2s2p C.3s3s D.3s3p 5.下述哪一个说法是不正确的?( B )A.核力具有饱和性;B.核力与电荷有关;C.核力是短程力;D.核力是交换力. 6.按泡利原理,主量子数n 确定后可有多少个状态?( D )A.n 2; B.2(2l +1); C.2j+1; D.2n 27.钠原子由nS 跃迁到3P 态和由nD 跃迁到3P 态产生的谱线分别属于:( D )A.第一辅线系和基线系B.柏格曼系和第二辅线系C.主线系和第一辅线系D.第二辅线系和第一辅线系8.碱金属原子光谱精细结构形成的根本物理原因:( A )A.电子自旋的存在B.观察仪器分辨率的提高C.选择定则的提出D.轨道角动量的量子化 9.铍(Be )原子若处于第一激发态,则其电子组态:( D ) A.2s2s ; B.2s3p ; C.1s2p; D.2s2p10如果l 是单电子原子中电子的轨道角动量量子数,则偶极距跃迁选择定则为:( C )A.0=∆l; B. 0=∆l 或±1; C. 1±=∆l ; D. 1=∆l11.设原子的两个价电子是p 电子和d 电子,在L-S耦合下可能的原子态有:C A.4个 ; B.9个 ; C.12个 ; D.15个12.氦原子由状态1s2p 3P 2,1,0向1s2s 3S 1跃迁,可产生的谱线条数为:( C )A.0;B.2;C.3;D.113.设原子的两个价电子是d 电子和f 电子,在L-S 耦合下可能的原子态有:( D )A.9个 ;B.12个 ;C.15个 ;D.20个 ; 14.原子发射X 射线特征谱的条件是:( C )A.原子外层电子被激发;B.原子外层电子被电离;C.原子内层电子被移走;D.原子中电子自旋―轨道作用很强 15正常塞曼效应总是对应三条谱线,是因为:CA .每个能级在外磁场中劈裂成三个; B.不同能级的郎德因子g 大小不同; C .每个能级在外场中劈裂后的间隔相同; D.因为只有三种跃迁16.钍23490Th 的半衰期近似为25天,如果将24克Th 贮藏100天,则钍的数量将存留多少克? ( A )A.1.5;B.3;C.6;D.12. 17.如果原子处于2P 1/2态,它的朗德因子g 值:( A ) A.2/3; B.1/3; C.2; D.1/26.氖原子的电子组态为1s 22s 22p 6,根据壳层结构可以判断氖原子基态为:( C ) A.1P1; B.3S1; C .1S0; D.3P0 . 18.原子发射伦琴射线标识谱的条件是:( C )A.原子外层电子被激发;B.原子外层电子被电离;C.原子内层电子被移走;D.原子中电子自旋―轨道作用很强。