微生物学检验--操作流程及评分标准
- 格式:doc
- 大小:83.00 KB
- 文档页数:9


微生物检测操作流程《微生物检测操作流程》微生物检测是一项重要的实验室技术,用于检测和鉴定各种微生物,包括细菌、真菌、病毒等。
本文将介绍一般的微生物检测操作流程。
一、样品采集与处理1. 样品选择:根据实验目的选择适当的样品类型,如水样、食品样、土壤样等。
2. 采集样品:采集样品时要注意避免污染和交叉污染。
3. 处理样品:根据具体情况,对样品进行处理,如稀释、研磨、过滤等。
二、培养基的制备1. 选择合适的培养基:根据待检微生物的特性选择适当的培养基类型。
2. 制备培养基:按照标准的配方和操作规程制备培养基。
三、菌落计数1. 加样和摇匀:将样品加入培养基中,并充分摇匀。
2. 培养:将培养基装入培养皿或培养瓶中,进行恒温培养。
3. 菌落计数:根据菌落的外观、形态等特征,进行菌落计数。
四、纯化和鉴定1. 提取纯种菌:从培养基上选取单个菌落,进行传代培养,获得纯种菌。
2. 形态鉴定:通过观察微生物的形态特征,如形状、大小、颜色等,进行初步鉴定。
3. 生理生化特性鉴定:通过对微生物的生理生化特性进行检测,如氧需求性、产气性、酶活性等,进一步鉴定。
五、分子生物学检测(可选)1. 提取DNA/RNA:采用适当的方法提取待检微生物的DNA或RNA。
2. PCR扩增:利用聚合酶链式反应(PCR)扩增目标序列。
3. 凝胶电泳:将PCR产物进行凝胶电泳分析,确定目标序列的存在与否。
六、结果分析与报告1. 结果解读:根据实验结果判断待检微生物是否合格。
2. 报告编写:撰写实验报告,包括实验方法、结果、分析和结论。
3. 结果验证:可以进行复核实验或委托第三方实验室进行验证。
以上即是一般的微生物检测操作流程,不同类型的微生物检测可能会有一些差异。
在实验中,操作人员应严格遵循操作规程,做好实验安全和样品处理,保证检测结果的准确性和可靠性。

食品微生物检验技能操作考核方案与评分标准食品微生物检验技能操作考核方案与评分标准食品微生物检验技能操作考核方案与评分标准一、食品微生物检验技能操作试题本次考试有五组技能测试题供学生随机抽取,每一组题满分均为100分,占该门课程总成绩的70%。
第一组:使用高压灭菌锅进行培养基的灭菌,并回答相关问题。
第二组:微生物划线分离技术操作,并回答相关问题。
第三组:食品中细菌总数的测定操作,并回答相关问题。
第四组:食品中大肠菌群测定,并回答相关问题。
第五组:常用仪器的使用二、考试程序1、组织学生抽取考试序号,按照此序号依次进行技能考试。
2、按照考试序号组织学生在考前5分钟抽取试题,拿到试题后可以准备5分钟,然后开始操作和回答。
其他学生集中在另一教室等待。
3、考试完的学生不允许与等待考试的学生接触,要迅速离开考场,防止学生利用通讯工具交流试题内容。
三、评分标准第一组湿热灭菌操作一、一、操作用具及物品:高压灭菌锅、试管培养基、三角瓶、线绳、报纸或牛皮纸等。
二、操作过程及评分标准1.首先将内层灭菌桶取出,再向外层锅内加入适量的水,使水面与三角搁架相平为宜。
(10分)2.放回灭菌桶,并装入待灭菌物品。
注意不要装得太挤,以免防碍蒸汽流通而影响灭菌效果。
三角烧瓶与试管口端均不要与桶壁接触,以免冷凝水淋湿包口的纸而透入棉塞。
(10分)3.加盖,并将盖上的排气软管插入内层灭菌桶的排气槽内。
再以两两对称的方式同时旋紧相对的两个螺栓,使螺栓松紧一致,勿使漏气。
(10分)4.用电炉或煤气加热,并同时打开排气阀,使水沸腾以排除锅内的冷空气。
(或等压力上升到0.5时,打开放气阀排出冷空气)待冷空气完全排尽后,关上排气阀,让锅内的温度随蒸汽压力增加而逐渐上升。
当锅内压力升到所需压力时,控制热源,维持压力至所需时间。
本实验用 1.05kg/cm2,121.3℃,20分钟灭菌。
(10分)提问:1.为什么要放出冷空气?答:因空气是热的不良导体,当高压锅内的压力升高后,它聚集在锅的中下部,使饱和热蒸汽难与被灭菌物品接触。

微生物限度检查操作规程《微生物限度检查操作规程》一、目的微生物限度检查是用于确认产品是否符合微生物水平要求的一种分析方法。
本操作规程的目的是制定微生物限度检查的操作步骤,确保检查结果的准确性和可靠性。
二、适用范围本操作规程适用于所有需要进行微生物限度检查的产品,包括食品、医药和化妆品等。
三、操作步骤1. 准备工作:清洁实验室工作台面和仪器设备,准备所需的培养基和试剂,并确保仪器设备的正常运转。
2. 取样:按照产品的取样标准,从不同批次或不同位置进行取样,并确保取样的代表性。
3. 样品制备:将取样的产品进行样品制备,包括稀释、搅拌和过滤等步骤,以便于后续的微生物检查。
4. 培养:将样品接种在适当的培养基上,根据不同的微生物种类和要求进行培养,并进行恒温培养一定时间。
5. 计数:在培养一定时间后,对培养基上的菌落进行计数,并按照标准方法进行结果的记录和确认。
6. 结果判定:将检查结果与产品的微生物限度标准进行比对,根据结果作出是否合格的判定。
7. 结果记录:将微生物限度检查的结果进行记录,包括样品信息、操作步骤、检查结果和判定等信息,并将结果报告给相关部门或供应商。
四、注意事项1. 操作人员应具备一定的微生物检测知识和操作技能,严格按照操作规程执行。
2. 实验室应保持清洁、卫生,并进行定期消毒和验证。
3. 实验室设备应定期维护和校准,确保设备的准确性和可靠性。
4. 所使用的培养基和试剂应符合相关标准,存放在干燥、阴凉、避光的环境中。
5. 检查结果应及时报告,并根据结果采取相应的控制措施。
以上就是《微生物限度检查操作规程》的主要内容,希望能够帮助大家更好地进行微生物限度检查,确保产品质量和安全。

微生物检验的基本操作技术一、样品的制备与处理1.样品的选择与采集:根据检验目的和要求,选择适当的样品,并根据采样规范进行取样。
比如,对食品的微生物检验,可以选择不同部位的样品,如表面、内部等;对饮用水的微生物检验,可以选择源头水、管网水等;对环境的微生物检验,可以选择空气、地表水等。
2.样品的保存与运输:为了避免样品中微生物的生长和变化,需要将样品保存在适当的条件下(如低温、暗处等)。
同时,在运输过程中,需要避免样品的污染和损坏。
3.样品的处理:样品处理过程通常包括样品的搅拌、过滤、稀释等。
搅拌可以均匀样品中的微生物分布;过滤可以去除样品中的固体颗粒;稀释可以将样品中微生物的浓度调整到适宜的浓度范围,以便后续的检测操作。
二、微生物的分离与纯化1.微生物培养基的选择:根据待检微生物的特性和对检测结果的要求,选择适当的培养基。
常用的培养基有通用培养基、选择性培养基和特殊培养基。
2.菌落计数:将经过处理的样品按照一定的稀释倍数进行均匀悬浮,并于培养基平板上进行接种。
经过一段时间的培养,可通过菌落的外观、形状、大小、颜色等来初步判断微生物的种类和数量。
3.纯化子菌株:从菌落中选取代表性菌落,通过反复传代培养,最终得到纯种菌株。
三、微生物的鉴定与鉴别1.形态学观察:通过显微镜观察微生物的形态特征,如细胞形状、大小、结构等,可以初步鉴定微生物的类别。
2.生理生化试验:通过微生物的代谢特性进行鉴定。
常用的生理生化试验包括氧需求性试验、酸碱反应试验、温度试验、营养需求试验、代谢产物试验等。
3.分子生物学手段:通过分子生物学技术,如聚合酶链反应(PCR)、DNA序列比对等,对微生物进行进一步的鉴定和鉴别。
例如,利用16SrRNA基因作为分子标志物,可以快速、准确地识别微生物种类。
四、微生物的计数与统计1.液体中微生物的计数:通过在培养基中逐级稀释样品,最后将稀释液接种于平板上,培养一段时间后,根据培养基中菌落的数量进行计数,以反推样品中微生物的浓度。

微生物检测操作规程《微生物检测操作规程》一、目的微生物检测操作规程旨在规范微生物检测实验的操作流程,确保检测结果的准确性和可靠性。
二、适用范围本规程适用于实验室内进行微生物检测实验的操作人员,包括但不限于食品、医药、环境等领域的微生物检测。
三、操作流程1. 实验前准备(1)检查所需物品和设备的完整性和清洁度;(2)准备好所需的培养基、培养皿、移液器等实验用品;(3)佩戴实验服和手套,保持操作环境清洁。
2. 样品处理(1)按照标准操作程序采集样品,并确保准确记录样品信息;(2)样品处理前进行必要的预处理,如稀释、离心等。
3. 培养和检测(1)按照操作规程在培养基上均匀涂布样品;(2)标注培养皿的信息,包括样品编号、培养基种类、培养温度等;(3)放置在适当的培养温度下培养一定时间;(4)观察培养皿的生长情况,记录培养时间和结果。
4. 结果分析(1)根据培养结果进行初步鉴定和计数;(2)必要时进行进一步的分离、鉴定和鉴定。
四、质控要求(1)实验操作人员应具备相应的微生物检测知识和技能,并接受相关的培训;(2)严格遵守操作规程,确保实验操作的准确性和一致性;(3)定期对实验室设备、试剂和培养基等进行检查和质量控制,确保其完好和有效。
五、记录和报告实验过程中产生的数据和结果应当及时记录,并进行审查和验证。
对于检测结果,应当制作详细的技术报告,包括检测方法、样品信息、结果分析和结论等内容。
六、实施本规程由实验室主管负责组织实施,并由实验室操作人员严格遵守。
七、附则本规程自发布之日起施行,如有变动将另行制定修订,并及时通知相关人员。
以上即为《微生物检测操作规程》的内容,希望广大实验室操作人员严格按照规程执行,确保微生物检测工作的准确性和可靠性。

微生物检验操作步骤1.样品收集:根据检验目的选择合适的样品,如食品样品、水样、医疗器械等。
正确采集样品,避免样品受到污染。
2.样品制备:将收集到的样品进行处理,以适应后续的检验步骤。
例如,对食品样品进行均质处理、稀释等。
3.样品接种:将处理后的样品接种到含有合适培养基的培养皿或培养瓶中。
根据不同的微生物类型和检验目的,选择适当的培养基。
4.培养条件设置:根据微生物的生长特点,设置适当的培养条件,包括温度、湿度、氧气含量等。
常见的培养条件是37℃下的静态培养。
5.培养皿封闭:将培养皿或培养瓶盖封闭,避免外部的污染物进入。
可以使用透明胶带或铝箔密封。
6.培养:将已封闭的培养皿或培养瓶放入恒温培养箱中进行培养。
培养的时间因微生物的生长速度不同而不同,通常为24小时至7天。
7.观察:在培养过程中,定期观察微生物的生长状况。
可以在显微镜下观察细菌的形态、颜色、大小等特征,并记录下来。
8.制备涂片:当微生物生长到一定程度时,将培养皿中的细菌涂抹到玻璃片上。
涂片可以用于后续的染色和显微观察。
9.染色:选择合适的染色方法对涂片进行染色,以便更清晰地观察细菌的形态。
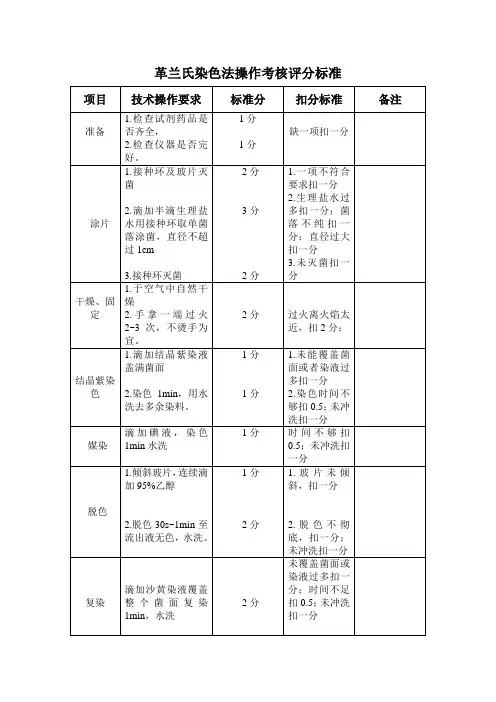
常用的染色方法包括革兰染色和抗酸染色。
10.显微观察:在显微镜下观察染色后的涂片,注意细菌的形态、排列方式、胞内结构等细节特征。
根据观察结果,确定微生物的种类。
11.计数:根据涂片的观察结果,使用细菌计数板或其他方法对微生物的数量进行估计。
通常会进行稀释和培养后计数。
12.结果分析:根据观察和计数结果,判断微生物是否符合相应的标准。
根据检验目的,确定微生物的种类和数量,判定样品是否合格。
13.结果报告:将检验结果整理成报告,包括微生物的种类和数量等信息。
报告应准确明确,便于评估和决策。
14.结束处理:检验完成后,对实验室设备进行清洁和消毒处理,避免细菌的传播和污染。
同时,将培养出的微生物进行适当的处理,如灭菌或安全处置。
以上是微生物检验的一般操作步骤,不同类型的微生物检验可能存在一些差异,具体操作步骤应根据实验方法和检验目的进行调整。

微生物检验流程及操作标准全文共四篇示例,供读者参考第一篇示例:微生物检验是一种重要的实验室技术,用于检测食品、水质、环境等样品中的微生物存在情况。
微生物检验需要严格遵守一系列操作标准和流程,以确保检验结果的准确性和可靠性。
下面我们将介绍一下微生物检验的流程及操作标准。
一、样品采集1. 样品的采集需要采用无菌工具,并保持样品在采集过程中不受到外界环境的污染。
2. 样品的采集过程应尽量避免接触到任何可能引入外源微生物的物质,比如皮肤、空气等。
3. 采集的样品应标明正确的标识信息,包括样品名称、采集地点、采集日期等。
二、样品处理1. 样品收到实验室后,需要尽快进行处理,避免样品内的微生物增殖或死亡。
2. 样品处理过程需要保持在无菌条件下进行,使用无菌工具进行操作。
3. 样品处理过程中需要按照检验要求进行适当的稀释,以确保实验得出准确的结果。
三、培养基准备1. 培养基的制备需要按照标准的配方和步骤进行,以确保培养基的质量符合要求。
2. 制备培养基时需要严格遵守无菌操作规范,避免细菌、真菌等外源微生物的污染。
3. 制备好的培养基需要在适当的条件下保存,确保培养基的稳定性和有效性。
四、接种操作1. 在进行微生物检验之前,需要准备好无菌的接种环、移液器等工具。
2. 采取适当的方法将处理好的样品接种到培养基上,避免接种时引入外源微生物。
3. 接种操作需要在无菌条件下进行,避免培养物受到任何污染。
五、培养与观察1. 接种后的培养基需要置于适当的温度和湿度条件下进行培养,促使样品中的微生物生长。
2. 定期观察培养基上的生长情况,记录生长的数量和形态,用于后续的分析和鉴定。
3. 在观察过程中需要注意反复进行无菌操作,避免细菌、真菌等外源微生物的污染。
六、鉴定与结果解读1. 当样品中的微生物生长到一定程度时,需要进行鉴定和分析,确定其种属和数量。
2. 鉴定过程需要参考相关的鉴定手册和标准,进行适当的试验和测试。
3. 根据鉴定结果进行结果解读,判断样品中微生物的种类和数量是否符合标准要求。

微生物检验操作规程《微生物检验操作规程》一、检验前准备1. 确保实验室环境清洁整洁,无菌操作台面及仪器设备;2. 熟悉操作规程,准备好所需的培养基、试剂和消毒液;3. 检查培养基和试剂的有效期,确保使用的培养基和试剂符合要求。
二、样本处理1. 将样本送检单与样本一同接收,并核对相关信息;2. 对样本进行消毒处理,避免污染实验室环境;3. 定量取样,确保取样的准确性和可靠性。
三、培养基制备1. 按照培养基说明书的要求,准备培养基,注意培养基的稀释和灭菌;2. 根据需要,将培养基注入培养皿中,准备好后放置在无菌条件下。
四、微生物接种1. 根据样本的来源,选择合适的培养基进行接种;2. 采用无菌技术,进行微生物接种,避免外部污染;3. 对接种的培养皿进行标记,清晰记录接种的菌种和数量。
五、培养条件1. 根据不同微生物的生长要求,设置适当的培养条件,包括温度、湿度、气体组成等;2. 定期观察培养皿的生长情况,记录菌落形态、数量和颜色等信息。
六、鉴定和鉴定1. 根据菌落形态、生理生化特性等进行初步鉴定;2. 利用鉴定试剂或生化指标进行进一步鉴定;3. 如有需要,可进行分子生物学方法进行鉴定。
七、结果记录和报告1. 将鉴定结果详细记录在报告中,包括鉴定的微生物种类、数量、鉴定方法和结果等;2. 及时向送检单位提交检验报告,确保检验结果准确无误。
八、实验后清洁1. 将使用过的培养皿和试剂进行正确的处理和清洁;2. 对实验室操作台面和设备进行消毒,保持实验室环境整洁。
以上是《微生物检验操作规程》的基本操作流程,每一步的操作都应严格遵守操作规范,保证微生物检验结果的准确性和可靠性。

微生物学检查步骤临床微生物学实验室接到标本后应立即进行微生物学检验。
主要包括直接镜检、检测特异性抗原或病原体成分、进行分离培养和鉴定、体外药敏试验等。
(一)直接镜检1.初步诊断;2.指导进一步检出步骤和鉴定方法的选择;3.评价标本的质量。
(二)快速诊断快速检测病原体成分主要是指特异性抗原和核酸检测。
特异性抗原检测包括免疫荧光技术、胶乳凝集试验、酶免疫技术、对流免疫电泳、化学发光免疫测定等。
(免疫学检验技术)核酸检测包括核酸探针杂交、PCR技术。
(分子生物学检验技术)其他快速检测法还有气-液相色谱法、化学发光、生物发光测定法和基因或蛋白微型阵列芯片技术等。
(三)直接药敏试验鉴定结果快,但结果不明确,故分离出纯培养物后应再作体外药物敏感试验。
(四)常规检验1.分离培养:通常由正常无菌部位采取的标本接种血平板,置于空气或含5%~10%CO2的气缸中培养,大部分细菌可于24~48h生长良好。
若原始培养为阴性,但据镜检结果和临床信息提示可能有病原菌存在,则应再采集大量标本,离心浓缩或溶解离心法处理,取沉淀接种营养丰富的需氧或厌氧培养基来培养。
对于存在正常菌群部位采集的标本,分离时应采用选择培养基以利于病原菌生长,也可加某些抗生素抑制污染菌的生长。
对于某些感染标本中发现的细菌,如尿路感染的尿液中检出大肠埃希菌,可能是病原菌,也可能是污染菌或正常菌群,其临床意义的确定有赖于定量培养法。
2.鉴定:分离出的细菌一般应经过细菌形态、菌落特点、生化反应、血清学试验、动物接种等鉴定。
目前尚有某些微量鉴定系统,其鉴定快速、简便,值得推广。
如用于鉴定肠杆菌科的20E,鉴定非发酵菌的20NE及鉴定厌氧菌的20A等。
3.体外纯菌药物敏感性试验:常用方法包括抑菌试验、杀菌试验、医学。
教育网整理联合药敏试验和检测细菌产生的抗生素灭活酶等。
(五)报告①直接镜检要求2h报告,说明标本是否合格,发现微生物情况和特点;②初步鉴定和直接药敏结果于24h或次晨报告,报告可能的病原菌和直接药敏结果;③最后鉴定和细菌药敏结果一般不超过3天,还规定除血培养外,所有送检标本必须在24h内预报。
微生物检验操作规程微生物检验操作规程一、实验室的准备工作1.确保实验室环境整洁卫生,空气流通。
2.检查实验室设备及试剂的完好性,如有损坏或过期的试剂应予以更换。
3.准备所需的培养基、试剂和培养器具,并确保其质量符合要求。
4.准备好必要的个人防护用品,如实验手套、口罩、护目镜、实验服等。
二、标本采集和处理1.标本的采集应遵循无菌操作的原则,采集器具需经过高温高压消毒处理。
2.将采集的标本迅速送至实验室,避免暴露于空气中。
3.对于液体标本,如尿液、血液等,应进行无菌操作并进行适当的稀释。
4.对于固体标本,如组织、分泌物等,应进行无菌取样,并进行适当的处理。
三、培养基的准备和使用1.根据需要,准备所需的培养基,并按照说明书进行正确的配制。
2.确保培养基的无菌性,防止细菌、真菌等污染。
3.使用培养基前应进行质控试验,确保培养基的质量符合要求。
4.在使用培养基前,要检查培养基是否出现变质、褪色等异常情况,若有发现,应立即更换。
四、微生物的分离和培养1.将标本取适量,在无菌条件下均匀涂抹于培养基表面,避免重叠。
2.将涂抹好的培养基置于细菌培养箱中,设置适当的温度和湿度,促使微生物的生长。
3.培养箱内不宜存放过多的培养基,以免影响空气流通和温度控制。
4.定期观察培养基的生长情况,并进行记录,一般培养时间为24小时至48小时。
五、微生物的鉴定和鉴定1.根据菌落的形态、大小、颜色等特征,初步判断微生物的种类。
2.利用显微镜观察菌液或菌落的形态、数量、运动性等特征,进一步鉴定微生物。
3.对于不易鉴定的微生物,可使用生化试剂或分子生物学方法进行鉴定。
4.鉴定微生物的结果应进行记录,并与对应的标准对照互相核对。
六、微生物的灭活和处理1.工作台和实验器具在使用前后应进行消毒,以防止微生物的传播。
2.将已鉴定的微生物进行灭活处理,可使用高温高压或化学消毒剂。
3.遵循规定将已处理的微生物进行妥善的处置,防止对环境和人员造成污染和危害。
微生物培养操作评分标准该评分标准以详细描述正确的微生物培养操作方法,旨在确保实验人员进行准确、规范和安全的微生物培养。
本文档列举了培养基准备、操作环境、接种操作、培养条件和结果判读等方面的评分标准。
1. 培养基准备- 严格按照实验方案准备培养基,包括准确称量培养基成分、正确配制和调节pH值等。
严格按照实验方案准备培养基,包括准确称量培养基成分、正确配制和调节pH值等。
- 确保培养基质量的可靠性,如确认培养基无菌、培养基成分无明显异常等。
确保培养基质量的可靠性,如确认培养基无菌、培养基成分无明显异常等。
- 妥善保存培养基,包括密封、避光和冷藏等。
妥善保存培养基,包括密封、避光和冷藏等。
2. 操作环境- 消毒实验台面,确保操作环境清洁无菌。
消毒实验台面,确保操作环境清洁无菌。
- 使用消毒酒精喷雾对工作区域进行消毒,确保操作区域无菌。
使用消毒酒精喷雾对工作区域进行消毒,确保操作区域无菌。
- 佩戴手套和口罩,防止操作人员对微生物产生污染。
佩戴手套和口罩,防止操作人员对微生物产生污染。
3. 接种操作- 正确取样,包括使用无菌技术取得样品、正确挑取菌落等。
正确取样,包括使用无菌技术取得样品、正确挑取菌落等。
- 避免交叉感染,使用无菌技术在无菌培养基上进行接种操作。
避免交叉感染,使用无菌技术在无菌培养基上进行接种操作。
- 控制接种量,确保每次接种的菌量符合实验要求。
控制接种量,确保每次接种的菌量符合实验要求。
4. 培养条件- 保持适宜的温度和湿度,根据不同微生物的要求设置合适的培养条件。
保持适宜的温度和湿度,根据不同微生物的要求设置合适的培养条件。
- 控制培养时间,根据实验方案要求进行合理的培养时间。
控制培养时间,根据实验方案要求进行合理的培养时间。
- 避免培养基受到外界污染,如避光、保持培养条件稳定等。
避免培养基受到外界污染,如避光、保持培养条件稳定等。
5. 结果判读- 准确判读培养结果,包括菌落形态、颜色、数量等。
微生物检验流程及操作标准微生物检验的流程包括以下步骤:1. 标本采集:根据患者的症状和规章制度正确采集标本,及时将采集到的标本送至检验科进行接种处理。
在运送标本的过程中,需要保持相应的温度和氧气,以防止标本干燥。
2. 镜检:检验人员运用显微镜直接观察标本,辨别相关致病菌的形态与数目,并进行初步判断。
必要时,还需要对标本进行染色后再观察,以对致病菌的性质和来源进行鉴别,更能排除污染因素,使标本致病菌的检出率得到大幅度提升。
3. 分离培养:采集的标本中不可避免地会吸附细菌,如果在镜检环节发现标本上吸附的细菌,就需要对标本实施分离纯化,并将其接种于适宜的培养基上,如显色培养基、血平板培养基、营养琼脂培养基等。
再将空气和温度调整至适合细菌生长的数值,获得便于进一步鉴定的细菌。
4. 细菌鉴定:检验人员通过细菌形态、菌落特点、酶类检测、血清学试验、生化反应等方式鉴定分析分离获得的标本,明确致病原因。
微生物检验的操作标准如下:1. 尽量在病程早期、症状典型以及在使用抗生素之前采集标本。
2. 标本应使用无菌容器盛放。
3. 血液为无菌液体,因此在采集时要避免皮肤的正常菌群污染。
多采用血培养瓶运送,随后放入血培养系统自动培养。
如有报阳则进行下一步检验:涂片镜检报给临床初步结果;需氧和厌氧瓶分别转种血平板,巧克力平板与厌氧血平板等;随后进行菌种鉴定以及药敏试验。
4. 脑脊液标本一般需要进行离心,以富集细胞。
一般检验流程为进行涂片镜检,包括革兰染色,抗酸染色与墨汁染色等。
增菌管进行增菌,分离培养转至血平板,巧克力平板,沙保弱平板等。
5. 痰液镜检一般包括革兰染色与抗酸染色,分离培养多用巧克力平板和血平板。
6. 尿液常做定量检测,取10微升尿液进行连续划线。
7. 粪便常用革兰染色做菌群比检测;分离培养多用麦康凯与SS平板。
8. 各类微生物标本应通过传递窗进行传递。
以上信息仅供参考,建议咨询专业人士获取准确信息。
1.菌落总数操作步骤检样稀释及培养以无菌操作,取样25g放入225mL灭菌生理盐水或灭菌乳钵中,经充分振摇作成1:10均匀稀释液。
用1mL灭菌吸管吸取1:10稀释液1mL,沿管壁徐徐注入含有9mL灭菌生理盐水或其他稀释液的试管内(注意吸管尖端不要触及管内稀释液),振摇试管,混合均匀,做成1:100的稀释液。
另取1mL灭菌吸管,按上条操作顺序,做10倍递增稀释液,如此每递增稀释一次,即换用1支1mL火菌吸管。
根据食品卫生标准要求或对标本污染情况的估计,选择2〜3个适宜稀释度,分别在做10倍递增稀释的同时,即以吸取该稀释度的吸管移1mL稀释液于灭菌平皿内,每个稀释度做两个平皿。
稀释液移入平皿后,应及时将凉至45°C营养琼脂培养基,注入平皿约15mL,并转动平皿使混合均匀。
同时将营养琼脂培养基倾入加有1mL稀释液的灭菌平皿内作空白对照待琼脂凝固后,翻转平板(使平皿底朝上),置36±1C温箱内培养48±2h。
菌落计数方法做平板菌落计数时,可用肉眼观查,必要时用放大镜检查,以防遗漏。
在记下各平板的菌落数后,求出同稀释度的各平板平均菌落总数。
菌落计数的报告平板菌落数的选择选取菌落数在30〜300之间的平板作为菌落总数测定标准。
一个稀释度使用两个平板,应采用两个平板平均数,其中一个平板有较大片状菌落生长时,则不宜采用,而应以无片状菌落生长的平板作为该稀释度的菌落数,若片状菌落不到平板的一半,而其余一半中菌落分布又很均匀,即可计算半个平板后乘2以代表全皿菌落数。
稀释度的选择应选择平均菌落数在30〜300之间的稀释度,乘以稀释倍数报告之(见表1中例1)。
若有两个稀释度,其生长的菌落数均在30〜300之间,则视两者之比如何来决定。
若其比值小于或等于2,应报告其平均数;若大于2则报告其中较小的数字(见表中例2及3)。
若所有稀释度的平均菌落数均大于300,则应按稀释度最高的平均菌落数乘以稀释倍数报告之(见表1中例4)。