化学无机物思维导图ppt课件
- 格式:ppt
- 大小:850.50 KB
- 文档页数:10

2020-2-269:09:5【老师】俸・KH 高中化経套思“.版).pdf (18.11MB )髙中化学全套思谁导图(高清版),pdf}来目群文件打开打开文骸 转发三1【老师】俸自己没有思维导图的可以借鉴。
1 /43高中化学 第一章 从实验学化学第一节化学实验基础知识取用固体取用液体防火与灭火常见危险与安全措施了解实验安全常识及意外事故处理方法学法指导操作的先后顺序 操作的注意事项 操作的目的 适用范围化学与人类健康 不溶性固体与液体的分萬 实验安全化学与环境保护分离溶于溶液中的固体溶质适用范围1 .蒸发过程不断搅拌I 注意事项蒸发是否易潮解.物质的提纯是将混合物中的少 量杂质除去而得到纯净物质将物质的分 萬与提纯混淆吸取少量液体用滴管 (专用,垂直悬滴,不倒置)实验基本操作物质分离提 纯必须遵循注意防火、防爆炸、防倒吸不増、不减、易分离、易复原2.当大量固体析岀时,停止加热,余热蒸干知识 梳理 化学实解通过动手实验,熟练掌握常用化学 仪器的使用方法和操作注意事项 较多液体用倾倒法 (瓶塞倒放,标签向手心,抓住物质的特性寻找突破口物质检验和实验综合题块状固体用锻子 粉末状用药匙中及故取用药 品的仪器的意的热覗分离 仪器热源,温度可达400 - 500 r酒劈/龜精不超过2/3,不少于1/4,用外 / 5,不对火,不吹灯,先灭后添酒精喷灯温度可达I 000 X ) 水浴漏斗loop 以下 普通漏斗长颈漏斗分液 漏斗主要 用途萃取,分液, 反应加液体用器常仪冷凝管 洗气瓶于燥管注意事项用前先检査是否漏液, 分液时上层液体从上口倒岀,下层液体从下层放出,放液时应打开分液漏斗上玻璃塞或将塞 上的凹槽对准上口小孔。
使漏斗内外大气压相等反应器1 是否易被氧化 是否易燃、易爆 是否易与空W 中某些成分作用 是否易挥发、,1 尹华 是否具有毒性、 腐蚀度便于取用 防止变质 防独、防爆等 细口瓶、产口瓶、 通瓶 塑料瓶、赢r 笑是器等剂质试性则原仪器据依学剂保化试的存密封:水封、 油封、蜡封方式/开放式存放阴凉、避光处(干燥器中存放利用沸点不同,除去难挥发和不挥发的杂质适用范围1.蒸憎烧瓶加热要垫石棉网,温度、 计的水银球与支管口下缘位于同一水平线注意事项2.冷水是下口进,上口出3.要加碎瓷片,防暴沸在互不相溶的溶剂里溶解度差别较大的溶质适用范围1 .溶液总量不超过漏斗容积的3/4 2.把分液漏斗放在铁架台上静置、分层注意事项蒸饌分液3.打开塞子,先从下口放出下层 液体,再从上口倒出上层液体其他基本 操作计量仪器玻璃仪器的洗涤药品的取用药品的保存 装置气密性检验溶液的配勉气体的收集和体积的测量量筒试管、柑垠、隔网可加热或液浴烧杯、烧瓶、 蒸憎烧瓶、锥形瓶 乂_不能加热集气瓶、试剂瓶、滴瓶、 启普发生器主要用途粗略量取液体,精度0.1 mL刻度由下而上增大,无0刻度线, 读数平视。

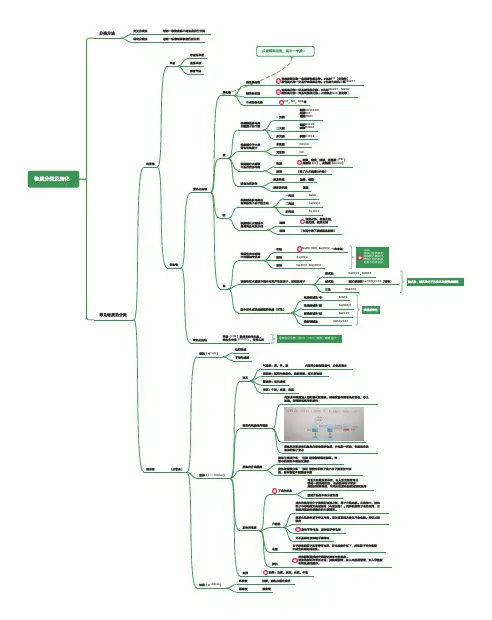
物质分类及转化分类方法常见物质的分类交叉分类法树状分类法对同一事物安装不同标准进行分类用同一标准对事物进行再分类纯净物单质非金属单质化合物金属单质稀有气体无机化合物有机化合物氧化物酸碱盐甲烷(CH4)最简单的有机物。
碳水化合物(CH2O ),较常见的酸性氧化物碱性氧化物非金属氧化物一定是酸性氧化物。
✘比如CO (无酸性)酸性氧化物一定是非金属氧化物。
✘比如七氧化二锰Mn2O7金属氧化物一定是碱性氧化物。
✘比如Mn2O7,Na2O2碱性氧化物一定是金属氧化物。
✔特殊点NH3(氢化物)不成盐氧化物根据酸最多电离出氢离子的个数根据酸分子中是否含有氧原子根据酸在水溶液中是否完全电离按有无挥发性一元酸醋酸CH3COOH 盐酸HCl 硝酸HNO3二元酸多元酸碳酸H2CO3硫酸H2SO4磷酸H3PO4含氧酸H2SO4无氧酸HCl强酸盐酸,硫酸,硝酸,氢溴酸(HBr ),氢碘酸(HI ),高氯酸(HClO4)弱酸(除了六大强酸以外的)挥发性酸难挥发性酸盐酸,硝酸硫酸根据碱最多电离出氢氧根离子的个数分成根据碱在水溶液中是否完全电离分成一元碱NaOH 二元碱多元碱Ca(OH)2Fe(OH)3强碱弱碱(在高中除了强碱就是弱碱)氢氧化钾,氢氧化钠,氧化钙,氢氧化钡根据盐在水溶液中的溶解性分成可溶微溶难溶根据盐在水溶液中能否电离产生氢离子,氢氧根离子CO ,NO ,NO2等口诀:碳酸只溶钾钠铵,溶碱钾钠氨钡钙,硫酸不溶钙钡银,盐酸不溶氯化银。
酸式盐碱式盐碱式碳酸铜Cu2(OH)2CO3(铜绿)正盐NaHCO3,KHSO4Na2CO3据中和生成盐的酸碱的强弱(正盐)强酸强碱盐(中)K2SO4强酸弱碱盐(酸)弱酸弱碱盐(碱)酸弱碱碱盐Fe(NO3)3Na2CO3(NH4)2CO3谁强显谁性酸式盐,碱式盐并不代表它显酸性或碱性混合物只含两种元素,其中一个是ONaOH , KOH , Ba(OH)2 , 一水合氨Ca(OH)2Fe(OH)3 , Mg(OH)2含碳的化合物,除CO ,CO2,碳酸,碳酸盐外(分散系)溶液(<1nm )胶体(1——100nm )浊液(>100nm )氢氧化铁胶体的制备向沸水中逐滴加入饱和氯化铁溶液,继续煮沸至溶液呈红褐色,停止加热,即得到氢氧化铁胶体绿氢氧化铁胶体和氢氧化铁溶液的物质,外观是一样的,但氢氧化铁胶体的离子更小胶体的性质丁达尔效应可见光束通过胶体时,在入射光侧面可以看到一条光亮的路 ,这是胶体粒子对光线散射而形成的,可用此性质来鉴别溶液和胶体介稳性电泳聚沉乳浊液悬浊液胶体的稳定性介于溶液和浊液之间,属于介稳体系。


