漂亮的晶体结构图片
- 格式:doc
- 大小:1.38 MB
- 文档页数:8



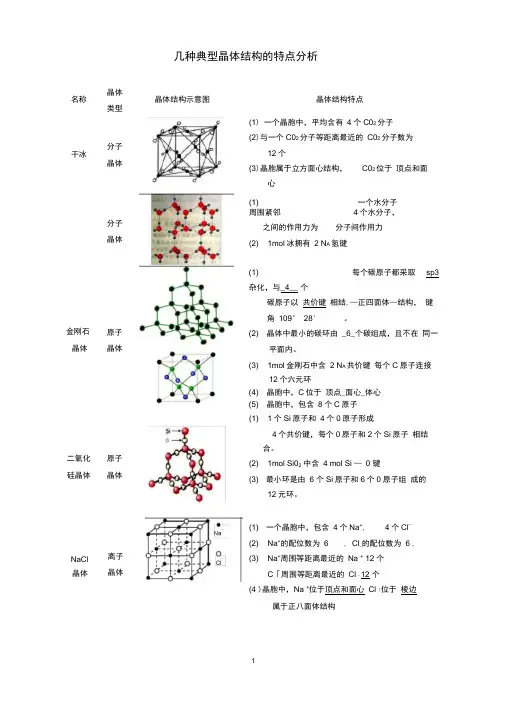
几种典型晶体结构的特点分析名称晶体类型晶体结构示意图晶体结构特点干冰分子晶体分子晶体(1) 一个晶胞中,平均含有4个C02分子(2)与一个C02分子等距离最近的C02分子数为12个(3)晶胞属于立方面心结构,C02位于顶点和面心金刚石晶体原子晶体(1) 一个水分子周围紧邻4个水分子,之间的作用力为分子间作用力(2) 1mol冰拥有2 N A氢键二氧化硅晶体原子晶体NaCl 晶体离子晶体(1) 每个碳原子都采取sp3杂化,与_4__ 个碳原子以共价键相结,—正四面体—结构,键角109° 28' 。
(2) 晶体中最小的碳环由_6_个碳组成,且不在同一平面内。
(3) 1mol金刚石中含2 N A共价键每个C原子连接12个六元环(4) 晶胞中,C位于顶点_面心_体心(5) 晶胞中,包含8个C原子(1) 1个Si原子和4个0原子形成4个共价键,每个0原子和2个Si原子相结合。
(2) 1mol Si02中含4 mol Si —0 键(3) 最小环是由6 个Si原子和6个0原子组成的12元环。
(1) 一个晶胞中,包含4个Na+, 4个Cl—(2) Na+的配位数为 6 , Cl_的配位数为 6 ,(3) Na+周围等距离最近的Na + 12 个C「周围等距离最近的Cl - 12 个(4 )晶胞中,Na +位于顶点和面心Cl「位于棱边属于正八面体结构CsCI 晶体离子晶体(1) Cs+的配位数为8 CI—的配位数为8(2) Cs+周围等距离最近的Cs+6个CI—周围等距离最近的CI—6个(3) —个晶胞中,包含1个Cs+,1个CI—(4) 晶胞中,Cs+位于―顶点_ C「位于体心CaF2 晶体离子晶体(1)Ca2+的配位数为8 , F—的配位数为4(2) Ca2+周围等距离最近的Ca2+12个F—周围等距离最近的F—8个(3) 晶胞中,包含J_个Ca2+, _8_个F—(4) 晶胞中,Ca2+位于顶点和面心_,F—位于—体心 ______石墨晶体混合晶体(1)层内一个碳原子与3个碳原子以共价键相结合,碳原子采取SP2杂化,键角120°(2)1moI石墨晶体中含_0.5_mol六元环(3)1moI石墨晶体中含_1.5_mol共价键(4)C原子与C —C键数之比为2:3(5)层间作用力是分子间作用力简单立方堆积金属晶体体心立方密堆积金属晶体(1 )典型代表Po(2) 空间利用率52%(3) 配位数6立方体的边长为 a cm,则r=a/2 cm。


晶体的七大晶系是十分专业的问题,它有时是鉴别晶体的关键,鉴藏矿晶的人多少应该知道一些。
概论已知晶体形态超过四万种,它们都是按七种结晶模式发育生长,即七大晶系。
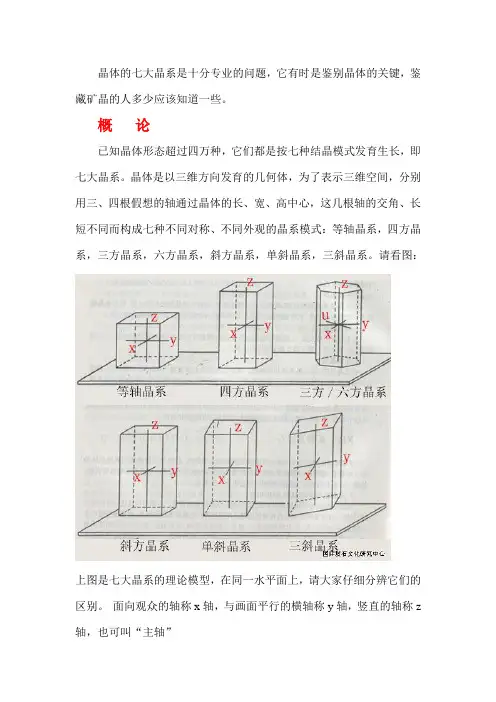
晶体是以三维方向发育的几何体,为了表示三维空间,分别用三、四根假想的轴通过晶体的长、宽、高中心,这几根轴的交角、长短不同而构成七种不同对称、不同外观的晶系模式:等轴晶系,四方晶系,三方晶系,六方晶系,斜方晶系,单斜晶系,三斜晶系。
请看图:上图是七大晶系的理论模型,在同一水平面上,请大家仔细分辨它们的区别。
面向观众的轴称x轴,与画面平行的横轴称y轴,竖直的轴称z 轴,也可叫“主轴”一,等轴晶系简介等轴晶系的三个轴长度一样,且相互垂直,对称性最强。
这个晶系的晶体通俗地说就是方块状、几何球状,从不同的角度看高低宽窄差不多。
如正方体、八面体、四面体、菱形十二面体等,它们的相对晶面和相邻晶面都相似,这种晶体的横截面和竖截面一样。
此晶系的矿物有黄铁矿、萤石、闪锌矿、石榴石,方铅矿等。
请看这种晶系的几种常见晶体的理论形态:等轴晶系的三个晶轴(x轴y轴z轴)一样长,互相垂直。
常见的等轴晶系的晶体模型图金刚石晶体八面体和立方体的聚形的方铅矿黄铁矿二,四方晶系简介四方晶系的三个晶轴相互垂直,其中两个水平轴(x轴、y轴)长度一样,但z轴的长度可长可短。
通俗地说,四方晶系的晶体大都是四棱的柱状体,(晶体横截面为正方形,但有时四个角会发育成小柱面,称“复四方”),有的是长柱体,有的是短柱体。
再,四方晶系四个柱面是对称的,即相邻和相对的柱面都一样,但和顶端不对称(不同形);所有主晶面交角都是九十度交角。
请看模型图:四方晶系的晶体如果z轴发育,它就是长柱状甚至针状;如果两个横轴(x 、y)发育大于竖轴z轴,那么该晶体就是四方板状,最有代表性的就是钼铅矿。
请看常见的一些四方晶系的晶体模型:这个晶系常见的矿物有锡石、鱼眼石、白钨矿、符山石、钼铅矿等。
请看实物图片:符山石的晶体锡石的长柱状晶体(顶端另有斜生的小晶体)。


七大晶系详细图解一、四方晶系四方晶系四方晶系的三条晶轴互相垂直,即α=β=γ=90°。
其中两个水平轴(X 轴、Y轴)长度一样,Z轴的长度可长可短,通俗的说:四方晶系的晶体大多是四棱的柱状体,有的是长柱体,有的是短柱体,即其晶胞必具有四方柱的形状。
横截面为正方形,四个柱面是对称的,即相邻和相对的柱面都是一样的,但和顶端不对称。
所有主晶面交角都是90。
特征对称元素为四重轴。
如果Z轴发育,它就是长柱状甚至针状;如果两个横轴(X轴、Y轴)发育大于Z轴,那么晶体就会呈现四方板状,最有代表的就是磷酸二氢钠和硫酸镍β了。
常见的立方晶系的晶体模型图:注:柱体的棱角发育成窄小晶面,此种晶体又叫“复四方”——四个主柱面,四个小柱面。
晶体实物图:三、斜方晶系斜方晶系的晶体中三个轴的长短完全不相等,它们的交角仍然是互为90度垂直。
即X≠Y≠Z。
Z轴和Y轴相互垂直90°。
X轴与Y轴垂直,但是不与Z轴垂直,即α=γ=90,β>90°与正方晶系直观相比,区别就是:x轴、y轴长短不一样。
如果围绕z轴旋转,四方晶系旋转九十度即可使x轴y轴重合,旋转一周使x轴y轴重合四次(使另两轴重合的次数多于两次,该轴称“高次轴”),四方晶系有一个高次轴,也叫“主轴”。
斜方晶系围绕z轴旋转,需180度才可使x轴y 轴重合,旋转一周只重合两次,属低次轴。
也就是说,斜方晶系的对称性比四方晶系要低。
特征对称元素是二重对称轴或对称面。
其实,斜方晶系的晶体如果围绕x轴或y轴旋转,情况与围绕z轴旋转相同。
换句话说,斜方晶系没有高次轴,或曰没有理论上的主轴。
从模型上看,四方晶系的x轴和y轴所指向的晶面完全都是对称相同的,斜方晶系的x轴和y轴所指向的晶面却是各自相等的。
常见立方晶系模型图:斜方晶系晶体两个轴(如x轴、y轴)构成的平面,即晶体横截面是长方形,也可以是菱形,或者两者的复合形,如下图:晶体实物图:四、单斜晶体单斜晶系的三个晶轴长短皆不一样,即X≠Y≠Z。


简介:分子式(u-SCH2CH2CH2S)Fe(CO)3Fe(CO)2[P(CH2OH)3],结晶为层状,两层分子的P(CH2OH)3基团通过氢键形成二维网络。
偶然发现二维氢键网络中的羟基氧原子从某个角度看恰好呈波浪状分布,遂画此图。
其中多面体为Fe2及其周围的配位原子,悬挂于波浪状网络的波峰和波谷。
这是首例在离子液体中的得到含有硫属阳离子族的化合物。
该化合物含有[Sb7S8Br2]3+阳离子族和[AlCl4]1-阴离子,[Sb7S8Br2]3+阳离子族由两个[Sb4S4Br]3+类立方烷通过公用一个Sb顶点组成。
[Sb7S8Br2]3+阳离子族沿a方向排列,形成的空隙被[AlCl4]1-四面体阴离子占据。
本文来自: 小木虫论坛/bbs/viewthread.php?tid=2149934&fpage=1
Angew. Chem. Int. Ed. 2004, 43, 2117 –2121
迄今最大的Mn84单分子磁体以及超分子纳米管
本文来自: 小木虫论坛
/bbs/viewthread.php?tid=2149934&fpage=1&view=&highlight=&page=2
这是从文献中找到的一个晶体的分子结构图,虽然比较简单,但是比较漂亮。
重要的是,它的结构清晰,行外人也可以理解看清!
它的中间部分是keggin结构的PMoV杂多酸,两边是2,2'-联吡啶合了Co的抗衡阳离子!本文来自: 小木虫论坛
/bbs/viewthread.php?tid=2149934&fpage=1&view=&highlight=&page=3
补充说明:第三大无机分子,分子中有176个钼,以及超过三倍的氧。
本文来自: 小木虫论坛
/bbs/viewthread.php?tid=2149934&fpage=1&view=&highlight=&page=3
分子中60个W(灰),8个P(红),12个Ti(蓝),全是最高价,全氧配位(多面体顶点)
本文来自: 小木虫论坛
/bbs/viewthread.php?tid=2149934&fpage=1&view=&highlight=&page=3
由Cu 和均苯三甲酸反应生成的一个金属有机骨架 本文来自: 小木虫论坛 /bbs/viewthread.php?tid=2149934&fpage=1&view=&highlight=&page=5。