二氟氯乙烷
- 格式:doc
- 大小:36.50 KB
- 文档页数:3

二氯二氟甲烷和二氟乙烷的抗氧化性比较分
析
二氯二氟甲烷和二氟乙烷是常见的氟代烷烃类化合物,在工业生产
和科学研究领域广泛应用。
本文将对这两种化合物的抗氧化性进行比
较分析。
二氯二氟甲烷,化学式CF2Cl2,又称Freon-12,是一种无色气体,常用作制冷剂和溶剂。
它具有较好的稳定性,能够抵抗氧化反应,因
此在一些特定领域有着重要的应用价值。
然而,随着环境保护意识的
提高,二氯二氟甲烷逐渐被淘汰,因为其在大气中可能破坏臭氧层。
相比之下,二氟乙烷,化学式C2H4F2,又称HFC-152a,是一种无
色气体,也常被用作制冷剂和发泡剂。
与二氯二氟甲烷相比,二氟乙
烷更加环保,不会对臭氧层产生危害。
因此,在目前的环境保护形势下,二氟乙烷逐渐成为了人们心目中更加理想的选择。
在抗氧化性方面,二氯二氟甲烷和二氟乙烷也有所不同。
二氯二氟
甲烷由于其分子结构的不饱和性,理论上来说在氧化反应中更容易失
去氢原子,因此其抗氧化性相对较弱。
而二氟乙烷由于分子中氢原子
的数量较多,较难被氧化,所以在一定程度上具有较好的抗氧化性。
总的来说,二氟乙烷在环保性和抗氧化性方面均优于二氯二氟甲烷。
在选择使用制冷剂和溶剂时,应该充分考虑到环境因素,并选择更加
环保和安全的替代品。
愿我们的工业生产和科学研究能够更加注重可
持续发展,共同建设一个更加美好的地球家园。

目录2.1 类易燃气体表-氢气的理化性质及危险特性 (1)表-甲烷[压缩的]的理化性质及危险特性 (2)表-天然气的理化性质及危险特性 (3)表-液化甲烷的理化性质及危险特性 (4)表-液化天然气的理化性质及危险特性 (5)表-乙烷的理化性质及危险特性 (6)表-液化乙烷的理化性质及危险特性 (7)表-丙烷的理化性质及危险特性 (8)表-正丁烷的理化性质及危险特性 (9)表-环丙烷的理化性质及危险特性 (10)表-液化乙烯的理化性质及危险特性 (11)表-丙烯的理化性质及危险特性 (12)表-异丁烯的理化性质及危险特性 (13)表-丁二烯的理化性质及危险特性 (14)表-乙炔的理化性质及危险特性 (15)表-1,1-二氟乙烷的理化性质及危险特性 (16)表-1,1,1-三氟乙烷的理化性质及危险特性 (17)表-氟乙烯[抑制了的]的理化性质及危险特性 (18)表-二氟氯乙烷的理化性质及危险特性 (19)表-环氧乙烷的理化性质及危险特性 (20)表-甲乙醚的理化性质及危险特性 (22)表-乙烯基甲醚的理化性质及危险特性 (23)表-三甲胺的理化性质及危险特性 (24)表-乙胺的理化性质及危险特性 (25)表-液化石油气的理化性质及危险特性 (26)2.2 类不燃气体表-氧气的理化性质及危险特性 (27)表-液氧的理化性质及危险特性 (28)表-空气[压缩的]的理化性质及危险特性 (29)表-氮气的理化性质及危险特性 (30)表-液氮的理化性质及危险特性 (31)表-氦气的理化性质及危险特性 (32)表-液氦的理化性质及危险特性 (33)表-氖气的理化性质及危险特性 (34)表-液氖的理化性质及危险特性 (35)表-氩气的理化性质及危险特性 (36)表-液氩的理化性质及危险特性 (37)表-一氧化二氮的理化性质及危险特性 (38)表-二氧化碳的理化性质及危险特性 (38)表-二氧化碳[液化的]的理化性质及危险特性 (39)表-六氟化硫的理化性质及危险特性 (40)表-稀有气体混合物的理化性质及危险特性 (42)表-稀有气体和氧气混合物的理化性质及危险特性 (43)表-稀有气体和氮气混合物的理化性质及危险特性 (44)表-二氧化碳和氧气混合物的理化性质及危险特性 (46)表-二氧化碳和一氧化二氮混合物的理化性质及危险特性 (47)表-二氧化碳和环氧乙烷混合物的理化性质及危险特性 (48)表-三氟甲烷的理化性质及危险特性表 (49)表-四氟甲烷的理化性质及危险特性 (50)表-氯二氟甲烷的理化性质及危险特性 (51)表-氯三氟甲烷的理化性质及危险特性 (52)表-氯四氟乙烷的理化性质及危险特性 (53)表-二氯二氟甲烷的理化性质及危险特性 (54)表-二氯四氟乙烷的理化性质及危险特性 (55)表-三氯一氟甲烷的理化性质及危险特性 (56)表-氯二氟甲烷和氯五氟乙烷共沸物的理化性质及危险特性 (57)2.3 类有毒气体表-液氯的理化性质及危险特性 (58)表-液氨的理化性质及危险特性 (59)无货物危险编号表- 1,1,1,2-四氟乙烷的理化性质及危险特性 (60)表-五氟乙烷的理化性质及危险特性 (61)表-氢气的理化性质及危险特性表-甲烷[压缩的]的理化性质及危险特性表-天然气的理化性质及危险特性表-液化甲烷的理化性质及危险特性表-液化天然气的理化性质及危险特性表-乙烷的理化性质及危险特性表-液化乙烷的理化性质及危险特性表-丙烷的理化性质及危险特性表-液化乙烯的理化性质及危险特性表-丙烯的理化性质及危险特性表-乙炔的理化性质及危险特性表-1,1-二氟乙烷的理化性质及危险特性表-1,1,1-三氟乙烷的理化性质及危险特性表-氟乙烯[抑制了的]的理化性质及危险特性表-二氟氯乙烷的理化性质及危险特性表-环氧乙烷的理化性质及危险特性表-(二)甲醚的理化性质及危险特性表-甲乙醚的理化性质及危险特性表-乙烯基甲醚的理化性质及危险特性表-三甲胺的理化性质及危险特性表-乙胺的理化性质及危险特性表-液化石油气的理化性质及危险特性表-氧气的理化性质及危险特性表-液氧的理化性质及危险特性表-空气[压缩的]的理化性质及危险特性表-一氧化二氮的理化性质及危险特性表-二氧化碳的理化性质及危险特性表-二氧化碳[液化的]的理化性质及危险特性表-六氟化硫的理化性质及危险特性表-氯化氢的理化性质及危险特性表-稀有气体混合物的理化性质及危险特性表-稀有气体和氧气混合物的理化性质及危险特性表-稀有气体和氮气混合物的理化性质及危险特性表-二氧化碳和氧气混合物的理化性质及危险特性表-二氧化碳和一氧化二氮混合物的理化性质及危险特性。

液化气体气瓶充装规定GB14193—93国家技术监督局1993—03—12批准1993—09—01实施1 主题内容与适用范围本标准规定了液化气体气瓶充装的基本原则和安全技术要求。
本标准适用于高压液化气体气瓶和在最高使用温度下饱和蒸气压力不小于0.1MPa(表压,下同)的低压液化气体气瓶的充装。
本标准不适用于用罐车充装液化气体。
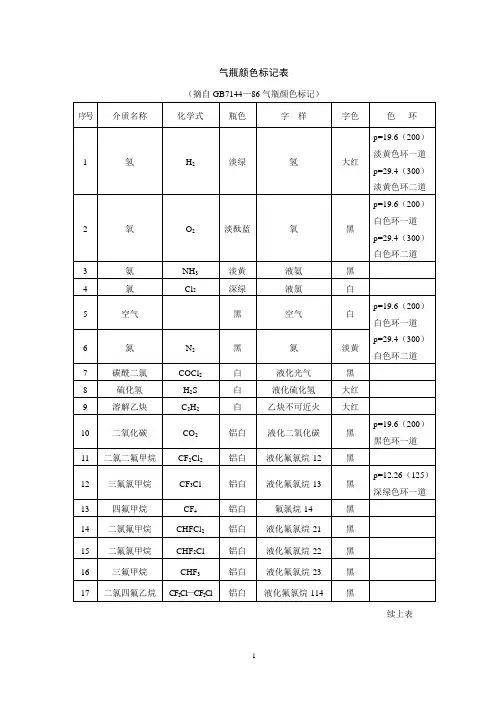
2 引用标准GB7144 气瓶颜色标记3 术语对本标准所采用的术语定义如下:3.1 液化气体介质在最高使用温度下的饱和蒸气压力不小于0.1MPa,且临界温度不低于-10℃的气体。
3.2 高压液化气体临界温度低于或等于70℃的液化气体。
3.3 低压液化气体临界温度高于70℃的液化气体。
3.4 最高使用温度高压液化气体气瓶在正常贮存、运输和使用过程中受环境条件的影响,瓶内气体可能达到的最高温度。
3.5 最高气相介质温度低压液化气体气瓶在正常贮存、运输和使用过程中受环境条件的影响,瓶内气相介质可能达到的最高温度。
3.6 最高液相介质温度低压液化气体气瓶在整个运行过程中受环境条件的影响,瓶内液相介质可能达到的最高平均温度。
3.7 充装系数气瓶单位容积内充装液化气体的质量。
3.8 许用压力为保证气瓶安全,允许瓶内达到的最高压强。
3.9 剩余压力气瓶充装前瓶内所剩余的液化气体的压强。
4 充装前的检查与处理4.1 充装操作人员应熟悉所装介质的特性(燃、毒及腐蚀性等)及其与气瓶材料(包括瓶体及瓶阀等附件)的相容性。
常用液化气体的特性及其与金属材料的相容性可参考附录A(参考件)。
4.2 充装前的气瓶应由专人负责,逐只进行检查,检查内容至少应包括:a.国产气瓶是否是由具有“气瓶制造许可证”的单位生产的;b.气瓶外表面的颜色标记是否与所装气体的规定标记相符;c.气瓶瓶阀的出口螺纹型式是否与所装气体的规定相符:即可燃气体用的瓶阀,出口螺纹是左旋的;非可燃性气体用的瓶阀,出口螺纹是右旋的;d.气瓶内有无剩余压力。

二氯二氟甲烷和二氟乙烷在医药领域中的应
用比较
在医药领域中,化学品的应用越来越广泛,其中二氯二氟甲烷和二
氟乙烷是两种常见的化学品。
它们在医药领域中的应用有着各自的优
势和特点。
本文将就二氯二氟甲烷和二氟乙烷在医药领域中的应用进
行比较。
首先,二氯二氟甲烷,又称为氟利昂,是一种惰性气体,具有较好
的稳定性和化学惰性。
它主要用于麻醉手术中,具有麻醉快速、深度
麻醉程度可控等优点。
二氯二氟甲烷在医药领域中广泛用于各种手术
麻醉,例如心脏手术、神经外科手术等。
其麻醉效果明显,操作方便,极大地减少了手术病人的疼痛感受,提高了手术的成功率。
相比之下,二氟乙烷也是一种用途广泛的麻醉剂。
它是一种液体麻
醉剂,具有挥发性好、麻醉速度快等特点。
二氟乙烷主要用于一些较
小规模的手术麻醉,如牙科手术、皮肤手术等。
它的作用持续时间短,醒来后恢复快,方便患者的手术康复。
在使用上,二氟乙烷相比较于二氯二氟甲烷更加灵活,医生可以更
准确地控制麻醉的深度和时间,避免因为过度麻醉或不足麻醉而导致
的风险。
此外,二氟乙烷在操作过程中更为方便,不需要像二氯二氟
甲烷那样需要特殊的麻醉设备,只需简单的吸入即可实现全身麻醉效果。
总的来说,二氯二氟甲烷和二氟乙烷在医药领域中都有着各自独特的优点和应用范围。
医生在选择使用时应根据患者的具体情况和手术类型来进行合理选择,以确保手术的顺利进行和患者的安全。
希望未来能有更多的研究和创新,使得医药领域的麻醉技术能够得到更好的发展和提升。

二氯二氟甲烷和二氟乙烷的电解性能比较分
析
二氯二氟甲烷和二氟乙烷是两种常见的卤代烷烃化合物,它们在化
工领域有着广泛的应用。
本文将对这两种化合物的电解性能进行比较
分析。
一、二氯二氟甲烷的电解性能
二氯二氟甲烷,化学式为CF2Cl2,又称为Freon-12,是一种无色气体,常用作制冷剂。
在电解方面,二氯二氟甲烷的电化学稳定性较好,其在电解过程中能够稳定地释放氯气和氟气,同时在电极上不易发生
副反应。
这使得二氯二氟甲烷在电化学领域有着一定的应用前景。
二、二氟乙烷的电解性能
二氟乙烷,化学式为C2F4,是一种化学稳定性较高的气体,常用
作离子交换膜和氟化合物的原料。
在电解方面,二氟乙烷的电化学活
性较低,其在电解过程中释放的氟气反应性较弱,且易于发生电解液
的水解反应。
这使得二氟乙烷在高效电解中表现不佳,限制了其在电
化学领域的应用。
三、二氯二氟甲烷和二氟乙烷的比较分析
综合比较二氯二氟甲烷和二氟乙烷的电解性能,可以得出以下结论:二氯二氟甲烷在电化学稳定性方面表现较好,适合用于要求高稳定性
的电解体系;而二氟乙烷在电化学活性方面表现较弱,适合用于要求
低活性的电解体系。
综上所述,二氯二氟甲烷和二氟乙烷在电解性能上存在一定的差异,选择合适的化合物应根据具体的电解要求来决定,以达到最佳的电解
效果。
希望本文的比较分析对读者在实际应用中有所帮助。

二氯二氟甲烷和二氟乙烷的分子结构和性质
比较
二氯二氟甲烷和二氟乙烷是两种常见的卤代烷烃化合物,它们在化学结构和性质上存在一些显著的区别。
在本文中,将对这两种化合物的分子结构和性质进行比较分析。
二氯二氟甲烷(CF2Cl2),又称为氟利昂12,是一种无色气味淡微类似氯仿的气体。
它的分子结构中含有两个氟原子和两个氯原子,呈现出对称的四氯乙烷结构。
而二氟乙烷(C2H4F2),又称为氟利昂152a,则是一种无色有刺激性气味的液体,其分子结构中含有两个氟原子和四个氢原子,呈现出对称的二氟环丙烷结构。
从分子结构来看,二氯二氟甲烷中含有氯原子,而二氟乙烷中不含氯原子,这导致了它们在化学性质上的一些差异。
二氯二氟甲烷具有较高的化学惰性,稳定性较好,不易发生化学反应;而二氟乙烷则相对较活泼,容易与其他物质发生反应。
在物理性质方面,二氯二氟甲烷的沸点较低,为29.8摄氏度,而二氟乙烷的沸点较高,为53.4摄氏度。
这是由于二氯二氟甲烷的分子质量更大,分子间的分子力较强,因此需要更高的温度才能使其蒸发。
此外,二氯二氟甲烷和二氟乙烷在实际应用中具有不同的用途。
二氯二氟甲烷主要用作制冷剂、干洗剂等工业用途,而二氟乙烷则更常用于制备高性能的聚酰胺树脂和医药领域。
综上所述,二氯二氟甲烷和二氟乙烷在分子结构和性质上存在一些明显的差异,这些差异导致了它们在化学性质、物理性质和应用领域上的不同表现。
对于化学研究和实际应用而言,了解和掌握这些差异将有助于更好地利用它们的特性。
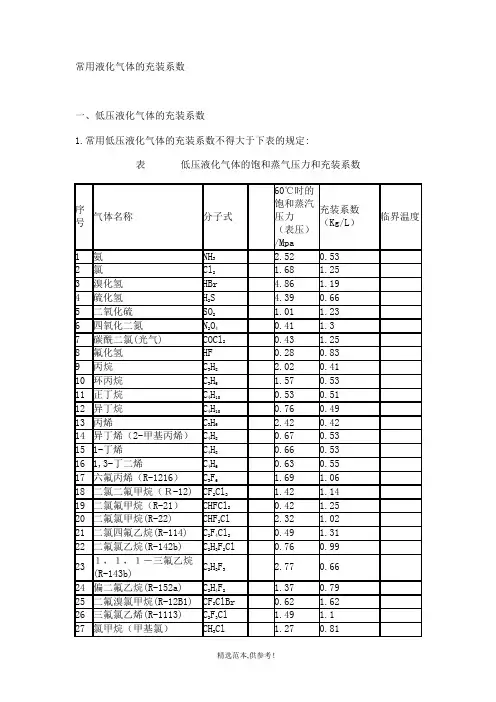
常用液化气体的充装系数
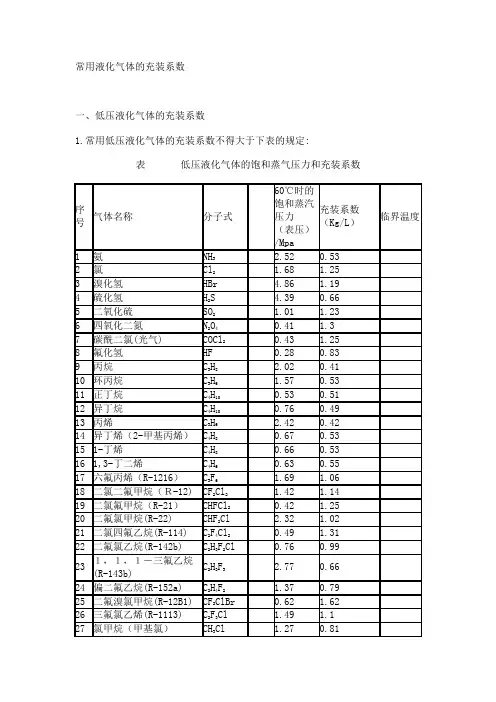
一、低压液化气体的充装系数
1.常用低压液化气体的充装系数不得大于下表的规定:
表低压液化气体的饱和蒸气压力和充装系数
2.其他液化气体的充装系数不得大于由以下公式计算确定的值
式中:
——低压液化气体的充装系数,单位为千克每升(kg/L);
——低压液化气体在最高液相介质温度下的密度,单位为千克每升(kg/L);C——液体密度的最大负偏差,一般情况,C取0~3。
【本文档内容可以自由复制内容或自由编辑修改内容期待
你的好评和关注,我们将会做得更好】。

2019年第50卷第8期1,1-二氟-1,2-二氯乙烷的应用徐卫国,张建君(浙江省化工研究院有限公司,浙江杭州310023)摘要:本文介绍了1,1-二氟-1,2-二氯乙烷的应用。
关键词:1,1-二氟-1,2-二氯乙烷;应用文章编号:1006-4184(2019)08-0001-050前言1,1-二氟-1,2-二氯乙烷是一种含氢氯氟烃化合物(HCFC-132b ,1),英文名:1,1-difluoro-1,2-dichloroethane ,CAS 号:1649-08-7,分子式:CF 2ClCH 2Cl ,分子量:134.94,熔点:-101.2℃,沸点:46℃~47℃,密度:1.416g/cm 3。
图1HCFC-132b 的结构1制备制冷剂1991年,美国纳幕尔杜邦公司的Edward 等人[1]发明了一种将HCFC-132b 一端的氯原子氟化的方法。
将粒度为6~8目的碳颗粒浸泡在20%(重量)KF 水溶液中,置于不锈钢反应管中,在200℃下用干燥N 2吹扫干燥。
然后将该反应管加热至238℃,同时使干燥N 2流通过反应管。
用气体HCFC-132b 代替N 2进气,以大约0.8g/min的速度送入蒸发器中,加热转化为蒸汽,流速为约130mL/min 。
反应开始后100min 即对流出的产物进行取样,在80min 内每5min 取样一次。
在100min 的时间点,HCFC-132b 的转化率约为30%,生成CF 2ClCH 2F 的选择性约为55%。
在之后的10min 内,HCFC-132b 的转化率和产物选择性都降至10%左右,而之后的操作时间内均维持在5%~10%。
得到产物基本上是CF 2ClCH 2F 。
1998年,林永达等人[2]发明了一种由HCFC-132b 氟化制备新型制冷剂1,1,1,2-四氟乙烷的方法,它对大气臭氧层是安全的,可用以代替氯氟烃CFC-12广泛用于家用冰箱、汽车空调及冰柜等作致冷剂。
常用液化气体的充装系数 (2011-02-27 14:58:17)一、低压液化气体的充装系数1.常用低压液化气体的充装系数不得大于下表的规定:表低压液化气体的饱和蒸气压力和充装系数序号气体名称分子式 60℃时的饱和蒸汽压力(表压)/Mpa 充装系数(Kg/L)临界温度1 氨 NH3 2.52 0.532 氯 Cl2 1.68 1.253 溴化氢 HBr 4.86 1.194 硫化氢 H2S 4.39 0.665 二氧化硫 SO2 1.01 1.236 四氧化二氮 N2O4 0.41 1.37 碳酰二氯(光气) COCl2 0.43 1.258 氟化氢 HF 0.28 0.839 丙烷 C3H8 2.02 0.4110 环丙烷 C3H6 1.57 0.5311 正丁烷 C4H10 0.53 0.5112 异丁烷 C4H10 0.76 0.4913 丙烯 C3H6 2.42 0.4214 异丁烯(2-甲基丙烯) C4H8 0.67 0.5315 1-丁烯 C4H8 0.66 0.5316 1,3-丁二烯 C4H6 0.63 0.5517 六氟丙烯(R-1216) C3F6 1.69 1.0618 二氯二氟甲烷(R-12) CF2Cl2 1.42 1.1419 二氯氟甲烷(R-21) CHFCl2 0.42 1.2520 二氟氯甲烷(R-22) CHF2Cl 2.32 1.0221 二氯四氟乙烷(R-114) C2F4Cl2 0.49 1.3122 二氟氯乙烷(R-142b) C2H3F2Cl 0.76 0.9923 1,1,1-三氟乙烷(R-143b) C2H3F3 2.77 0.6624 偏二氟乙烷(R-152a) C2H4F2 1.37 0.7925 二氟溴氯甲烷(R-12B1) CF2ClBr 0.62 1.6226 三氟氯乙烯(R-1113) C2F3Cl 1.49 1.127 氯甲烷(甲基氯) CH3Cl 1.27 0.8128 氯乙烷(乙基氯) C2H5Cl 0.35 0.829 氯乙烯(乙烯基氯) C2H3Cl 0.91 0.8230 溴甲烷(甲基溴) CH3Br 0.52 1.531 溴乙烯(乙烯基溴) C2H3Br 0.35 1.2832 甲胺 CH3NH2 0.94 0.633 二甲胺 (CH3)NH 0.51 0.5834 三甲胺 (CH3)3N 0.49 0.5635 乙胺 C2H5NH2 0.34 0.6236 二甲醚(甲醚) C2H6O 1.35 0.5837 乙烯基甲醚(甲基乙烯基醚) C3H6O 0.4 0.6738 环氧乙烷(氧化乙烯) C2H4O 0..44 0.7939 顺2-丁烯 C4H8 0.48 0.5540 反2-丁烯 C4H8 0.52 0.5441 五氟氯乙烷(R-115) C2F5Cl 1.97 1.0342 八氟环丁烷(RC-318) C4F8 0.76 1.3143 三氯化硼 BCl3 0.32 1.244 甲硫醇(硫氢甲烷) CH3SH 0.47 0.7845 三氟氯乙烷(R-133a) C2H2F3Cl 0.52 1.182.其他液化气体的充装系数不得大于由以下公式计算确定的值式中:——低压液化气体的充装系数,单位为千克每升(kg/L);——低压液化气体在最高液相介质温度下的密度,单位为千克每升(kg/L);C——液体密度的最大负偏差,一般情况,C取0~3。
第一部分化学品及企业标识化学品中文名:1-氯-1,1-二氟乙烷化学品英文名:1-chloro-1,1-dinuoroethane;RI42;chlorodi∩uoroethane化学品别名:R142;二氟氯乙烷CASNo.:75-68-3ECNo.:200-891-8分子式:C2H3C1F2第二部分危险性概述紧急情况概述液体。
极端易燃,有爆炸危险。
高压,遇热有爆炸危险。
对眼睛有刺激性。
对水生环境可能会引起长期有害作用。
对臭氧层有危害。
GHS危险性类别根据GB3()()()()-2013化学品分类和标签规范系列标准(参阅第十六部分),该产品分类如下:易燃气体,类别1;高压气体,压缩气体;眼损伤/眼刺激,类别2B;危害水生环境.慢性毒性,类别3:危害臭氧层,类别1。
标签要素象形图警示词:危险危险信息:极端易燃气体,内装高压气体;遇热可能爆炸,造成眼刺激,对水生生物有害并具有长期持续影响,破坏高层大气中的臭氧,危害公共健康和环境。
预防措施:远离热源、热表面、火花、明火以及其它点火源。
禁止吸烟。
作业后彻底清洗。
避免释放到环境中。
事故响应:漏气着火:切勿灭火,除非漏气能够安全地制止。
一旦发生泄漏,除去所有点火源。
如仍觉眼刺激:求医/就诊。
如进入眼睛:用水小心冲洗几分钟。
如戴隐形眼镜并可方便地取出,取出隐形眼镜。
继续冲洗。
安全储存:存放在通风良好的地方。
防日晒。
存放于通风良好处。
废弃处置:按照地方/区域/国家/国际规章处置内装物/容器。
物理化学危险:极端易燃气体,有爆炸危险。
高压压缩气体,遇热有爆炸危险。
健康危害:吸入该物质可能会引起对健康有害的影响或呼吸道不适。
意外食入本品可能对个体健康有害。
通过割伤、擦伤或病变处进入血液,可能产生全身损伤的有害作用。
本品对眼睛有轻微刺激。
眼睛直接接触本品可导致暂时不适。
环境危害:本品对水生生物有害并具有长期持续影响。
请参阅SDS第十二部分。
第三部分成分/组成信息V物质混合物第四部分急救措施一般性建议:急救措施通常是需要的,请将本SDS出示给到达现场的医生。
制冷剂r22 成分
制冷剂R22,也称为氟利昂22,是一种氟氯烃类化合物,化学名称为氯二氟一氯乙烷(chlorodifluoromethane)。
其化学结构为CHClF2,由1个氯原子、2个氟原子和1个氢原子组成。
R22是一种无色、无味、无毒的气体,在工业和家用空调系统中被广泛使用作为制冷剂。
然而,由于其对臭氧层的破坏作用,R22已经被列为温室气体,逐渐被淘汰和取代。
从化学成分角度来看,R22是由氯、氟和碳三种元素组成的化合物。
氯元素赋予了其制冷性能,而氟元素则提供了稳定性和其他特性。
这些成分的比例和结构使R22成为一种理想的制冷剂,但也导致了其对环境的负面影响。
除了化学成分外,我们还可以从其他角度来看R22的成分。
例如,从环境影响的角度来看,R22的成分对臭氧层的破坏效应已经得到广泛认可。
因此,国际社会已经采取了措施逐步淘汰R22的使用,以减少对臭氧层的破坏。
从替代品的角度来看,由于R22的逐渐淘汰,人们开始寻找更环保的替代品,例如R410A和R134a等制冷剂,这些替代品在化学成分上也有所不同。
总的来说,R22的化学成分是氯、氟和碳的化合物,但从不同角度来看,我们可以对其成分有不同的理解和关注点。
二氯二氟甲烷和二氟乙烷在化妆品中的应用
对比
二氯二氟甲烷和二氟乙烷是两种在化妆品中广泛应用的气体。
它们分别具有不同的特性和用途。
下面将对二氯二氟甲烷和二氟乙烷在化妆品中的应用进行比较。
二氯二氟甲烷,化学式为CCl2F2,常用作喷雾剂中的推进剂。
它是一种无色无味的气体,具有较低的沸点和较高的压缩性。
在化妆品中,二氯二氟甲烷常被用于雾化喷雾瓶中,可以帮助将产品均匀地喷洒在皮肤表面,使化妆品更容易被吸收。
相比之下,二氟乙烷的化学式为C2H4F2,也是一种常用的气体推进剂。
二氟乙烷气体具有较高的稳定性和较低的毒性,被广泛用于医药领域和化妆品生产中。
在化妆品中,二氟乙烷可以作为喷雾剂的推进剂,同样具有促进产品均匀喷洒的功能。
从使用效果来看,二氟乙烷相对于二氯二氟甲烷具有更好的稳定性和安全性。
二氟乙烷在喷雾剂中可以更好地控制流量和喷洒范围,同时对环境的影响也较小。
因此,在许多高端化妆品中,二氟乙烷更受欢迎。
综上所述,二氯二氟甲烷和二氟乙烷都是常见的化妆品中推进剂,但二氟乙烷在稳定性和安全性方面更具优势。
在选择化妆品时,可以根据个人喜好和肤质选择适合自己的产品。
1、物质的理化常数
CA
国标编号: 21033
75-68-3
S:
中文名称: 二氟氯乙烷
英文名称: chlorodifluoroethane;1,1-diflu
别名: R142;一氯二氟乙烷;1,1-二氟-1-氯乙烷
分子
分子式: C2H3ClF2;CH3CClF2
100.5
量:
熔点: -131℃
密度: 相对密度(水=1)1.1;?
蒸汽压:
溶解性: 微溶于水
稳定性: 稳定
外观与性
无色气体
状:
危险标记: 4(易燃气体)
用途: 用作致冷剂
2.对环境的影响:
该物质对环境有危害,应特别注意对大气臭氧层的污染。
氟代烃在低层大气中比较稳定,而在上层大气中可被能量更强的紫外线分解。
该物质对大气臭氧层破坏力极强。
一、健康危害
侵入途径:吸入。
健康危害:吸入高浓度本品,有可能引起心律不齐、昏迷甚至死亡。
接触本品液体可致冻伤。
二、毒理学资料及环境行为
毒性:属低毒类。
急性毒性:LC50523520mg/m3,4小时(大鼠吸入);豚鼠吸入58%×8分钟,致死;豚鼠吸入16%×55分钟,肌肉颤动,痉挛
亚急性和慢性毒性:兔吸入14200ppm×6小时/日×30日,存活,心、肝、肾及神经系统有退行性变。
特殊毒性:Ames试验鼠伤寒沙门氏菌,TA1535TA100阳性。
危险特性:与空气混合能形成爆炸性混合物。
遇热源和明火有燃烧爆炸的危险。
受热分解放出有毒的氟化物气体。
与氧化剂接触会猛烈反应。
气体比空气重,能在较低处扩散到相当远的地方,遇明火会引着回燃。
燃烧(分解)产物:一氧化碳、二氧化碳、氟化氢、氯化氢。
3.现场应急监测方法:
4.实验室监测方法:
气相色谱法
5.环境标准:
前苏联车间空气中有害物质的最高容许浓度 3000mg/m3
6.应急处理处置方法:
一、泄漏应急处理
迅速撤离泄漏污染区人员至上风处,并进行隔离,严格限制出入。
切断火源。
建议应急处理人员戴自给正压式呼吸器,穿消防防护服。
尽可能切断泄漏源。
合理通风,加速扩散。
喷雾状水稀释、溶解。
构筑围堤或挖坑收容产生的大量废水。
如有可能,将残余气或漏出气用排风机送至水洗塔或与塔相连的通风橱内。
漏气容器要妥善处理,修复、检验后再用。
二、防护措施
呼吸系统防护:一般不需要特殊防护,高浓度接触时可佩戴自吸过滤式防毒面具(半面罩)。
眼睛防护:一般不需要特殊防护。
身体防护:穿防静电工作服。
手防护:戴一般作业防护手套。
其它:工作现场严禁吸烟。
避免高浓度吸入。
三、急救措施
皮肤接触:若有冻伤,就医治疗。
吸入:迅速脱离现场至空气新鲜处。
保持呼吸道通畅。
如呼吸困难,给输氧。
如呼吸停止,立即进行人工呼吸。
就医。
灭火方法:切断气源。
若不能立即切断气源,则不允许熄灭正在燃烧的气体。
喷水冷却容器,可能的话将容器从火场移至空旷处。
灭火剂:雾状水、泡沫、干粉、二氧化碳。