常用标准溶液的配制和标定
- 格式:doc
- 大小:99.50 KB
- 文档页数:19

标准溶液的配置及标定方法1、0.1moL/L 氢氧化钠的配制及标定(1) 配制:将氢氧化钠配制成饱和溶液(约为52%),贮存于乙烯塑料瓶内,密闭放置数日,使碳酸钠沉淀。
小心吸取8.2mL上清液,加无二氧化碳的纯水稀释为1000mL。
(2)标定:准确称取0.5~0.6g于105~110℃烘干至恒重的基准邻苯二甲酸氢钾,共称三份。
分别置于250mL三角瓶内,加入不含二氧化碳的纯水使邻苯二甲酸氢钾溶解。
加2滴1%酚酞指示剂溶液,用0.1moL/L氢氧化钠溶液滴定至溶液显淡粉红色,即到终点。
同时作空白。
按下式计算氢氧化钠溶液的准确浓度:C=m×1000/(V-V)×204.22 21式中:C-----氢氧化钠溶液的浓度,moL/L;m----邻苯二甲酸氢钾质量,g;V----滴定邻苯二甲酸氢钾氢氧化钠用量,mL;1V----空白试验氢氧化钠用量,mL;2204.22--邻苯二甲酸氢钾的式量。
(3)贮存于塑料瓶中,如需要其它浓度的氢氧化钠溶液,可取浓氢氧化钠溶液照上法稀释后标定,或直接以0.1moL/L标准溶液稀释即得。
2、0.1moL/L盐酸标准溶液配制及标定(1)配制:量取9mL浓盐酸,用纯水稀释为1000mL,混匀。
此溶液的浓度为0.1moL/L。
(2)标定:准确称取0.15~0.2g于270~300℃灼烧至恒重的基准无水碳酸钠。
共称三份,分别于250mL三角烧瓶中,各加50mL纯水使之溶解,加1~2滴甲基橙指示剂,用上述盐酸滴定至溶液由黄色变为橙色。
同时作空白试验。
按下式计算HCL溶液的准确浓度:C= 2m×1000/(V-V)*M21 1式中:C-----盐酸溶液的浓度,moL/L;m---无水碳酸钠的质量,g;V---滴定碳酸钠消耗的盐酸溶液体积,mL;1V---空白试验消耗盐酸的体积,mL;2M(106.0)--碳酸钠的式量。
3、0.02moL/L乙二胺四乙酸二钠标准溶液配制及标定(1)配制:称取7.5g乙二胺四乙酸二钠(即EDTA—2Na),溶于纯水中,并稀释为1000mL,摇匀即得。

标准溶液的配制与标定国标一、引言。
标准溶液是化学分析中常用的一种溶液,它的配制和标定对于化学实验的准确性和可靠性具有重要意义。
本文将就标准溶液的配制和标定国标进行详细介绍,希望能够为广大化学实验工作者提供一些帮助。
二、标准溶液的配制。
1. 选择适当的试剂。
在配制标准溶液时,首先要选择优质的试剂。
试剂的纯度和稳定性对于标准溶液的质量起着决定性的作用,因此在选择试剂时应该选择国家标准规定的优质产品。
2. 精确称量。
在配制标准溶液时,要求精确称量试剂,尽量避免误差的产生。
可以使用精密天平进行称量,确保所称量的试剂质量准确无误。
3. 溶解和稀释。
将精确称量的试剂溶解于适量的溶剂中,并进行充分的混合。
在稀释时,应该严格按照配制标准溶液的要求进行,避免溶液浓度的误差。
三、标准溶液的标定。
1. 标定条件。
在进行标准溶液的标定时,需要在一定的条件下进行,如恒温、恒压、恒容等条件下进行标定,以保证实验结果的准确性。
2. 使用标准物质。
在进行标定时,需要使用已知浓度的标准物质作为参比物质,通过与标准物质进行比较,来确定待测溶液的浓度。
3. 计算标定结果。
通过标定实验的数据,可以利用相关的计算方法来计算出标准溶液的浓度,得到准确的标定结果。
四、国家标准。
我国对于标准溶液的配制和标定制定了一系列的国家标准,其中包括溶液的配制方法、标定方法、质量要求等内容。
在进行标准溶液的配制和标定时,应该严格按照国家标准的要求进行,以确保标准溶液的质量和准确性。
五、结论。
标准溶液的配制和标定是化学实验中非常重要的环节,它直接关系到实验结果的准确性和可靠性。
在进行配制和标定时,需要严格按照相关的要求进行,并且要选择优质的试剂和严格控制实验条件,以确保标准溶液的质量和准确性。
同时,要遵守国家标准的要求,以确保实验结果的可比性和可靠性。
六、参考文献。
[1] 《标准溶液的配制和标定国家标准》。
[2] 《化学实验技术手册》。
[3] 《化学分析实验指导》。

标准溶液的配制与标定一、引言。
标准溶液是化学分析中常用的一种溶液,它的浓度和成分都是已知的,可以作为定量分析的参照物。
因此,准确配制和标定标准溶液是化学分析中非常重要的实验操作。
二、标准溶液的配制。
1. 选择适当的试剂。
在配制标准溶液时,首先要选择纯度高、稳定性好的试剂作为原料。
同时,要根据需要选择适当的试剂浓度,以便于后续的稀释操作。
2. 精确称量。
在配制标准溶液时,必须使用精密的天平进行称量,保证称取的质量准确无误。
在称取试剂时,应该避免试剂的飞溅和挥发,以免影响溶液的浓度。
3. 溶解和稀释。
将称取的试剂溶解到容量瓶中,使用蒸馏水或者其他纯净水进行稀释,直至液面达到刻度线。
在溶解和稀释的过程中,要充分搅拌,保证试剂充分混合。
4. 校正容量。
配制好标准溶液后,要使用已知浓度的标准溶液对其进行校正,确保其浓度准确无误。
校正容量的过程中,要注意控制温度和操作规范,以保证标准溶液的准确性。
三、标准溶液的标定。
1. 选择适当的指示物。
在标定标准溶液时,需要选择适当的指示物,以便于观察溶液的终点。
常用的指示物有酚酞、甲基橙等,选择指示物要根据实验的需要和溶液的性质来确定。
2. 逐滴加入。
在标定标准溶液时,需要逐滴加入滴定液,直至出现颜色变化。
在加入滴定液的过程中,要缓慢搅拌,控制加液速度,以免出现误差。
3. 计算浓度。
标定完成后,根据滴定液的用量和标准溶液的浓度,可以计算出被测物质的浓度。
在计算浓度时,要注意数据的准确性和计算方法的正确性。
四、实验注意事项。
1. 实验操作要规范。
在配制和标定标准溶液时,实验操作要规范,遵循实验操作规程,严格按照操作步骤进行操作,以保证实验结果的准确性。
2. 仪器仪表要准确。
在实验中要使用准确的仪器仪表,如精密天平、容量瓶、滴定管等,以保证实验数据的准确性。
3. 废液处理要当心。
实验结束后,废液要进行妥善处理,避免对环境造成污染。
五、结论。
标准溶液的配制和标定是化学分析中重要的实验操作,正确的操作方法和严格的操作规范对实验结果的准确性起着决定性的作用。
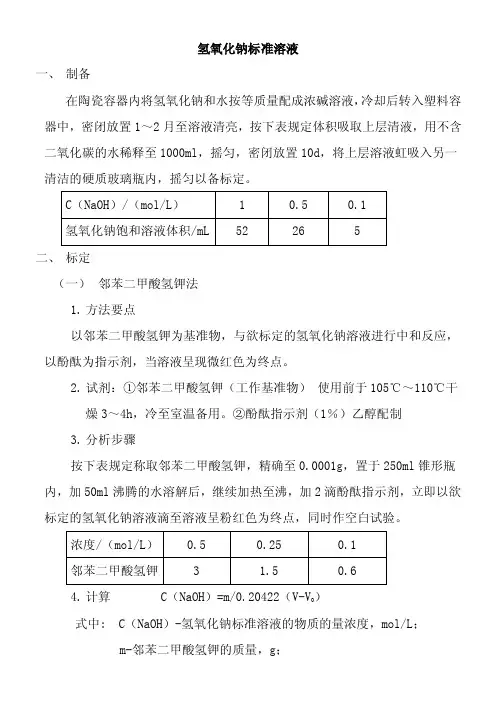
氢氧化钠标准溶液一、制备在陶瓷容器内将氢氧化钠和水按等质量配成浓碱溶液,冷却后转入塑料容器中,密闭放置1~2月至溶液清亮,按下表规定体积吸取上层清液,用不含二氧化碳的水稀释至1000ml,摇匀,密闭放置10d,将上层溶液虹吸入另一清洁的硬质玻璃瓶内,摇匀以备标定。
二、标定(一)邻苯二甲酸氢钾法1.方法要点以邻苯二甲酸氢钾为基准物,与欲标定的氢氧化钠溶液进行中和反应,以酚酞为指示剂,当溶液呈现微红色为终点。
2.试剂:①邻苯二甲酸氢钾(工作基准物)使用前于105℃~110℃干燥3~4h,冷至室温备用。
②酚酞指示剂(1%)乙醇配制3.分析步骤按下表规定称取邻苯二甲酸氢钾,精确至0.0001g,置于250ml锥形瓶内,加50ml沸腾的水溶解后,继续加热至沸,加2滴酚酞指示剂,立即以欲标定的氢氧化钠溶液滴至溶液呈粉红色为终点,同时作空白试验。
4.计算 C(NaOH)=m/0.20422(V-V0)式中: C(NaOH)-氢氧化钠标准溶液的物质的量浓度,mol/L;V-氢氧化钠溶液的用量,mL;V0-空白试验氢氧化钠溶液的用量,mL.(二)酸碱对照法1.方法要点以酸标准溶液为基准物,与欲标定的氢氧化钠溶液进行中和反应,生成盐和水。
2.试剂:①酸标准溶液。
②甲基橙指示剂(0.1%)3.分析步骤量取20.00~30.00ml欲标定的碱溶液于250ml锥形瓶内,加1滴甲基橙指示剂,用酸标准溶液滴至溶液由黄色转为橙色为终点。
4.计算 C(NaOH)=c1*V1/V式中 :C(NaOH)-氢氧化钠标准溶液的物质的量浓度,mol/L;C1-酸标准溶液的物质的量浓度,mol/L;V1-酸标准溶液的用量,mL;V-氢氧化钠的用量,mL。
锌盐标准溶液国家标准GB/T601-1988中有:氯化锌标准溶液。
国家军用标准GJB1886-1994中有:乙酸锌标准溶液,硫酸锌标准溶液,氯化锌标准溶液,硝酸锌标准溶液。
本节介绍乙酸锌标准溶液。

标准溶液的配制及标定标准一、引言。
标准溶液是化学分析中常用的一种溶液类型,其浓度和成分都是已知的,可以用于测定未知物质的浓度或者进行定量分析。
因此,正确地配制和标定标准溶液对于化学分析工作至关重要。
本文将详细介绍标准溶液的配制方法和标定标准的标准操作流程。
二、标准溶液的配制。
1. 选择适当的试剂。
在配制标准溶液之前,首先需要选择适当的试剂。
试剂的纯度和稳定性对于标准溶液的质量有着重要的影响,因此在选择试剂时需要严格按照实验要求进行。
同时,要注意试剂的保存条件,避免因为试剂的质量不佳而影响标准溶液的质量。
2. 确定浓度。
确定所需标准溶液的浓度是配制标准溶液的第一步。
根据实验需求和已知试剂的浓度,可以通过计算来确定所需试剂的用量和稀释倍数。
3. 按照配制方法进行操作。
在配制标准溶液时,需要按照一定的配制方法进行操作。
通常情况下,可以先称取一定质量的试剂,然后加入适量的溶剂进行稀释,最终得到所需浓度的标准溶液。
三、标准溶液的标定。
1. 标定设备准备。
在进行标定标准溶液之前,需要准备好标定所需的设备。
通常情况下,需要使用容量瓶、分析天平、移液器等设备,并且需要对这些设备进行预处理,以确保实验的准确性。
2. 标定操作流程。
标定标准溶液的操作流程通常包括以下几个步骤,首先是称取一定体积的标准溶液,然后将其转移至容量瓶中,并用去离子水稀释至刻度线。
接着是使用分析天平称取待测溶液,加入适量指示剂,最后滴定至终点。
3. 数据处理和结果分析。
在完成标定操作后,需要对实验数据进行处理和结果分析。
通常情况下,可以通过计算实验数据来得到标准溶液的浓度,然后根据实验需求来进行结果分析。
四、结论。
标准溶液的配制和标定是化学分析工作中的重要环节,正确地进行标准溶液的配制和标定可以保证实验结果的准确性和可靠性。
因此,在进行标准溶液的配制和标定时,需要严格按照操作要求进行,并且对实验数据进行仔细处理和结果分析,以确保实验结果的准确性和可靠性。
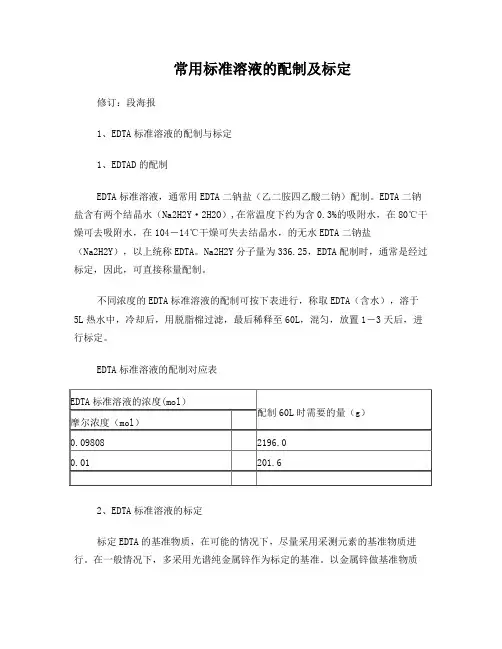
常用标准溶液的配制及标定修订:段海报1、EDTA标准溶液的配制与标定1、EDTAD的配制EDTA标准溶液,通常用EDTA二钠盐(乙二胺四乙酸二钠)配制。
EDTA二钠盐含有两个结晶水(Na2H2Y·2H2O),在常温度下约为含0.3%的吸附水,在80℃干燥可去吸附水,在104-14℃干燥可失去结晶水,的无水EDTA二钠盐(Na2H2Y),以上统称EDTA。
Na2H2Y分子量为336.25,EDTA配制时,通常是经过标定,因此,可直接称量配制。
不同浓度的EDTA标准溶液的配制可按下表进行,称取EDTA(含水),溶于5L热水中,冷却后,用脱脂棉过滤,最后稀释至60L,混匀,放置1-3天后,进行标定。
EDTA标准溶液的配制对应表2、EDTA标准溶液的标定标定EDTA的基准物质,在可能的情况下,尽量采用采测元素的基准物质进行。
在一般情况下,多采用光谱纯金属锌作为标定的基准。
以金属锌做基准物质时,金属表面的氧化层,要用干净的剪刀刮干净,或用3M盐酸洗净,再以二次水,乙醚或丙酮洗净,在100℃烘干5min。
金属锌原子质量=65.38锌标液的配制将金属锌粒(99.99%以上),先用1%的硝酸浸泡除去表面上的氧化膜至光亮,然后用水冲洗三次,再用少量无水乙醇洗涤三次,在105℃烘干。
(不宜过久,以免又产生氧化膜,保存于磨口瓶中)。
配制0.09808M锌标准溶液称取12.825g的锌粒于500ml的烧杯中,加水150ml,然后分数次加入120ml (1+1)硝酸,在电热板上低温加热溶解,并彻底赶出NO2,将体积浓缩到150ml,使溶液呈无色透明。
取下来冷却,移入2L容量瓶中,稀释至刻度。
Zn标准溶液的配制对应表按照下表的取样量,移取锌标准溶液于500ml锥形瓶中,加水约80ml,加入溴酚绿指示剂(0.1%)2滴,加氨水(1+1)至溶液刚好呈蓝色,加PH=5.5的HAc-NaAc溶液15ml,二甲酚橙指示剂0.03g(或0.25%指示剂3滴)以4-6ml/min的滴定速度,用配好的EDTA溶液滴定至亮黄色即为终点。

常用标准溶液的配制和标定常用标准溶液的配制和标定标准溶液的配制、标定的一般方法如下:1、配制公式(1)用固体试剂配制(欲配浓度为N 的浓度VmL ):应称试剂克数W=Q (克当量)×N ×V/1000(2) 用浓度为N0的浓溶液加水稀释配制(欲配浓度为N 的溶液VmL ):应加浓溶液00/N V N ml V ⨯= (3)用已知相对密度的浓酸或碱液配制(欲配浓度为N 的溶液VmL ):浓酸或碱液应取量(mL )=1000⨯⋅⋅⋅P D V N Q 式中:Q-------克当量;D-------酸或碱溶液的比重;P--------百分含量;2、标定(浓度计算)(1)用已知浓度(0N )的标准浓溶液标定: N=0N ·0V /V(2)用基准物质(固体试剂)标定:N=VQ W⨯⨯1000 3、浓度补正(1)用浓溶液将稀溶液向浓的方向补正时应补加的浓溶液△V(mL)=V N N N N⨯--1式中: N--------增浓后要求浓度: ---------增浓前浓度。
--------浓溶液浓度。
(2)用稀溶液将浓溶液向稀的方向补正时 应补加的稀溶液式中:0N ---------稀释前浓度; N--------稀释后要求浓度; 1N ---------稀溶液浓度。
用水稀释时n=0。
也可用NV v N=00救得V ,计算△V=V-0V 。
本标准适用于制备准确浓度的溶液。
应用于容量法测定化学试剂的纯度和杂质含量。
本标准中凡规定用“标定”和“比较”两种方法测定浓度时,不得略去其中任何一种。
10N N且两种方法测得的浓度值之相对误差不得大于0.2%。
以“标定”所得数字为准。
配制0.02N(M)或更稀的标准溶液时,应于临用前将浓度较高的标准溶液用煮沸后冷却的水稀释,必要时重新标定。
一0.05moL/L和0.02moL/L乙二胺四乙酸二钠标准溶液(即EDTA-2Na标准液)1、配制(1)0.05moL/L乙二胺四乙酸二钠标准溶液:称取20g乙二胺四乙酸二钠溶于1000mL水中,摇匀。

常用标准溶液的配制及标定修订:段海报一、EDTA标准溶液的配制与标定1、EDTAD的配制EDTA标准溶液,通常用EDTA二钠盐(乙二胺四乙酸二钠)配制。
EDTA二钠盐含有两个结晶水(Na2H2Y·2H2O),在常温度下约为含0.3%的吸附水,在80℃干燥可去吸附水,在104-14℃干燥可失去结晶水,的无水EDTA二钠盐(Na2H2Y),以上统称EDTA。
Na2H2Y分子量为336.25,EDTA配制时,通常是经过标定,因此,可直接称量配制。
不同浓度的EDTA标准溶液的配制可按下表进行,称取EDTA (含水),溶于5L热水中,冷却后,用脱脂棉过滤,最后稀释至60L,混匀,放置1-3天后,进行标定。
EDTA标准溶液的配制对应表2、EDTA标准溶液的标定标定EDTA的基准物质,在可能的情况下,尽量采用采测元素的基准物质进行。
在一般情况下,多采用光谱纯金属锌作为标定的基准。
以金属锌做基准物质时,金属表面的氧化层,要用干净的剪刀刮干净,或用3M盐酸洗净,再以二次水,乙醚或丙酮洗净,在100℃烘干5min。
金属锌原子质量=65.38锌标液的配制将金属锌粒(99.99%以上),先用1%的硝酸浸泡除去表面上的氧化膜至光亮,然后用水冲洗三次,再用少量无水乙醇洗涤三次,在105℃烘干。
(不宜过久,以免又产生氧化膜,保存于磨口瓶中)。
配制0.09808M锌标准溶液称取12.825g的锌粒于500ml的烧杯中,加水150ml,然后分数次加入120ml(1+1)硝酸,在电热板上低温加热溶解,并彻底赶出NO2,将体积浓缩到150ml,使溶液呈无色透明。
取下来冷却,移入2L容量瓶中,稀释至刻度。
Zn标准溶液的配制对应表按照下表的取样量,移取锌标准溶液于500ml锥形瓶中,加水约80ml,加入溴酚绿指示剂(0.1%)2滴,加氨水(1+1)至溶液刚好呈蓝色,加PH=5.5的HAc-NaAc溶液15ml,二甲酚橙指示剂0.03g(或0.25%指示剂3滴)以4-6ml/min的滴定速度,用配好的EDTA溶液滴定至亮黄色即为终点。
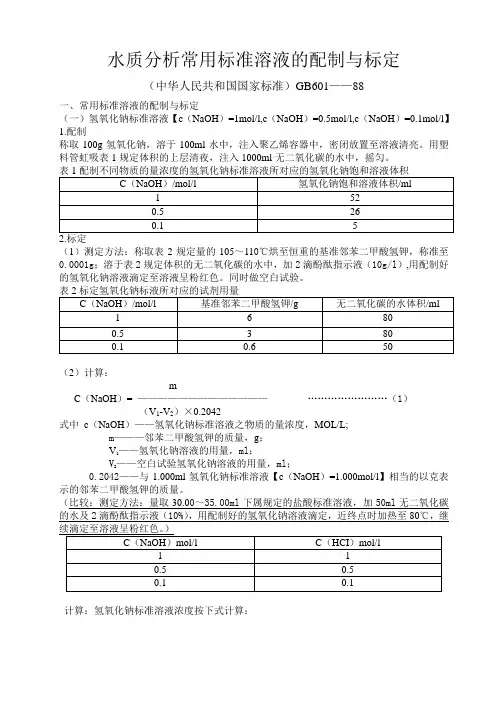
水质分析常用标准溶液的配制与标定(中华人民共和国国家标准)GB601——88一、常用标准溶液的配制与标定(一)氢氧化钠标准溶液【c(NaOH)=1mol/l,c(NaOH)=0.5mol/l,c(NaOH)=0.1mol/l】1.配制称取100g氢氧化钠,溶于100ml水中,注入聚乙烯容器中,密闭放置至溶液清亮。
用塑料管虹吸表1规定体积的上层清夜,注入1000ml无二氧化碳的水中,摇匀。
(1)测定方法:称取表2规定量的105~110℃烘至恒重的基准邻苯二甲酸氢钾,称准至0.0001g;溶于表2规定体积的无二氧化碳的水中,加2滴酚酞指示液(10g/l),用配制好的氢氧化钠溶液滴定至溶液呈粉红色。
同时做空白试验。
(2)计算:mC(NaOH)=————————————— (1)(V1-V2)×0.2042式中c(NaOH)——氢氧化钠标准溶液之物质的量浓度,MOL/L;m———邻苯二甲酸氢钾的质量,g;V1——氢氧化钠溶液的用量,ml;V2——空白试验氢氧化钠溶液的用量,ml;0.2042——与1.000ml氢氧化钠标准溶液【c(NaOH)=1.000mol/l】相当的以克表示的邻苯二甲酸氢钾的质量。
(比较:测定方法:量取30.00~35.00ml下属规定的盐酸标准溶液,加50ml无二氧化碳的水及2滴酚酞指示液(10%),用配制好的氢氧化钠溶液滴定,近终点时加热至80℃,继计算:氢氧化钠标准溶液浓度按下式计算:V1×C1C(NaOH)==————————V式中:C(NaOH)——氢氧化钠标准溶液之物质的量浓度,mol/l;V1———盐酸溶液之用量,ml;C1————盐酸标准溶液之物质的量浓度,mol/l;V————氢氧化钠溶液之用量,ml.(二)盐酸标准溶液【c(HCI)=1mol/l,c(HCI)=0.5mol/l,c(HCI)=0.1mol/l】1. 配制量取表3规定体积的盐酸,注入1000ml水中,摇匀。
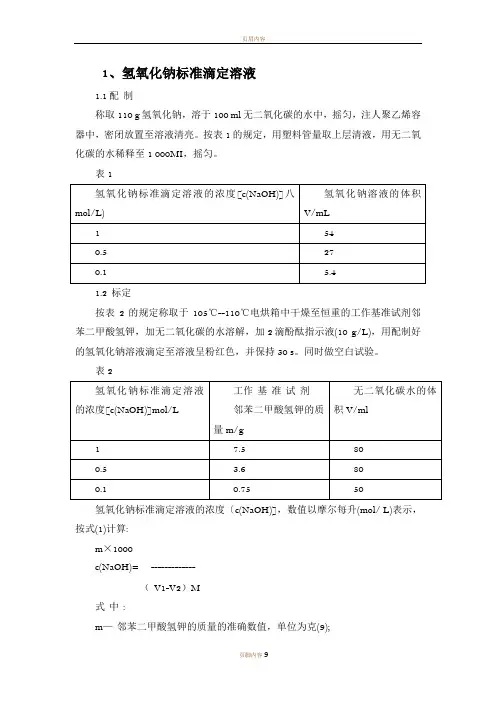
1、氢氧化钠标准滴定溶液1.1配制称取110 g氢氧化钠,溶于100 ml无二氧化碳的水中,摇匀,注人聚乙烯容器中,密闭放置至溶液清亮。
按表1的规定,用塑料管量取上层清液,用无二氧化碳的水稀释至1 000MI,摇匀。
表11.2 标定按表2 的规定称取于105℃--110℃电烘箱中干燥至恒重的工作基准试剂邻苯二甲酸氢钾,加无二氧化碳的水溶解,加2滴酚酞指示液(10 g/L),用配制好的氢氧化钠溶液滴定至溶液呈粉红色,并保持30 s。
同时做空白试验。
表2氢氧化钠标准滴定溶液的浓度〔c(NaOH)],数值以摩尔每升(mol/ L)表示,按式(1)计算:m×1000c(NaOH)= -------------(V1-V2)M式中:m—邻苯二甲酸氢钾的质量的准确数值,单位为克(9);V1 —氢氧化钠溶液的体积的数值,单位为毫升(mL);V2 一空白试验氢氧化钠溶液的体积的数值,单位为毫升(mL);M一邻苯二甲酸氢钾的摩尔质量的数值,单位为克每摩尔(g/mol)【M(KHC8H4O4)= 204.22 】2、硫酸标准滴定溶液2.1配制按表3的规定量取硫酸,缓缓注人1 000 mL水中,冷却,摇匀。
表32.2标定按表4的规定称取于270℃—300℃高温炉中灼烧至恒重的工作基准试剂无水碳酸钠,溶于50m l.水中,加5甲基红—亚甲基蓝指示剂(或滴澳甲酚绿一甲基红指示液),用配制好的硫酸溶液滴定至溶液由绿色变为紫色(绿色变为暗红色),煮沸2 min,冷却后继续滴定至溶液再呈紫色(暗红色)。
同时做空白试验。
表4硫酸标准滴定溶液的浓度[c(1/2H2SO4)],数值以摩尔每升(mol/L)表示m×1000c(1/2H2SO4)= -------------(V1-V2)M式中:m—无水碳酸钠的质量的准确数值,单位为克(g);V1—硫酸溶液的体积的数值,单位为毫升(mL) ;V2—空白试验硫酸溶液的体积的数值,单位为毫升(mL) ;M—无水碳酸钠的摩尔质量的数值,单位为克每摩尔(g/mol)[M(1/2Na2CO3 )=52.994]3、氯化钠标准溶液(1ml含1mg氯离子):称取基准试剂或者优级纯的3-4g氯化钠置于瓷坩埚内,于高温炉内升温至500度灼烧10分钟,然后放入干燥器内冷却至室温,然后准确称取1.649g氯化钠,先溶于少量除盐水,然后在容量瓶中稀释至1000ml。

标准溶液的配制与标定一、硫代硫酸钠标准溶液1、称取30;60;120;……克硫代硫酸钠溶解于水中,稀释至10ml,加5ml三氯甲烷,1克无水碳酸钠,摇匀备用。
2、称取纯铜(电解99.99%)1.0000克于烧杯中,加10ml(1+1)硝酸,微热溶解后,加5ml硫酸(1+1),加热至冒白烟,(加盖表皿)。
冷却、次洗,加水约100ml,加热溶解,冷却。
移入1000ml容量瓶中,定容。
摇匀备用。
(此溶液含铜为1毫克/毫升)3、吸取纯铜溶液20.00或25.00ml于烧杯中,加氨水(1+1)中和并过量2滴,溶液显纯蓝色,加醋酸变成醋酸酸性,过量1ml,溶液显浅蓝色。
加碘化钾2克,摇匀后,用硫代硫酸钠标准液滴至浅黄色,加5ml淀粉溶液(0.5%)以硫代硫酸钠标准液滴至微蓝,加硫氢酸钾0.1克,用硫代硫酸钠标准液滴至蓝色消失。
4、计算:T硫代硫酸钠铜=消耗体积毫升克或/001.02520二、碘标准溶液1、称取纯碘25克于杯中,加少许水,加120克碘化钾,再加少许水,摇动溶解,于10升容量瓶中定容,此溶液对锡的滴定度约在0.0012克/毫升2、准称纯锡(99.99%)1.0000克于杯中,加50ml盐酸(1+1)水浴或低温加热溶解(时间会很长,可加双氧水少许会加快溶解速度)。
冷却,移入1000ml 容量瓶中,加80ml浓盐酸,然后用水定容。
溶液酸度保持在10%左右。
此溶液含锡为0.001克/毫升,也相当于1豪克/毫升。
3、吸取25.00或20.00ml纯锡溶液于500ml锥形瓶中,加30ml盐酸,加45或50ml水,加2克铝片(分成三小块,不可太碎),剧烈反应结束后,加盖格克尔漏斗(内装饱和碳酸氢钠溶液),加热至溶液澄清,冒均匀大气泡。
取下,冷却,随即补加饱和碳酸氢钠溶液。
冷却到室温,取下格克尔漏斗,立即加入5ml淀粉溶液,立即用碘标准溶液滴定稳定蓝色出现(30秒内不褪色)。
三、溴酸钾标准溶液1、称取1.4-1.5克溴酸钾加7.4-7.5克溴化钾,少许水溶液。
标准溶液的配制与标定实训一氢氧化钠标准溶液的配制和标定一、目的要求1.掌握NaOH标准溶液的配制和标定。
2.掌握碱式滴定管的使用,掌握酚酞指示剂的滴定终点的判断。
二、方法原理NaOH有很强的吸水性和吸收空气中的CO2,因而,市售NaOH中常含有Na2CO3。
反应方程式: 2NaOH + CO2→ Na2CO3 + H2O由于碳酸钠的存在,对指示剂的使用影响较大,应设法除去。
除去Na2CO3最通常的方法是将NaOH先配成饱和溶液(约52%,W/W),由于Na2CO3在饱和NaOH溶液中几乎不溶解,会慢慢沉淀出来,因此,可用饱和氢氧化钠溶液,配制不含Na2CO3的NaOH溶液。
待Na2CO3沉淀后,可吸取一定量的上清液,稀释至所需浓度即可。
此外,用来配制NaOH溶液的蒸馏水,也应加热煮沸放冷,除去其中的CO2。
标定碱溶液的基准物质很多,常用的有草酸(H2C2O4•2H2O)、苯甲酸(C6H5COOH)和邻苯二甲酸氢钾(C6H4COOHCOOK)等。
最常用的是邻苯二甲酸氢钾,滴定反应如下: C6H4COOHCOOK + NaOH → C6H4COONaCOOK + H2O计量点时由于弱酸盐的水解,溶液呈弱碱性,应采用酚酞作为指示剂。
三、仪器和试剂仪器:碱式滴定管(50ml)、容量瓶、锥形瓶、分析天平、台秤。
试剂:邻苯二甲酸氢钾(基准试剂)、氢氧化钠固体(A.R)、10g/L酚酞指示剂:1g酚酞溶于适量乙醇中,再稀释至100mL。
四、操作步骤1.0.1mol/L NaOH标准溶液的配制用小烧杯在台秤上称取120g固体NaOH,加100mL水,振摇使之溶解成饱和溶液,冷却后注入聚乙烯塑料瓶中,密闭,放置数日,澄清后备用。
准确吸取上述溶液的上层清液5.6mL到1000毫升无二氧化碳的蒸馏水中,摇匀,贴上标签。
2.0.1mol/L NaOH标准溶液的标定将基准邻苯二甲酸氢钾加入干燥的称量瓶内,于105-110℃烘至恒重,用减量法准确称取邻苯二甲酸氢钾约0.6000克,置于250 mL锥形瓶中,加50 mL无CO2蒸馏水,温热使之溶解,冷却,加酚酞指示剂2-3滴,用欲标定的0.1mol/L NaOH溶液滴定,直到溶液呈粉红色,半分钟不褪色。
氢氧化钠标准溶液一、制备在陶瓷容器内将氢氧化钠和水按等质量配成浓碱溶液,冷却后转入塑料容器中,密闭放置1~2月至溶液清亮,按下表规定体积吸取上层清液,用不含二氧化碳的水稀释至1000ml,摇匀,密闭放置10d,将上层溶液虹吸入另一清洁的硬质玻璃瓶内,摇匀以备标定。
二、标定(一)邻苯二甲酸氢钾法1.方法要点以邻苯二甲酸氢钾为基准物,与欲标定的氢氧化钠溶液进行中和反应,以酚酞为指示剂,当溶液呈现微红色为终点。
2.试剂:①邻苯二甲酸氢钾(工作基准物)使用前于105℃~110℃干燥3~4h,冷至室温备用。
②酚酞指示剂(1%)乙醇配制3.分析步骤按下表规定称取邻苯二甲酸氢钾,精确至0.0001g,置于250ml锥形瓶内,加50ml沸腾的水溶解后,继续加热至沸,加2滴酚酞指示剂,立即以欲标定的氢氧化钠溶液滴至溶液呈粉红色为终点,同时作空白试验。
4.计算 C(NaOH)=m/0.20422(V-V0)式中: C(NaOH)-氢氧化钠标准溶液的物质的量浓度,mol/L;m-邻苯二甲酸氢钾的质量,g;V-氢氧化钠溶液的用量,mL;V0-空白试验氢氧化钠溶液的用量,mL.(二)酸碱对照法1.方法要点以酸标准溶液为基准物,与欲标定的氢氧化钠溶液进行中和反应,生成盐和水。
2.试剂:①酸标准溶液。
②甲基橙指示剂(0.1%)3.分析步骤量取20.00~30.00ml欲标定的碱溶液于250ml锥形瓶内,加1滴甲基橙指示剂,用酸标准溶液滴至溶液由黄色转为橙色为终点。
4.计算 C(NaOH)=c1*V1/V式中 :C(NaOH)-氢氧化钠标准溶液的物质的量浓度,mol/L;C1-酸标准溶液的物质的量浓度,mol/L;V1-酸标准溶液的用量,mL;V-氢氧化钠的用量,mL。
锌盐标准溶液国家标准GB/T601-1988中有:氯化锌标准溶液。
国家军用标准GJB1886-1994中有:乙酸锌标准溶液,硫酸锌标准溶液,氯化锌标准溶液,硝酸锌标准溶液。
标准溶液配制及标定一、确定浓度范围在进行标准溶液配制及标定前,首先需要确定所需的标准溶液浓度范围。
这个范围可以根据实验或测量的需求来确定。
在选择浓度范围时,应考虑到实际应用场景中的变化范围,以确保标准溶液的适用性。
二、选择合适的基准物质基准物质是用于配制标准溶液的化学物质。
选择合适的基准物质需要考虑其纯度、稳定性、易得性等因素。
常用的基准物质有氧化钠、氧化钙、重铬酸钾等。
三、配制标准溶液根据选定的基准物质和确定的浓度范围,按照以下步骤进行配制:1.精密称量适量的基准物质,以备用。
2.准备适量的溶剂,如去离子水或有机溶剂。
3.将称量好的基准物质溶解在溶剂中,配制成高浓度的标准溶液。
4.根据需要,将高浓度的标准溶液稀释至所需浓度。
四、标定标准溶液为了确定标准溶液的实际浓度,需要进行标定。
以下是标定标准溶液的步骤:1.准备适量的待测样品,以满足实验或测量的需求。
2.按照实验或测量方法,将待测样品处理成可测量的溶液或状态。
3.取一定量的待测溶液进行测量,得到待测样品的测量值。
4.根据测量值和所选用的基准物质,计算得到标准溶液的实际浓度。
五、计算浓度值根据基准物质的质量和所取待测样品的测量值,可以计算得到标准溶液的实际浓度。
计算公式如下:C = (m/M) × c其中,C为标准溶液的浓度(mol/L),m为基准物质的质量(g),M为待测样品的摩尔质量(g/mol),c为标准溶液的体积(L)。
六、验证浓度准确性为了验证标准溶液浓度的准确性,可以使用已知浓度的标准溶液进行对比或使用其他可靠的方法进行验证。
如果验证结果符合预期要求,则说明配制和标定的准确性较高。
如果验证结果存在较大偏差,则需要重新进行配制和标定。
七、记录标定结果将标定结果记录在记录表中,包括标定时间、操作者、浓度值等信息。
记录结果应清晰、完整,以便于日后查阅和使用。
同时,记录的结果应经过审核和批准,以确保数据的准确性和可靠性。
八、存储标准溶液配制好的标准溶液应存储在干燥、阴凉、避光的地方,以避免其变质或受到污染。
标准溶液的配制与标定标准溶液是在实验室中常用的一种溶液,它具有已知浓度和组成的特点,可以用来进行定量分析和质量测定等实验。
标准溶液的配制和标定是实验室中常见的操作,本文将详细介绍标准溶液的配制和标定的方法和步骤。
一、标准溶液的配制标准溶液的配制是根据实验需求和目的来确定的。
在配制标准溶液之前,首先需要准备好所需的化学物质和实验器材。
1.选择合适的化学物质:根据实验需求选择合适的化学物质作为标准溶液的原料,确保其纯度和稳定性。
2.准备实验器材:准备好容量瓶、量筒、移液器等实验器材,确保其干净无残留。
3.计算配制所需质量或体积:根据所需的浓度和体积计算出所需的化学物质的质量或体积。
注意要根据化学物质的相对分子质量和浓度单位进行计算。
4.溶解和稀释:将计算好的化学物质加入到容量瓶中,加入适量的溶剂溶解,并用溶剂稀释至刻度线。
5.混合均匀:将容量瓶中的溶液充分混合均匀,可以轻轻倾斜容量瓶几次或使用磁力搅拌器进行搅拌。
二、标准溶液的标定标准溶液的标定是确定其准确浓度的过程,常用的方法包括酸碱滴定法、物质定量法、电位滴定法等。
1.酸碱滴定法:这是一种常用的标定方法,其原理是通过酸碱反应的滴定过程来确定待测溶液的浓度。
首先准备好标准溶液和与之反应的滴定试剂,然后逐滴加入滴定试剂,直到出现酸碱中和反应的终点。
根据滴定试剂的浓度和消耗的体积,计算出待测溶液的浓度。
2.物质定量法:这是一种通过反应物质的质量关系来确定浓度的方法。
首先准备好标准溶液和与之反应的定量试剂,然后按照一定的比例将定量试剂加入到标准溶液中反应,根据反应物质的质量关系计算出待测溶液的浓度。
3.电位滴定法:这是一种利用电位变化来确定溶液浓度的方法。
通过电位滴定仪测量待测溶液的电位变化,根据已知浓度的标准溶液的电位值和溶液浓度的关系,计算出待测溶液的浓度。
标定标准溶液时,需要注意选择适当的指示剂或电位滴定仪的电极,并进行仪器的校准和调试。
三、注意事项在配制和标定标准溶液时,需要注意以下事项:1.实验室环境要干净整洁,避免有杂质和污染物进入溶液中。
溴酸钾标准溶液的配制与标定配制:c(1/6KBrO3)=0.1mol/l称取3g溴酸钾,溶于1000ml水中,摇匀标定方法及计算同溴标准溶液的标定及计算碘标准溶液的配制与标定配制:c(1/2I2)=0.1mol/l称取13g碘及25g碘化钾,溶于100ml水中,稀释至1000ml,摇匀,保存于棕色具塞瓶中。
标定:称取0.15g预先在硫酸干燥器中干燥至恒重的基准三氧化二砷,称准至0.0001g。
置于碘量瓶中,加4ml氢氧化钠溶液[C(NaOH)=1.0mol/l]溶解,加50ml水,加2滴酚酞指示剂,用硫酸溶液[C(1/2H2SO4)=1.0mol/l]中和,加3g碳酸氢钠及3ml5g/l 淀粉指示剂,用配好的碘溶液c(1/2I2)=0.1mol/l滴定至溶液呈浅蓝色。
同时作空白试验。
计算:c(1/2I2)=硫酸标准溶液配制与标定配制:称取上述规定定量的于270-300℃灼烧至恒重的基准无水碳酸钠,称准至0.0001g。
溶于50ml水中,加10滴溴甲酚绿-甲基红混合指示剂,用配好的硫酸溶液滴定至溶液由绿色变为暗红色,煮沸2min,冷却后继续滴定至溶液再呈暗红色。
同样做空白试验,计算:C(1/2H2SO4)=m/[(V1-V2)*0.05299)]V1--------硫酸之用量,mlV2--------空白试验硫酸之用量,ml0.05299-------于1.0000ml硫酸标准溶液相当的以克表示的无水碳酸钠的质量比较方法:量取30.00-35.00ml上述规定浓度的氢氧化钠标准溶液,加50ml无二氧化碳的水及2滴酚酞指示剂(10g/l),用配好的硫酸溶液滴定,近终点时加热至80度,继续滴定至溶液呈粉红色。
计算:C(1/2H2SO4)=v1*c1/vV1--------氢氧化钠标准溶液之用量,mlV----------硫酸之用量,mlC1----------氢氧化钠标准溶液之物质的量浓度,mol/l氢氧化钠标准溶液的配制与标定配制:称取100g氢氧化钠,溶于100ml水中,摇匀,注入聚乙烯容器,密闭放置至溶液清亮,用塑料管虹吸下述规定体积的上层清液,注入1000ml无二氧化碳的水称取上述规定的量于105-110℃烘至恒重的基准邻苯二甲酸氢钾,称准至0.0001g。
一、氢氧化钠标准滴定溶液1、配制:称取110g氢氧化钠,溶于100ml无二氧化碳的水中,摇匀,注入聚乙烯容器中,密闭放置至溶液清亮;按下表用量,用塑料管量取上层清液,用无二氧化碳的水稀释至1000mL,摇匀;2、标定:按下表的规定量,称取于105℃~110℃电烘箱中干燥至恒量的工作基准试剂邻苯二甲酸氢钾,加无二氧化碳的水溶解,加2滴酚酞指示液10g/L,用配制的氢氧化钠滴定至溶液呈粉红色,并保持30s;同时做空白试验;氢氧化钠标准滴定溶液的浓度cNaOH,按式1计算:cNaOH=m×1000(V1−V2)×M (1)式中:m—邻苯二甲酸氢钾质量,单位为克g;V1—氢氧化钠溶液体积,单位为毫升mL;V2—空白试验消耗氢氧化钠溶液体积,单位为毫升mL;M—邻苯二甲酸氢钾的摩尔质量,单位为克每摩尔g/molMKHC8H4O4=204.22二、盐酸标准滴定溶液1、配制:按下表规定量,量取盐酸,注入1000mL水中,摇匀;2、标定按下表规定量,称取于270℃~300℃高温炉中灼烧至恒量的工作基准试剂无水碳酸钠,溶于50mL水中,加10滴溴甲酚绿-甲基红指示液,用配制的盐酸溶液滴定至溶液由绿色变为暗红色,煮沸2min,加盖具钠石灰管的橡胶塞,冷却,继续滴定至溶液再呈暗红色;同时做空白试验;盐酸标准滴定溶液的浓度cHCl,按式2计算:cHCl=m×1000(V1−V2)×M (2)式中:m—无水碳酸钠质量,单位为克g;V1—盐酸溶液体积,单位为毫升mL;V2—空白试验消耗盐酸溶液体积,单位为毫升mL;M—无水碳酸钠的摩尔质量,单位为克每摩尔g/molM1/2Na2CO3=52.994三、硫酸标准滴定溶液1、配制:按下表规定量,量取硫酸,缓缓注入1000mL水中,冷却,摇匀;2、标定按下表规定量,称取于270℃~300℃高温炉中灼烧至恒量的工作基准试剂无水碳酸钠,溶于50mL水中,加10滴溴甲酚绿-甲基红指示液,用配制的硫酸溶液滴定至溶液由绿色变为暗红色,煮沸2min,加盖具钠石灰管的橡胶塞,冷却,继续滴定至溶液再呈暗红色;同时做空白试验;硫酸标准滴定溶液的浓度c1/2H2SO4,按式3计算:c1/2H2SO4=m×1000(V1−V2)×M (3)式中:m—无水碳酸钠质量,单位为克g;V1—硫酸溶液体积,单位为毫升mL;V2—空白试验消耗硫酸溶液体积,单位为毫升mL;M—无水碳酸钠的摩尔质量,单位为克每摩尔g/molM1/2Na2CO3=52.994四、硫代硫酸钠标准滴定溶液cNa2S2O3=0.1mol/L1、配制称取26g五水合硫代硫酸钠或16g无水硫代硫酸钠,加0.2g无水碳酸钠,溶于1000mL水中,缓缓煮沸10min,冷却;放置2周后用4号玻璃滤锅过滤;2、标定称取0.18g已于120℃±2℃干燥至恒量的工作基准试剂重铬酸钾,置于碘量瓶中,溶于25mL水,加2g碘化钾及20mL硫酸溶液20%,摇匀,于暗处放置10min;加150mL水15℃~20℃,用配制的硫代硫酸钠溶液滴定,近终点时加2mL淀粉指示液10g/L,继续滴定至溶液由蓝色变为亮绿色;同时做空白试验;硫代硫酸钠标准滴定溶液的浓度cNa2S2O3,按式4计算:cNa2S2O3=m×1000(V1−V2)×M (4)式中:m—重铬酸钾质量,单位为克g;V1—硫代硫酸钠溶液体积,单位为毫升mL;V2—空白试验消耗硫代硫酸钠溶液体积,单位为毫升mL;M—重铬酸钾的摩尔质量,单位为克每摩尔g/molM1/6K2Cr2O7=49.031五、硫酸铁Ⅱ铵标准滴定溶液{cNH42FeSO42=0.1mol/L}1、制剂配制1.1硫磷混酸溶液于100mL水中缓慢加入150mL硫酸和150mL磷酸,摇匀,冷却至室温,用高锰酸钾溶液调至微红色;1.2N-苯代邻氨基苯甲酸指示液2g/L临用前配制称取0.2gN-苯代邻氨基苯甲酸,溶于少量水,加0.2g无水碳酸钠,温热溶解,稀释至100mL;2、配制:称取40g六水合硫酸铁Ⅱ铵,溶于300mL硫酸溶液20%中,加700mL水,摇匀;3、标定临用前标定:称取0.18g已于120℃±2℃电烘箱中干燥至恒量的工作基准试剂重铬酸钾,溶于25mL水中,加10mL硫磷混酸溶液,加70mL水,用配制的硫酸铁Ⅱ铵溶液滴定至橙黄色消失,加2滴N-苯代邻氨基苯甲酸指示液2g/L,继续滴定至溶液由紫红色变为亮绿色;硫酸铁Ⅱ铵标准滴定溶液的浓度{cNH42FeSO42},按式5计算:cNH42FeSO42=m×1000V×M (5)式中:m—重铬酸钾质量,单位为克g;V—硫酸铁Ⅱ铵溶液体积,单位为毫升mL;M—重铬酸钾的摩尔质量,单位为克每摩尔g/molM1/6K2Cr2O7=49.031六、乙二胺四乙酸二钠标准滴定溶液1、配制:按下表规定量,称取乙二胺四乙酸二钠,加1000mL水,加热溶解,冷却,摇匀;2、标定:2.1乙二胺四乙酸二钠标准滴定溶液cEDTA=0.1mol/L,cEDTA=0.05mol/L按下表规定量,称取于800℃±50℃的高温炉中灼烧至恒量的工作基准试剂氧化锌,用少量水湿润,加2mL盐酸溶液20%溶解,加100mL水,用氨水溶液10%将溶液PH调至7~8,加10mL氨-氯化铵缓冲溶液甲PH≈10及5滴铬黑T指示液5g/L,用配制的乙二胺四乙酸二钠溶液滴定至溶液由紫色变为纯蓝色;同时做空白试验;乙二胺四乙酸二钠标准滴定溶液的浓度cEDTA,按式6计算:cEDTA=m×1000(V1−V2)×M (6)式中:m—氧化锌质量,单位为克g;V1—乙二胺四乙酸二钠溶液体积,单位为毫升mL;V2—空白试验消耗乙二胺四乙酸二钠溶液体积,单位为毫升mL;M—氧化锌的摩尔质量,单位为克每摩尔g/molMZnO=81.4082.2乙二胺四乙酸二钠标准滴定溶液cEDTA=0.02mol/L称取0.42g于800℃±50℃的高温炉中灼烧至恒量的工作基准试剂氧化锌,用少量水湿润,加3mL盐酸溶液20%溶解,移入250mL容量瓶中,稀释至刻度,摇匀;取35.00mL~40mL,加70mL水,用氨水溶液10%将溶液PH调至7~8,加10mL氨-氯化铵缓冲溶液甲PH≈10及5滴铬黑T指示液5g/L,用配制的乙二胺四乙酸二钠溶液滴定至溶液由紫色变为纯蓝色;同时做空白试验;乙二胺四乙酸二钠标准滴定溶液的浓度cEDTA,按式7计算:cEDTA=m×(V1250)×1000(V2−V3)×M (7)式中:m—氧化锌质量,单位为克g;V1—氧化锌溶液体积,单位为毫升mL;V2—乙二胺四乙酸二钠溶液体积,单位为毫升mL;V3—空白试验消耗乙二胺四乙酸二钠溶液体积,单位为毫升mL;M—氧化锌的摩尔质量,单位为克每摩尔g/molMZnO=81.408七、硝酸银标准滴定溶液cAgNO3=0.1mol/L1、配制:称取17.5g硝酸银,溶于1000mL水中,摇匀;溶液贮存于密闭的棕色瓶中;2、标定:称取0.22g于500℃~600℃的高温炉中灼烧至恒量的工作基准试剂氯化钠,溶于70mL水中,滴3滴铬酸钾试剂,用配制的硝酸银溶液滴定至溶液由黄色变为橙黄色;同时做空白试验;硝酸银标准滴定溶液的浓度cAgNO3,按式8计算:cAgNO3=m×1000(V1−V2)×M (8)式中:m—氯化钠质量,单位为克g;V1—硝酸银溶液体积,单位为毫升mL;V—空白试验消耗硝酸银溶液体积,单位为毫升mL;2M—氯化钠的摩尔质量,单位为克每摩尔g/molMNaCl=58.442。
标准溶液的配制与标定实训一氢氧化钠标准溶液的配制和标定一、目的要求1.掌握NaOH标准溶液的配制和标定。
2.掌握碱式滴定管的使用,掌握酚酞指示剂的滴定终点的判断。
二、方法原理NaOH有很强的吸水性和吸收空气中的CO2,因而,市售NaOH中常含有Na2CO3。
反应方程式:2NaOH + CO2→ Na2CO3+ H2O由于碳酸钠的存在,对指示剂的使用影响较大,应设法除去。
除去Na2CO3最通常的方法是将NaOH先配成饱和溶液(约52%,W/W),由于Na2CO3在饱和NaOH溶液中几乎不溶解,会慢慢沉淀出来,因此,可用饱和氢氧化钠溶液,配制不含Na2CO3的NaOH溶液。
待Na2CO3沉淀后,可吸取一定量的上清液,稀释至所需浓度即可。
此外,用来配制NaOH溶液的蒸馏水,也应加热煮沸放冷,除去其中的CO2。
标定碱溶液的基准物质很多,常用的有草酸(H2C2O4•2H2O)、苯甲酸(C6H5COOH)和邻苯二甲酸氢钾(C6H4COOHCOOK)等。
最常用的是邻苯二甲酸氢钾,滴定反应如下:C6H4COOHCOOK + NaOH →C6H4COONaCOOK + H2O 计量点时由于弱酸盐的水解,溶液呈弱碱性,应采用酚酞作为指示剂。
三、仪器和试剂仪器:碱式滴定管(50ml)、容量瓶、锥形瓶、分析天平、台秤。
试剂:邻苯二甲酸氢钾(基准试剂)、氢氧化钠固体(A.R)、10g/L酚酞指示剂:1g酚酞溶于适量乙醇中,再稀释至100mL。
四、操作步骤1.0.1mol/L NaOH标准溶液的配制用小烧杯在台秤上称取120g固体NaOH,加100mL水,振摇使之溶解成饱和溶液,冷却后注入聚乙烯塑料瓶中,密闭,放置数日,澄清后备用。
准确吸取上述溶液的上层清液5.6mL到1000毫升无二氧化碳的蒸馏水中,摇匀,贴上标签。
2.0.1mol/L NaOH标准溶液的标定将基准邻苯二甲酸氢钾加入干燥的称量瓶内,于105-110℃烘至恒重,用减量法准确称取邻苯二甲酸氢钾约0.6000克,置于250 mL锥形瓶中,加50 mL无CO2蒸馏水,温热使之溶解,冷却,加酚酞指示剂2-3滴,用欲标定的0.1mol/L NaOH溶液滴定,直到溶液呈粉红色,半分钟不褪色。
同时做空白试验。
要求做三个平行样品。
五、结果结算NaOH标准溶液浓度计算公式:mC NaOH=(V1-V2)×0.2042式中:m---邻苯二甲酸氢钾的质量,gV1---氢氧化钠标准滴定溶液用量,mLV2---空白试验中氢氧化钠标准滴定溶液用量,mL0.2042---与1mmol氢氧化钠标准滴定溶液相当的基准邻苯二甲酸氢钾的质量,g思考题1、配制标准碱溶液时,用台秤称取固体NaOH是否会影响浓度的准确度?2、能否用称量纸称取固体NaOH?为什么?实训二盐酸标准溶液的配制和标定一、目的要求1.掌握减量法准确称取基准物的方法。
2.掌握滴定操作并学会正确判断滴定终点的方法。
3.学会配制和标定盐酸标准溶液的方法。
二、原理由于浓盐酸容易挥发,不能用它们来直接配制具有准确浓度的标准溶液,因此,配制HCl标准溶液时,只能先配制成近似浓度的溶液,然后用基准物质标定它们的准确浓度,或者用另一已知准确浓度的标准溶液滴定该溶液,再根据它们的体积比计算该溶液的准确浓度。
标定HCl溶液的基准物质常用的是无水Na2CO3,其反应式如下:Na2CO3 +2HCl 2NaCl +CO2 +H2O滴定至反应完全时,溶液pH为3.89,通常选用溴甲酚绿-甲基红混合液作指示剂。
三、试剂1.浓盐酸(密度1.19)2.溴甲酚绿-甲基红混合液指示剂:量取30mL溴甲酚绿乙醇溶液(2g/L),加入20mL甲基红乙醇溶液(1g/L),混匀。
四、步骤1.0.1mol·L-1HCl溶液的配制用量筒量取浓盐酸9mL,倒入预先盛有适量水的试剂瓶中,加水稀释至1000mL,摇匀,贴上标签。
2.盐酸溶液浓度的标定用减量法准确称取约0.15g在270~300℃干燥至恒量的基准无水碳酸钠,置于250mL锥形瓶,加50mL水使之溶解,再加10滴溴甲酚绿-甲基红混合液指示剂,用配制好的HCl溶液滴定至溶液由绿色转变为紫红色,煮沸2min,冷却至室温,继续滴定至溶液由绿色变为暗紫色。
由Na2CO3的重量及实际消耗的HCl溶液的体积,计算HCl 溶液的准确浓度。
五、注意事项1.干燥至恒重的无水碳酸钠有吸湿性,因此在标定中精密称取基准无水碳酸钠时,宜采用“减量法”称取,并应迅速将称量瓶加盖密闭。
2.在滴定过程中产生的二氧化碳,使终点变色不够敏锐。
因此,在溶液滴定进行至临近终点时,应将溶液加热煮沸,以除去二氧化碳,待冷至室温后,再继续滴定。
思考题1.作为标定的基准物质应具备哪些条件?2.欲溶解Na2CO3基准物质时,加水50mL应以量筒量取还是用移液管吸取?为什么?3.本实验中所使用的称量瓶、烧杯、锥形瓶是否必须都烘干?为什么?4.标定HCl溶液时为什么要称0.15g左右Na2CO3基准物?称得过多或过少有何不好?实训三EDTA标准溶液的配制和标定一、目的要求1.了解EDTA标准溶液标定的原理。
2.掌握配制和标定EDTAB标准溶液的方法。
二、原理乙二胺四乙酸二钠盐(习惯上称EDTA)是一种有机络合剂,能与大多数金属离子形成稳定的1∶1螯合物,常用作配位滴定的标准溶液。
EDTA在水中的溶解度为120g/L,可以配成浓度为0.3mol/L以下的溶液。
EDTA标准溶液一般不用直接法配制,而是先配制成大致浓度的溶液,然后标定。
用于标定EDTA标准溶液的基准试剂较多,例如Zn、ZnO、CaCO3、Bi、Cu、MgSO4·7H2O、Ni、Pb等。
用氧化锌作基准物质标定EDTA溶液浓度时,以铬黑T作指示剂,用pH=10的氨缓冲溶液控制滴定时的酸度,滴定到溶液由紫色转变为纯蓝色,即为终点。
三、试剂1.乙二胺四乙酸二钠盐(EDTA)。
2.氨水-氯化铵缓冲液(pH=10):称取5.4g氯化铵,加适量水溶解后,加入35mL 氨水,再加水稀释至100mL。
3.铬黑T指示剂:称取0.1g铬黑T,加入10g氯化钠,研磨混合。
4.40%氨水溶液:量取40mL氨水,加水稀释至100mL。
5.氧化锌(基准试剂)。
6.盐酸四、步骤3.0.01mol·L-1EDTA溶液的配制称取乙二胺四乙酸二钠盐(Na2H2Y·2H2O)4g,加入1000mL水,加热使之溶解,冷却后摇匀,如混浊应过滤后使用。
置于玻璃瓶中,避免与橡皮塞、橡皮管接触。
贴上标签。
4.锌标准溶液的配制准确称取约0.16g于800℃灼烧至恒量的基准ZnO,置于小烧杯中,加入0.4mL盐酸,溶解后移入200mL容量瓶,加水稀释至刻度,混匀。
5.E DTA溶液浓度的标定吸取30.00~35.00mL锌标准溶液于250mL锥形瓶中,加入70mL水,用40%氨水中和至pH为7~8,再加10mL氨水-氯化铵缓冲液(pH=10),加入少许铬黑T指示剂,用配好的EDTA溶液滴定至溶液自紫色转变为纯蓝色。
记下所消耗的EDTA溶液的体积,根据消耗的EDTA溶液的体积,计算其浓度。
思考题1.用铬黑T指示剂时,为什么要控制pH=10?2.配位滴定法与酸碱滴定法相比,有哪些不同?操作中应注意哪些问题?附:0.05mol·L-1EDTA滴定液的配制与标定(药典方法)一、试剂a)稀盐酸:取盐酸234mL,加水稀释至1000mL。
b)0.025%甲基红的乙醇液:取甲基红0.025g,加无水乙醇100mL,即得。
c)氨试液:取浓氨水400mL,加水使成1000mL。
d)氨-氯化铵缓冲液(pH=10.0):取氯化铵5.4g,加水20mL溶液后,加浓氨水溶液35mL,再加水稀释至100mL,即得。
e)铬黑T指示剂:取0.1g铬黑T,加氯化钠10g,研磨均匀,即得。
二、步骤1.配制:称取乙二胺四醋酸二钠盐(Na2H2Y·2H2O)19g,加适量的水使溶解成1000mL,摇匀。
2.标定:取于800℃灼烧至恒重的基准氧化锌约0.12g,精密称定,加稀盐酸3mL 使溶解,加水25mL,加0.025%甲基红的乙醇溶液1滴,滴加氨试液至溶液显微黄色,加水25mL与氨-氯化氨缓冲液(Ph=10.0)10ml,再加铬黑T指示剂少量,用本液滴定至溶液由紫色变为纯蓝色,并将滴定的结果用空白试验校正。
每1ml乙二胺四醋酸二钠滴定液(0.05mol/L)相当于 4.069mg的氧化锌。
根据本液的消耗量与氧化锌的取用量,算出本液的浓度,即得。
3.贮藏:置玻璃塞瓶中,避免与橡皮塞、橡皮管等接触。
实训四硫代硫酸钠标准溶液的配制和标定一、实训目的1、掌握硫代硫酸钠标准滴定溶液的配制、标定和保存方法。
2、掌握以碘酸钾为基准物间接碘量法标定硫代硫酸钠的基本原理、反应条件、操作方法和计算。
二、实训原理Na2S2O3·5H2O容易风化、潮解,且易受空气和微生物的作用而分解,因此不能直接配制成准确浓度的溶液。
但其在微碱性的溶液中较稳定。
当标准溶液配制后亦要妥善保存。
标定Na2S2O3溶液通常是选用KIO3、KBrO3或K2Cr2O7等氧化剂作为基准物,定量地将I—氧化为I2,再用Na2S2O3溶液滴定,其反应如下;上述几种基准物中一般使用KIO3和KBrO3较多,因为不会污染环境。
三、试剂1、基准试剂KIO3;2、20%KI溶液;3、0.5 mol/LH2SO4溶液;4、5g/L淀粉溶液:0.5g可溶性淀粉放入小烧杯中,加水10mL,使成糊状,在搅拌下倒入90 mL沸水中,继续微沸2min,冷却后转移至试剂瓶中。
四、实训步骤1、0.l mol/L Na2S2O3标准溶液的配制称取13克Na2S2O3·5H2O置于400 mL烧怀中,加入200 mL新煮沸的冷却的蒸馏水,待完全溶解后,加入0.1g Na2CO3,然后用新煮沸经冷却的蒸馏水稀释至500 mL,保存于棕色瓶中,在暗处放置7—14天后标定;2、Na2S2O3标准溶液的标定准确称取基准试剂KIO3约0.9克于250 mL烧杯中,加入少量蒸馏水溶解后,移入250 mL容量瓶中,用蒸馏水稀释至刻度,摇匀。
用移液管吸取上述KIO3标准溶液25 mL置于250mL锥形瓶中,加入KI溶液5 mL 和H2SO4溶液 5 mL,以水稀释至100mL,立即用待标定的Na2S2O3溶液滴定至淡黄色;再加入5 mL淀粉溶液,继续用Na2S2O3溶液滴定至蓝色恰好消失,即为终点。
根据消耗的Na2S2O3溶液的毫升数及KIO3的量,计算Na2S2O3溶液的准确浓度。
若选用KBrO3作基准物时其反应较慢,为加速反应需增加酸度,因而改为取1mol/LH2SO4溶液溶液5mL,井需在暗处放置5 min,使反应进行完全,并且改用碘量瓶。