浓硫酸工业制法
- 格式:ppt
- 大小:684.50 KB
- 文档页数:17



教案:硫酸的制备和性质(温州中学化学组:谢昭全)【学习目标】1.了解工业上生产硫酸的基本原理2.掌握稀硫酸的性质3.理解浓硫酸的三大特性3.了解硫酸的用途【设计意图】通过实验探究理解浓硫酸的特性【重点和难点】浓硫酸的特性【教学过程】一、硫酸的工业制法硫酸的工业制法在中国已经有上千年历史,中国历史上制取硫酸有胆矾法和绿矾法,故硫酸俗名绿矾油。
现代制取硫酸则一般采用接触法。
接触法制硫酸的主要原料:含硫物质(硫磺矿或硫铁矿,我国由于硫磺矿资源较少,故用硫铁矿为原料制硫酸)、空气、水。
无论是用硫铁矿还是硫磺为原料,都有三个主要步骤、三个主要设别和三个反应原理1.三个步骤:造气、氧化、吸收2.三个设备沸腾炉(若以硫磺为原料则为焚硫炉)、接触室(接触法这个名称由此而来)、吸收塔3.三个反应FeS 2+11O 28SO 2+2Fe 2O 3、 2SO 2 +O 2 2SO 3 、SO 3 +H 2O ═H 2SO 4 几点说明:沸腾炉名称的由来接触室名称的由来吸收剂为浓硫酸而不是纯水或稀硫酸由于第二步反应为可逆反应,故尾气中含二氧化硫,必须进行尾气处理二、硫酸的物理性质1.(纯)浓硫酸:无色、粘稠、油状液体2.沸点338℃,属高沸点、难挥发酸(可用来制取低沸点、易挥发酸)3.常用浓硫酸的几个数据:质量分数(可见其溶解性如何?)、密度、物质的量浓度4.水溶性:跟水任意比互溶,溶解时放出大量热【思考】如何稀释浓硫酸?浓硫酸粘到皮肤上应如何处理?三、稀硫酸的性质——酸的通性1.与指示剂作用2.与活泼金属作用(强调不与Cu 作用)3.与碱4.与碱性氧化物5.与盐【讨论】浓、稀硫酸中所含有的粒子是否相同?不同,稀硫酸中主要含氢离子和硫酸根离子及水的粒子,不含硫酸分子;浓硫酸中由于水太少,不足以让硫酸分子发生电离,故主要含硫酸分子。
(由此引出浓硫酸肯定有不催化剂△同于稀硫酸的性质)四、浓硫酸的(三大)特性【实验1】将铜片与浓硫酸混合加热,将产生的气体通入品红现象:铜片溶解、有气泡产生,品红溶液褪色原理:Cu+2H2SO4 (浓)CuSO4+SO2↑+2H2O稀硫酸不能氧化铜而浓硫酸能氧化铜,其中起氧化作用的是其中的硫元素,可见浓硫酸中硫元素的氧化性比稀硫酸中H的氧化性强,这样的酸称作氧化性酸1.强氧化性浓硫酸的强氧化性主要体现在四个方面(1)能氧化某些H后金属如铜(2)能氧化某些非金属如炭(3)常温下能Al、Fe等金属钝化(4)与H前金属反应时无氢气放出【实验2】向表面皿中加入少量胆矾,再加入约3mL浓硫酸,搅拌。

1、工业制硫酸4FeS2+11O2=2Fe2O3+8SO2(反应条件:高温)2SO2+O2=2SO3(反应条件:加热,催化剂作用下)SO3+H20=H2SO4(反应条件:常温)在沸腾炉,接触室,吸收塔内完成2、工业制硝酸4NH3+5O2=4NO+6H2O(反应条件:800度高温,催化剂铂铑合金作用下)2NO+O2=2NO23NO2+O2=2HNO3+NO3、工业制盐酸H2+C l2=2HCl(反应条件:点燃)然后用水吸收在合成塔内完成4、工业制烧碱(氯碱工业)2NaCl+2H2O=H2+Cl2+2NaOH(电解饱和食盐水)5、工业制取粉精2Ca(OH)2+2Cl2=CaCl2+Ca(ClO)2+2H2O6、工业制纯碱(侯氏).侯氏制碱法NaCl+NH3+CO2+H2O=NaHCO3+NH4Cl1)NH3+H2O+CO2=NH4HCO32)NH4HCO3+NaCl=NaHCO3+NH4Cl(NH4HCO3结晶析出)3)2NaHCO3=Na2CO3+H2O+CO2(反应条件:加热)7、工业制金属铝2Al2O3=4Al+3O2(反应条件:电解,催化剂为熔融的冰晶石)注:冰晶石化学式为NaAlF68.工业制硅利用反应SiO2+2C==高温== Si+2CO↑能得到不纯的粗硅。
粗硅需进行精制,才能得到高纯度硅。
首先,使Si跟Cl2起反应:Si+2Cl2=SiCl4(400 ℃~500 ℃)生成的SiCl4液体通过精馏,除去其中的硼、砷等杂质。
然后,用H2还原SiCl4:SiCl4+2H2==高温== Si+4HCl这样就可得到纯度较高的多晶硅。
9.硅酸盐工业(制普通玻璃)生石灰(高温煅烧石灰石)CaCO3 =高温= CaO+CO2↑玻璃工业(玻璃窑法)Na2CO3 + SiO2 =高温= Na2SiO3 +CO2↑CaCO3 + SiO2 =高温= CaSiO3 +CO2↑10.高炉炼铁Fe2O3+3C=2Fe+3CO[也可以生成CO2]11.工业制取水煤气C+H2O=CO+H22.粗铜的精炼电解:阳极用粗铜阳极:Cu-2e-=Cu2+阴极:Cu2++2e-=Cu13、工业制氨气3H2+N2=2NH3(反应条件:高温高压催化剂作用下)注:催化剂为铁触媒氯气中学二氧化锰浓盐酸加热工业电解食盐水氯化氢中学直接买/浓硫酸氯化钠加热(溴化氢同)工业氢气氯气燃烧氟化氢实验室氟化钙浓硫酸共热溴碘中学直接买工业海水中的离子相应电解/氧化还原氧气中学高锰酸钾加热/氯酸钾二氧化锰加热/双氧水二氧化锰/ 工业压缩空气二氧化硫中学硫酸(稍浓)加亚硫酸盐/铜,浓硫酸加热工业硫铁矿,黄铜矿,硫燃烧三氧化硫工业二氧化硫氧气钒催化剂氧化硫酸工业三氧化硫溶于98%硫酸得到发烟硫酸,稀释氮气中学无工业压缩空气氨中学氨水一般自己买,氨气消石灰氨盐加热(推荐氯化铵)/浓氨水工业氮气氢气催化反应硝酸中学有个二氧化氮溶于水的反应,不过一般自己买工业氨氧化成一氧化氮再生成NO2(还有电弧生成氮氧化物的方法)然后好像是溶与浓硝酸再稀释硅中学无工业二氧化硅,碳高温还原铝中学无工业电解氧化铝加冰晶石助熔钠,镁,钙电解铜实验室氢气还原氧化铜工业粗铜碳还原法精铜电解精炼铁实验室氢气还原工业生铁碳还原法钢生铁精炼过氧化氢工业分有机法和过氧化钡法在惰性电极上,各种离子的放电顺序:阴极(夺电子的能力):Au3+ >Ag+>Hg2+ >Cu2+ >Pb2+ >Fa2+ >Zn2+ >H+ >Al3+>Mg2+ >Na+ >Ca2+ >K+阳极(失电子的能力):S2- >I- >Br–>Cl- >OH- >含氧酸根注意:若用金属作阳极,电解时阳极本身发生氧化还原反应(Pt、Au除外)有机酸酸性的强弱:乙二酸>甲酸>苯甲酸>乙酸>碳酸>苯酚>HCO3-在室温(20C。

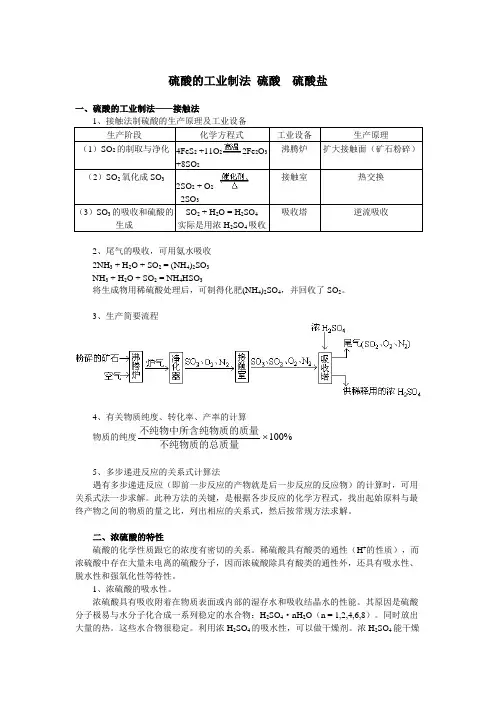
硫酸的工业制法硫酸硫酸盐一、硫酸的工业制法——接触法1、接触法制硫酸的生产原理及工业设备生产阶段化学方程式工业设备生产原理(1)SO2的制取与净化4FeS2+11O22Fe2O3+8SO2沸腾炉扩大接触面(矿石粉碎)(2)SO2氧化成SO32SO2 + O22SO3接触室热交换(3)SO3的吸收和硫酸的生成SO2 + H2O = H2SO4实际是用浓H2SO4吸收吸收塔逆流吸收2、尾气的吸收,可用氨水吸收2NH3 + H2O + SO2 = (NH4)2SO3NH3 + H2O + SO2 = NH4HSO3将生成物用稀硫酸处理后,可制得化肥(NH4)2SO4,并回收了SO2。
3、生产简要流程4、有关物质纯度、转化率、产率的计算物质的纯度不纯物中所含纯物质的质量不纯物质的总质量100%5、多步递进反应的关系式计算法遇有多步递进反应(即前一步反应的产物就是后一步反应的反应物)的计算时,可用关系式法一步求解。
此种方法的关键,是根据各步反应的化学方程式,找出起始原料与最终产物之间的物质的量之比,列出相应的关系式,然后按常规方法求解。
二、浓硫酸的特性硫酸的化学性质跟它的浓度有密切的关系。
稀硫酸具有酸类的通性(H+的性质),而浓硫酸中存在大量未电离的硫酸分子,因而浓硫酸除具有酸类的通性外,还具有吸水性、脱水性和强氧化性等特性。
1、浓硫酸的吸水性。
浓硫酸具有吸收附着在物质表面或内部的湿存水和吸收结晶水的性能。
其原因是硫酸分子极易与水分子化合成一系列稳定的水合物:H2SO4·nH2O(n = 1,2,4,6,8)。
同时放出大量的热。
这些水合物很稳定。
利用浓H2SO4的吸水性,可以做干燥剂。
浓H2SO4能干燥H 2、O 2、CO 等中性气体,也能干燥SO 2、Cl 2、CO 2、HCl 、HF 等酸性气体;但不能干燥NH 3等碱性气体,也不能干燥HBr 、HI 、H 2S 等有强还原性的气体。
2、浓硫酸的脱水性。
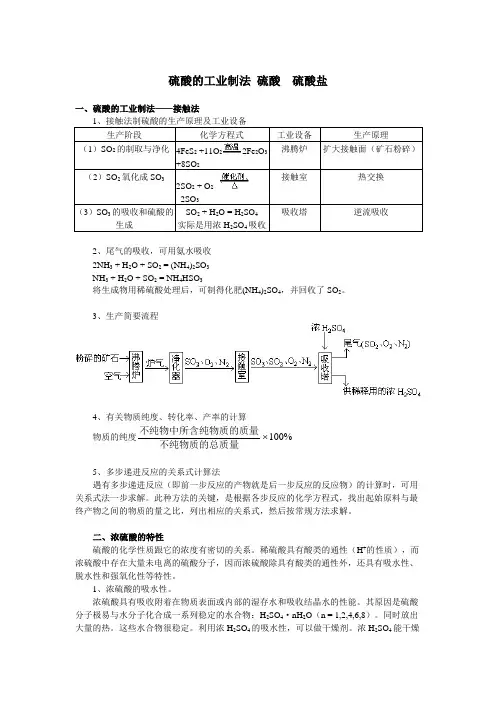
硫酸的工业制法硫酸硫酸盐一、硫酸的工业制法——接触法1、接触法制硫酸的生产原理及工业设备生产阶段化学方程式工业设备生产原理(1)SO2的制取与净化4FeS2+11O22Fe2O3+8SO2沸腾炉扩大接触面(矿石粉碎)(2)SO2氧化成SO32SO2 + O22SO3接触室热交换(3)SO3的吸收和硫酸的生成SO2 + H2O = H2SO4实际是用浓H2SO4吸收吸收塔逆流吸收2、尾气的吸收,可用氨水吸收2NH3 + H2O + SO2 = (NH4)2SO3NH3 + H2O + SO2 = NH4HSO3将生成物用稀硫酸处理后,可制得化肥(NH4)2SO4,并回收了SO2。
3、生产简要流程4、有关物质纯度、转化率、产率的计算物质的纯度不纯物中所含纯物质的质量不纯物质的总质量100%5、多步递进反应的关系式计算法遇有多步递进反应(即前一步反应的产物就是后一步反应的反应物)的计算时,可用关系式法一步求解。
此种方法的关键,是根据各步反应的化学方程式,找出起始原料与最终产物之间的物质的量之比,列出相应的关系式,然后按常规方法求解。
二、浓硫酸的特性硫酸的化学性质跟它的浓度有密切的关系。
稀硫酸具有酸类的通性(H+的性质),而浓硫酸中存在大量未电离的硫酸分子,因而浓硫酸除具有酸类的通性外,还具有吸水性、脱水性和强氧化性等特性。
1、浓硫酸的吸水性。
浓硫酸具有吸收附着在物质表面或内部的湿存水和吸收结晶水的性能。
其原因是硫酸分子极易与水分子化合成一系列稳定的水合物:H2SO4·nH2O(n = 1,2,4,6,8)。
同时放出大量的热。
这些水合物很稳定。
利用浓H2SO4的吸水性,可以做干燥剂。
浓H2SO4能干燥H 2、O 2、CO 等中性气体,也能干燥SO 2、Cl 2、CO 2、HCl 、HF 等酸性气体;但不能干燥NH 3等碱性气体,也不能干燥HBr 、HI 、H 2S 等有强还原性的气体。
2、浓硫酸的脱水性。


硫酸的配制1. 硫酸简介硫酸(H2SO4)是一种常见的无机化合物,化学式为H2SO4,分子量为98.09 g/mol。
它是一种无色、无臭、具有强烈腐蚀性的液体,广泛应用于工业生产和实验室研究中。
2. 硫酸的用途硫酸是一种重要的化学原料,在许多工业和实验室应用中起着关键作用。
主要用途包括: - 作为强酸催化剂,用于有机合成反应; - 用于制造肥料、合成纤维和染料; - 用作电池中的电解液; - 用于清洗金属表面和去除锈蚀; - 用于制造化学药品和塑料等。
3. 硫酸的配制方法硫酸的配制方法有多种,下面介绍两种常见的方法:浓硫酸的配制和稀硫酸的配制。
3.1 浓硫酸的配制浓硫酸是指含有高浓度硫酸的溶液,通常浓度在95%以上。
浓硫酸的配制方法如下:3.1.1 材料准备•浓硫酸饱和溶液(98%硫酸)•蒸馏水•配制容器(如玻璃烧杯)3.1.2 配制步骤1.将配制容器放在防护设施下,确保安全操作。
2.慢慢地向配制容器中加入蒸馏水,同时搅拌,直到容器装满为止。
3.小心地向容器中加入浓硫酸饱和溶液,同时继续搅拌。
4.等待溶液充分混合,直至温度稳定。
5.检查溶液浓度,确保其达到所需浓度。
3.2 稀硫酸的配制稀硫酸是指含有较低浓度硫酸的溶液,通常浓度在1%到10%之间。
稀硫酸的配制方法如下:3.2.1 材料准备•浓硫酸饱和溶液(98%硫酸)•蒸馏水•配制容器(如烧杯)3.2.2 配制步骤1.将配制容器放在防护设施下,确保安全操作。
2.慢慢地向配制容器中加入蒸馏水,同时搅拌,直到容器装满为止。
3.小心地向容器中加入浓硫酸饱和溶液,同时继续搅拌。
4.等待溶液充分混合,直至温度稳定。
5.检查溶液浓度,确保其达到所需浓度。
4. 硫酸的安全注意事项在配制硫酸时,必须注意以下安全事项,以避免事故和伤害:•硫酸具有强腐蚀性,必须佩戴防护手套、护目镜和防护服等个人防护装备。
•配制过程中要小心操作,避免溅洒和吸入硫酸蒸气。
•配制容器应选择耐腐蚀的材料,如玻璃或特殊塑料。

硫酸的工业制备方程式
硫酸化学式是H2SO4。
硫酸的工业制备主要运用的是接触法,以下是硫酸的工业制备方程式:
1、将硫黄或黄铁矿在空气中燃烧或焙烧得到二氧化硫气体。
方程式:4FeS2+11O2=8SO2+2Fe2O3。
2、将二氧化硫氧化为三氧化硫,方程式:2SO2+O2=2SO3。
3、用98.3%的浓硫酸吸收,再稀释的所需浓度的硫酸,方程式:SO3+H2O=H2SO4。
注意事项:浓硫酸可吸收空气或其他气体中的水蒸气、混在固体中的湿存水、结晶水合物中的结晶水,常用盛有浓硫酸的洗气瓶干燥某些气体,不能干燥碱性气体和强还原性气体。
工业制浓硫酸化学方程式
工业制浓硫酸是一项重要的化学工艺,其化学方程式如下所示:2SO2(g) + O2(g) → 2SO3(g)。
SO3(g) + H2O(l) → H2SO4(l)。
这两个方程描述了工业制造浓硫酸的两个关键步骤。
首先,二
氧化硫和氧气在催化剂的作用下反应生成三氧化硫。
然后,三氧化
硫与水反应生成硫酸。
这个化学过程是通过联系高温、高压和催化
剂来实现的。
工业制造浓硫酸的化学方程式背后是复杂的工艺流程和设备。
这项工艺不仅需要高效的反应器和分离装置,还需要严格的控制和
监测。
在工业生产中,安全性和环保性也是至关重要的考虑因素。
浓硫酸是许多化学工业过程的重要原料,它被用于制造肥料、
塑料、纺织品和其他化学品。
因此,工业制造浓硫酸的化学方程式
不仅代表着一种化学反应,更代表着现代工业生产中不可或缺的一环。