溶质的质量分数练习题
- 格式:docx
- 大小:70.64 KB
- 文档页数:3

有关溶质质量分数的计算的五种典型题目第1课时题型一:例题1.每天补充适量的维生素C,有利于提高人体免疫力。
某维生素C泡腾片,每片含1g维生素C,将1片该泡腾片投入适量水中,最终得到250g溶液,计算此溶液中维生素C的质量分数。
练习1.蒸干15克NaCl溶液得到1.2克NaCl,计算原溶液中NaCl的质量分数。
练习2.在一定温度时,NaCl饱和溶液的质量是12g,把它蒸干后,得到3.2gNaCl,计算:(1)该温度时NaCl饱和溶液中溶质的质量分数(2)配制该温度时NaCl饱和溶液1000g,需水和NaCl各多少g?(3)这一温度下NaCl的溶解度?练习3.在80g质量分数为15%NaNO3溶液里加入20g水或20g NaNO3,计算这两种方法制成的两种溶液中溶质的质量分数。
题型二:例题1.某温度时,氯化钾的溶解度为40g,求该温度时,氯化钾饱和溶液中溶质的质量分数。
例题2.10L密度为1.84g/cm3、溶质质量分数为98%的浓硫酸,其中溶液质量为 ,溶质质量为。
练习1.配制500mL质量分数为10%NaOH溶液(密度为1.1g/cm3),需NaOH和H2O 各多少克?练习2.从10L密度为1.84 g/cm3、溶质的质量分数为98%的浓硫酸中取出1L,取出的溶液中溶质的质量分数为,溶质质量为,含纯硫酸的质量为。
练习3.下列四种KCl溶液,溶质的质量分数最大的是()A.15gKCl溶于85g水中B.85g溶液中含有KCl的质量为15gC.20gKCl配成120g溶液D.一定量的KCl加入80g水配成100g溶液第2课时题型三:例题1.把50g质量分数为98%的H2SO4溶液稀释成质量分数为20%的硫酸溶液,需要加水多少克?练习1.需要配制500g质量分数为10%的盐酸,需要质量分数为38%的盐酸(密度为1.19g/cm3)多少毫升?练习2.配制500mL质量分数为20%的H2SO4溶液,需要质量分数为98%H2SO4溶液多少毫升?需要加水多少毫升?查阅资料:密度(g/cm3) 1.07 1.14 1.30 1.5 1.81 1.84% 10 20 40 60 90 98练习3:将100g10%的蔗糖溶液的溶质质量分数为20%,可采用的方法有 ( ) A.加入10g蔗糖 B.蒸发掉50g水C.把溶剂蒸发掉一半D.加入12.5g蔗糖题型四:例题1.50g10%的KNO3溶液与50g30%的KNO3溶液混合后,所得混合溶液的溶质质量分数是多少?练习1.100mL20%的食盐水与200mL20%的食盐水相混合,得到食盐水的溶质质量分数为()A.5% B.10% C.15% D.20%题型五:例题1.含80g碳酸钙的石灰石跟稀盐酸反应来制取二氧化碳,求:(1)制得多少克二氧化碳?(2)若所用盐酸的质量分数为36.5%,密度为1.19g/cm3,需用盐酸多少毫升?例题2.32.5g锌可以与200g某稀硫酸恰好完全反应,计算:(1)这种稀硫酸中溶质的质量分数是多少?(2)反应后所得溶液中溶质的质量分数是多少?(3)若将100g这种稀硫酸稀释成溶质的质量分数为20%的硫酸溶液,需要加水多少克?练习1.139mL密度为1.05g/cm3的盐酸与石灰石25g恰好完全反应,生成8.8g 二氧化碳.计算:(1)盐酸中溶质质量分数;(2)石灰石中碳酸钙的质量分数;(3)生成溶液中溶质的质量分数。

溶质的质量分数练习卷1.下列措施后所得溶液的溶质质量分数一定变大的是【答案】C2.对“溶质的质量分数为20%的NaCl溶液”的含义,解释正确的是A.在该溶液中,溶质和溶剂的质量比为1∶5B.100克水中含有20克NaClC.在该溶液中,溶质与溶液的质量比为1∶6D.50克该溶液中含有NaCl为10克【答案】D3.用质量分数为98%的浓硫酸配置20%的硫酸溶液,全部用到的一组实验仪器是A.天平、量筒、烧杯、酒精灯B.烧杯、量筒、玻璃棒、胶头滴管C.天平、量筒、药匙、烧杯D.量筒、试管、烧杯、玻璃棒【答案】B4.配制6%的氯化钠溶液溶质质量分数偏大的可能原因是A.转移称量好的氯化钠固体时有少量洒落在桌面上B.量取水的体积时仰视量筒读数C.溶解时用玻璃棒搅拌,有少量液体溅出D.转移配置好的溶液时有少量液体溅出【答案】C5.下列说法正确的是A.100g 10%的硝酸钾溶液的溶质质量分数增大到20%,需再加入10g硝酸钾固体B.将10g食盐溶解在100g水中,所得溶液的溶质质量分数为10%C.20%的食盐溶液中取出的5 g溶液的溶质质量分数比原溶液小D.当溶液被水稀释时,溶液中保持不变的是溶质的质量6.将20℃时一定质量的饱和硝酸钾溶液,分别进行如下实验后,所得结论正确的是A.升温至30℃时,溶液中溶质的质量分数不变B.保持温度不变,蒸发10g水后,硝酸钾的溶解度增大C.保持温度不变,蒸发10g水后,溶液中溶质的质量分数减小D.保持温度不变,加入10g硝酸钾后,溶液中溶质的质量分数增大【答案】A7.把20 g溶质质量分数为95%的酒精,稀释为溶质质量分数为50%的酒精,根据需加水的体积(水的密度为1g/cm3),为了减少实验误差,最好选用量筒的量程为A.10 mL B.50 mL C.20 mL D.100 mL【答案】C8.现有100g溶质质量分数为10%的某溶液,使其浓度增大一倍,采用的方法达不到目的是(假设蒸发溶剂时没有晶体析出)A.将溶剂的质量蒸发掉一半B.再加入溶质12.5gC.蒸发掉的溶剂的质量等于溶液质量的一半D.加入200g溶质质量分数为25%的此溶液【答案】A9.传统“陈醋”生产过程中有一步称为“冬捞夏晒”,是指冬天捞出醋中的冰,夏日曝晒蒸发醋中的水分,以提高醋的质量.假设用醋酸的质量分数为3%的半成醋,生产500g醋酸的质量分数为5.4%的优级醋,过程中醋酸没有损失,捞出的冰和蒸发的水分的总质量为A.500 g B.400 g C.200 g D.100 g【答案】B10.40℃时,烧杯中盛有100g硝酸钾的饱和溶液,恒温下蒸发部分溶剂,然后再将溶液逐渐升温到60℃.能表示此过程溶质质量分数a%与时间t关系的示意图的是11.今年某各学区进行了部分学生化学实验操作竞赛,某学区竞赛题目之一是“配制100 g 20%的氯化钠溶液”。

溶质的质量分数练习卷1.下列措施后所得溶液的溶质质量分数一定变大的是【答案】C2.对“溶质的质量分数为20%的NaCl溶液”的含义,解释正确的是A.在该溶液中,溶质和溶剂的质量比为1∶5B.100克水中含有20克NaClC.在该溶液中,溶质与溶液的质量比为1∶6D.50克该溶液中含有NaCl为10克【答案】D3.用质量分数为98%的浓硫酸配置20%的硫酸溶液,全部用到的一组实验仪器是A.天平、量筒、烧杯、酒精灯B.烧杯、量筒、玻璃棒、胶头滴管C.天平、量筒、药匙、烧杯D.量筒、试管、烧杯、玻璃棒【答案】B4.配制6%的氯化钠溶液溶质质量分数偏大的可能原因是A.转移称量好的氯化钠固体时有少量洒落在桌面上B.量取水的体积时仰视量筒读数C.溶解时用玻璃棒搅拌,有少量液体溅出D.转移配置好的溶液时有少量液体溅出【答案】C5.下列说法正确的是A.100g 10%的硝酸钾溶液的溶质质量分数增大到20%,需再加入10g硝酸钾固体B.将10g食盐溶解在100g水中,所得溶液的溶质质量分数为10%C.20%的食盐溶液中取出的5 g溶液的溶质质量分数比原溶液小D.当溶液被水稀释时,溶液中保持不变的是溶质的质量【答案】D6.将20℃时一定质量的饱和硝酸钾溶液,分别进行如下实验后,所得结论正确的是A.升温至30℃时,溶液中溶质的质量分数不变B.保持温度不变,蒸发10g水后,硝酸钾的溶解度增大C.保持温度不变,蒸发10g水后,溶液中溶质的质量分数减小D.保持温度不变,加入10g硝酸钾后,溶液中溶质的质量分数增大【答案】A7.把20 g溶质质量分数为95%的酒精,稀释为溶质质量分数为50%的酒精,根据需加水的体积(水的密度为1g/cm3),为了减少实验误差,最好选用量筒的量程为A.10 mL B.50 mL C.20 mL D.100 mL【答案】C8.现有100g溶质质量分数为10%的某溶液,使其浓度增大一倍,采用的方法达不到目的是(假设蒸发溶剂时没有晶体析出)A.将溶剂的质量蒸发掉一半B.再加入溶质12.5gC.蒸发掉的溶剂的质量等于溶液质量的一半D.加入200g溶质质量分数为25%的此溶液【答案】A9.传统“陈醋”生产过程中有一步称为“冬捞夏晒”,是指冬天捞出醋中的冰,夏日曝晒蒸发醋中的水分,以提高醋的质量.假设用醋酸的质量分数为3%的半成醋,生产500g醋酸的质量分数为5.4%的优级醋,过程中醋酸没有损失,捞出的冰和蒸发的水分的总质量为A.500 g B.400 g C.200 g D.100 g【答案】B10.40℃时,烧杯中盛有100g硝酸钾的饱和溶液,恒温下蒸发部分溶剂,然后再将溶液逐渐升温到60℃.能表示此过程溶质质量分数a%与时间t关系的示意图的是【答案】D11.今年某各学区进行了部分学生化学实验操作竞赛,某学区竞赛题目之一是“配制100 g 20%的氯化钠溶液”。

一. 选择题1.在25℃时,向不饱和氯化钾溶液加入少量氯化钾固体至溶液刚好饱和,在这一过程中,下列各量:①溶液中水的质量,②溶液中溶质的质量,③溶液中氯化钾的质量分数,④25℃时氯化钾的溶解度,⑤氯化钾溶液的质量。
其中不变的是()A.①和④;B.②和③C.③和④D.④和⑤2.下列有关溶液的说法中,正确的是A.溶液不一定都是混合物B.将100g KCl饱和溶液蒸干得到25g固体,则KCl在该温度下的溶解度为25gC.常温下将饱和Ca(OH)2溶液加热到50℃,会使溶液由饱和变为不饱和D.从25%的H2SO4溶液中取出10mL,则取出溶液的质量分数仍为25%3.把100mL10%的氯化钠溶液稀释50倍,稀释后溶液中的溶质质量()A.减少50倍B.增加50倍C.不变D.减少5倍4.某溶液溶质的质量分数为10%,下面说法正确的是()①在100份质量溶液中含有10份质量溶质②在110份质量溶液中含有10份质量溶质③在100份质量溶剂中含有10份质量溶质④在90份质量溶剂中溶有10份质量溶质.A.①②B.③④C.②③D.①④5.某次蔗糖溶解实验过程如图所示,不考虑水分蒸发,下列判断错误的是()A.②中溶液是饱和溶液B.③中溶液一定是不饱和溶液C.②③中溶液的溶质质量分数不相同D.③中溶液的溶质质量大于②中溶液的溶质质量6.如图是a、b、c三种物质的溶解度曲线,a与c的溶解度曲线相交于P点,根据图中已给信息判断下列说法错误的是()A.P点的含义是t1℃时,a与c的溶解度相等B.t2℃时,a、b、c三种物质溶解度由小到大顺序为c b aC.将t2℃时a、b两种饱和溶液降温到t1℃时,析出晶体的质量a大于bD.将t1℃时,a、c两种物质饱和溶液的温度升高到t2℃时,所得两种溶液的质量分数a大于c7.甲、乙、丙三种固体物质的溶解度曲线如图所示.下列叙述错误的是A.t1℃时,将等质量的甲、乙分别配成饱和溶液,所得溶液质量:甲>乙B.将t1℃时甲、丙的饱和溶液升温到t2℃,两种溶液中溶质的质量分数相等C.将t2℃时甲的饱和溶液变为t3℃时甲的饱和溶液,可以采用蒸发水的方法D.将t3℃时三种物质的饱和溶液恒温蒸发等量水后,析出溶质的质量:甲>乙>丙8.如图为甲、乙两种固体物质的溶解度曲线。
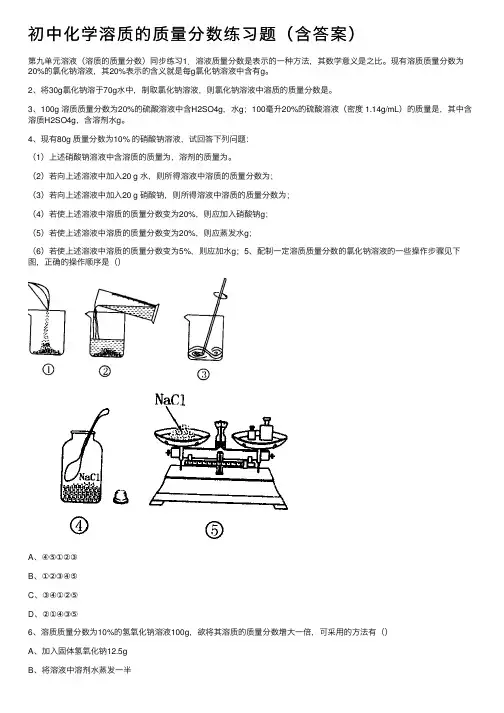
初中化学溶质的质量分数练习题(含答案)第九单元溶液(溶质的质量分数)同步练习1.溶液质量分数是表⽰的⼀种⽅法,其数学意义是之⽐。
现有溶质质量分数为20%的氯化钠溶液,其20%表⽰的含义就是每g氯化钠溶液中含有g。
2、将30g氯化钠溶于70g⽔中,制取氯化钠溶液,则氯化钠溶液中溶质的质量分数是。
3、100g 溶质质量分数为20%的硫酸溶液中含H2SO4g,⽔g;100毫升20%的硫酸溶液(密度 1.14g/mL)的质量是,其中含溶质H2SO4g,含溶剂⽔g。
4、现有80g 质量分数为10% 的硝酸钠溶液,试回答下列问题:(1)上述硝酸钠溶液中含溶质的质量为,溶剂的质量为。
(2)若向上述溶液中加⼊20 g ⽔,则所得溶液中溶质的质量分数为;(3)若向上述溶液中加⼊20 g 硝酸钠,则所得溶液中溶质的质量分数为;(4)若使上述溶液中溶质的质量分数变为20%,则应加⼊硝酸钠g;(5)若使上述溶液中溶质的质量分数变为20%,则应蒸发⽔g;(6)若使上述溶液中溶质的质量分数变为5%,则应加⽔g;5、配制⼀定溶质质量分数的氯化钠溶液的⼀些操作步骤见下图,正确的操作顺序是()A、④⑤①②③B、①②③④⑤C、③④①②⑤D、②①④③⑤6、溶质质量分数为10%的氢氧化钠溶液100g,欲将其溶质的质量分数增⼤⼀倍,可采⽤的⽅法有()A、加⼊固体氢氧化钠12.5gB、将溶液中溶剂⽔蒸发⼀半C 、加⼊100g10%的氢氧化钠溶液D 、蒸发掉50g ⽔E 、加⼊50g40%的氢氧化钠溶液7、将m g 硝酸钾的不饱和溶液恒温蒸发⽔分⾄有晶体析出,在此变化过程中溶液⾥溶质质量分数 p % 与时间t 的关系正确的是()8、在45g20%的KCl 溶液中加⼊ 8g KCl 后再加⼊14g ⽔,所得溶液恰好为20℃的饱和溶液,则所得溶液中溶质的质量分数为。
9、下图是某同学配制⼀定质量的0.9%⽣理盐⽔的全过程:(1)请找出上图中的错误:①;②。

溶质的质量分数(北京习题集)(教师版)一.选择题(共6小题)1.(2007•攀枝花)下列仪器只需用水就能清洗干净的是()A.附有食盐的试管B.附有植物油的试管C.附有铁锈迹的试管D.久置的装石灰水的试管2.(1999•鄂州)0.05克某物质在室温时溶于10克水中即达到饱和,则一般把这种物质划分为()A.易溶物质B.可溶物质C.微溶物质D.难溶物质3.(2019•朝阳区校级模拟)下列操作中一定能改变溶液中溶质质量分数的是()A.增加溶质B.改变温度C.增加溶剂D.析出晶体4.(2018•海淀区二模)KCl和KNO3在不同温度下的溶解度数据如表所示,下列说法中正确的是()温度/℃203040溶解度/gKCl333845 KNO33164110A.40℃时,100g水中最多溶解45 g KClB.随着温度的升高,某饱和KCl溶液中会有固体析出C.KNO3的溶解度始终大于KClD.40℃时,某KNO3溶液中溶质的质量分数一定为×100% 5.(2017秋•北京期末)下表中的选项不符合如图所示曲线的是()选项横坐标纵坐标A向一定量稀硫酸中加入锌粉的质量产生氢气的体积B向一定量的铁粉中加入硫酸铜溶液的质量固体的质量C给一定量高锰酸钾固体加热的时间产生气体的质量D在一定温度下,向一定量的水中加入食盐晶体的质量溶液中溶质的质量分数A.A B.B C.C D.D6.(2017•通州区一模)下列四个图象中,能正确反映对应关系的是()A.一定温度下,向一定量水中加入KNO3固体B.加热一定量的高锰酸钾固体C.向一定量的硫酸铜溶液中加入铁粉D.向一定量的MnO2中加入H2O2溶液二.多选题(共2小题)7.(2015秋•房山区期末)如图表所示,图象能正确反映对应变化关系的是()A.向一定量的氯化钠不饱和溶液中加入氯化钠B.加热一定量的高锰酸钾固体C .将水通电一段时间D .向一定量的二氧化锰中加入过氧化氢溶液8.(2014•北京模拟)如图是A、B两种物质的饱和溶液的溶质的质量分数随温度变化的曲线,现将20gA和40gB 分别置于100g水中,加热使其完全溶解,然后再冷却到t℃,下列有关叙述中正确的是()A.t℃时,A溶液的溶质的质量分数小于BB.t℃时,A溶液的溶质的质量分数等于BC.t℃时,两溶液中均无固体物质析出D.t℃时,二者的溶解度相等三.填空题(共3小题)9.(2017•海淀区一模)2017年1月《科学报告》一篇文章称,只需在普通口罩上添加氯化钠涂层,就能将其转化为“特效口罩”。

人教版九年级化学下册《9.3溶质的质量分数》同步练习题及答案【基础篇】1.溶液加水稀释时,没有发生变化的是()A.溶质的质量分数B.溶质的质量C.溶剂的质量D.溶液的质量2.温度不变的条件下,欲使溶质的质量分数变为原来的2倍,下列方法一定可行的是()A.20g硝酸钾饱和溶液蒸发掉10g水B.20g硝酸钾不饱和溶液蒸发掉10g水C.在10g10%的硝酸钾溶液中加入5g40%的硝酸钾溶液D.在10g10%的硝酸钾不饱和溶液中加入10g硝酸钾固体3.从100g 1%的硫酸溶液中取出10g,这10g溶液中溶质质量分数是()A. 1%B. 0.1%C. 10%D. 无法判断4.向饱和氯化钾溶液中加入一定量氯化钾,保持温度不变,则()A.溶液质量增加B.溶液中溶质质量分数不变C.溶液中溶质质量分数增大D.溶液中溶质质量增加5.右图为A、B、C三种物质的溶解度曲线,下列说法正确的()A. B的溶解度大于C的溶解度。
B. t1℃时,A溶液与C溶液溶质质量分数相等。
C. t1℃时A的饱和溶液升温到t2℃,溶质质量分数不变。
D. 将t2℃时C物质接近饱和的溶液变为饱和溶液,可采用降温的方法。
【能力篇】一、单选题:1.向盛有Fe和Cu的试管中加入过量稀H2SO4,所得溶液中溶质有()A. 1种B. 2种C. 3种D. 4种2.下列说法正确的是()A. 10g硫酸铜溶于100g水配得的溶液溶质质量分数是10%B. 将50g10%的氯化钠溶液稀释成100g5%的溶液稀释后溶液中溶质质量是稀释前溶质质量的一半C. 20℃时,氯化钠的溶解度是36g,该温度下,将40g氯化钠放入100g水中,所得溶液溶质质量分数为26.5%D. 100mL98%的浓硫酸(密度为1.84g/cm3)中含硫酸184g3.蔗糖是生活中常用的调味品,其溶解度曲线如下图。
下列说法正确的是( )A.蔗糖在热水中的溶解度比在冷水中的小B.将蔗糖饱和溶液蒸发溶剂后恢复至原温度,有结晶现象C.温度升高,溶液中蔗糖的质量分数一定增大D.t1℃和t2℃时的两份蔗糖溶液,所含溶质的质量不可能相等4.KCl是一种常用钾肥,其溶解度如下表。

化学溶质的质量分数习题1.现有20℃时NH4Cl饱和溶液200g,今欲改变该饱和溶液中溶质的质量分数,可采取的措施是()A.保持温度不变,蒸发掉20g水B.保持温度不变,加入20gNH4Cl固体C.保持温度不变,取出20g溶液D.保持温度不变,加入20g水2.用溶质的质量分数为98%的H2SO4(密度为1.84g/cm3)来配制44mL 20%的H2SO4(密度为1。
14g/cm3),需要98%H2SO4的体积是()A.1。
8mLB.5.6mLC.7。
8mLD.10.2mL3.把70%的硝酸(密度为1。
44g/cm3)与等体积的水混合,所得稀硝酸中溶质的质量分数是( )A.等于35%B.小于35%C.大于35%D.无法确定4.今有60g溶质的质量分数为10%的NaNO3溶液,欲将其溶质的质量分数增大一倍,应采用的方法是( )A.把溶剂蒸发掉一半B.加入6gNaNO3晶体C.把溶剂蒸发掉30gD.加入20%的NaNO3溶液30g5.将80g10%的NaOH溶液与20g15%的NaOH溶液混合,混合溶液中溶质的质量分数为( )A.13%B.12%C.11%D.16%6.下图是a、b两种固体物质的溶解度曲线,下列说法中不正确的是()A.a的溶解度大于b的溶解度B.在25℃时,a、b的饱和溶液中溶质的质量分数相等C.当a中混有少量b时,可用结晶法提纯D.a、b都属于易溶物质7.将质量各为mg的Na2O和NaCl,分别加入到ng水中,完全溶解后得到a和b两种溶液.下列说法中正确的是( )A.该温度下NaCl的溶解度为(100m/n)gB.a、b两种溶液中溶质的质量分数相同C.a比b溶液中溶质的质量分数大D.a、b两种溶液的质量相等8.20℃时,某物质R的不饱和溶液中溶质的质量分数为10%,若向该溶液中再加入5g R或蒸发掉32。
26g水,都可以形成饱和溶液。
那么该物质在20℃时其饱和溶液中溶质的质量分数是()A.10%B.13。

有关溶质的质量分数的计算练习类型一溶质质量分数概念的应用1.要配制30%60克硝酸钾溶液,需要硝酸钾多少克?水多少克?2.20克氯化钾溶于水后,取得的溶液其溶质的质量分数为40%,那么取得的溶液的质量为多少?需要的水的质量为多少?3.向30克溶质质量分数为20%的硝酸钾溶液中加入70克水,那么所得溶液的溶质质量分数为多少?4.向50克溶质质量分数为10%的硝酸钾溶液中加入50克硝酸钾, 那么所得溶液的溶质质量分数为多少? 5.把120克10%的硝酸钾溶液平均分成三等分⑴第一份升高温度,求溶质质量分数⑵第二份加入10克硝酸钾求溶质质量分数⑶第三分加入10水求溶质的质量分数类型二稀释与浓缩问题1.将100克10%的硝酸钾溶液蒸发50克水求所得溶液的溶质质量分数为多少?2.向200克20%的氯化钠溶液中加入100克水, 求所得溶液的溶质质量分数为多少?3.把50克50%氯化钾溶液稀释成10%的,需加水多少克?4.将20克溶质质量分数为10%的氢氧化钠溶液质量分数增至20%,需蒸发水多少克?5.汽车蓄电池中稀硫酸的溶质质量分数为28%,密度为1.2 g·cm-3。
假设要在实验室用溶质质量分数为98%的浓硫酸配制这种稀硫酸630 g,求:(1)630g稀硫酸的体积是多少毫升? (2)需要浓硫酸多少克?6.配制500毫升质量分数为20%硫酸溶液,需质量分数为98%的硫酸多少毫升?需水多少毫升?(20%的硫酸密度为1.14g/cm3,98%的硫酸密度为1.84 g/cm3)7.配制100克10%的盐酸,需要20%的盐酸(密度为1.1 g/cm3)的体积体积为多少?水的质量为多少?8.将80 g 10%的NaOH溶液与20 g 15%的NaOH溶液混合,混合溶液中溶质的质量分数为多少?9.100克40%的蔗糖溶液和多少克60%的蔗糖溶液混合,能取得50%的蔗糖溶液10.现有100克溶质的质量分数为10%的氢氧化钠溶液,欲将其溶质质量分数增大一倍,可采纳的方式有⑴加入氢氧化钠多少克?⑵蒸发掉水多少克?⑶加入多少克40%的氢氧化钠溶液?⑷加入多少克60%的氢氧化钠溶液?类型三与溶解度相关的计算20℃时,硝酸钾溶解度为30克,现将18克的硝酸钾溶于50克的水中,那么所得溶液的质量为多少?溶质的质量分数为多少?类型四溶质质量分数与化学反映方程式的综合计算1.向400g溶质的质量分数为4.9%的稀硫酸中加入足量的锌粒,充分反映后,求所得溶液中溶质的质量分数为多少?2.13克含杂质的锌粒与73克10%的稀盐酸恰好完全反映求(1)纯锌的质量分数(2)生成氢气的质量(3)所得溶液中溶质的质量分数3.32.5克锌粉与245克稀硫酸恰好完全反映,问:(1)生成氢气多少克?(2)所用稀硫酸的质量分数是多少?(3)生成物溶液的溶质质量分数是多少?4.100克溶质的质量分数为18.25%的稀盐酸与碳酸钙恰好完全反映,求反映后溶液中溶质的质量分数取24克大理石放入烧杯中,加入必然量的10%的稀盐酸,恰好完全反映,搜集到二氧化碳的质量是8.8克,求(1)大理石中碳酸钙的质量分数(2)所用稀盐酸溶液的质量(3)配制10%的这种稀盐酸需要38%的盐酸(密度为1.1 g/cm3)多少毫升?。


溶质的质量分数分题型练习(备注:请写出每题的计算过程,每题4分满分100分)一、溶解度问题【解题思路】一定温度下,不同质量的同种溶质与溶剂饱和时,溶质、溶剂、溶液三者的...质量之比保持不变。
可用下式进行计算S\100=m质\m剂或者S\(100+S)=m质\m液。
【例】t℃时,m克硝酸钾溶解在n克水中,恰好饱和,则硝酸钾在t℃时的溶解度是多少?解:Sg\100g=mg\ng 解得S=100m\n g 答:硝酸钾在t℃时的溶解度是100m\n 克。
【练习】1、20℃时,将9克某物质溶于25克水中,刚好制得饱和溶液34 克,则20℃时该物质的溶解度为多少?2、20℃时,某物质的饱和溶液中,溶质和溶液的质量比为2:7,则20℃时该物质的溶解度为多少?3、20℃时,20克水中最多能溶解0.3克A物质,则A物质在该温度下地溶解度为多少?4、在25℃时,将某浓度的芒硝溶液分为等质量的两份溶液,一份加热蒸发掉20g水后降至25℃成为饱和溶液,另一份加入10g芒硝晶体后也成为饱和溶液。
则25℃时芒硝的溶解度是多少?二、已知质量,求质量分数。
【解题思路】溶质的质量分数=溶质的质量÷溶液的质量×100%溶剂的质量分数=溶剂的质量÷溶液的质量×100% 溶质的质量分数+溶剂的质量分数=1【练习】5、10克氯化钠溶于40克水中,求所得容易的溶质的质量分数为多少?溶剂的质1 / 5 量分数为多少?6、10g氯化钠完全溶于水,得到40g溶液,求所得溶液的溶质质量分数为多少?溶剂的质量分数为多少?7、一定量的氯化钠溶于40g水中,得到50g溶液,求所得溶液的溶质质量分数为多少?溶剂的质量分数为多少?8、已知某物质在t℃时溶解度为S,则(1)溶质的质量:溶剂的质量:溶液的质量为多少?(2)溶质的质量分数为多少?(3)溶剂的质量分数为多少?9、20℃时食盐的溶解度为36g,20℃时将20g食盐放入50g水中,充分溶解后,所得溶液溶质的质量为多少?溶剂的质量分数为多少?三、已知质量分数,求质量【解题思路】由“溶质的质量分数=溶质的质量÷溶液的质量×100% 、溶剂的质量分数=溶剂的质量÷溶液的质量×100% ”变形可得:“溶液的质量=溶质的质量÷溶质的质量分数、溶液的质量=溶剂的质量÷溶剂的质量分数”【练习】10、40克10%的氯化钠溶液中含氯化钠多少克?水多少克?11、40克氯化钠配置成10%的氯化钠溶液,溶液的质量为多少?需要加多少水?2 / 512、现有16g硫酸铜,要配制成溶质质量分数为10%的硫酸铜溶液,溶液的质量为多少?需要加多少水?13、晓晓同学为了制作“叶脉书签”,要用24g氢氧化钠颗粒来配置12%的氢氧化钠溶液来。
初二溶质质量分数练习题溶质质量分数是指溶液中溶质的质量与溶液总质量的比值。
它是描述溶液中溶质质量占比的一种方式,是化学中重要的概念之一。
下面是一些关于初二溶质质量分数的练习题,帮助你提高对该概念的理解和应用能力。
练习题1:某化学实验中,向100g纯水中加入20g盐,搅拌均匀后得到溶液。
求这个溶液的溶质质量分数。
解答:溶质质量分数 = 溶质质量 / 溶液质量溶液质量 = 溶质质量 + 溶剂质量根据题目,溶质质量为20g,溶剂质量为100g,所以溶液质量为20g + 100g = 120g溶质质量分数= 20g / 120g = 1/6 ≈ 0.1667练习题2:用质量分数来描述盐酸溶液中盐酸的含量。
如果盐酸溶液的质量分数为0.2,说明这个溶液中含有多少质量百分比的盐酸?解答:质量分数 = 溶质质量 / 溶液质量溶质质量百分比 = 质量分数 × 100%根据题目,质量分数为0.2,即溶质质量为20%,则溶质质量百分比为20%。
练习题3:溶液1中含有20g NaCl,溶液2中含有30g NaCl。
求这两个溶液按质量混合后的溶质质量分数。
解答:溶液1的溶质质量分数 = 20g / (20g + 80g) = 0.2溶液2的溶质质量分数 = 30g / (30g + 70g) = 0.3混合后的总溶质质量 = 20g + 30g = 50g混合后的总溶液质量 = (20g + 80g) + (30g + 70g) = 200g混合后的溶质质量分数 = 50g / 200g = 0.25练习题4:某化学实验中,用200g水稀释25g的NaOH溶液,问稀释后的溶液中NaOH的质量分数是多少?解答:稀释后的溶液总质量 = 原溶液中的溶剂质量 + 稀释用的溶剂质量 = 25g + 200g = 225g稀释后溶液中NaOH的质量 = 原溶液中NaOH的质量 = 25g稀释后的溶液中NaOH的质量分数= 25g / 225g ≈ 0.1111通过以上练习题,我们可以更好地理解溶质质量分数的计算和应用方法。
1.5溶质质量分数习题分类集训一、溶质质量分数1.某溶液中溶质的质量分数为10%,下列说法正确的是()A.在100g 溶剂中溶有10g 溶质B.在110g 溶剂中溶有10g 溶质C.在100g 溶液中含有10g 溶质D.在110g 溶液中含有10g 溶质2.从100g 9%的氯化钠溶液中取出10g,那么剩下的90g 氯化钠溶液的质量分数是()A.1%B.9%C.10%D.11.1%3.现有一瓶溶质质量分数为10%的食盐水,关于该食盐水的说法正确的是()A.m 质:m 剂=1:10B.m 质:m 液=1:10C.m 质:m 液=1:11D.m 剂:m 液=10:114.对“20%的蔗糖溶液”含义的理解错误的是()A.20g 蔗糖溶于水配成100g 溶液B.40g 水中溶解了10g 蔗糖C.将蔗糖和水按照1:9质量比配成的溶液D.溶质和溶液的质量比为1:55.从100g10%的氢氧化钠溶液中取出5g,取出的溶液中溶质的质量分数是()A.10%B.1%C.0.1%D.无法判断6.在t℃时将5克某纯净物完全溶解在95克水中,所得溶液中溶质的质量分数()A.等于5%B.大于5%C.小于5%D.三种情况都有可能7.浓度为10%的食盐溶液100克,将其浓度增加到20%,可采用的方法()A.加入20克食盐固体B.把溶液中的水蒸发掉一半C.加入200克30%的食盐溶液D.把水蒸发掉50克8.要将50克质量分数为a%的某溶液变为2a%(溶解度允许值内),可采用的方法有()A.蒸发掉一半溶剂(恒温)B.蒸发掉25克溶剂(恒温C.加入50克a%的该溶液D.加入0.5a 克该溶质9.有40g 溶质质量分数为5%的氯化钙溶液,若将其溶质的质量分数增加到10%,应采用的方法是()A.把溶剂蒸发掉一半B.加入40g 溶质质量分数为10%的氯化钙溶液C.把溶剂蒸发掉20g D.加入3g 氯化钙晶体10.在温度不变的条件下,欲使溶质的质量分数变为原来2倍,下列最可行的是()。
课题3 溶质的质量分数1、(1)溶质的质量分数 = ———————————×100%。
(2)溶质质量 = 。
(3)溶剂质量 = 。
(4)溶液质量 = + 。
2、某溶液溶质的质量分数为10%,含义是:,则溶质、溶剂、溶液的质量比为:。
3、t℃时,氯化钠的溶解度为36克,表示的意义是:,则溶质、溶剂、溶液的质量比为:,溶质的质量分数为。
4、50克20%的硝酸钾溶液,含有克硝酸钾,克水。
(1)若向此溶液中加入10克水,则溶质质量分数为。
(2)若向此溶液中加入10克硝酸钾完全溶解,则溶质质量分数为。
(3)若向此溶液中加入10克硝酸钾和10克水完全溶解,则溶质质量分数为。
5、20℃时,硝酸钠的溶解度是88克。
将50克硝酸钠放入50克水中,充分溶解后,形成20℃时硝酸钠的,此时溶液中硝酸钠的质量分数等于。
6、在常温下,向100克5%的氯化钠溶液中加入5克氯化钾粉末。
完全溶解后,氯化钠的质量分数为。
7、如何配制20克10%的蔗糖溶液?写出所需的步骤和实验仪器。
答:(1)配制步骤:①:需克蔗糖,克水。
②:用称量克蔗糖,放入烧杯中,再用 mL的量筒量取 mL 水,倒入烧杯中。
③:用不断搅拌,使之充分溶解。
(2)所需仪器:。
8、已知40℃时氯化钾的溶解度为40克。
现有40℃时氯化钾的饱和溶液500克,则该溶液中含氯化钾克,含水,溶质的质量分数为。
先将该溶液平均分成5等分,则:(1)40℃时向第一份溶液中再加入10克氯化钠,则:所得溶质质量分数为,溶解度。
(变大、变小或不变)(2)40℃时将第二份溶液恒温蒸发10克水,则:所得溶质质量分数为,溶解度。
(3)40℃时向第二份溶液中加入10克水,则:所得溶质质量分数为,溶解度。
(4)降温,称量析出晶体质量为5克,则:所得溶质质量分数为,溶解度,所得溶液为溶液。
(5)升高温度至60℃,溶质质量分数,溶解度,所得溶液为溶液。
再加入2克氯化钠完全溶解,则溶质的质量分数为。
溶质质量分数计算
1、将25克食盐完全溶解在100克水中,得到的食盐溶液的溶质质量分数是多少?
2、恒温蒸发100克食盐溶液得到15克食盐,则该溶液的溶质质量分数是多少?
3、已知20℃时,食盐的溶解度为36克,在该温度下向50克水中加入20克食盐,得到的溶液的溶质质量分数为多少?
4、现有200克溶质质量分数为50%的食盐溶液,欲将其稀释成溶质质量分数为20%的食盐溶液,可得该溶液多少克?
5、现有100克溶质质量分数为30%的硝酸钾溶液,将其稀释成溶质质量分数为10%的硝酸钾溶液,问应加入多少毫升水?
6、现欲配置溶质质量分数为15%的食盐溶液200克,问需要溶质质量分数为40%的食盐溶液多少克?
7、配置1000克溶质质量分数为9.8%的硫酸溶液,需要溶质质量分数为98%的硫酸溶液多少毫升?(已知98%的硫酸密度为1.84g/cm3)
8、现有溶质质量分数为20%的食盐溶液100克,欲将其变成溶质质量分数为25%的食盐溶液,问应蒸发多少克水或加入多少克食盐?
9、向50克稀硫酸中加入100克溶质质量分数为16%的硫酸溶液,混合后硫酸溶液的质量分数为12%,则原稀硫酸溶液的溶质质量分数是多少?
10、实验室需要配置10%的盐酸500毫升,需要38%的盐酸多少毫升?需要加水多少毫升?(已知10%盐酸的密度是1.047g/cm3,38%盐酸的密度是1.19g/cm3)。
初中化学溶质的质量分数练习题(含答案)1.溶液质量分数是表示溶质质量与溶液总质量之比的一种方法。
例如,一个溶质质量分数为20%的氯化钠溶液,其20%表示每克溶液中含有0.2克氯化钠。
2.将30克氯化钠溶解在70克水中,制得氯化钠溶液,其溶质的质量分数为:溶质质量 = 30克,溶液总质量 = 30克 + 70克 = 100克质量分数 = (30克 / 100克) × 100% = 30%3.100克溶质质量分数为20%的硫酸溶液中含有H2SO420克,水80克;100毫升20%的硫酸溶液(密度1.14克/毫升)的质量是11.4克,其中含有溶质H2SO4 2.28克,含有溶剂水9.12克。
4.现有80克质量分数为10%的硝酸钠溶液,回答下列问题:1)上述硝酸钠溶液中含有溶质的质量为8克,溶剂的质量为72克。
2)加入20克水后,所得溶液中溶质的质量分数为8%。
3)加入20克硝酸钠后,所得溶液中溶质的质量分数为13.33%。
4)为使上述溶液中溶质的质量分数变为20%,应加入硝酸钠16克。
5)为使上述溶液中溶质的质量分数变为20%,应蒸发水20克。
6)为使上述溶液中溶质的质量分数变为5%,应加水128克。
5.配制一定质量分数的氯化钠溶液的正确操作顺序是①②③④⑤。
6.将溶质质量分数为10%的氢氧化钠溶液100克,欲将其溶质的质量分数增大一倍,可采用的方法是加入12.5克固体氢氧化钠。
7.在将mg硝酸钾的不饱和溶液恒温蒸发水分至有晶体析出的过程中,溶液中溶质质量分数p%与时间t的关系应为p%随着t的增加而逐渐增加。
8.在45克质量分数为20%的KCl溶液中加入8克KCl后再加入14克水,所得溶液恰好为20℃的饱和溶液,则所得溶液中溶质的质量为17克。
9.上图中的错误为①和②。
2)可能造成配制的生理盐水中NaCl质量分数小于0.9%的原因有:①称量不准确;②误差发生在配制过程中;③水量加多或少。
10.用1升浓硫酸配制稀硫酸溶液的步骤如下:先取出98克浓硫酸(98%质量分数),加入适量的水,再将稀硫酸溶解在其中,最后加入足够的水,调整溶液体积至1升。
课题9.3 溶质的质量分数(练习)【基础篇】1.关于100g 10%的硝酸钾溶液,下列叙述正确的是()A.100g水中溶有10g硝酸钾B.溶液中硝酸钾与水的质量比为1:10C.将硝酸钾和水按9:1的质量比配成的溶液D.将10g硝酸钾溶于90g水中,可制得该溶液2.按下列方法配制的溶液,其溶质质量分数为5%的是()A.称取5.0g氯化钠,放入95mL水中,充分搅拌B.称取5.0g生石灰,放入95mL水中,充分搅拌C.量取5.0mL浓盐酸,倒入95mL水中,充分搅拌D.称取5.0g二氧化锰,放入95mL水中,充分搅拌3.用浓硫酸配制一定溶质质量分数的稀硫酸时,需要用到的一组实验仪器是()A.托盘天平、玻璃棒、烧杯B.量筒、漏斗、试管C.烧杯、玻璃棒、量筒D.烧杯、蒸发皿、量筒4.用氯化钠固体配制一定溶质质量分数的NaCl溶液时,不需要的操作是()A.称量B.蒸发C.溶解D.取样5.如图,对淡化膜右侧的海水加60倍大气压,水分子可以透过淡化膜进入左侧淡水池,而海水中的其它成分不能通过淡化膜,从而得到淡水。
对加压后右侧海水成分变化进行分析,正确的是()A.溶质质量增加B.溶剂质量不变C.溶液的密度不变D.溶质质量分数增大6.配制9.8%的硫酸溶液1000g需要98%的浓硫酸多少g()A.10g B.100g C.98g D.9.8g7.向一定溶质质量分数的硝酸钾溶液中逐渐加水稀释,下列图象中符合此溶液中溶质质量变化规律的是()A.B.C.D.8.20℃时氯化钠的溶解度为36克,把36克氯化钠放入64克水中,使其充分溶解。
对所得溶液的有关说法错误的是()A.该溶液是饱和溶液B.溶液中Na和Cl﹣个数一定相等C.20℃NaCl饱和溶液溶质质量分数是36%D.溶质与溶剂质量比为9:259.某次蔗糖溶解实验过程如图所示,不考虑水分蒸发,下列判断正确的是()A.②中溶液不是饱和溶液B.③中溶液是不饱和溶液C.②与③中溶质质量分数不相同D.②与③溶液中的溶质质量相同10.现有300g溶质质量分数为10%的氯化钠溶液。
第九单元溶液(溶质的质量分数)同步练习
1 •溶液质量分数是表示_______________ 的一种方法,其数学意义是________________ 之比。
现有溶质质量分数为20%的氯化钠溶液,其20%表示的含义就是每______________ g氯化钠溶液中含有__________________ g o
2、将30g氯化钠溶于70g水中,制取氯化钠溶液,则氯化钠溶液中溶质的质量分数
3、100g 溶质质量分数为20%的硫酸溶液中含H2SO4 _______________ g,水___________ g; 100毫升20%的硫酸溶液(密度 1.14g/mL )的质量是_____________ ,其中含溶质H2SO4 __________ g, 含溶剂水___________ g o
4、现有80g质量分数为10%的硝酸钠溶液,试回答下列问题:
(1)上述硝酸钠溶液中含溶质的质量为________________________________ ,溶剂的质量为___________________ o
(2 )若向上述溶液中加入20 g水,则所得溶液中溶质的质量分数
(3 )若向上述溶液中加入20 g硝酸钠,则所得溶液中溶质的质量分数
(4 )若使上述溶液中溶质的质量分数变为20% ,则应加入硝酸钠
g;
(5)若使上述溶液中溶质的质量分数变为
20%,则应蒸发水____________________ g;
(6)若使上述溶液中溶质的质量分数变为5%,则应加水g;
5、配制一定溶质质量分数的氯化钠溶液的一些操作步骤见下图,正确的操作顺序是 ( )
① ② ③ ④
A、④⑤①②③
B、①②③④⑤
C、③④①②⑤
6、溶质质量分数为10%的氢氧化钠溶液100g,欲将其溶质的质量分数增大一倍,可采
用的方法有( )
A、加入固体氢氧化钠12.5g
B、将溶液中溶剂水蒸发一半
C、加入100g10%的氢氧化钠溶液
D、蒸发掉50g水
E、加入50g40%的氢氧化
钠溶液
7、将m g硝酸钾的不饱和溶液恒温蒸发水分至有晶体析出,在此变化过程中溶液里溶
8、在45g20%的KCI溶液中加入8g KCI后再加入14g水,所得溶液恰好为20C的饱和溶液,则所得溶液中溶质的质量分数
为_________________________________________________________ 。
9、下图是某同学配制一定质量的0.9%生理盐水的全过程:
(1 )请找出上图中的错误:
① _____________________________ :②________________________ 。
(2)如果配制的生理盐水中NaCI的质量分数小于0.9%,则可能造成误差的原因有(至
少举出三点)
① ___________________ ②____________ ③____________
10、汽车、电机车一般要使用铅酸蓄电池。
某铅酸蓄电池用的酸溶液是溶质质量分数
为28%的稀硫酸,现用 1 L溶质质量分数为98%的浓硫酸(密度为1.84g/cm3)配制该稀硫酸。
问:
⑴1 L溶质质量分数为98%的浓硫酸的质量为______________________ ,其中溶质的质量
为___________________ 。
⑵将1 L溶质质量分数为98%的浓硫酸配制成28%的稀硫酸,需要蒸馏水(密度为1g/cm3)___________________________________ L,酉己得稀硫酸的质量为_______________ kg。
11、根据氯化钠和硝酸钾的溶解度表,回答下列问题:。