VSEPR模型判别分子构型
- 格式:doc
- 大小:140.50 KB
- 文档页数:7

分子空间构型与vsepr模型分子空间构型与VSEPR模型一、引言分子空间构型和VSEPR模型是描述分子几何形状和电子排布的两种重要理论模型。
本文将从分子空间构型和VSEPR模型的基本概念、原理和应用等方面进行介绍和讨论。
二、分子空间构型1.基本概念分子空间构型是指分子中原子的三维排列方式。
它决定了分子的几何形状和化学性质。
分子空间构型的研究是理解和预测分子性质的重要基础。
2.原理分子空间构型的形成受到原子间的相互作用力的影响。
主要有键长、键角和二面角等几何参数来描述原子之间的相对位置关系。
3.应用分子空间构型的研究对于理解和预测分子性质具有重要意义。
例如,通过研究分子空间构型可以预测分子的热力学稳定性、化学反应性和光学性质等。
三、VSEPR模型1.基本概念VSEPR模型是指通过分子中的电子对排布来预测分子的三维几何形状。
它是基于电子排斥原理和原子间的相互作用力来建立的。
2.原理VSEPR模型认为,分子中的电子对会尽量远离彼此,以减少电子间的排斥力。
根据电子对的种类(孤对电子或共价键电子对)和数目,可以推导出分子的几何形状。
3.应用VSEPR模型的应用广泛,可以用于预测分子的几何形状和极性。
通过准确预测分子的几何形状,可以进一步推断分子的化学性质和反应行为。
四、分子空间构型与VSEPR模型的关系分子空间构型和VSEPR模型是密切相关的。
分子空间构型确定了分子中原子的相对位置关系,而VSEPR模型则通过分子中的电子对排布来预测分子的几何形状。
在VSEPR模型中,分子空间构型的信息被用来确定电子对的排布方式。
通过分子空间构型的分析,可以确定分子中的孤对电子和共价键电子对的数目和位置,从而推导出分子的几何形状。
分子空间构型的研究也可以通过实验技术如X射线衍射、核磁共振等手段进行验证和确定。
五、结论分子空间构型和VSEPR模型是描述分子几何形状和电子排布的两种重要理论模型。
分子空间构型决定了分子的几何形状和化学性质,而VSEPR模型通过分子中的电子对排布来预测分子的几何形状。


价层电子对互斥理论(VSEPR )现代化学的重要基础之一是分子(包括带电荷的离子)的立体结构。
实验测出,SO 3分子是呈平面结构的,O —S —O 的夹角等于120º,而 SO 32-离子却是呈三角锥体,硫是锥顶,三个氧原子是三个锥角,象一架撑开的照相用的三角架。
又例如SO 2的三个原子不在一条直线上,而CO 2却是直线分子等等。
价层电子对互斥理论用以预测简单分子或离子的立体结构,我们不难学会用这种理论来预测和理解分子或离子的立体结构,并用来进一步确定分子或离子的结构。
价层电子对互斥理论认为,在一个共价分子中,中心原子周围电子对排布的几何构型主要决定于中心原子的价电子层中电子对的数目。
所谓价层电子对包括成键的σ电子对和孤电子对。
价层电子对各自占据的位置倾向于彼此分离得尽可能地远些,这样电子对彼此之间的排斥力最小,整个分子最为稳定。
这样也就决定了分子的空间结构。
也正因此,我们才可以用价层电子对很方便地判断分子的空间结构。
例如:甲烷分子(CH 4),中心原子为碳原子,碳有4个价电子,4个氢原子各有一个电子,这样在中心原子周围有8个电子,4个电子对,所以这4个电子对互相排斥,为了使排斥力最小,分子最稳定,它们只能按正四面体的方式排布。
这样就决定了CH 4的正四面体结构。
利用VSEPR 推断分子或离子的空间构型的具体步骤如下:①确定中心原子A 价层电子对数目。
中心原子A 的价电子数与配位体X 提供共用的电子数之和的一半,就是中心原子A 价层电子对的数目。
例如BF 3分子,B 原子有3个价电子,三个F 原子各提供一个电子,共6个电子,所以B 原子价层电子对数为3。
计算时注意:(ⅰ)氧族元素(ⅥA 族)原子作为配位原子时,可认为不提供电子(如氧原子有6个价电子,作为配位原子时,可认为它从中心原子接受一对电子达到8电子结构),但作为中心原子时,认为它提供所有的6个价电子。
(ⅱ)如果讨论的是离子,则应加上或减去与离子电荷相应的电子数。

1940年,西奇威克(Sidgwick)等在总结实验事实的基础上提出了一种简单的模型,用于预测简单分子或离子的立体结构。
六十年代初,吉列斯比(RJ.Gillespie)和尼霍尔姆(Nyholm)等发展了这一模型。
因该模型思想方法质朴浅显,在预见分子结构方面简单易行,而成为大学基础化学的基本教学内容,并于新一轮课程改革中引入高中化学教学。
这就是价层电子对互斥模型(Valence Shell Electron Pair Repulsion),常以其英文的缩写形式VSEPR来表示。
1、来自生活中的一个游戏现象吹气球是大家熟悉的生活游戏,如果将每个气球吹成一样大小,将其中的两个通过吹气口系在一起,你会发现这两个气球自然成一直线,再向其中加入一个气球并通过吹气口系在一起,你会发现这三个气球均匀地分开成正三角形分布。
依次再向其中加入一个气球并通过吹气口系在一起,你会有什么预期?你会发现结果与你的预期如此地吻合:四个大小相同的气球成正四面体分布,五个大小相同的气球成三角双锥分布,六个大小相同的气球成正八面体分布。
见图:我们很容易从这一游戏现象受到启迪:当物体所占空间因素相同时,它们彼此趋向均匀分布。
这一规律在自然界乃至人类社会生活中并不鲜见,我们不难找到类似的和接近的例子。
2、VSEPR模型要点VSEPR模型认为,分子的几何构型总是采取电子对排斥作用最小的那种结构。
因为这样可使体系的能量最低,中心原子价层的电子对总是按照最合适的空间方式进行分布。
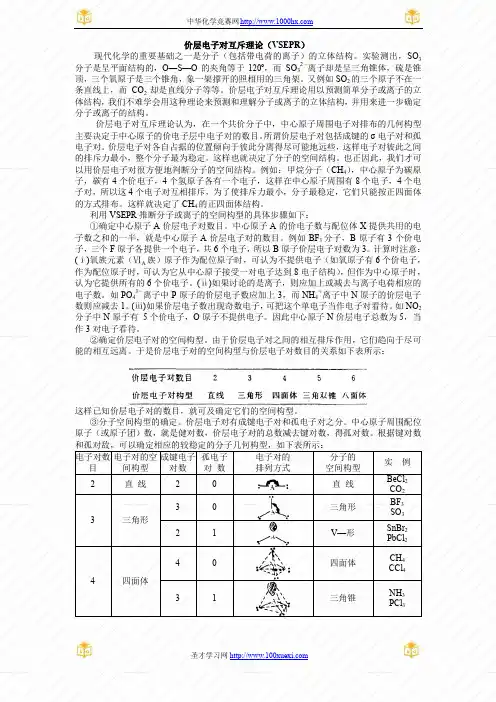
见下表。
电子对的空间分布电子对数空间分布几何构型2 直线3 在角形4 四面体5 三角双锥6 八面体VSEPR模型简朴通俗,应用简单易行,显现了它的独特魅力并引人入胜。
3、VSEPR模型判别分子构型的基本程序中心原子的价层如果没有孤电子对,那么每一个电子对就代表一个共价键,此时电子对的空间分布就是分子的几何构型。
例如,BeCl2分子中Be原子的两个价电子分别与两个Cl原子形成的两个共价键,没有孤电子对,故它是直线型结构。


VSEPR模型判别分子构型VSEPR模型(類向導電子域排斥模型)是一种用統計物理學和原子結構理論來解釋分子的電子結構的理論,它於1960年由魯納斯·米歇爾斯和泰特羅德·德勒爾一起提出,可以用來判斷分子與見面和看不到的原子之間緊密結合的極性,以及分子架構和極性之間的關係。
VSEPR模型假定有六種孤電子域,即取代原子價電子域,空間性屬性和結構的分析圍繞這些域的兩個或更多的孤電子密度中心。
這種取代原子價電子域包括分子軸中的splitting patterns,其中分子軸體積增加,分子受體效應增加和電子重新分配,這會影響分子極性。
VSEPR模型可以用來預測影響分子架構的極性因素。
根據它,原子通過方向交互影響這些孤電子集中在三角形或其他型狀中,以減少孤電子間能量的相互作用。
通過對空間性屬性進行描述,VSEPR模型分類分子形狀和極性。
VSEPR模型可以用來幫助理解分子的極性和穩定的整體架構。
該模型可以用於解釋原子間的鍵的種類和強度。
例如,水分子由中心空氣和兩個水素分子構成,並且水平作用於O原子左右兩側的電子密度,產生非常規形態的四面體。
此外,VSEPR模型可以用來探索分子極性,例如氟分子由中心碳和四個氟原子構成,並且可以假定它們之間存在開放式的雙面體形狀,碳原子中心在氟原子之間為中性,而對極性效應的異質孤電子場,導致该分子具有極性。
VSEPR模型能夠用來確定分子與晶體極性的影響,因為它們的極性可以用裝置的複雜性來預測,从而限制了分子對它們的環境的反應。
VSEPR理論與傳統分子獲得力學(MMFF)結合在一起,為分子力學提供了更多信息,可以用來猜測分子形態和其極性,使其適應不同的環境條件,例如自由基化學反應。
VSEPR模型的發展已經使人們對分子的微觀結構和極性有了更加完整的了解,並提供了一種基於排斥原理的架構來分析分子架構和極性。
這將有助於解釋分子的穩定性,以及分子的反應情況。
2价层电子对互斥模型的应用——判断分子或离子的立体构型价层电子对互斥模型认为,在一个共价分子中,中心原子周围电子对排布的立体构型主要决定于中心原子的价电子层中电子对的数目。
所谓价层电子对包括成键的σ电子对和未成键的孤电子对。
价层电子对各自占据的位置倾向于彼此分离得尽可能地远些,这样电子对彼此之间的排斥力最小,整个分子最为稳定。
这样也就决定了分子的立体结构。
因此利用价层电子对互斥模型可以预测简单分子或离子的立体结构。
利用VSEPR模型推断分子或离子的立体构型的具体步骤如下:1.确定中心原子A价层电子对数目中心原子A的价电子数与配位体X提供共用的电子数之和的一半,就是中心原子A价层电子对的数目。
例如BF3分子,B原子有3个价电子,三个F原子各提供一个电子,共6个电子,所以B原子价层电子对数为3。
如果讨论的是离子,则应加上或减去与离子电荷相应的电子数。
如PO3-4中P原子的价层电子数应加上3,而NH+4中N原子的价层电子数则应减去1。
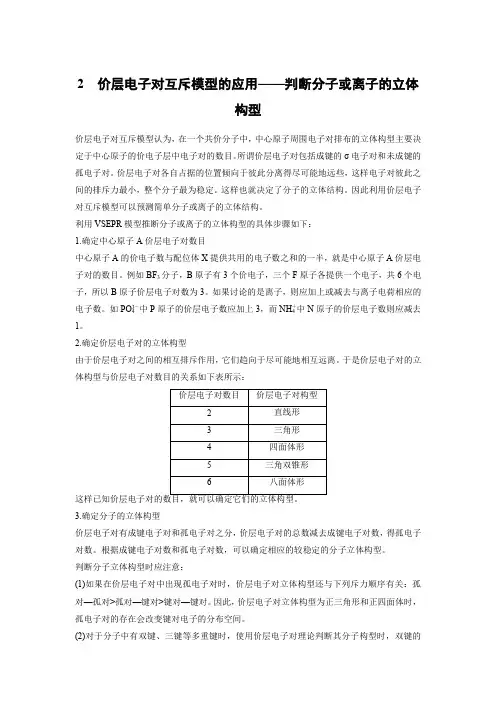
2.确定价层电子对的立体构型由于价层电子对之间的相互排斥作用,它们趋向于尽可能地相互远离。
于是价层电子对的立体构型与价层电子对数目的关系如下表所示:3.确定分子的立体构型价层电子对有成键电子对和孤电子对之分,价层电子对的总数减去成键电子对数,得孤电子对数。
根据成键电子对数和孤电子对数,可以确定相应的较稳定的分子立体构型。
判断分子立体构型时应注意:(1)如果在价层电子对中出现孤电子对时,价层电子对立体构型还与下列斥力顺序有关:孤对—孤对>孤对—键对>键对—键对。
因此,价层电子对立体构型为正三角形和正四面体时,孤电子对的存在会改变键对电子的分布空间。
(2)对于分子中有双键、三键等多重键时,使用价层电子对理论判断其分子构型时,双键的两对电子和三键的三对电子只能作为一对电子来处理。
或者说在确定中心原子的价电子层电子对总数时,不包括形成π键的电子。
实例分析:判断HCHO分子和HCN分子的立体构型。


类似地,重键较单键占据较大的空间,故有斥力大小的顺序:t-t>t-d>d-d>d-s>s-s(t-叁键,d-双键,s-单键)又如,SO2Cl2分子属AX4L=AY4,因S=O键是双键,S-Cl键是单键,据顺序有:∠OSO>109°28''''∠ClSCl<∠OSCl<109°28''''。
此外,键的极性对键角也有影响。
中心原子电负性较大,成键电子对将偏向中心原子,成键电子对之间斥力增大,键角增大,如:NH3、PH3、AsH54c分子中的键角(∠HAH)依次为107°、93.08°、91.8°;配位原子电负性较大,成键电子对将偏离中心原子,成键电子对之间斥力减小,键角减小,如:H2O、OF2分子中的键角(AOA)依次为104.5°、102°。
据此,可解释下列键角变化:NO2+、NO2、NO2-键角(∠ONO)依次为180°、134.3°、115.4°。
价层电子对互斥模型是一个定性模型,与杂化轨道理论相比,它只能对分子的空间构型作定性的描述,而不能对分子的成键原理、键的稳定性做出相应的说明。
但该模型抓住了价层电子对间斥力的大小比较,因此它的很多预测有着相当的正确性。
但由于模型较简单,用来解释某些分子的空间构型时却有困难,例如过渡元素配离子的空间构型,用价层电子对互斥模型就得不到正确的解释。

杂化轨道理论与VSEPR理论对分子空间构型判断的比较大学的第一篇课程论文,为写好这篇论文,学会了不少东西——用数据库查文献,编辑公式,上标、下标,英文的摘要,论文的基本格式摘要:介绍了用杂化轨道理论与价层电子对互斥理论(VSEPR理论)判断分子空间构型的基本要点以及理论之间的不足。
相对而言杂化轨道理论应用的范围较广,但VSEPR理论在判断和预言分子空间几何构型方面仍有重要意义。
二者的结合运用将有助于提高判断分子空间结构的准确性。
比较二者的不同更有利于我们理解。
关键词:杂化;斥力;孤对电子;电子的空间构型在价键理论解释分子的空间结构遇到困难的时候,L .Pauling和J.C.Stater于1931年提出了杂化(hybridization)的概念,以完善和发展价键理论。
之后,N.V.Sidgwick和H.Powell 于1940年前后提出价层电子对互斥理论(valence shell electron pair repulsion,简称VSEPR 法)。
虽然不少教材都对这两种理论作了介绍,但很少把二者相比较起来。
在解释同一个分子的空间构型时,很少从两种理论的不同角度去分析。
笔者认为用两种不同的理论去对同一个分子的空间结构做出解释时,更能有效地比较二者的优缺点,从而加深对它们的认识。
1 杂化轨道理论1.1 杂化轨道理论的内容要点Pauling从原子的价电子构型出发,依据电子的波动性以及波的可叠加性,认为中心原子在与其他原子形成分子时,由于其他原子的影响,中心原子中能量相近的不同类型轨道(s,p,d,…)会发生杂化,形成同等数目的杂化轨道。
在杂化过程中,中心原子的部分轨道上的电子被激发到空轨道上,成单电子增多,杂化之后易于形成多个化学键。
成键时,杂化轨道与邻近原子的原子轨道发生重叠,成键的能力增强,整个分子体系的总能量降到最低,使分子能稳定存在。
所以,原子轨道的杂化是可能的,也是必须的。
对于分子AX n,将A和X从基态激发到价态所需的能量叫价态激发能(P.E.),如P sp 即表示从s轨道激发一个电子到p轨道所需的能量。
whisper模型和分子的立体构型
一、VSEPR模型(即whisper模型):
(1)在ABn型分子中,A原子周围的电子(包括孤对电子和成键电子)尽可能采取斥力最小的方式排列,排列成理想模型。
(2)所以该模型可以说是尽量使得A周围的电子远离,孤对电子之间距离很远,斥力不考虑。
是一种理想模型
二、分子构型:
ABn分子的实际空间构型,这个时候需要考虑孤对电子、成键电子对整个分子构型的影响,因此是一个实际模型。
举个例子吧:以NH3为例,它是AB3的分子。
VSEPR模型看,它是SP3杂化,正四面体形;分子构型看,还有一堆孤对电子,三角锥形。
VSEPR模型,即N为中心,孤对电子连同成键电子在正四面体四个顶点;分子构型,即N为三角锥顶点,三个氢是底边三角形的三个顶点。
vsepr模型有5种。
vsepr是一个用来预测单个共价分子形态的化学模型。
理论通过计算中心原子的价层电子数和配位数来预测分子的几何构型,并构建一个合理的路易斯结构式来表示分子中所有键和孤对电子的位置。
价层电子对互斥理论常用AXE方法计算分子构型。
这种方法也叫ABE,其中A代表中心原子,X或B代表配位原子,E代表孤电子对。
一个分子的形状不但受配位原子影响,也受孤对电子影响。
氨分子中心原子杂化类型与甲烷相同,分子中有四个电子云密集区,电子云分布依然呈四面体。
价电子对互斥理论(VSEPR )与分子几何构型(原载《结构化学问题选讲》,杨宗璐等编,科学出版社2000年)多原子分子的结构比双原子分子要复杂得多,因此一般需要用一组键长和键角的数据来表征其几何构型.原则上可以通过越来越多的计算方案来求解波动方程,得到所需的结合能、平衡几何构型和电荷密度.另一方面,针对大量的复杂分子,人们总是力图采用简化的模型和图象来推理和总结多原子分子中电子行为的规律.价电子对互斥理论(VSEPR )正是这样一种简明、直观、可广泛预测许多简单多原子分子结构的一种方法.价电子对互斥理论(VSEPR )实际上是建立在定域模型基础上的静电理论.按照定域键模型,分子中的电子可划分为:内层电子、孤对电子及成键电子(价电子)等独立组份.分子的能量则与这些独立组份能量及它们的相互作用有关.通过核间距的调整使键长和键角的相互适应,产生了能量最低的几何结构.此外,价电子的分布又受到Pauli 不相容原理和静电库仑作用的支配,除了要求分子中的电子尽量配对外,为使体系电子云分布具有能量最低值,还要求已配对的电子之间彼此尽可能远离,以降低库仑排斥作用.以ALmEn 代表多原子分子,其中A 为中心原子,L 为配位原子,E 则为A 原子价层上的孤对电子对,m 为价层总电子对数P,则可借上述价电子互斥理论提出判断分子几何构型的以下规则:n +1.一定数目的价电子对必定与一定的几何构型相联系.假定价电子对的中心与原子A的距离都是R,为使彼此间斥力最小,价电子对等距离地排布在以R为半径的球面上,形成规则的多面体.根据立体几何的知识,当P为2时,呈直线形(键角为180o);P为3 时呈平面三角形(键角为120o);P为4时呈四面体形(键角为10928′o );P为5时呈三角双锥形;P为6时呈八面体形;P为7 时则呈五角双锥形等.2. 价电子对互斥理论将分子的共价双键或三重键均视为一个电子对来计算.由于多重键中的电子对数多,占据的空间比一个单键电子对大,它对其它单键电子对的排斥作用较强,使分子中含多重键的键角变大,不同键电子对之间排斥作用的大小顺序为三键排斥>双键排斥>单键排斥显然,多重键的存在会影响分子的几何构型.例如 X 2C=0 型分子属于三角形构型,各键角标准值应为120o,不含双键的键角受到前者的影响应小于120o .具体实例见表1.表1 键角的比较X2C=0 ∠XCO ∠XCXF2C=0 123.20112.50Cl2C=0 124.30111.30H2C=0 1210118.00(NH2)2 C =0 1210118.00X2C=CX2∠XCX ∠XCCH2C=CH2116.60121.70(CH3)2C=CH2109012503.用于推测分子结构时,不能忽略孤对电子和成键电子的区别.因为孤对电子对比键电子对更集中于原子核附近,因而增加了排斥能.此外,成键电子对于两个原子核的吸引,电子云显得不如孤对电子的“肥大”,对邻近电子对的斥力也小.孤对电子与键对电子间的排斥强度符合以下排序:孤对/孤对>孤对/键对>键对/键对.一般情况下,由于孤对与键对的不同取向可形成一组异构构型,以上的排斥作用顺序可以帮助辨认能量最低的稳定构型.当某个构型中孤对与孤对的交角小于或等于90o,则必定是不稳定构型.例如,ICl4-的6对价电子对指向正八面体6个顶点,由于只有二对孤对电子,故可形成两种不同的异构构型(见图1).在平面正方形的构型中,两对孤对电子相距最远,应为稳定构型.又如,在SF4,ClF3和IF2-的价电子层中,价电子对数P均为5,但孤对电子对数分别为1、2、3.根据价电子对互斥理论,孤对电子对应选择赤道方向的位置,这样可使与孤对电子对互成90o相互作用的键对数目最少.从图2可知,在它们各自的最稳定构型中,孤对电子对均处于三角平面内.4. 配位原子的电负性增大或中心原子电负性减小,也会使键角偏离标准值.端原子电负性增加时,共享电子对将偏向配位体,从而减少成键电子对之间的斥力,键角的度数随之减小.例如OF2的键角(103.2o)比OH2的键角(104.5o)要小.NF3的键角(102o)比NH3的键角(107.3o)也要小.此外,中心原子的半径增大使与端原子之间的键长增加,减小键电子对之间的排斥力,使键角缩小.实例参见表2.表2 键角的比较分子式 键角 分子式 键角NH3107.30H2O 104.50PH393.30H2S 92.20AsH391.80H2Se 91.00SbH391.30H2Te 89.005.价电子对的相邻电子对越多,所受斥力就越大,距离原子核也越远.当配位数为5和7时,分子呈三角双锥和五角双锥构型,这时主轴上两对电子受到的斥力较大,因而键长较长.例如PCl5分子中,垂直方向的键长为219pm,水平方向键长为204pm,见图3.价电子对互斥理论能够广泛地用于定性预测各类ABn型分子的几何构型,解释键长和键角变化,偏离标准值的规律性,但也有少数化合物的推测出现例外.例如BaI2,SrCl2都是弯曲形构型而非预计的直线性型.此外,对过渡金属化合物几何构型的判断也有一定的局限性.实际上,应用价电子对互斥理论的分子体系,都有一个共同的特点,即分子中所有电子都是成对的.如果分子中有未成对的电子,则不能简单地以此方法来推测分子的几何构型.对于不具有半满或全满d轨道的过渡元素,由于d轨道上电子分布不对称,将使分子形状不规则化,无法用价电子对互斥理论作出判断,因而配位场理论则能说明得更好.价电子对互斥理论被看成是杂化轨道理论简化了的方法.而它相当于只考虑了中心原子利用杂化轨道成键后,各电子对之间的相互排斥,因而只能作出大致的定性说明.而杂化轨道理论则还考虑了整个的杂化过程,并可得出定量的结果,如计算键角等.。
1940年,西奇威克(Sidgwick)等在总结实验事实的基础上提出了一种简单的模型,用于预测简单分子或离子的立体结构。
六十年代初,吉列斯比(RJ.Gillespie)和尼霍尔姆(Nyholm)等发展了这一模型。
因该模型思想方法质朴浅显,在预见分子结构方面简单易行,而成为大学基础化学的基本教学内容,并于新一轮课程改革中引入高中化学教学。
这就是价层电子对互斥模型(Valence Shell Electron Pair Repulsion),常以其英文的缩写形式VSEPR来表示。
1、来自生活中的一个游戏现象吹气球是大家熟悉的生活游戏,如果将每个气球吹成一样大小,将其中的两个通过吹气口系在一起,你会发现这两个气球自然成一直线,再向其中加入一个气球并通过吹气口系在一起,你会发现这三个气球均匀地分开成正三角形分布。
依次再向其中加入一个气球并通过吹气口系在一起,你会有什么预期?你会发现结果与你的预期如此地吻合:四个大小相同的气球成正四面体分布,五个大小相同的气球成三角双锥分布,六个大小相同的气球成正八面体分布。
见图:我们很容易从这一游戏现象受到启迪:当物体所占空间因素相同时,它们彼此趋向均匀分布。
这一规律在自然界乃至人类社会生活中并不鲜见,我们不难找到类似的和接近的例子。
2、VSEPR模型要点VSEPR模型认为,分子的几何构型总是采取电子对排斥作用最小的那种结构。
因为这样可使体系的能量最低,中心原子价层的电子对总是按照最合适的空间方式进行分布。
见下表。
电子对的空间分布电子对数空间分布几何构型2 直线3 在角形4 四面体5 三角双锥6 八面体VSEPR模型简朴通俗,应用简单易行,显现了它的独特魅力并引人入胜。
3、VSEPR模型判别分子构型的基本程序中心原子的价层如果没有孤电子对,那么每一个电子对就代表一个共价键,此时电子对的空间分布就是分子的几何构型。
例如,BeCl2分子中Be原子的两个价电子分别与两个Cl原子形成的两个共价键,没有孤电子对,故它是直线型结构。
又如CH4分子中的C原子价层有四个电子对,这四个价电子对代表了四条C-H 健,C原子价层无孤电子对,故CH4属四面体结构。
如果中心原子的价层存在孤电子对时,则应先考虑不同电子对之间的斥力后,再确定分子的构型。
不同电子对间斥力的大小的顺序是:孤电子对-孤电子对>孤电子对-键电子对>键电子对-键电子对。
价层电子对互斥模型是根据中心原子周围价层电子对的数目,确定价层电子对在中心原子周围的理想排布,然后再根据价层电子对间斥力的大小,以体系的排斥能最小为原则来确定分子的几何构型。
4、价层电子对和孤电子对的确定用通式AX n L m来表示所有只含一个中心原子的分子或离子的组成,式中A表示中心原子,X表示配位原子(也叫端基原子),下标n表示配位原子的个数,L表示中心原子上的孤电子对,下标m是电子对数。
已知分子或离子的组成和原子的排列顺序时,m值可用下式确定:例如:分子或离子SO2SO3SO32-SO42-NO2+ m 1 0 1 0 0注:有时计算出来的m值不是整数,如NO2,m=0.5,这时应当作m=1来对待,因为单电子也要占据一个孤对电子轨道。
通式AX n L m里的(n+m)的数目称为价层电子对数,令n+m=z,则可将通式改写成另一种通式AY z。
因此,z 的数目决定了一个分子或离子中的价层电子对在空间的分布,由此可以画出VSEPR理想模型。
值得一提的是,这里的价层电子对的“对”未必就是二个电子,事实上一个价层电子对表示一个成键区或表示一个空间占位,这就是如果出现有奇电子(有一个成单电子)或重键,可把这个单电子或重键当作电子对来看待的原因。
5、应用VSEPR模型中的“8n+2m”规则确定孤电子对用VSEPR判断分子构型,困难就在于中心原子周围有没有孤电子对。
一种更简便的方法——(8n+2m)较好地解决了这一困惑。
设中心原子为A,配位原子为X,孤电子对为L,再设配位原子数为n,孤电子对数为m,则分子式可为AX n L m。
若组成分子的元素都是主族元素,整个分子的价电子总数为V,则V与n、m有如下关系:V=8n+2m m=(V-8n)/2例如,三氧化硫分子,价电子总数为:V=6+6×3=24,m=(V-8×3)/2=(24-8×3)/2=0可知S原子价层无孤电子对,故三氧化硫是平面三角形结构。
又如,五氯化磷分子的价电子总数:V=5+7×5=40,m=(V-8×5)/2=(40-8×5)/2=0P原子价层无孤电子对,故五氯化磷为三角双锥结构。
再如硝酸根的价电子总数为(离子的电荷计入总价电子数):V=5+6×3+1=24,m=(V-8×3)12=(24-8×3)12=0N原子价层无孤电子对,故硝酸根的结构是平面三角形。
亚硝酸根的价电子总数为:V=5+6×2+1=18,m=(V-8×2)/2=(18-8×2)12=1可知氮原子价层有一个孤电子对,故亚硝酸根为V型结构。
通过上述诸例可以看出V=8n+2m是以“八隅体”结构为基础的。
所以,本规则主要是适合主族元素的化合物,若配位原子是氢原子时,应改为V=2n+2m,因为氢原子仅需两个电子就可达稳定结构。
6、根据价层电子对斥力最小原则确定分子或离子的实际几何构型对于含有5个及5个以上价层电子对、其中并含有孤电子对的分子或离子,如何根据价层电子对斥力最小原则判断其实际构型,是VSEPR应用的又一难点。
例如,SF4属于AX4L1=AY5,其VSEPR理想模型为三角双锥体,排除孤对电子的分子立体结构(由于孤对电子的位置不同)有两种可能的模型:哪一种结构更合理呢?价层电子对之间的斥力分别有90°、120°、180°三种方向角,最小方向角的斥力是决定分子几何构型的主要因素。
下表为90°方向角斥力分析:作用对数目90°方向角斥力I II孤对电子-孤对电子0 0孤对电子-成键电子对 3 2成键电子对-成键电子对 3 4故预测其分子几何构型是II。
再如,ClF3属AX3L2=AY5,价层电子对理想模型为三角双锥型,其分子几何构型可能有以下三种:下表为90°方向角斥力分析:作用对数目90°方向角斥力I II III孤对电子-孤对电子无 1 无孤对电子-成键电子对 6 3 4成键电子对-成键电子对无 3 2故预测其分子几何构型是III,即“T”形。
由以上两例可知,按斥力大小的顺序:孤电子对-孤电子对>孤电子对>键电子对>键电子对-键电子对,只要最小方向角斥力最小,即得偏离理想模型发生“畸变”的实际分子或离子几何构型。
据此,可得以下AX n L m排布图:中心原子价电子对数成键电子对数中心原子孤电子对数微粒空间构型实例2 2 0 CO2,BeCl2,HgCl2 33 0 BF3,SO32 1 SnCl2,SO2,O34 4 0 CH4,NH4+ 3 1 NH3,PCl3 2 2 H2O,OF2,ClO25 5 0 PCl5 4 1 SF4 3 2 BrF32 3 XeF2,I3-6 6 0 SF65 1 IF5,XeOF4 4 2 XeF47、价层电子对斥力作用对键角影响的定性解释键角是描述分子几何结构的重要参数,键角大小是价层电子对斥力作用的综合体现。
由于键合电子对受到左右两端带正电原子核的吸引,而孤对电子对只受到一端原子核吸引,相比之下,孤对电子对较“胖”,占据较大的空间,而键合电子对较“瘦”,占据较小的空间。
这样就解释了斥力大小的顺序:孤电子对-孤电子对>孤电子对-键电子对>键电子对-键电子对。
如:CH4、NH3、H2O中的键角∠HAH 分别为109.5°、107.3°、104.5°。
类似地,重键较单键占据较大的空间,故有斥力大小的顺序:t-t>t-d>d-d>d-s>s-s(t-叁键,d-双键,s-单键) 又如,SO2Cl2分子属AX4L0=AY4,因S=O键是双键,S-Cl键是单键,据顺序有:∠OSO>109°28''''∠ClSCl<∠OSCl<109°28''''。
此外,键的极性对键角也有影响。
中心原子电负性较大,成键电子对将偏向中心原子,成键电子对之间斥力增大,键角增大,如:NH3、PH3、AsH54c分子中的键角(∠HAH)依次为107°、93.08°、91.8°;配位原子电负性较大,成键电子对将偏离中心原子,成键电子对之间斥力减小,键角减小,如:H2O、OF2分子中的键角(AOA)依次为104.5°、102°。
据此,可解释下列键角变化:NO2+、NO2、NO2-键角(∠ONO)依次为180°、134.3°、115.4°。
价层电子对互斥模型是一个定性模型,与杂化轨道理论相比,它只能对分子的空间构型作定性的描述,而不能对分子的成键原理、键的稳定性做出相应的说明。
但该模型抓住了价层电子对间斥力的大小比较,因此它的很多预测有着相当的正确性。
但由于模型较简单,用来解释某些分子的空间构型时却有困难,例如过渡元素配离子的空间构型,用价层电子对互斥模型就得不到正确的解释。