实习指南实验三、四: 亚硝酸盐中毒复制和解救;亚硝酸盐定性和定量分析参考Word
- 格式:doc
- 大小:32.00 KB
- 文档页数:4

急性亚硝酸盐中毒治疗方法及效果评价急性亚硝酸盐中毒是一种由于摄入过量亚硝酸盐所引起的急性中毒症状,严重的时候可以危及生命。
亚硝酸盐是一种常见的化学物质,在食品加工和工业生产中被广泛使用。
过量的亚硝酸盐摄入会对人体健康造成严重威胁。
一旦出现中毒症状,及时采取有效的治疗方法至关重要。
一、急性亚硝酸盐中毒的症状急性亚硝酸盐中毒的症状多样,包括头痛、头晕、恶心、呕吐、心悸、呼吸困难、低血压、窒息等。
中毒程度的严重程度取决于摄入的亚硝酸盐量和中毒时间,严重的中毒症状可能导致神经系统和循环系统的损害,甚至危及生命。
一旦发现中毒症状,应立即就医进行治疗。
1. 医院治疗急性亚硝酸盐中毒患者需要尽快送往医院进行治疗。
在医院,医生会根据患者的症状和体征进行全面的评估,采取相应的处理措施。
通常情况下,治疗方法包括:(1)洗胃或促进排泄对于急性亚硝酸盐中毒患者,洗胃是一种常见的治疗方法。
医生会通过口服给予大量的清水或生理盐水来帮助患者清洗胃部,以减少亚硝酸盐对胃黏膜的刺激和损害。
还可以采用促进排泄的方法,如使用利尿剂或强制利尿,以帮助患者尽快排出体内过量的亚硝酸盐。
(2)吸氧治疗急性亚硝酸盐中毒患者常常出现呼吸困难的症状,需要及时给予吸氧治疗,以保持呼吸道通畅,维持机体的氧供需平衡。
(3)抗中毒治疗在医院治疗过程中,医生还会根据患者的具体情况给予抗中毒药物治疗,如亚硝酸盐的拮抗剂硫代硫酸钠等,以减轻和控制中毒症状。
2. 对症治疗除了医院治疗外,患者还需要进行一些对症治疗,如:(1)维持生命体征稳定急性亚硝酸盐中毒患者通常需要维持生命体征的稳定,包括监测血压、心率、呼吸等生命体征指标,及时处理并预防因中毒引起的心脏、呼吸系统等多系统功能障碍。
(2)预防并处理并发症急性亚硝酸盐中毒患者还需要预防并处理相关的并发症,如低血压、心律失常、呼吸衰竭等。
急性亚硝酸盐中毒的治疗效果主要依赖于早期发现和及时处理。
在医院治疗和对症治疗的过程中,医生需要密切关注患者的病情变化,并及时调整治疗方案和药物使用,以确保患者能够尽快恢复健康。

亚硝酸盐的测定实验报告实验目的,通过本实验,掌握亚硝酸盐的定性和定量分析方法,以及相关实验操作技能。
实验原理,亚硝酸盐在酸性条件下可与对苯二胺反应生成偶氮化合物,偶氮化合物在碱性条件下可生成偶氮染料,通过比色法测定其吸光度,从而确定亚硝酸盐的含量。
实验仪器,分光光度计、移液管、比色皿、恒温水浴器等。
实验步骤:1. 取适量水样置于锥形瓶中,加入适量醋酸钠使水样呈酸性。
2. 取适量对苯二胺溶液,加入醋酸钠水样中,摇匀。
3. 加入碱液,形成偶氮染料。
4. 将偶氮染料转移至比色皿中,用分光光度计测定吸光度。
5. 根据标准曲线计算亚硝酸盐的含量。
实验结果:实验组测得吸光度值如下,0.23、0.25、0.22、0.24。
标准曲线方程为,y=0.5x+0.02,相关系数R²=0.99。
计算得到水样中亚硝酸盐的含量分别为,0.45mg/L、0.50mg/L、0.44mg/L、0.48mg/L。
实验结论,通过本实验,成功测定了水样中亚硝酸盐的含量,实验结果准确可靠。
实验中遇到的问题及解决方法:1. 实验中对苯二胺与水样混合不均匀,导致反应不完全。
解决方法,加大搅拌时间,确保充分混合。
2. 实验中偶氮染料转移至比色皿时有波动,影响吸光度测定。
解决方法,尽量避免振荡,确保稳定吸光度测定。
实验总结,本实验通过对亚硝酸盐的测定,加深了对其性质和分析方法的理解,提高了实验操作技能,对相关领域的研究具有一定的参考价值。
参考文献,《分析化学实验》第三版,XXX出版社。
以上为亚硝酸盐的测定实验报告内容,希望对您有所帮助。

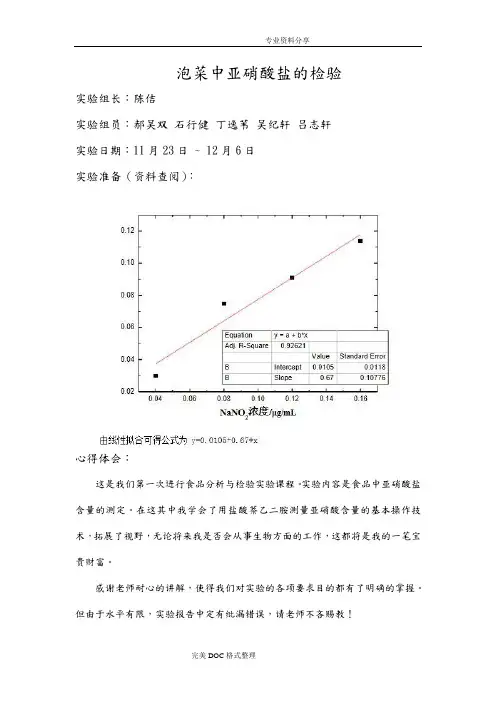
泡菜中亚硝酸盐的检验实验组长:陈佶实验组员:郝吴双石行健丁逸苇吴纪轩吕志轩实验日期:11月23日 ~ 12月6日实验准备(资料查阅):心得体会:这是我们第一次进行食品分析与检验实验课程。
实验内容是食品中亚硝酸盐含量的测定。
在这其中我学会了用盐酸萘乙二胺测量亚硝酸含量的基本操作技术,拓展了视野,无论将来我是否会从事生物方面的工作,这都将是我的一笔宝贵财富。
感谢老师耐心的讲解,使得我们对实验的各项要求目的都有了明确的掌握。
但由于水平有限,实验报告中定有纰漏错误,请老师不吝赐教!一、前言“亚硝酸盐”这一名词对我们来说并不陌生,这是一类无机化合物的总称。
主要指亚硝酸钠,这是一种白色至淡黄色粉末或颗粒状,味微咸,易溶于水。
其外观及滋味都与食盐相似,并在工业、建筑业中广为使用,肉类制品中也允许作为发色剂限量使用。
由亚硝酸盐引起食物中毒的机率较高。
食入0.3~0.5克的亚硝酸盐即可引起中毒甚至死亡。
我们通过实验测定了泡菜中不同时期的亚硝酸盐的含量,这不仅是一次美妙的实践,更为我们的生活提供了指南,让我真真正正的接触到了这个平时只出现在报道上的奇妙物质。
二、实验原理泡菜的制作离不开乳酸菌,乳酸菌是厌氧细菌,在无氧的情况下,将葡萄糖分解成乳酸。
这其中也生成了一定量的的亚硝酸盐。
在盐酸酸化条件下,亚硝酸盐与对氨基苯磺酸发生重氮化反应后,与N-1-萘基乙二胺盐酸盐结合形成玫瑰色染料。
将显色反应后的样品与已知浓度的标准液进行目测比较,可以大致估算出泡菜中亚硝酸盐的含量。
三、设备及试剂泡菜坛、蔬菜、三角瓶、量筒、烧杯、pH试纸、玻璃棒、微量可调移液器、试管、亚硝酸盐含量的测定试剂盒。
四、实验※泡菜制作实验准备:泡菜坛子一个、高粱白酒、花椒、辣椒、大料、冰糖、盐。
具体制作方法如下:(1)各种菜(萝卜、白菜等)洗净并切成3~4cm长的小块。
(2)按照清水与盐的质量比4:1的比例配制盐水,将盐水煮沸冷却。
(3)将经过预处理的新鲜蔬菜混合均匀,装入泡菜坛内,使盐水没过全部菜料,盖好坛盖。

亚硝酸盐的中毒与解救(1)
亚硝酸盐是一种广泛存在于环境中的化学物质。
它可以在自然界中的硝化反应中形成,或者人类活动中的化学反应中释放出来。
亚硝酸盐在化肥、食品、医药等领域中都有广泛的应用。
但是,它也是一种有害物质。
亚硝酸盐中毒是一种常见的中毒现象,特别是在饮食和工作的环境中。
如何对亚硝酸盐的中毒进行解救,是一个需要掌握的重要技能。
一、亚硝酸盐中毒的症状
1.轻度中毒:头痛、眩晕、乏力、恶心、呕吐、食欲不振等。
2.中度中毒:上述症状加重,出现中毒性休克、低血压、心动过速、呼吸困难等。
3.重度中毒:上述症状更加严重,出现神经系统损伤,如口唇、指甲床发绀,惊厥、昏迷等。
二、亚硝酸盐中毒的原因
1.进食含有亚硝酸盐的食物,如盐腌菜、烧烤食品等。
2.长期接触含有亚硝酸盐的环境,如化肥厂、农药生产厂、染料厂等工作场所。
三、亚硝酸盐中毒的解救方法
1.中毒者应立即停止进食含有亚硝酸盐的食物,远离工作场所。
2.及时送医院治疗,针对中毒程度采取不同的治疗方法。
如轻度中毒者可以采取胃洗、吸氧等方法进行解毒;中度中毒者需要注射解毒药物、输液等治疗;重度中毒者需要紧急进行氧疗、呼吸机辅助等治疗措施。
3.保持患者清醒,鼓励患者多饮水。
4.预防亚硝酸盐中毒的发生,减少接触有害环境,避免食用过量的含亚硝酸盐的食物。
总之,亚硝酸盐中毒是一种常见的中毒现象,对人体健康造成了严重的威胁。
在发生中毒时应及时采取解毒措施,尽量避免给患者带来更严重的伤害。
未发生中毒时要采取预防措施,减少接触有害环境和食用过多的含亚硝酸盐的食物。

一、实训目的本次实训旨在通过实验操作,使学生掌握亚硝酸盐的测定方法,了解亚硝酸盐在食品中的存在形式及其对人体健康的影响,提高学生的实验技能和数据分析能力。
二、实训时间2023年10月25日三、实训地点化学实验室四、实训仪器与试剂1. 仪器:- 高速离心机- 分光光度计- 电子天平- 磁力搅拌器- 容量瓶(100mL、50mL)- 试管- 移液管(1mL、10mL)2. 试剂:- 亚硝酸钠标准溶液- 对氨基苯磺酸溶液- N-1-萘基乙二胺盐酸盐溶液- 硫酸溶液- 氨水- 食品样品五、实验原理亚硝酸盐在食品中主要存在于腌制肉类、鱼类等加工食品中,其含量对人体健康有重要影响。
本实验采用比色法测定食品中亚硝酸盐的含量。
其原理是:在酸性条件下,亚硝酸盐与对氨基苯磺酸发生重氮化反应,生成的重氮盐与N-1-萘基乙二胺盐酸盐结合形成紫红色偶氮染料,通过测定吸光度,可以计算出亚硝酸盐的含量。
六、实验步骤1. 样品处理:- 称取适量的食品样品,加入适量的硫酸溶液,用高速离心机离心分离。
- 取上清液备用。
2. 标准曲线的绘制:- 取一系列不同浓度的亚硝酸钠标准溶液,按照实验步骤进行操作。
- 测定吸光度,以亚硝酸钠浓度(mg/L)为横坐标,吸光度为纵坐标,绘制标准曲线。
3. 样品测定:- 按照实验步骤,对处理后的样品进行测定。
- 测定吸光度。
4. 结果计算:- 根据标准曲线,计算出样品中亚硝酸盐的含量。
七、实验结果与分析1. 标准曲线:- 通过绘制标准曲线,得出线性回归方程:y = 0.0486x + 0.0013,R² =0.9969。
2. 样品测定结果:- 根据实验结果,样品中亚硝酸盐的含量为2.5mg/kg。
3. 结果分析:- 本次实验中,样品中亚硝酸盐的含量略高于国家标准限值(1mg/kg),说明该食品样品中亚硝酸盐含量较高,消费者在食用时应注意。
八、实验总结1. 通过本次实训,我们掌握了亚硝酸盐的测定方法,了解了亚硝酸盐在食品中的存在形式及其对人体健康的影响。

一、实验目的本实验旨在学习亚硝酸盐的测定方法,了解亚硝酸盐在食品中的存在及其对人体健康的影响。
通过实验,掌握亚硝酸盐的提取、分离和定量分析方法,提高对食品中亚硝酸盐含量的检测能力。
二、实验原理亚硝酸盐(NO2-)是一种常见的食品添加剂,广泛应用于肉制品的加工中,具有发色、防腐和抗微生物作用。
然而,过量的亚硝酸盐摄入对人体健康有害,可能导致急性中毒、慢性疾病甚至癌症。
因此,对食品中亚硝酸盐含量的检测具有重要意义。
本实验采用盐酸萘乙二胺法测定亚硝酸盐含量。
该方法基于亚硝酸盐与对氨基苯磺酸在酸性条件下发生重氮化反应,生成重氮盐,再与N-1-萘基乙二胺盐酸盐偶合形成玫瑰红色染料。
通过比色法测定染料的吸光度,可以计算出样品中亚硝酸盐的含量。
三、实验材料与仪器1. 实验材料:- 火腿肠样品- 试剂:对氨基苯磺酸、N-1-萘基乙二胺盐酸盐、盐酸、亚硝酸钠标准溶液等- 仪器:酸度计、分光光度计、离心机、移液器、容量瓶、试管等2. 实验步骤:1. 样品处理:将火腿肠样品剪碎,称取适量,加入蒸馏水溶解,搅拌均匀。
2. 提取:将样品溶液用酸度计调至pH 2.0,加入适量的亚铁氰化钾和乙酸锌,充分混合,静置30分钟,使蛋白质沉淀。
3. 分离:将上层清液转移至离心管中,离心分离蛋白质沉淀。
4. 测定:取一定量的上层清液,加入对氨基苯磺酸和N-1-萘基乙二胺盐酸盐,充分混合,静置15分钟,使染料形成。
5. 比色:用分光光度计测定染料的吸光度,与标准曲线比较,计算出样品中亚硝酸盐的含量。
四、实验结果与分析1. 标准曲线绘制:根据亚硝酸钠标准溶液的浓度和吸光度,绘制标准曲线。
2. 样品测定:对火腿肠样品进行测定,得到样品中亚硝酸盐的吸光度。
3. 结果计算:根据标准曲线和样品吸光度,计算出样品中亚硝酸盐的含量。
五、实验讨论1. 实验过程中,酸度对亚硝酸盐的测定结果有较大影响。
实验过程中应严格控制酸度,确保测定结果的准确性。
2. 亚铁氰化钾和乙酸锌在实验中起到沉淀蛋白质和除去脂肪的作用,提高实验的灵敏度。

亚硝酸盐的中毒与解救-V1
亚硝酸盐是一种常见的食品添加剂,在加工腌制食品时会使用到。
但是,亚硝酸盐过量摄入会导致中毒,甚至对健康造成严重威胁。
因此,了解亚硝酸盐的中毒症状和解救方法显得尤为重要。
下面将详细介绍亚硝酸盐中毒的发生原因、症状及解救方法。
一、亚硝酸盐中毒的发生原因
1. 摄入过多的含亚硝酸盐的食品或饮料,如腌制肉类、加工肉制品等。
2. 不恰当的储存方式。
亚硝酸盐在高温、潮湿的环境下易于分解,释
放出亚硝胺等有害物质。
3. 长时间吸入亚硝酸盐的蒸气,如工业生产过程中。
二、亚硝酸盐中毒的症状
1. 肠胃道反应:恶心、呕吐、腹痛、腹泻等。
2. 神经系统反应:头痛、头晕、视力模糊、心悸等。
3. 呼吸系统反应:气短、气喘、呼吸困难等。
4. 其他症状:发热、虚弱、抽搐等。
三、亚硝酸盐中毒的解救方法
1. 立即停止摄入亚硝酸盐。
2. 给予充足的清洁水,促进肾功能,加速亚硝酸盐的排泄。
3. 白蛋白、鲨肝油等富含维生素C的食物可有一定的解毒效果。
4. 严重中毒情况下要及时就医,进行相应的治疗。
总之,亚硝酸盐中毒虽然常见,但只要我们注意饮食卫生、储存方式
以及避免长时间接触含亚硝酸盐的环境,还是很容易避免中毒的发生。
一旦出现中毒症状,应该及时采取解救措施,避免症状加重。

一、实训背景亚硝酸盐是一种常见的食品添加剂,广泛应用于肉类、水产、糕点等食品的生产过程中。
然而,过量摄入亚硝酸盐对人体健康具有潜在危害。
为了提高食品生产过程中的安全性,本实训旨在通过对亚硝酸盐的检测、分析及安全性评价,为食品生产提供科学依据。
二、实训目的1. 掌握亚硝酸盐的检测方法;2. 了解亚硝酸盐对人体健康的危害;3. 提高食品生产过程中的安全性意识。
三、实训内容1. 亚硝酸盐的检测(1)原理亚硝酸盐在酸性条件下与对氨基苯磺酸发生重氮化反应,生成重氮盐,再与N-1-萘基乙二胺盐酸盐结合,形成紫红色偶氮化合物,通过比色法测定其含量。
(2)仪器与试剂仪器:紫外可见分光光度计、酸度计、电子天平、恒温水浴锅等。
试剂:亚硝酸钠标准溶液、对氨基苯磺酸、N-1-萘基乙二胺盐酸盐、盐酸、硫酸、无水碳酸钠等。
(3)操作步骤①制备标准曲线:将亚硝酸钠标准溶液稀释成不同浓度的系列溶液,按操作步骤测定吸光度,以吸光度为纵坐标,浓度(mg/L)为横坐标,绘制标准曲线。
②样品测定:准确称取适量样品,加入适量蒸馏水,按照操作步骤测定吸光度,从标准曲线上查得样品中亚硝酸盐的含量。
2. 亚硝酸盐对人体健康的危害亚硝酸盐在人体内可转化为亚硝胺,亚硝胺是一种强致癌物质,长期摄入可能导致癌症。
此外,亚硝酸盐还可能引起以下危害:(1)引起急性中毒:摄入大量亚硝酸盐可导致血压下降、呼吸困难、头痛、头晕等症状。
(2)引起慢性中毒:长期摄入低剂量亚硝酸盐可能导致消化系统、呼吸系统、神经系统等器官的损害。
(3)影响人体铁代谢:亚硝酸盐可抑制血红蛋白的合成,导致贫血。
3. 食品生产过程中的安全性评价(1)合理使用亚硝酸盐:严格按照国家相关标准使用亚硝酸盐,控制使用量,避免过量添加。
(2)加强食品生产过程中的卫生管理:确保食品生产环境的清洁卫生,防止亚硝酸盐的污染。
(3)加强食品质量检测:定期对食品中亚硝酸盐含量进行检测,确保食品质量符合国家标准。

亚硝酸盐中毒及其解救设计者:梁贞萍沈文佳梁伟豪伍永裕陈志淳专业、班别:法医1班一、实验目的:观察亚硝酸盐中毒时的症状及亚甲蓝、高渗葡萄糖对亚硝酸盐中毒的解救方法。
了解法医学鉴定中毒,判定是否中毒,毒物的种类,及中毒性质等问题。
二、立题依据(附参考文献)亚硝酸根离子是一种血液毒,进入机体后将原来含有二价铁的血红蛋白氧化为三价的高铁血红蛋白,使其失去携带氧的能力,从而发生高铁血红蛋白症。
口服纯亚硝酸盐0.2~0.5g可引起中毒,1~2g即可致死。
常见的有亚硝酸钠和亚硝酸钾。
主要用于炸药、染料工业,建筑用防冻剂,食品加工,肉类腌制等。
亚硝酸盐最常见的中毒原因为误服。
中毒者口唇、指甲、面颊、耳廓以至全身青紫,发生抽搐、昏厥等缺氧症状。
尸斑为蓝褐色样青紫,血液呈巧克力色,且不凝固。
针对亚硝酸盐的毒理作用,使用还原剂亚甲蓝加高渗葡萄糖。
亚甲蓝是亚硝酸盐中毒的特效解毒剂,能还原高铁血红蛋白,恢复正常输氧功能。
用量以每公斤体重1~2mg计算。
高渗葡萄糖可提高血液渗透压,能增加解毒功能并有短暂利尿作用。
参考文献:[1] 陈灏珠主编. 实用内科学. 第二版. 北京: 人民卫生出版社,1997:56-59 【教材引用格式】[2] 杨明川主编.实用危重病抢救手册. 上海技教育出版社三、实验方案1.实验材料家兔、兔手术台、注射器、肛表、手术刀、手术剪、针头、纱布、2%亚硝酸钠、1%亚甲蓝、20%葡萄糖溶液2.实验分组1、2、3组用药亚甲蓝和高渗葡萄糖 3、4、5组用药亚甲蓝 6组不做任何处理3.观察指标•眼结膜、鼻唇黏膜、耳血管颜色•记录体温、心率、血压体温的测定一般采用肛门测温法,测温时,用左臂夹住兔体,左手提起尾巴,右手将体温表插入肛门,深度3.5-5厘米,保持3-5分钟。
家兔的正常体温为38.5-39.5℃。
可视粘膜检查家兔的可视粘膜包括眼结膜、鼻腔粘膜、口腔粘膜和阴道粘膜。
正常时呈粉红色。
检查眼结膜时,可用左手固定头部,右手食、拇指拨开眼睑即可观察。

一起因亚硝酸盐引起的食物中毒的实验室分析发表时间:2012-09-27T15:03:10.810Z 来源:《医药前沿》2012年第9期供稿作者:高静[导读] 注: × 表示将5.00g样品处理后定容至500ml,取此稀释液1ml,定容至100ml,取25ml进行测定。
高静(重庆市永川区疾病预防控制中心重庆 402160)【摘要】目的:分析一起食物中毒原因。
方法:用亚硝酸盐检测试纸和盐酸奈乙二胺法对所采样品进行定性和定量分析。
结果:在所采4件剩余食物和呕吐物中均检出大量亚硝酸盐。
结论:患者因食用含有大量亚硝酸盐的食物导致中毒,提示实验室应随时做好各项应急检验准备工作,卫生监督部门对食品加工企业加强监管,做好企业从业人员相关知识的培训和宣传,严格按照国家标准使用食品添加剂,严防食物中毒的发生。
【关键词】亚硝酸盐食物中毒【中图分类号】R155.3+2 【文献标识码】A 【文章编号】2095-1752(2012)09-0370-02 1 流行病学调查1.1事件经过2010年2月11日20时左右,接重庆市第二人民医院电话报告,该院收治的陈桐等5名患者,因头痛、头晕、恶心、呕吐、嘴唇发绀等症状入院治疗,疑似食物中毒引起,我中心立即赶赴现场进行调查并采样。
经调查了解5名患者均食用了本区锦城肺片烧腊店烧腊。
1.2主要临床表现发病急速,潜伏期最短为15min,最长为60min,发病时间比较集中。
特点:共同饮食,相似症状,中毒程度不同;主要症状:头晕、头疼、乏力、心跳加速、恶心、呕吐、腹痛、嘴唇发绀。
其中1人有呕吐物,5人中有1人昏迷伴抽搐,意识不清。
2 实验室检验2.1采集的样品有:卤水500g,剩余卤鸭80g,呕吐物100g,卤鸭脖200g,共4份检样。
2.2定性实验2.2.1检验方法:亚硝酸盐检测试纸2.2.2检验结果:在采集的4份样品中,亚硝酸盐定性实验均为阳性反应。
2.3定量分析2.3.1检验方法:定量实验按照GB/T5009.33-2008《食品中亚硝酸盐与硝酸盐的测定》盐酸奈乙二胺法测定。
亚硝酸盐中毒机理以及急救亚硝酸盐是一种在工业和农业中广泛使用的化学物质,但它也存在着潜在的健康风险。
亚硝酸盐中毒是一种由于体内亚硝酸盐含量过高而引起的急性或慢性中毒。
本文将重点介绍亚硝酸盐中毒的机理以及相关的急救方法。
亚硝酸盐的来源和作用亚硝酸盐可以通过多种途径进入人体,包括食物、饮水和空气等。
在食物中,亚硝酸盐主要存在于加工食品(如腌制肉类和香肠)、含氮肥料施用的农产品和食物添加剂中。
在饮水中,亚硝酸盐可以由自然地下水和人为污染导致。
此外,汽车尾气和工业废气可以释放出大量亚硝酸盐,从而污染空气。
亚硝酸盐在体内可以转化为一氧化氮(NO),后者是一个重要的信号分子,在血管扩张、神经传递和炎症调节等生理过程中发挥重要作用。
然而,当亚硝酸盐摄入过度或暴露于过高浓度时,就会引发亚硝酸盐中毒。
亚硝酸盐中毒机理亚硝酸盐中毒的主要机理是其与人体内的血红蛋白结合,形成亚硝酸血红蛋白(MetHb)。
亚硝酸血红蛋白无法有效地运输氧气到组织和器官,导致氧供应不足。
此外,亚硝酸盐还可以进一步转化为亚硝酸,后者是一种高效的氧化剂,可以与细胞内的生物分子发生反应,导致氧化应激和细胞损伤。
除了直接影响血红蛋白和细胞功能外,亚硝酸盐还可以干扰一些重要的生物化学反应,例如抑制DNA合成和酶活性等。
这些细胞和分子水平的改变进一步加剧了亚硝酸盐中毒的严重性。
亚硝酸盐中毒的症状亚硝酸盐中毒的症状取决于暴露时间、暴露剂量和个体的敏感性等因素。
急性亚硝酸盐中毒的症状包括头痛、恶心、呕吐、腹痛、胃肠道炎症、心悸、脱水和低血压等。
长期慢性暴露于亚硝酸盐的人可能会出现慢性头痛、疲劳、心血管疾病和癌症等症状。
急救方法如果怀疑某人中毒了亚硝酸盐,应立即进行急救。
以下是亚硝酸盐中毒的常见急救方法:1.立即将中毒者转移到通风良好的地方,并迅速将其与可能的亚硝酸盐源隔离。
2.如果中毒者出现呼吸困难或停止呼吸,立即进行人工呼吸或使用自动体外除颤器进行心肺复苏。
实习指南实验三、四:亚硝酸盐中毒复制和解救;亚硝酸盐定性和定量分析实验三亚硝酸盐中毒的复制和解救一、实验目的掌握亚硝酸盐中毒的诊断要点。
了解亚硝酸盐中毒的解毒原理和治疗措施。
二、实验方法教师讲解后、学生分组操作。
三、实验属性和学时验证,3学时。
四、实验材料和器械兔若干只、一次性注射器、胃管、听诊器、体温计、亚硝酸盐钠、美兰、酒精棉球等。
五、实验内容(一)高铁血红蛋白检验1、原理亚硝酸盐(钾)离子,在血液中使血红细胞内正常的低铁血红蛋白(氧化)氧化为异常的高铁血红蛋白(正铁),从而失去携氧作用。
2、方法(1)取血5mL于试管中,在空气中用力振荡15min。
在有高铁血红蛋白的情况下,血液仍保持棕色,健畜则由于血红蛋白与氧结合而变为鲜红色。
(2)取血5mL于试管中,滴加1%氰化钾(钠)溶液数滴,在有高铁血红蛋白的情况下,血液立即变为鲜红色。
(3)血液分光镜检验:取血用水稀释10-20倍后置于分光镜上检验,可在红色区640-650nm波长发现高铁血红蛋白的吸光谱带。
当加入5%氰化钾(钠)溶液数低后,由于氰血蛋白形成,此吸光带立即消失。
但经急救治疗过的家畜,高铁蛋白大部分已被还原,故用此法检验宜早进行。
(二)治疗措施可用特效解毒药甲蓝或甲苯胺兰溶液静脉注射,若与Vc和高渗葡萄糖(亦有较弱的还原作用)溶液合用,则疗效更佳。
1、亚甲蓝又名美蓝,为一种氧化还原剂,是治疗本病的特效药物。
原理小剂量美蓝进入机体,在还原型辅酶Ⅰ脱氢酶的作用下,还原成“白色美蓝”,可使高铁血红蛋白还原为正常的低铁血红蛋白。
在此同时,本身被氧化成美蓝并重又参与反应,但大剂量美蓝进入机体,却养具有氧化作用,反使正常的低铁血红蛋白氧化成高铁血红蛋白。
因此,治疗只宜用小剂量。
反映如下:剂量标准剂量为每公斤体重1-2mg,浓度为1%的酒精生理盐水或水溶液。
给药途径静脉注射或分点肌肉注射。
2、甲苯胺蓝原理同美蓝,但其还原高铁血红蛋白的速度比美蓝快37%。
实验三:亚硝酸盐、有机磷农药中毒与解救一、亚硝酸盐中毒与解救亚硝酸盐中毒是畜禽由于采食富含硝酸盐或亚硝酸盐的饲料,使血红蛋白变性,失去携氧功能,导致组织缺氧的一种急性、亚急性中毒。
临床上以黏膜发绀、血液褐变、呼吸困难、胃肠道炎症为特征。
本病常为急性经过,多发于猪,禽,其次是牛、羊,马和其他动物很少发生。
【实验内容】观察家兔亚硝酸盐中毒的主要症状,同时进行治疗实验。
【实验目的要求】通过对家兔亚硝酸盐中毒的临床观察和治疗,掌握亚硝酸盐中毒的发病原因,中毒后的症状,诊断及救治措施。
【实验对象】家兔【实验药品与器材】亚硝酸钠、1%亚甲蓝、针头、注射器【实验步骤】取兔一只,称重,记录呼吸、体温,观察精神状态,眼结膜及耳血管的颜色。
→①组:iv.亚硝酸钠(4%,2-2.5ml/kg)→观察→解救→观察→抽血(用塑料管,不抗凝)②组:PO.亚硝酸钠(4%,4-5ml/kg)→观察→解救→观察→抽血(用塑料管,不抗凝)③组:PO.亚硝酸钠(4%,4-5ml/kg)→观察→不解救→采血(用塑料管,不抗凝)→剖杀→胃内容检测④组:iv.亚硝酸钠(4%,2-2.5ml/kg)→观察→不解救→采血→剖杀→胃内容物检测观察项目:动物的呼吸、眼结膜及耳血管颜色的变化。
当开始出现发绀现象时,检查体温。
胃内容物:观察颜色并用试剂盒检测,观察结果。
血液:观察其性状,血凝时间等。
救治出现典型亚硝酸盐中毒症状后(iv.5min后,PO.30min后),即用1%亚甲蓝按0.2ml/kg.BW静脉注射,观察并记录解救效果。
过半小时后发绀不退或再度出现,应重复用药。
或用有效解毒剂:2倍量的5% VitC + 50%的葡萄糖1-2ml/kg iv.【思考题】1.亚硝酸盐中毒的原因?亚硝酸盐中毒的临床症状?2.亚甲蓝解救亚硝酸盐中毒的机理?二、有机磷中毒与解救有机磷农药中毒是由于接触、吸入或采食了某种有机磷制剂所引致的病理过程,以体内的胆碱酯酶活性受抑制、从而导致神经生理机能的紊乱为特征。
一起亚硝酸盐中毒的实验室检测结果与调查分析发表时间:2013-09-24T17:04:43.497Z 来源:《医药前沿》2013年第26期供稿作者:胡亚奇俎志平毛斐[导读] ⑴相关部门应积极宣传和贯彻食品安全法,加强食品安全监管力度。
⑵胡亚奇俎志平毛斐(许昌市疾病预防控制中心河南许昌 461000)【摘要】目的:对一起亚硝酸盐引起的食物中毒事件进行调查分析。
方法:通过现场调查,临床症状及实验室检验结果进行判断分析。
结果:根据现场调查、患者临床症状及实验室检测,确认为一起亚硝酸盐引起的食物中毒。
结论:发生食物中毒的原因为狗肉加工过程中添加了过量的亚硝酸盐作为发色剂,患者食用后引起食物中毒。
【关键词】亚硝酸盐中毒检测调查【中图分类号】R195 【文献标识码】A 【文章编号】2095-1752(2013)26-0363-01 2012年3月20日,许昌县某乡发生一起食物中毒事件,接到报告后,中心立即组织人员与卫生监督人员一起奔赴现场,根据病人临床表现,现场流行病学调查及实验室检测结果分析,确认是食用亚硝酸盐含量超标的狗肉引起的食物中毒,现将实验室检测与调查结果报告如下:1 流行病学调查就餐者共8人,其中5人在中午就餐后相继出现头晕、恶心、呕吐、口唇青紫、指甲发黑等症状。
对3名未出现症状者进行个案调查,证实其余5人都食用了狗肉。
现将采集患者呕吐物3份,盘中剩余狗肉一份,卤肉摊点狗肉一份,调菜用味精、盐各一份送实验室进行检测。
2 临床表现与治疗本次事件患者5人,3人症状较重。
临床表现与亚硝酸盐中毒较吻合。
送许昌市中心医院,经医务人员积极救治,采取亚甲兰静脉推注,大剂量维生素C静脉滴注、吸氧等对症治疗后,症状均已缓解,无死亡病例。
3 实验室检测3.1 定性检测采集样品参照《常规化学性食物中毒检验与救治手册》[1]中亚硝酸盐定性分析方法进行测定。
结果见表1。
3.2 定量检测采集样品参照《食品卫生检验方法理化部分》[2]GB/T 5009.33-2003盐酸茶乙二胺法进行测定。
实验三亚硝酸盐中毒的复制和解救
一、实验目的
掌握亚硝酸盐中毒的诊断要点。
了解亚硝酸盐中毒的解毒原理和治疗措施。
二、实验方法
教师讲解后、学生分组操作。
三、实验属性和学时
验证,3学时。
四、实验材料和器械
兔若干只、一次性注射器、胃管、听诊器、体温计、亚硝酸盐钠、美兰、酒精棉球等。
五、实验内容
(一)高铁血红蛋白检验
1、原理亚硝酸盐(钾)离子,在血液中使血红细胞内正常的低铁血红蛋白(氧化)氧化为异常的高铁血
红蛋白(正铁),从而失去携氧作用。
2、方法
(1)取血5mL于试管中,在空气中用力振荡15min。
在有高铁血红蛋白的情况下,血液仍保持棕色,健畜则由于血红蛋白与氧结合而变为鲜红色。
(2)取血5mL于试管中,滴加1%氰化钾(钠)溶液数滴,在有高铁血红蛋白的情况下,血液立即变为鲜红色。
(3)血液分光镜检验:取血用水稀释10-20倍后置于分光镜上检验,可在红色区640-650nm波长发现高铁血红蛋白的吸光谱带。
当加入5%氰化钾(钠)溶液数低后,由于氰血蛋白形成,此吸光带立即消失。
但经急救治疗过的家畜,高铁蛋白大部分已被还原,故用此法检验宜早进行。
(二)治疗措施
可用特效解毒药甲蓝或甲苯胺兰溶液静脉注射,若与Vc和高渗葡萄糖(亦有较弱的还原作用)溶液合用,则疗效更佳。
1、亚甲蓝又名美蓝,为一种氧化还原剂,是治疗本病的特效药物。
原理小剂量美蓝进入机体,在还原型辅酶Ⅰ脱氢酶的作用下,还原成“白色美蓝”,可使高铁血红蛋白还原为正常的低铁血红蛋白。
在此同时,本身被氧化成美蓝并重又参与反应,但大剂量美蓝进入机体,却养具有氧化作用,反使正常的低铁血红蛋白氧化成高铁血红蛋白。
因此,治疗只宜用小剂量。
反映如下:剂量标准剂量为每公斤体重1-2mg,浓度为1%的酒精生理盐水或水溶液。
给药途径静脉注射或分点肌肉注射。
2、甲苯胺蓝
原理同美蓝,但其还原高铁血红蛋白的速度比美蓝快37%。
剂量每公斤体重5mg,浓度为5%。
给药途径静脉注射或腹腔注射。
3、维生素C
原理使高铁血红蛋白还原为正常的低铁血红蛋白,而脱氢的Vc又被体内谷胱甘肽还原为Vc,又重新参与高铁血红蛋白的还原过程。
但其作用不及美蓝和甲苯胺蓝迅速、彻底。
故常与美蓝或甲苯胺蓝配合应用。
剂量牛、马0.5—2.0g,猪、羊0.1—0.5g。
(三)亚硝酸盐中毒的复制与解放
复制方法取试验动物(兔)2只,分别称量,并观察记录其呼吸、体温及可视黏膜的颜色,然后,按每公斤体重58—77mg(猪)或100mg(兔)的4%亚硝酸钠溶液静脉注射。
解救待亚硝酸盐中毒症状出现后,一只用亚甲蓝或甲苯胺蓝溶液静脉注射,观察并记录解毒效果。
另一只使其自然发展,死亡后进行剖检,以观察记录病理变化。
六、作业
1、如何用快速简洁的实验室方法诊断动物亚硝酸盐中毒?
2、亚甲蓝的解毒原理是什么?怎么使用?
3、根据各组实验结果分析家兔亚硝酸盐中毒死亡或存活的原因。
实验四亚硝酸盐的定性与定量检验
一、实验目的
熟悉亚硝酸盐中毒的定性检验方法;掌握亚硝酸盐中毒的定量检验方法。
二、实验方法
教师讲解后、学生分组操作。
三、实验属性和学时
验证,3学时。
四、实验材料和器械
可见光分光光度计、半自动生化分析仪、比色管、容量瓶、移液管、移液枪、烧杯、饲料等。
五、实验内容
(一)亚硝酸盐的定性检验
对氨基苯磺酸重氮法(格林氏法)
1、原理亚硝酸盐在酸性溶液中与与对氨基苯磺酸作用生成重氮化合物,然后与α一萘胺偶合生成紫红色
偶氮染料。
2、试剂
(1)对氨基苯磺酸溶液。
取0.5g对氨基苯磺酸溶于150mL12%醋酸溶液中。
贮存于棕色瓶中。
如溶液有颜色,临用时加入少许活性炭加热至80℃并过滤,即可脱色。
(2)α—萘胺溶液。
取α一萘胺0.2g,加水20mL,微热溶解,过滤。
滤液加蒸馏水至100 mL,贮存棕色瓶中。
对有色者可按上法脱色。
3、操作方法
取2mL滤液于小试管中,加对氨基苯磺酸溶液2~3滴。
2~3分钟后,再加入α—萘胺溶液2-3滴。
数分钟后,有亚硝酸盐存在时则出现紫红色,颜色的深浅表示亚硝酸盐含量的多少。
如将试管在70℃水浴中加热数分钟,颜色更明显。
粗略比例如下表。
溶液的颜色NO2 –的含量(毫克/升)
刚刚呈现玫瑰红小于0.01
淡玫瑰色0.01-0.1
玫瑰色0.1-0.2
鲜艳玫瑰色0.2-0.5
深红色或橙黄色大于0.5
格林氏粉法
1、原理同对氨基苯磺酸重氮法(格林氏法)
2、试剂
对氨基苯磺酸 1.0g
α—萘胺0.1g
酒石酸8.9g
研磨均匀,储于棕色广口瓶备用。
3、操作方法取滤液1-2 mL于小试管中,然后加入少许试粉,摇匀,如滤液变紫红色,表明检材中有
亚硝酸盐存在。
联苯胺冰醋酸法
1、原理亚硝酸盐在酸性溶液中,将联苯胺重氮化生成黄色或红棕色颜料。
2、试剂0.1%联苯胺冰醋酸溶液:取0.1g联苯胺溶于10mL冰醋酸中,加蒸馏水稀释至100mL,过滤,
滤液置于棕色瓶中备用。
3、操作方法取对氨基苯磺酸重氮法样品制备液2滴于滤纸或点滴板上,加联苯胺一冰醋酸液2滴,如
出现棕红色则示有亚硝酸盐存在。
二苯胺浓硫酸反应
1、原理由于亚硝酸盐有氧化作用(有浓硫酸存在),可使二苯胺氧化,其氧化产物呈兰色。
2、试剂二苯胺浓硫酸溶液:二苯胺0.1g加100 mL浓硫酸溶解后储存于棕色瓶中。
3、操作方法取滤液1-2滴于点滴板上,加1-2滴二苯胺浓硫酸溶液,立即出现兰色,证明有亚硝酸盐
存在。
注意要点:
1、亚硝酸盐在酸性条件下易分解,如送检不及时,夏天往往在死后第二天就不易检出。
剩余饲料较易获
得阳性结果。
2、格林氏反应十分灵敏,反应很强烈时可以证明亚硝酸盐中毒,反应微弱时,需用灵敏度较小的方法进
行,一般要求两种以上方法都呈现阳性,才能证明亚硝酸盐中毒。
同时需做空白对照,必要时可进行定量检验。
(二)亚硝酸盐的定量检验------α-萘胺比色法
1、原理在微酸性条件下,亚硝酸盐与对氨基苯磺酸作用生成重氮化合物,再与α一萘胺偶合而生成紫黄
色偶氮染料。
颜色强度与亚硝酸盐含量成正比。
2、试剂
(1)α-萘胺溶液:同定性检验对氨基苯磺酸重氮法。
(2)对氨基苯磺酸溶液:同定性检验对氨基苯磺酸重氮法。
(3)亚硝酸钠标准液:准确称取0.1495g亚硝酸钠溶于水中,稀释至100mL。
此液每mL相当于1mgNO2–。
临用时,精确吸取1.00mL,加水稀释至100mL。
此液每毫升则相当手0.01mgNO2–。
(4)醋酸钠缓冲液:取16.4g醋酸钠溶于100mL水中。
3、操作方法
(1)取5-10g样品置研钵中,加少许玻璃砂和少许70℃水,研成粥状。
分次加70℃左右热水提取,将上清液转入100mL容量瓶中。
最后定容至刻度。
(如颜色深,可加少许活性炭脱色),过滤,弃去最初几毫升滤液。
(2)吸取续滤液10mL于25mL比色管中,加水至刻度。
(3)另取25mL比色管7支,依次加入0,0.002,0.005,0.01,0.015,0.020,0.025mgNO2–.,加水稀释至刻度。
(4)于标准管和样品管中分别加入0.05mL醋酸钠缓冲液,对氨基苯磺酸液1mL,α—萘胺溶液1mL,摇匀。
放置10分钟后,以零管作参比,用1cm比色皿于波长525nm处测定吸光度,绘制工作曲线与之比较。
4、.结果计算
A
亚硝酸盐含量(mg/kg)=
M/10
式中:A—样品管中测得含量,μg;M—称取样品量,g 。
六、作业
1、亚硝酸盐定性检验的方法有那些?其原理是什么?各有什么优缺点?
2、在亚硝酸盐可疑样品的定量检测中,要保证结果的准确,应注意那些问题?
(本资料素材和资料部分来自网络,仅供参考。
请预览后才下载,期待您的好评与关注!)。