无菌检查法及其验证(精选)
- 格式:ppt
- 大小:6.04 MB
- 文档页数:85

妥布霉素滴眼液无菌检查法方法验证一、验证目的根据中国药典2010年版(二部)附录XI H 无菌检查法方法验证,对妥布霉素滴眼液无菌检查方法进行验证,确定在设定的条件下能满足该产品的无菌检查需求,保证检验结果的可靠性。
二、供试品妥布霉素滴眼液规格:0.4ml/支。
批号:三、培养基硫乙醇酸盐流体培养基批号:中国药品生物制品检定所改良马丁培养基批号:中国药品生物制品检定所营养肉汤培养基批号:中国药品生物制品检定所改良马丁琼脂培养基批号:中国药品生物制品检定所营养琼脂培养基批号:中国药品生物制品检定所玫瑰红钠琼脂培养基批号:中国药品生物制品检定所营养琼脂对照培养基批号:中国药品生物制品检定所玫瑰红钠琼脂对照培养基批号:中国药品生物制品检定所四、试剂:蛋白胨批号:氯化钠(AR)批号:磷酸二氢钾(AR)批号:磷酸氢二钠(AR)批号:聚山梨酯80 批号:五、仪器HTY-2000A型集菌仪,一次性使用全封闭集菌培养器型号KDGB330批号20100602 均由杭州泰林生物技术设备有限公司。
立式压力蒸汽灭菌器:YXQ-LS-50SII,上海博讯实业有限公司医疗设备厂;霉菌培养箱:MJX-160B-Z型,上海博迅实业有限公司生化培养箱:MJX-160B-Z型,上海博迅实业有限公司电热恒温鼓风干燥箱:GZX-9076 MBE,上海博讯实业有限公司医疗设备厂百级超净工作台:SW-CJ-1F,苏州佳宝净化工程设备有限公司六、冲洗液pH7.0 无菌氯化钠蛋白胨缓冲液,自制,根据《中国药典》2010版二部附录XI H 稀释液,冲洗液配置方法:取磷酸二氢钾3.56g、磷酸氢二钠7.23g、氯化钠4.30g、蛋白胨1.0g,加水1000ml,微热溶解,滤清,分装,灭菌。
灭菌条件:121°C高压蒸汽灭菌20min。
七、缓冲液0.9%无菌氯化钠溶液,自制,根据《中国药典》2010版二部附录XIH 稀释液,冲洗液配置方法:取氯化钠9.0g,加水溶解使成1000ml,过滤,分装,灭菌。

无菌检查方法学验证1. 概述将规定量的供试品按无菌检查法中的薄膜过滤法进行操作,并接种小于100cfu 的试验菌,同时设置阳性对照,按规定温度培养3~5 天,与各相应的阳性对照管比较: 如含供试品各管中的试验菌均生长良好,则供试品的该检验量在该检验条件下无抑菌作用,可按此法进行供试品的无菌检查;如含供试品的任一管中的试验菌生长微弱、缓慢或不生长,则说明供试品的该检验量在该检验条件下有抑菌作用,应采用增加冲洗量或使用中和剂等方法消除供试品的抑菌作用,并再重新进行验证试验。
2. 验证前提条件供试品的选择原则:相同配方,不同规格的制品,选择其中装量最大的制品进行验证。
种类相同,含量不同的制品,选择含量最高的制品进行验证。
照此原则,多规格制品按下表选择供试品进行验证。
3. 验证方法3.1菌液制备3.1.1细菌菌液制备程序①取金黄色葡萄球菌、枯草芽抱杆菌、铜绿假单胞菌的冻干菌种管各一支,分别在无菌操作下打开,以毛细吸管加入适量营养肉汤,轻柔吹吸数次,使菌种融化分散后,吸出滴入营养琼脂斜面上,使均匀分布,置30~35C培养18h~24h。
用接种环取适量第1代培养菌苔,划线接种于营养琼脂培养基斜面上,于30~35C培养18h~24h o 同法操作,培养得第3代培养物。
②取生抱梭菌的冻干菌种管一支,在无菌操作下打开,以毛细吸管加入适量营养肉汤,轻柔吹吸数次,使菌种融化分散后,吸出滴入胃酶肉肝疱斜面上,使均匀分布,置30~35C培养18h~24h o用接种环取适量第1代培养菌苔,划线接种于胃酶肉肝疱斜面上,于30~ 35°C培养18h~24h。
取生抱梭菌的第二代新鲜培养物至硫乙醇酸盐流体培养基中,30~35C培养18h~24h,得第3代培养物。
③分别取金黄色葡萄球菌、枯草芽抱杆菌、铜绿假单胞菌的第3代营养琼脂斜面新鲜培养物,用5.0ml吸管吸取3.0ml~5.0ml稀释液加入斜面试管内,反复吹吸,洗下菌苔。

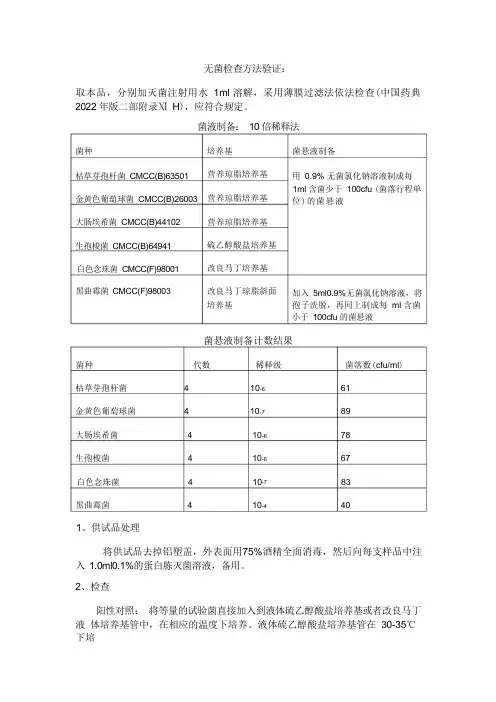
无菌检查方法验证:取本品,分别加灭菌注射用水 1ml 溶解,采用薄膜过滤法依法检查(中国药典 2022 年版二部附录Ⅺ H ),应符合规定。
菌液制备: 10 倍稀释法培养基 营养琼脂培养基营养琼脂培养基营养琼脂培养基硫乙醇酸盐培养基改良马丁培养基改良马丁琼脂斜面 培养基菌悬液制备计数结果菌种 代数 稀释级 菌落数(cfu/ml )枯草芽孢杆菌 4 10-6 61金黄色葡萄球菌 4 10-7 89大肠埃希菌 4 10-6 78生孢梭菌 4 10-6 67白色念珠菌 4 10-7 83黑曲霉菌 4 10-4 401、供试品处理将供试品去掉铝塑盖,外表面用75%酒精全面消毒,然后向每支样品中注 入 1.0ml0.1%的蛋白胨灭菌溶液,备用。
2、检查阳性对照: 将等量的试验菌直接加入到液体硫乙醇酸盐培养基或者改良马丁液 体培养基管中,在相应的温度下培养。
液体硫乙醇酸盐培养基管在 30-35℃下培菌种枯草芽孢杆菌 CMCC(B)63501 金黄色葡萄球菌 CMCC(B)26003 大肠埃希菌 CMCC(B)44102生孢梭菌 CMCC(B)64941白色念珠菌 CMCC(F)98001黑曲霉菌 CMCC(F)98003菌悬液制备用 0.9% 无菌氯化钠溶液制成每 1ml 含菌少于 100cfu (菌落行程单 位)的菌悬液加入 5ml0.9%无菌氯化钠溶液,将 孢子洗脱,再同上制成每 ml 含菌 小于 100cfu 的菌悬液养;改良马丁液体培养基管在23-28℃下培养3-5 天。
观察记录。
阴性对照:将灭菌的液体硫乙醇酸盐培养基或者改良马丁液体培养基管直接放在相应的温度下培养。
液体硫乙醇酸盐培养基管在30-35℃下培养;改良马丁液体培养基管在23-28℃下培养3-5 天。
观察记录。
样品 (薄膜过滤法):每种实验菌取10 支处理好的供试品溶液,将溶液合并后加入制备好的菌悬液1ml,用0.1%的蛋白胨灭菌溶液稀释至100ml,按薄膜过滤法过滤,取出滤膜,将其分为3 等份,分别置于含硫乙醇酸盐流体培养基及改良马丁培养基的容器中,其中一份作为阳性对照用。




文件制修订记录1. 概述:无菌检查法系用于检查药典要求无菌的药品、原料、辅料及其他品种是否无菌的一种方法。
本公司的无菌检查只是针对于灭菌注射用水的无菌检查。
灭菌注射用水灭菌工艺采用121℃30min过度杀菌法,按照2005年版《中国药典》的规定,注射剂的无菌检查应采用薄膜过滤法。
制定的《无菌检查法标准操作规程》(SOP4.14.038-B)应经过验证后,才能批准使用。
2. 验证目的:验证所采用的方法和条件是否适合于供试品的无菌检查。
即确认供试品在该检验量、该检验条件下无抑菌活性或其抑菌活性以被充分消除到可以忽略不计。
3. 验证范围:适用于灭菌注射用水无菌检查法的验证。
4. 验证人员及职责质量部负责该验证方案的起草及组织实施;验证小组负责验证方案的审批;质量部参与验证的实施及监督。
5. 文件准备和培训检查验证所需的各类文件资料,应齐全;相关的文件草案是否已具备。
6.1. 无菌检查室空气净化系统已经过验证并合格,仪器安装完成;仪表量器经过校验合格,且在有效期内。
6.2. 供试品:3批,批号:批号:批号:6.3. 培养基及试剂:6.3.1. 试剂试液:氯化钠:临用前配成0.9%浓度的溶液,配制记录见附件1。
冲洗液:0.1%蛋白胨水溶液,配制记录见附件2。
6.3.2. 培养基硫乙醇酸盐流体培养基生产厂家:批号:改良马丁培养基生产厂家:批号:营养肉汤培养基生产厂家:批号:改良马丁琼脂培养基生产厂家:批号:蛋白胨生产厂家:批号:培养基配制记录见附件3。
6.4. 验证用菌株:金黄色葡萄球菌【CMCC(B)26003】铜绿假单胞菌【CMCC(B)10104】枯草芽孢杆菌【CMCC(B)63501】生孢梭菌【CMCC(B)64941】白色念珠菌【CMCC(F)98001】黑曲霉【CMCC(F)98003】购自:各验证用菌种传代记录见附件4。
6.5. 无菌检验仪器及相关设备:压力蒸汽灭菌器型号:生产厂家:校验日期:有效期:生化培养箱(细菌培养)型号:生产厂家:校验日期:有效期:生化培养箱(霉菌培养)型号:生产厂家:校验日期:有效期:7. 验证内容:7.1. 培养基无菌性检查:每批培养基随机取不少于5支,培养14天,应无菌生长。


无菌检查方法的验证无菌检查方法的验证无菌检查方法是为了检查药典要求无菌的制剂及其他制品是否无菌而建立的试验方法,是作为无菌产品批放行的重要依据及药监部门对无菌产品质量监管的一个重要工程。
因此如何确保无菌检查方法的准确可靠至关重要,而检查方法的验证是保证检查结果的公正、科学和准确的根底,因此各个主要国家的GMP或药典都对无菌检查方法的验证提出了严格的要求,2022版中国药典对分析方法验证和检查的要求也有大幅度的提高,同时也是GMP检查中检查的重点和容易发现问题的区域。
验证要求与方法无菌检查方法验证一般分为前验证和再验证两种。
前验证,也称预验证,指在无菌分析方法正式使用前,按照预定验证方案进行的验证。
如果没有充分的理由,任何检查方法必须进行前验证。
再验证,指某一检查方法经过验证并在使用一段时间后进行的,旨在证实已验证状态没有发生飘移而进行的重新验证及对检查方法进行修订、改变时进行的验证。
通常一个无菌产品的检查流程为:首先基于产品的剂型、溶解度等性质,按照药典的要求确定是否需要进行前处理;然后根据产品的特性是否有抑菌性,确定是否需要增加去除产品抑菌性的方法;最后验证整个检查方法中用到的一切及试验过程中的每一个环节包括样品的预处理方式、检查过程、培养条件等均不影响样品中微生物的生长。
这里,验证的重点环节包括:前处理方法直接影响后续步骤的效果和重现性,应是验证的重点。
供试品中抑菌活性的去除是当前验证工作的重点,尤其强调应充分验证供试品本身对微生物生长的影响。
具体的验证方法如下:菌种的选择无菌检查方法验证中通常选择以下6种试验中常用的控制菌的标准菌株,它们分别代表不同类型的菌种:枯草芽孢杆菌 [CMCC(B)63 501]代表药品中常见的污染菌——芽孢杆菌、金黄色葡萄球菌 [CMCC(B)26 003]代表革兰阳性菌、生孢梭菌 [CMCC(B)64 941]代表厌氧菌、大肠埃希菌 [CMCC(B)44 102]代表革兰阴性菌、白色念珠菌 [CMCC(F)98 001]代表酵母菌、黑曲霉菌 [CMCC(F)98 003]代表霉菌。
无菌检查方法验证方案无菌检查是用来验证产品的无菌性的方法。
无菌性是指产品中不存在可繁殖的微生物。
无菌检查的目的是确保产品的安全性和质量,避免由于微生物污染而引起的感染或降低产品的有效性。
1.检测方法的选择:根据产品的特性和要求,选择合适的无菌检测方法。
常用的无菌检测方法包括微生物限度试验、膜过滤法、直接刨片法和填充法等。
2.样品准备:根据产品的特性和要求,合理选择样品的采集方法和数量。
样品的采集应在无菌条件下进行,以避免外部微生物的污染。
样品的存储和运输也需要符合无菌条件。
3.控制样品:准备一批已知无菌的样品作为正对照,以验证无菌检测方法的准确性和灵敏度。
正对照的准备应在无菌条件下进行,并进行相关记录。
4.负对照:准备一批已知含有可繁殖的微生物的样品作为负对照,以验证无菌检测方法的特异性和无菌性。
5.实验操作:根据选定的无菌检测方法,进行实验操作。
实验操作应在无菌条件下进行,包括无菌操作台、无菌培养基和无菌器具的使用。
所有操作人员都应接受相关的培训和认证。
6.试验结果的解释和判定:根据实验结果,判断样品是否无菌,并根据相应的标准和规范进行判定。
试验结果的解释和判定应由经过培训和认证的人员进行。
7.系统的记录和存档:对于每一次无菌检测,应记录实验过程、实验结果和相关的数据。
实验记录应具备可追溯性,便于审核和查找。
所有记录和相关数据应进行适当的存档,以备将来参考。
8.系统的验证:根据无菌检测方法验证方案的内容和要求,对整个无菌检测系统进行验证,包括设备、物料和人员。
验证应由专业的第三方机构进行,确保验证结果的客观性和可靠性。
验证结果和报告应进行适当的存档,以供将来参考。
以上就是一个完整的无菌检查方法验证方案。
通过合理的无菌检查方法验证方案的制定和实施,可以确保无菌检测的准确性和可靠性,保证产品的质量和安全性。
产品无菌检查方法验证方案无菌检查方法验证1.概述无菌检查是用于检查药典要求无菌的药品、医疗器具、原料、辅料及其它品种是否无菌的一种方法。
无菌检查工作量大、操作不规范、人员的知识匮乏、检查方法应用不当等都会导致试验失败,因此在对一个产品进行无菌检查之前应先对无菌检查方法进行验证。
2.验证目的2.1确认所用的无菌检查方法适用于“本公司所有无菌产品”的无菌检查。
2.2确保检查结果的准确性、可靠性、准确性和重现性以及检查方法的完整性。
2.3通过对不同批次产品无菌检查的比较,对医用即无菌产品的生产全过程进行质量监控。
3.验证范围“本公司所有无菌产品”的无菌检查。
4.验证人员及职责验证委员会负责验证项目的确定;质控部负责该验证方案的起草及组织实施;验证小组负责验证方案的审批;质控部参与验证的实施及监督。
验证小组成员:5.文件准备和培训5.1检查验证所需的各类文件资料,应齐全;相关的文件草案是否已具备。
5.2培训参加验证人员需进行本文件及下述内容的培训:微生物知识、无菌检查及微生物检验操作培训。
6.验证条件及验证时间安排6.1验证条件6.1.1检验公用系统验证及仪器安装完成;仪表量器经过校验合格,且在有效期内。
6.1.2供试品3批①②③培养基及试剂:氯化钠:临用前配成0.9%浓度的溶液硫乙醇酸盐流体培养基批号:生产厂家:TSB 批号:生产厂家:6.1.3验证用菌株:微生物培养基质控品(来源:杭州微球科技有限公司)金黄色葡萄球菌【CMCC(B)26003】菌种传代次数铜绿假单胞菌【CMCC(B)10104】枯草芽孢杆菌【CMCC(B)63501】生孢梭菌【CMCC(B)64941】白色念珠菌【CMCC(F)98001】6.1.4无菌检验仪器及相关设备压力蒸汽灭菌器型号:编号:生化培养箱型号:编号:霉菌培养箱型号:编号:超净工作台型号:编号:6.2验证时间验证小组提出完整的验证计划,经批准后实施,整个验证活动按下面时间安排完成。
无菌检查方法(中国药典2010版)验证方案验证方案编号:起草单位(Composed by):质检部(QC Department)起草人(Composer):日期(Date):审核人(Reviewed by QC):日期(Date):审核人(Reviewed by QA):日期(Date):批准人(Approved by):日期(Date):目录1. 验证目的2. 验证人员3. 验证依据及参考文件4. 仪器与设备5. 验证过程5.1 培养基及稀释液5.2 菌液的培养与制备5.3 方法验证试验6. 验证总结1. 验证目的:本试验是注射液的抑细菌、抑真菌活性及所用的无菌检查方法的可靠性进行验证,以确认该产品在该检验量、该检验条件下无抑菌活性或其抑菌活性已被充分消除至可以忽略。
即:保证所用的无菌检验方法能对该产品进行准确、可靠的检验。
2. 验证人员:验证小组组长:验证小组副组长:验证小组成员:3. 验证依据及参考文件:验证依据:中华人民共和国药典2010版二部参考文件:2010年版中国药典无菌检查方法、验证操作学习班讲稿汇编(中国药品检验所)4. 仪器与设备XG1.DM-0.36B型机动门脉冲真空灭菌器细菌培养箱霉菌培养箱净化工作台5. 验证过程:5.1 培养基及稀释液5.1.1 培养基及稀释液的配制按“中国药典2010版二部附录Ⅺ H无菌检查法”中,有关规定配制本验证所需培养基:5.1.2培养基的适用性检验5.1.2.1 培养基无菌性检查从以上培养基及稀释液中,每批随机取5支(瓶),培养14天,应无菌生长。
结果记录:结论:5.1.2.2 培养基灵敏度检查取每管装量为12ml的硫乙醇酸盐流体培养基9支,分别接种小于100cfu的金黄色葡萄球菌、铜绿假单胞菌、枯草芽孢杆菌、生孢梭菌各2支,另1支不接种作为空白对照,培养3天,逐日观察结果。
取每支装量为9ml的改良马丁培养基5支,分别接种小于100cfu的白色念珠菌、黑曲霉各2支,另1支不接种作为空白对照,培养5天,逐日观察结果。