应用电化学简单题附答案
- 格式:docx
- 大小:16.58 KB
- 文档页数:4

应⽤电化学简单题附答案1.何谓电⽑细曲线?何谓零电荷电势?由lippman 公式可进⼀步得到界⾯双电层的微分电容Cd ,请给出Cd 的数学表达式。
答:①将理想极化电极极化⾄不同电势(Φ),同时测出相应的界⾯张⼒(σ值),表征Φ-6关系的曲线为“电⽑细曲线”。
②“零电荷电势”是指σ-Φ曲线上最⾼点处d σ/d Φ=0即q=0(表⾯不带有剩余电荷)相应的电极电势,⽤Φ0表⽰。
③由lippman 公式:q=-(d σ/d Φ)µ1 ,µ2 ,...µi ;及Cd=dq/d Φ得Cd=-d 2σ/d Φ22.何谓电化学极化?产⽣极化的主要原因是什么?试分析极化在电解⼯业(如氯碱⼯业)﹑电镀⾏业和电池⼯业的利弊。
答:①电化学极化是指外电场作⽤下,由于电化学作⽤相对于电⼦运动的迟缓性改变了原有的电偶层⽽引起电极电位变化。
(即电极有净电流通过时,阴、阳电流密度不同,使平衡状态受到了破坏,⽽发⽣了电极电位的“电化学极化”)。
②原因:电化学反应迟缓、浓差极化。
③从能量⾓度来看,极化对电解是不利的;超电势越⼤,外加电压越⼤,耗能⼤。
极化在电镀⼯业中是不利的,氢在阴极上析出是不可避免的副反应,耗能⼤,但同时使阴极上⽆法析出的⾦属有了析出的可能。
极化使电池放电时电动势减少,所做电功也减⼩,对电池⼯业不利3.参⽐电极需选⽤理想极化电极还是不极化电极?⽬前参⽐电极有那些类型?选择参⽐电极需考虑什么?答:①参⽐电极选⽤理想不极化电极。
②类型:标准氢电极,饱和⽢汞电极,Ag/Agcl 电极,Hg/HgO/OH -电极。
③考虑的因素:电极反应可逆,稳定性好,重现性好,温度系数⼩以及固相溶解度⼩,与研究体系不反应4.零电荷的电势可⽤哪些⽅法测定?零电荷电势说明什么现象?能利⽤零电荷电势计算绝对电极电位吗?答:①电⽑细法和微分电容法。
②零电荷电势表明了“电极/溶液”界⾯不会出现由于表⾯剩余电荷⽽引起的离⼦双电层现象;③不能将此电势看成相间电势的绝对零点,该电势也是在⼀定参⽐电极下测得的,所以不能⽤于计算绝对电极电位。

完整版)电化学练习题带答案1.铁镍蓄电池是一种常见的电池,其放电反应为Fe +NiO3 + 3H2O → Fe(OH)2 + 2Ni(OH)2.下列说法中,错误的是:A。
电池的电解液为碱性溶液,正极为NiO3,负极为Fe。
B。
电池放电时,负极反应为Fe + 2OH- → Fe(OH)2 + 2e。
C。
电池充电过程中,阴极附近溶液的pH降低。
D。
电池充电时,阳极反应为2Ni(OH)2 + 2OH- + 2e → NiO3 + 3H2O。
2.当镀锌铁发生析氢腐蚀时,有0.2mol电子发生转移。
正确的说法是:④在标准状况下有1.12L气体放出。
3.某固体酸燃料电池以CsHSO4固体为电解质传递H,其基本结构如图,电池总反应可表示为:2H2 + O2 → 2H2O。
以下说法正确的是:A。
电子通过外电路从b极流向a极。
B。
b极上的电极反应式为:O2 + 2H2O + 4e → 4OH-。
C。
每转移0.1mol电子,消耗1.12L的H2.D。
H由a极通过固体酸电解质传递到b极。
4.如图是某公司批量生产的笔记本电脑所用的甲醇燃料电池的构造示意图。
甲醇在催化剂作用下提供质子(H)和电子,电子经过电路、质子经内电路到达另一极与氧气反应,该电池总反应式为:2CH3OH + 3O2 → 2CO2 + 4H2O。
以下说法中,错误的是:A。
右边的电极为电池的负极,b处通入的是空气。
B。
左边的电极为电池的正极,a处通入的是甲醇。
C。
电池负极的反应式为:2CH3OH + 2H2O - 12e → 2CO2↑ + 12H+。
D。
电池正极的反应式为:3O2 + 12H+ + 12e → 6H2O。
5.铅蓄电池的工作原理为:Pb + PbO2 + 2H2SO4 →2PbSO4 + 2H2O。
以下判断不正确的是:A。
K闭合时,d电极反应式:PbSO4 + 2H2O - 2e → PbO2 + 4H+。
B。
当电路中转移0.2mol电子时,Ⅰ中消耗的H2SO4为0.2mol。
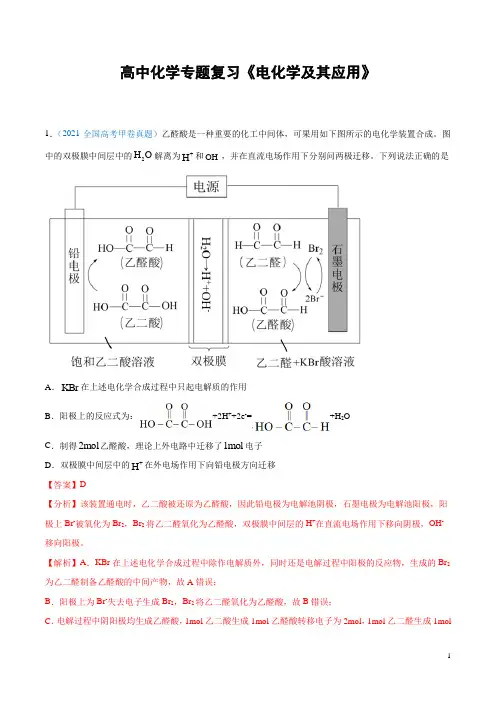
高中化学专题复习《电化学及其应用》1.(2021·全国高考甲卷真题)乙醛酸是一种重要的化工中间体,可果用如下图所示的电化学装置合成。
图中的双极膜中间层中的2H O 解离为+H 和-OH ,并在直流电场作用下分别问两极迁移。
下列说法正确的是A .KBr 在上述电化学合成过程中只起电解质的作用B .阳极上的反应式为:+2H ++2e -=+H 2OC .制得2mol 乙醛酸,理论上外电路中迁移了1mol 电子D .双极膜中间层中的+H 在外电场作用下向铅电极方向迁移 【答案】D【分析】该装置通电时,乙二酸被还原为乙醛酸,因此铅电极为电解池阴极,石墨电极为电解池阳极,阳极上Br -被氧化为Br 2,Br 2将乙二醛氧化为乙醛酸,双极膜中间层的H +在直流电场作用下移向阴极,OH -移向阳极。
【解析】A .KBr 在上述电化学合成过程中除作电解质外,同时还是电解过程中阳极的反应物,生成的Br 2为乙二醛制备乙醛酸的中间产物,故A 错误;B .阳极上为Br -失去电子生成Br 2,Br 2将乙二醛氧化为乙醛酸,故B 错误;C .电解过程中阴阳极均生成乙醛酸,1mol 乙二酸生成1mol 乙醛酸转移电子为2mol ,1mol 乙二醛生成1mol乙醛酸转移电子为2mol ,根据转移电子守恒可知每生成1mol 乙醛酸转移电子为1mol ,因此制得2mol 乙醛酸时,理论上外电路中迁移了2mol 电子,故C 错误;D .由上述分析可知,双极膜中间层的H +在外电场作用下移向阴极,即H +移向铅电极,故D 正确; 综上所述,说法正确的是D 项,故答案为D 。
2.(2021·全国高考乙卷真题)沿海电厂采用海水为冷却水,但在排水管中生物的附着和滋生会阻碍冷却水排放并降低冷却效率,为解决这一问题,通常在管道口设置一对惰性电极(如图所示),通入一定的电流。
下列叙述错误的是A .阳极发生将海水中的Cl 氧化生成2Cl 的反应B .管道中可以生成氧化灭杀附着生物的NaClOC .阴极生成的2H 应及时通风稀释安全地排入大气D .阳极表面形成的2Mg(OH)等积垢需要定期清理 【答案】D【分析】海水中除了水,还含有大量的Na +、Cl -、Mg 2+等,根据题干信息可知,装置的原理是利用惰性电极电解海水,阳极区溶液中的Cl -会优先失电子生成Cl 2,阴极区H 2O 优先得电子生成H 2和OH -,结合海水成分及电解产物分析解答。

高中化学电化试题及答案1. 单选题:下列关于电解水实验的描述中,正确的是:A. 电解水时,连接电源负极的一端产生的气体是氧气B. 电解水时,连接电源正极的一端产生的气体是氧气C. 电解水时,产生的氢气和氧气体积比为1:2D. 电解水时,产生的氢气和氧气体积比为2:1答案:D2. 填空题:在电解池中,阳极发生______反应,阴极发生______反应。
答案:氧化;还原3. 判断题:电解池中,电流通过电解质溶液时,溶液中的离子会向相反的电极移动。
A. 正确B. 错误答案:A4. 多选题:下列关于电镀的描述中,正确的有:A. 电镀是一种利用电解原理在金属表面镀上一层金属膜的过程B. 电镀过程中,镀层金属作为阴极C. 电镀过程中,待镀金属作为阳极D. 电镀过程中,待镀金属作为阴极答案:A, D5. 简答题:请简述电解池和原电池的区别。
答案:电解池和原电池都是基于氧化还原反应的电化学装置,但它们的主要区别在于能量的转换方向。
电解池是将电能转换为化学能的装置,通过外部电源提供电能,使电解质中的离子发生氧化还原反应。
而原电池则是将化学能转换为电能的装置,它利用自发的氧化还原反应产生电流。
在电解池中,阳极发生氧化反应,阴极发生还原反应;而在原电池中,阳极发生氧化反应,阴极发生还原反应。
此外,电解池需要外部电源供电,而原电池则能够自发产生电流。
6. 实验题:设计一个简单的实验,验证锌和铜的电化学活性顺序。
答案:实验步骤如下:(1) 准备一根锌棒和一根铜棒,以及一个电源和导线。
(2) 将锌棒和铜棒分别连接到电源的正负极。
(3) 观察连接铜棒的电极上是否有气泡产生。
(4) 根据实验现象,可以得出锌比铜更容易失去电子,因此锌的电化学活性比铜高。
7. 计算题:在电解饱和食盐水的实验中,若通电时间为2小时,电流强度为1安培,计算生成氢气和氯气的体积(标准状况下)。
答案:根据法拉第定律,Q = It,其中Q是电量,I是电流强度,t是时间。

电化学原理及其应用(习题及答案)work Information Technology Company.2020YEAR第六章电化学原理及其应用一、选择题1.下列电极反应中,溶液中的pH值升高,其氧化态的氧化性减小的是( C )A. Br2+2e = 2Br-B. Cl2+2e=2Cl—C. MnO4—+5e+8H+=2Mn2++4H2OD. Zn2++2e=Zn2.已知H2O2在酸性介质中的电势图为 O2 0.67V H2O2 1.77V H2O,在碱性介质中的电势图为O2-0.08V H2O2 0.87V H2O,说明H2O2的歧化反应(C)A.只在酸性介质中发生B.只在碱性介质中发生C.无论在酸、碱性介质中都发生D.与反应方程式的书写有关3.与下列原电池电动势无关的因素是 Zn | Zn2+‖H+,H2 | Pt (B)A. Zn2+的浓度B. Zn电极板的面积C.H+的浓度D.温度4.298K时,已知Eθ(Fe3+/Fe)=0.771V,Eθ(Sn4+/Sn2+)=0.150V,则反应2Fe2++Sn4+=2Fe3++Sn2+的△r G mθ为(D)kJ/mol。
A. -268.7B. -177.8C. -119.9D. 119.95.判断在酸性溶液中下列等浓度的离子哪些能共存(D)A Sn2+和Hg2+ B. SO32—和MnO4—C. Sn4+和FeD. Fe2+和Sn4+已知Eθ(Hg2+/Hg)=0.851V,Eθ(Sn4+/Sn2+)=0.15V ,Eθ(MnO4—/Mn2+)=1.49V Eθ(SO42—/H2SO3)=1.29V ,Eθ(Fe2+/Fe)= —0.44V6.已知下列反应在标准状态下逆向自发进行Sn4++Cu = Sn2++Cu2+Eθ(Cu2+/Cu)=(1) , Eθ(Sn4+/Sn2+)=(2) 则有(C)A. (1) = (2)B. (1)<(2)C. (1)>(2)D. 都不对二、填空题1.将下列方程式配平3 PbO2 + 2 Cr3+ + ____H2O___ =1 Cr2O72— + 3 Pb2+ + __2H+___ (酸性介质)2 MnO2 +3 H2O2 +__2OH-___ =2 MnO4— + ___4H2O______ (碱性介质)2.现有三种氧化剂Cr2O72—,H2O2,Fe3+,若要使Cl—、Br—、I—混合溶液中的I—氧化为I2,而Br-和Cl-都不发生变化,选用Fe3+最合适。

电化学方法原理和应用习题答案1. 电化学方法的原理电化学方法是一种利用电化学过程来研究物质性质和进行分析的方法。
它基于物质与电流之间的相互作用,通过测量电流、电势和电荷量等参数来获得与物质性质相关的信息。
电化学方法的原理基于两个基本的电化学过程:电解和电化学反应。
电解是指通过外加电势将电解质溶液中的离子转化为氧化还原反应中的氧化剂和还原剂。
电化学反应是指在电极表面发生的氧化还原反应,通过测量电极电势的变化来了解物质的电化学性质。
2. 电化学方法的应用2.1 电化学分析:电化学分析是利用电化学方法来定量或定性地分析化合物和物质的方法。
常见的电化学分析方法包括电位滴定法、极谱法、电位滴定法等。
这些方法可以广泛应用于环境监测、水质分析、生化分析等领域。
2.2 电化学腐蚀研究:电化学腐蚀研究是通过电化学方法来研究和评估材料在特定环境条件下的腐蚀性能。
它可以帮助我们了解材料在不同环境中的腐蚀行为,并采取措施来延缓或防止材料的腐蚀。
2.3 电化学储能:电化学储能是指利用电化学反应来存储和释放能量的技术。
常见的电化学储能装置包括电池和超级电容器。
电化学储能技术在电动汽车、可再生能源储存、能量回收等领域有着广泛的应用。
2.4 电化学合成:电化学合成是通过电流驱动反应来合成化合物的方法。
它可以用于有机合成、金属粉末的制备等。
电化学合成具有高选择性、高效率等优点,是一种绿色、可持续发展的合成方法。
3. 习题答案3.1 问题1:电解质溶液中是如何进行电解的?电解质溶液中的电解过程可以分为两个步骤:阳极反应和阴极反应。
在阳极处,氧化反应会发生,而在阴极处会进行还原反应。
阳极和阴极之间通过电解质溶液中的离子传递电荷。
3.2 问题2:电极电势的测量原理是什么?电极电势可以通过将电极与参比电极相连,通过测量电势差来确定。
参比电极是一个具有已知电势的电极,它提供了一个稳定的电势参考。
电极与参比电极之间的电势差可以通过测量电流或电势差来确定。
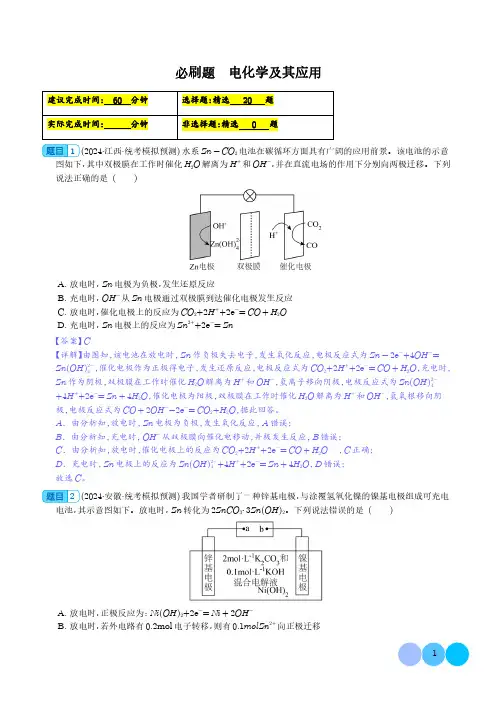
必刷题电化学及其应用建议完成时间:60分钟选择题:精选20题实际完成时间:分钟非选择题:精选0题1(2024·江西·统考模拟预测)水系Zn-CO2电池在碳循环方面具有广阔的应用前景。
该电池的示意图如下,其中双极膜在工作时催化H2O解离为H+和OH-,并在直流电场的作用下分别向两极迁移。
下列说法正确的是()A.放电时,Zn电极为负极,发生还原反应B.充电时,OH-从Zn电极通过双极膜到达催化电极发生反应C.放电时,催化电极上的反应为CO2+2H++2e-=CO+H2OD.充电时,Zn电极上的反应为Zn2++2e-=Zn【答案】C【详解】由图知,该电池在放电时,Zn作负极失去电子,发生氧化反应,电极反应式为Zn-2e-+4OH-=Zn(OH)2-4,催化电极作为正极得电子,发生还原反应,电极反应式为CO2+2H++2e-=CO+H2O,充电时,Zn作为阴极,双极膜在工作时催化H2O解离为H+和OH-,氢离子移向阴极,电极反应式为Zn(OH)2-4+4H++2e-=Zn+4H2O,催化电极为阳极,双极膜在工作时催化H2O解离为H+和OH-,氢氧根移向阴极,电极反应式为CO+2OH--2e-=CO2+H2O,据此回答。
A.由分析知,放电时,Zn电极为负极,发生氧化反应,A错误;B.由分析知,充电时,OH-从双极膜向催化电移动,并极发生反应,B错误;C.由分析知,放电时,催化电极上的反应为CO2+2H++2e-=CO+H2O ,C正确;D.充电时,Zn电极上的反应为Zn(OH)2-4+4H++2e-=Zn+4H2O,D错误;故选C。
2(2024·安徽·统考模拟预测)我国学者研制了一种锌基电极,与涂覆氢氧化镍的镍基电极组成可充电电池,其示意图如下。
放电时,Zn转化为2ZnCO3⋅3Zn(OH)2。
下列说法错误的是()A.放电时,正极反应为:Ni(OH)2+2e-=Ni+2OH-B.放电时,若外电路有0.2mol电子转移,则有0.1molZn2+向正极迁移C.充电时,a为外接电源负极D.充电时,阴极反应为:2ZnCO3⋅3Zn(OH)2+10e-=5Zn+2CO2-3+6OH-【答案】B【详解】放电时,锌基电极为负极,Zn转化为2ZnCO3⋅3Zn(OH)2,电极反应式为:5Zn+2CO2-3+6OH--10e-=2ZnCO3⋅3Zn(OH)2,镍基电极为正极,电极反应式为:Ni(OH)2+2e-=Ni+2OH-,充电时,a接电源负极,锌基电极为阴极,电极反应式为:2ZnCO3⋅3Zn(OH)2+10e-=5Zn+2CO2-3+6OH-,b接电源正极,镍基电极为阳极,电极反应式为:Ni+2OH--2e-=Ni(OH)2。

应用电化学,辉卢文庆 全书思考题和习题 第一章习题解答:1试推导下列各电极反应的类型及电极反应的过程。
(1)++→+242Ce e Ce解:属于简单离子电迁移反应,指电极/溶液界面的溶液一侧的氧化态物种4Ce +借助于电极得到电子,生成还原态的物种2Ce+而溶解于溶液中,而电极在经历氧化-还原后其物理化学性质和表面状态等并未发生变化, (2) -→++OH e O H O 44222解:多孔气体扩散电极中的气体还原反应。
气相中的气体2O 溶解于溶液后,再扩散到电极表面,然后借助于气体扩散电极得到电子,气体扩散电极的使用提高了电极过程的电流效率。
(3) Ni e Ni→++22解:金属沉积反应。
溶液中的金属离子2Ni +从电极上得到电子还原为金属Ni ,附着于电极表面,此时电极表面状态与沉积前相比发生了变化。
(4) -+→++OH s MnOOH O H e s MnO )()(22解:表面膜的转移反应。
覆盖于电极表面的物种(电极一侧)经过氧化-还原形成另一种附着于电极表面的物种,它们可能是氧化物、氢氧化物、硫酸盐等。
(5)2)(22OH Zn e OH Zn→-+-;--→+242])([2)(OH Zn OH OH Zn解:腐蚀反应:亦即金属的溶解反应,电极的重量不断减轻。
即金属锌在碱性介质中发生溶解形成二羟基合二价锌络合物,所形成的二羟基合二价锌络合物又和羟基进一步形成四羟基合二价锌络合物。
2.试说明参比电极应具有的性能和用途。
参比电极(reference electrode ,简称RE):是指一个已知电势的接近于理想不极化的电极,参比电极上基本没有电流通过,用于测定研究电极(相对于参比电极)的电极电势。
既然参比电极是理想不极化电极,它应具备下列性能:应是可逆电极,其电极电势符合Nernst 方程;参比电极反应应有较大的交换电流密度,流过微小的电流时电极电势能迅速恢复原状;应具有良好的电势稳定性和重现性等。

应用电化学基础答案谢德明1、在溶剂沉淀法中,主要是在溶液中加入另一种溶剂一改变混合溶剂的什么实现的()[单选题] *ApH值B溶解度C极性(正确答案)D体积2、属于倍半萜的化合物是()[单选题] *A龙脑B莪术醇C薄荷醇D青蒿素(正确答案)3、南五味子保肝的主要效药效成分是()[单选题] *A蒽醌B香豆素C黄酮D木脂素(正确答案)4、下列含有蒽醌类成分的中药是()*A丹参B决明子(正确答案)C芦荟(正确答案)D紫草5、E易酶解苷类成分关于亲水性有机溶剂,说法正确的有()*A极性大(正确答案)B极性小C水不相溶D与水部分相溶6、以橙皮苷为指标成分进行定性鉴别的中药是()[单选题] *A葛根B黄芩C槐花D陈皮(正确答案)7、适用于队热及化学不稳定的成分、低极性成分的提取()[单选题] * A渗漉法B超声提取法C回流提取法D超临界流体提取法(正确答案)8、具有酚羟基或羧基的游离蒽醌类成分有一定酸性,可用的提取方法是()[单选题]* A酸溶碱沉法B碱溶酸沉法(正确答案)C水提醇沉法D醇提水沉法9、以葛根素为指标成分进行定性鉴别的中药是()[单选题] *A葛根(正确答案)B黄芩C槐花D陈皮10、大黄素型蒽醌母核上的羟基分布情况是()[单选题] *A一个苯环的β位B苯环的β位C在两个苯环的α或β位(正确答案)D一个苯环的α或β位11、挥发油可析出结晶的温度是()[单选题] *A0~-20℃(正确答案)B0~10℃C0~20℃D0~15℃12、分馏法分离挥发油的主要依据是()[单选题] *A密度的差异B沸点的差异(正确答案)C溶解性的差异D旋光性的差异13、游离生物碱和生物碱盐都易溶解的溶剂是()[单选题] * A三氯甲烷B正丁醇C乙醇(正确答案)D水14、下列应用最广的经典提取方法是()[单选题] *A水蒸气蒸馏法B溶剂提取法(正确答案)C超临界流体萃取法D超声提取法15、溶剂极性由小到大的是()[单选题] *A石油醚、乙醚、乙酸乙酯(正确答案)B石油醚、丙酮、乙酸乙酯C石油醚、乙酸乙酯、三氯甲烷D三氯甲烷、乙酸乙酯、乙醚16、薄层吸附色谱中的Rf的大小说明了吸附程度的大小,吸附力越大,则Rf()[单选题] *A越大B越小(正确答案)C越接近1D越接近017、下列基团在极性吸附色谱中的被吸附作用最强的是()[单选题] *A羧基(正确答案)B羟基C氨基D醛基18、凡具有()的木脂素,与三氯化铁反应,呈阳性()[单选题] *A酚羟基(正确答案)B羧酸C醇羟基D氨基19、从香豆素类的结构看,香豆素是一种()[单选题] *A内酯(正确答案)B羧酸C酰胺D糖20、E连续回流提取法(正确答案)用乙醇作溶剂提取时,下列说法正确的是()* A对植物细胞壁穿透力强(正确答案)B溶解范围广,提取较全面(正确答案)C提取液中蛋白质、多糖等水溶性杂质少(正确答案)D有防腐作用,提取液不易发霉变质(正确答案)21、巴豆的致泻成分是()[单选题] *A丁二酸B巴豆油酸(正确答案)C绿原酸D抗内毒素22、萃取法是利用混合物中各成分在两相溶剂中的分配.系数不同而到达分离的方法,所谓两相溶剂是指()[单选题] *A两种相互接触而又不相溶的溶剂(正确答案)B两种不相互接触而又互相溶的溶剂C两种不相互接触而又不相容的溶剂D两种互相接触而又互相溶的溶剂23、属于挥发油特殊提取方法的是()[单选题] *A酸提碱沉B水蒸气蒸馏(正确答案)C煎煮法D浸渍法24、挥发油的溶解性难溶于()[单选题] *A水(正确答案)B乙醇C石油醚D乙醚25、香豆素及其苷发生异羟肟酸铁反应的条件为()[单选题] * A在酸性条件下B在碱性条件下C先碱后酸(正确答案)D在中性条件下26、厚朴酚的结构类型为()[单选题] *A简单木脂素B单环氧木脂素C木脂内酯D新木脂素(正确答案)27、倍半萜和二萜在化学结构上的明显区别是()[单选题] * A氮原子数不同B碳原子数不同(正确答案)C碳环数不同D硫原子数不同28、下列方法哪一个不是按照色谱法的分离原理不同进行分类的是()[单选题] * A离子交换色谱B薄层吸附色谱(正确答案)C凝胶色谱D分配色谱29、中药紫草中的主要有效成分属于()[单选题] *A苯醌类B萘醌类(正确答案)C蒽醌类D菲醌类30、在高效液相色谱法中,常用的柱内填料是()[单选题] *A氧化铝B活性炭C十八烷基硅烷键和硅胶(正确答案)D羧甲基纤维素。

电化学试题及答案一、选择题(每题2分,共20分)1. 电化学中,原电池的工作原理是:A. 通过化学反应产生电流B. 通过电流产生化学反应C. 通过电场作用产生化学反应D. 通过化学反应产生电场答案:A2. 哪种金属在标准氢电极电位表中具有最高的电位?A. 铜B. 银C. 金D. 铂答案:C3. 电化学腐蚀的类型包括:A. 均匀腐蚀B. 局部腐蚀C. 应力腐蚀D. 所有以上答案:D4. 电化学中的过电位是指:A. 电极电位与平衡电位之间的差值B. 电极电位与标准电位之间的差值C. 电极电位与理论电位之间的差值D. 电极电位与实际电位之间的差值答案:A5. 电镀过程中,阴极上发生的反应是:A. 还原反应B. 氧化反应C. 吸附反应D. 扩散反应答案:A二、填空题(每空1分,共20分)6. 在电化学中,______是指电极反应中电子的转移数。
答案:电荷数7. 电化学腐蚀的防护措施包括______、______和______。
答案:牺牲阳极保护、外加电流阴极保护、涂层保护8. 电化学传感器的工作原理基于______的变化,以检测特定化学物质的存在。
答案:电位或电流9. 电化学中的法拉第定律表明,电极上沉积或溶解的物质的量与______成正比。
答案:通过电极的电荷量10. 电化学中的电解质溶液通常具有______性,以促进离子的移动。
答案:导电三、简答题(每题10分,共30分)11. 描述电化学腐蚀的基本原理,并给出两种常见的腐蚀类型。
答案:电化学腐蚀的基本原理是金属表面与环境中的电解质溶液发生电化学反应,导致金属的溶解或损坏。
常见的腐蚀类型包括均匀腐蚀和点蚀。
12. 解释电化学中的极化现象,并说明它对电池性能的影响。
答案:极化现象是指在电化学反应过程中,电极电位偏离平衡电位的现象。
它通常由电极反应动力学的减缓或电极表面物质的积累引起。
极化会降低电池的性能,因为它增加了电池内部的电阻,导致电池效率下降和输出电压降低。

电化学试题及答案一、选择题(每题2分,共20分)1. 电化学中,原电池的负极发生的反应是:A. 还原反应B. 氧化反应C. 还原反应和氧化反应D. 无反应答案:B2. 标准氢电极的电势是:A. -0.059 VB. 0.059 VC. 1.23 VD. 0 V答案:D3. 在电化学腐蚀中,金属的腐蚀速度与电解质的浓度关系是:A. 无关B. 正比C. 反比D. 先增后减答案:B4. 电化学分析中,电位分析法的基本原理是:A. 测量电流B. 测量电阻C. 测量电位D. 测量电压答案:C5. 电化学腐蚀中,阳极保护法的基本原理是:A. 使金属表面形成氧化膜B. 使金属表面形成还原膜C. 使金属表面形成钝化膜D. 使金属表面形成导电膜答案:C6. 电化学合成中,电解水时产生的气体是:A. 氢气和氧气B. 氮气和氧气C. 氢气和二氧化碳D. 氮气和二氧化碳答案:A7. 电化学传感器中,pH传感器的工作原理是:A. 测量电流B. 测量电阻C. 测量电位D. 测量电压答案:C8. 电化学腐蚀中,阴极保护法的基本原理是:A. 使金属表面形成氧化膜B. 使金属表面形成还原膜C. 使金属表面形成钝化膜D. 使金属表面形成导电膜答案:A9. 电化学合成中,电解氯化钠溶液时产生的气体是:A. 氢气和氧气B. 氯气和氢气C. 氯气和二氧化碳D. 氮气和氢气答案:B10. 电化学腐蚀中,金属腐蚀速度与温度的关系是:A. 无关B. 正比C. 反比D. 先增后减答案:B二、填空题(每题2分,共20分)1. 电化学腐蚀中,金属腐蚀速度与______成正比。
答案:电解质浓度2. 电化学分析中,电位分析法的基本原理是测量______。
答案:电位3. 电化学传感器中,pH传感器的工作原理是测量______。
答案:电位4. 电化学合成中,电解水时产生的气体是______和氧气。
答案:氢气5. 电化学腐蚀中,阳极保护法的基本原理是使金属表面形成______。
电化学原理及其应用(习题及答案)一、电化学原理概述电化学是研究化学反应与电现象之间关系的科学。
电化学反应涉及电子的转移,是化学能与电能之间的转化过程。
电化学原理广泛应用于电镀、电池、电解、电合成等领域。
1. 电化学反应的基本概念电化学反应包括氧化还原反应和电解质溶液中的离子反应。
氧化反应是指物质失去电子的过程,还原反应是指物质获得电子的过程。
电解质溶液中的离子反应是指阳离子和阴离子在电极上发生反应。
2. 电极与电解质电极是电化学反应中传递电子的导体,分为阳极和阴极。
阳极是电子流出的地方,阴极是电子流入的地方。
电解质是能在水溶液中导电的物质,包括酸、碱、盐等。
3. 电动势与电极电位电动势是指电池两极间的电位差。
电极电位是指电极在电解质溶液中的电位。
根据电极电位可以判断氧化还原反应的方向。
二、电化学应用1. 电池电池是利用电化学反应将化学能转化为电能的装置。
电池分为一次性电池和可充电电池。
一次性电池包括碱性电池、锌碳电池等;可充电电池包括铅酸电池、镍氢电池、锂电池等。
以下为几个习题及答案:习题1:碱性电池的正极材料是什么?答案:碱性电池的正极材料是二氧化锰(MnO2)。
习题2:铅酸电池的负极材料是什么?答案:铅酸电池的负极材料是海绵铅(Pb)。
2. 电解电解是利用电化学反应将电能转化为化学能的过程。
电解广泛应用于电镀、电解铝、电解水制氢等领域。
习题3:电解水制氢时,阳极产生的气体是什么?答案:电解水制氢时,阳极产生的气体是氧气(O2)。
习题4:电解铝时,阴极产生的物质是什么?答案:电解铝时,阴极产生的物质是铝(Al)。
3. 电镀电镀是利用电解原理在金属或非金属表面沉积一层金属或合金的过程。
电镀广泛应用于防护、装饰、修复等领域。
习题5:电镀过程中,阳极材料是什么?答案:电镀过程中,阳极材料是待镀金属。
习题6:电镀过程中,阴极材料是什么?答案:电镀过程中,阴极材料是待镀物体。
4. 电合成电合成是利用电解原理将两个或多个反应物在电极上发生化学反应,生成目标产物。
应用电化学习题4一简答题:1.碱性锌氧化银电池以锌粉为负极,以氧化银粉(Ag2O) 压制成正极,电解液为饱和了锌酸盐的浓碱溶液试写出其正极反应,负极反应,电池反应。
2.试述有关化学电源主要性能的概念,如电动势、开路电压、工作电压、截止电压。
3.防止钢铁腐蚀主要措施有?4.什么是析氢腐蚀和耗氧腐蚀?5.阴极保护的方法有哪几种,画图并简述一下各种方法,也可举例说明。
6.发生钝化的金属或合金具有的一些特点?有哪几种主要的钝化理论?7.什么叫缓冲剂,其防蚀机理如何?8.金属离子还原继而形成结晶层的电结晶一般过程由哪些基本步骤组成及次序?9.什么是电解的电流效率和电能效率?两者区别是?10.简述电解冶金的方法,并说出电解冶金与火法冶金比较有哪些特点?11.对镀锌层采用什么后处理方法?镀锌层为什么要进行钝化处置?12.试述一般的镀液的组成?并说明其作用和选择。
13.电镀的生产工艺有哪些?有何作用?14.在光亮硫酸盐镀铜中,阳极用什么材料?通常在电镀过程中呈现什么状态?15.作为复合电镀中的固体微粒主要有哪几类?粒径多大?举例说明。
16.电镀溶液中既不参加电极反应,又不对放电金属离子起络合作用,而只是用来提高溶液的导电能力的称之谓导电盐;这类物质不仅仅指盐,也包含酸或碱。
请在酸性光亮镀铜、氯化钾镀锌、氰化物镀铜的三种电镀液中,各指出那些物质属导电盐?导电盐含量的高或低,对镀液的性能有什么影响?二计算题:+2e,反应机理为:17.氯析出反应:2Cl-→Cl2在Pt电极上Cl-+M-→MCl+e (a)(b)2MCl→2M+Cl2在氧化的Ru电极上Cl-+M-→MCl+e (a)+e (c)MCl+ Cl-→M+Cl2MCl表示电极吸附物种。
已知这两种电极上的反应速度决定步骤分别为(b)和(c)。
试述不同电极上氯析出反应动力学的可能差异(如Tafel斜率、反应级数等)。
应用电化学复习题和习题答案第一章习题解答1.用Ag 做电极,AgNO 3溶液的浓度为0.00739g/g(水),通电一段时间后,阳极上有0.078gAg (s )析出,而阳极区内含0.236gAgNO 3和23.14g 水,求t (Ag +)和t (NO 3-)。
解:Ag →Ag ++e -Ag ++e -→Agn 原=23.4×0.00739/169=1.023×10-3mol n 析=0.078/107=7.29×10-4mol n 后=0.236/169=1.396×10-3mol n 迁=n 原+n 析-n 后=5.36×10-4t (Ag +)=n 迁(Ag +)/n 析=0.735 t(NO 3-)=1- t (Ag +)=0.2652.25℃时在电导池中盛有浓度0.02mol/dm ³的KCl 溶液,测得电阻为82.4Ω,若在同一电导池中盛有浓度为0.0025mol/dm ³的k 2SO 4溶液,测得电阻为326Ω,已知25℃时0.02mol/dm ³的KCl 溶液的电导率为0.2768 S/m ,试求(1)电导池常数(2)0.0025mol.dm ³的K 2SO 4溶液的电导率和摩尔电导率。
(1)K cell =K kcl /G kcl =K kcl ×R kcl =82.4×0.2768=22.81 (2)K K2SO4=K cell ×G K2SO4=K cell /R K2SO4=0.07 S/m ΛK2SO4=K K2SO4/C=28×10-3 S/(m ·mol)3. 25℃时AgCl 饱和溶液的电导率为3.41×10-4S/m ,已知同温下水的电导率为1.6×10-4S/m,计算25℃时AgCl 的溶解度。
应用电化学课后题答案谢德明1、挥发性成分的提取,常用的是()[单选题] *A溶剂提取法B水蒸气蒸馏法(正确答案)C超临界液体萃取法D超声提取法2、水蛭的主要化学成分是()[单选题] *A有机酸B蛋白质(正确答案)C多糖D生物碱3、结晶法一般是在分离纯化物质的哪个阶段常常使用的()[单选题] * A开始B中期C最后(正确答案)D以上均可4、可与异羟肟酸铁反应生成紫红色的是()[单选题] * A羟基蒽醌类B查耳酮类C香豆素类(正确答案)D二氢黄酮类5、区别挥发油与油脂常用的方法是()[单选题] *A相对密度B溶解性C油迹试验(正确答案)D沸点6、下列不能作为极性吸附剂的是()[单选题] *A活性炭(正确答案)B氧化铝C硅胶D氧化镁7、具有暖脾胃、散风寒、通血脉作用的是()[单选题] * A穿心莲内酯B青蒿素C莪术醇D桂皮醛(正确答案)8、下列关于香豆素的说法,不正确的是()[单选题] *A游离香豆素多具有芳香气味B分子量小的香豆素有挥发性和升华性C香豆素苷多无香味D香豆素苷多无挥发性,但有升华性(正确答案)9、关于前胡,说法正确的有(多选)()*A是伞形科前胡属植物(正确答案)B药理药效作用主要有祛痰、镇咳、平喘、抗炎、解痉、镇静等(正确答案) C可与皂荚、藜芦等药物一起放在药中煎煮D不溶乙醚等有机溶剂10、关于肿节风,说法正确的有(多选)()*A别名:接骨金粟兰、九节茶等(正确答案)B功能主治抗菌消炎凉血清热解毒(正确答案)C肿节风为白色针晶(正确答案)D不易溶于甲醇,乙醇11、E何首乌(正确答案)下列不含蒽醌类成分的中药是()*A丹参(正确答案)B决明子C芦荟D紫草(正确答案)12、组成木脂素的单体基本结构是()[单选题] *AC5-C3BC5-C2CC6-C3(正确答案)DC6-C413、苯丙素类的基本母核是具有一个或数个()单元的天然化合物()[单选题] * AC6-C3基团(正确答案)BC6-C6基团CC5-C3基团DC8-C8基团14、连续回流提取法在实验室用的装置为()[单选题] *A氏提取器(正确答案)B回流装置C蒸馏装置D分液漏斗15、单萜和倍半萜在化学结构上的明显区别是()[单选题] *A氮原子数不同B碳原子数不同(正确答案)C碳环数不同D硫原子数不同16、具有酚羟基或羧基的游离蒽醌类成分有一定酸性,可用的提取方法是()[单选题]* A酸溶碱沉法B碱溶酸沉法(正确答案)C水提醇沉法D醇提水沉法17、纸色谱是分配色谱中的一种,它是以滤纸为(),以纸上所含的水分为固定相的分配色谱。
化学电化学测试题及答案一、选择题(每题2分,共20分)1. 以下哪种物质不是电解质?A. 硫酸B. 氢氧化钠C. 蔗糖D. 氯化钠答案:C2. 原电池中,正极发生的反应是:A. 氧化反应B. 还原反应C. 既不氧化也不还原D. 既是氧化又是还原答案:B3. 标准氢电极的电势是:A. 0.00 VB. 1.00 VC. -1.00 VD. 0.10 V答案:A4. 电化学腐蚀的类型包括:A. 化学腐蚀B. 电化学腐蚀C. 物理腐蚀D. 以上都是答案:B5. 以下哪种金属在海水中腐蚀速率最快?A. 铜B. 铁C. 铝D. 锌答案:D6. 电镀过程中,阳极发生的反应是:A. 氧化反应B. 还原反应C. 既不氧化也不还原D. 既是氧化又是还原答案:A7. 电化学工作站中,测量电位的仪器是:A. 电流计B. 电压表C. 电阻计D. 电位计答案:D8. 以下哪种电解质溶液的导电性最强?A. 稀硫酸B. 稀盐酸C. 稀硝酸D. 稀醋酸答案:A9. 电化学腐蚀的防护措施不包括:A. 涂漆B. 镀层C. 增加氧气含量D. 阴极保护答案:C10. 以下哪种物质是强电解质?A. 醋酸B. 乙醇C. 硫酸D. 氨水答案:C二、填空题(每题2分,共20分)1. 原电池的工作原理是_______和_______的相互转化。
答案:氧化反应;还原反应2. 电化学腐蚀的防护措施之一是_______。
答案:阴极保护3. 电镀时,被镀金属作为_______极。
答案:阴极4. 标准氢电极的电势是_______。
答案:0.00 V5. 电化学腐蚀的类型包括化学腐蚀和_______。
答案:电化学腐蚀6. 电化学腐蚀的防护措施之一是_______。
答案:涂漆7. 电镀过程中,阳极发生_______反应。
答案:氧化8. 电化学工作站中,测量电流的仪器是_______。
答案:电流计9. 电化学腐蚀的防护措施之一是_______。
答案:镀层10. 强电解质在溶液中完全电离,而_______电解质则部分电离。
第六章电化学原理及其应用一、选择题1.下列电极反应中,溶液中的pH值升高,其氧化态的氧化性减小的是(C)A. Br2+2e = 2Br-B. Cl2+2e=2Cl—C. MnO4—+5e+8H+=2Mn2++4H2OD. Zn2++2e=Zn2.已知H2O2在酸性介质中的电势图为O2 0.67V H2O2 1.77V H2O,在碱性介质中的电势图为O2-0.08V H2O2 0.87V H2O,说明H2O2的歧化反应(C)A.只在酸性介质中发生B.只在碱性介质中发生C.无论在酸、碱性介质中都发生D.与反应方程式的书写有关3.与下列原电池电动势无关的因素是Zn |Zn2+‖H+,H2 | Pt (B)A. Zn2+的浓度B. Zn电极板的面积C.H+的浓度D.温度4.298K时,已知Eθ(Fe3+/Fe)=0.771V,Eθ(Sn4+/Sn2+)=0.150V,则反应2Fe2++Sn4+=2Fe3++Sn2+的△r G mθ为(D)kJ/mol。
A. -268.7B. -177.8C. -119.9D. 119.95.判断在酸性溶液中下列等浓度的离子哪些能共存(D)A Sn2+和Hg2+ B. SO32—和MnO4—C. Sn4+和FeD. Fe2+和Sn4+已知Eθ(Hg2+/Hg)=0.851V,Eθ(Sn4+/Sn2+)=0.15V ,Eθ(MnO4—/Mn2+)=1.49VEθ(SO42—/H2SO3)=1.29V ,Eθ(Fe2+/Fe)= —0.44V6.已知下列反应在标准状态下逆向自发进行Sn4++Cu = Sn2++Cu2+Eθ(Cu2+/Cu)=(1) , Eθ(Sn4+/Sn2+)=(2) 则有(C)A. (1) = (2)B. (1)<(2)C. (1)>(2)D. 都不对二、填空题1.将下列方程式配平3PbO2 + 2 Cr3+ + ____H2O___ =1Cr2O72—+ 3Pb2+ + __2H+___ (酸性介质)2MnO2 + 3 H2O2 +__2OH-___ =2MnO4—+ ___4H2O______ (碱性介质)2.现有三种氧化剂Cr2O72—,H2O2,Fe3+,若要使Cl—、Br—、I—混合溶液中的I—氧化为I2,而Br-和Cl-都不发生变化,选用Fe3+最合适。
1.何谓电毛细曲线?何谓零电荷电势?由lippman 公式可进一步得到界面双电层的微分电容Cd,请给出Cd的数学表达式。
答:①将理想极化电极极化至不同电势(①),同时测出相应的界面张力(c值),表征①-6关系的曲线为“电毛细曲线”。
②“零电荷电势” 是指c -①曲线上最高点处d c /d①=0即q=0(表面不带有剩余电荷)相应的电极电势,用①0表示。
③由lippman 公式:q=- (d c/d①)卩i ,卩2, (i)及Cd=dq/d①得Cd=-d2c/d ①22•何谓电化学极化?产生极化的主要原因是什么?试分析极化在电解工业(如氯碱工业)、电镀行业和电池工业的利弊。
答:①电化学极化是指外电场作用下,由于电化学作用相对于电子运动的迟缓性改变了原有的电偶层而引起电极电位变化。
(即电极有净电流通过时,阴、阳电流密度不同,使平衡状态受到了破坏,而发生了电极电位的“电化学极化”)。
②原因:电化学反应迟缓、浓差极化。
③从能量角度来看,极化对电解是不利的;超电势越大,外加电压越大,耗能大。
极化在电镀工业中是不利的,氢在阴极上析出是不可避免的副反应,耗能大,但同时使阴极上无法析出的金属有了析出的可能。
极化使电池放电时电动势减少,所做电功也减小,对电池工业不利3•参比电极需选用理想极化电极还是不极化电极?目前参比电极有那些类型?选择参比电极需考虑什么?答:① 参比电极选用理想不极化电极。
②类型:标准氢电极,饱和甘汞电极,Ag/Agcl 电极,Hg/HgO/OH-电极。
③考虑的因素:电极反应可逆,稳定性好,重现性好,温度系数小以及固相溶解度小,与研究体系不反应4. 零电荷的电势可用哪些方法测定?零电荷电势说明什么现象?能利用零电荷电势计算绝对电极电位吗?答:①电毛细法和微分电容法。
②零电荷电势表明了“电极/溶液”界面不会出现由于表面剩余电荷而引起的离子双电层现象;③不能将此电势看成相间电势的绝对零点,该电势也是在一定参比电极下测得的,所以不能用于计算绝对电极电位。
5. 为什么卤素离子在汞电极上吸附依F< Cl < I 的顺序而增强,特性吸附在电毛细曲线和微分电容曲线上有何表现?答:①卤素离子为表面活性物质,阴离子吸附主要发生在比零电荷电势更正的电势范围,由于F-、c 「、I■离子半径依次增大,可极化度增大,吸附能力增强,所以在汞电极上,l->c「>F-.②特性吸附在两种曲线上的左半支曲线不同,零电荷电势负移。
6•何谓非稳态扩散?其初始条件和一个边界条件是什么?另一边界条件由极化条件决定。
答:①非稳态扩散:在电化学反应开始阶段,由于反应粒子浓度变化幅度较小,液相传质不足,粒子被消耗,此时浓度极化处于发展阶段,称之为传质过程的非稳态阶段②初始条件:C i (x,0)=C i0开始电极前扩散粒子完全均匀分布在液相中。
边界条件:C i (^,t)=C i0,无穷远处不出现浓度极化。
③另一边界条件:极化条件7. 溶液中有哪几种传质方式,产生这些传质过程的原因是什么?答:对流、扩散、电迁移。
①对流:由于流体各部分之间存在浓度或温度差或者外部机械作用力下所引起;②扩散:由于某一组分存在浓度梯度,粒子由高浓度向低浓度转移;③电迁移:在外电场作用下,液相中带电粒子作定向移动。
8. 稳态扩散和非稳态扩散的特点是什么,可以用什么定律来表示?答:①稳态扩散:扩散粒子的浓度只与距离有关,与时间无关。
用Fick第一定律表示, J表示扩散流量。
②非稳态扩散:扩散粒子的浓度同时是距离和时间的函数。
用Fick第二定律9. 说明标准电极反应速度常数k s和交换电流密度i0的物理意义,并比较两者的区别。
答:①k s:当电极电势为反应体系的标准平衡及反应粒子为单位浓度时,电极反应进行的速率(md/s)。
i°:反应在平衡电势下的电流密度,即有i0=i a=i k②相同点:数值越大,表示该反应的可逆性越强。
不同点:k S与浓度无关,i0与反应体系各种组分的浓度有关。
10. 为什么有机物在电极上的可逆吸附总是发生在一定的电位区间内?答:越正的电势,有机物易被氧化;电势越负,易被还原,因此其可逆吸附发生在平衡电势附近值,即一定的电位区间内。
11. 试说明锂离子电池的正极和负极材料是何物质?为什么其溶剂要用非水有机溶剂?锂离子电池比一般的二次电池具有什么特点?答:①正极:主要是嵌锂化合物,包括三维层状的LiCoQ 丄iNiO 2,三维的TiO?。
负极:主要是碳素材料,如石墨、碳纤维。
②锂遇水反应生成H2, 可能有爆炸的危险,所以要用非水有机溶剂。
③ 特点:工作电压高,比能量高,稳定性好,寿命长,自放电小,无记忆效应,工作温度范围宽,不含有害金属铅、镉,无污染。
12. 何谓电池的放电曲线?从放电曲线可得到那些有关电池性能的信息?答:①放电曲线:在指定负载和温度下放电时,工作电压随时间的变化曲线;②从曲线上可知工作电压、终止电压、开路电压、理论电动势的值,放电平台越长,电池性能越好。
13. 如何得到Eva ns图?从该图可达到那些电化学信息?在一般条件下钢铁发生吸氧腐蚀,说明钢铁腐蚀过程的控制步骤是什么?答:①Evans图即腐蚀极化图,这种图是把表征腐蚀电池的阴、阳极极化曲线画在同一图上而成的②从该图可知极化曲线较陡,表明电极的极化率较大,反应阻力大;反之,反应容易进行。
极化作用使阴阳的电位交于一点,对应电位为腐蚀电位(Ecorr),电流为腐蚀电流(Icorr);金属以此电流不断地腐蚀。
③过程:阴极氧的扩散14. 钢铁腐蚀使用的电化学保护主要有几种?简述它们的基本原理。
答:阳极保护法和阴极保护法。
原理:阳极保护法是把被保护金属变成阳极,用极化的方式使金属钝化,并维持稳定状态,腐蚀速率降低,得以保护。
阴极保护法是提供阴极极化,改变金属表面电子能级结构,使金属电位负移进入免蚀区。
15•两种金属共沉积形成合金的基本条件是什么?如何才能实现合金电沉积?答:①基本条件:析出电位十分相近或相等;② 若析出电位相差较小,可采用改变浓度和改变沉积电流密度;若相差较大,可采用加入络合剂和添加剂。
16. —般金属镀层大多为多晶体,试根据金属电结晶理论,若要得到晶体细小的镀层一般要采用什么措施进行电沉积?答:即抑制核的生长速度,通过增加阴极极化、适当的降低主盐浓度,在较大的电流密度下进行电沉积。
17. 目前氯碱工业阳极广泛使用形稳电极代替石墨,其组成是什么?什么叫形稳电极?答:DSA的组成:以钛为基地,涂镀Ti02、RuO2 加催化剂(Pt、PbO2)。
形稳电极是指电解过程中耐腐蚀、尺寸稳定、寿命长的不溶性阳极。
18. 二次电池要求充放电反应可逆性要好,一般要求电极的结构具备什么特点?试举例说明之。
答:如锂离子电池,电极材料二维层状;自由嵌入、嵌出;体积膨胀率小;尖晶石,三维轨道结构。
19. 镍氢电池(储氢电池)是一种重要的二次电池,该电池正极和负极材料是何物质?写出电池反应。
何谓储氢合金?答:①正极材料:Ni(OH)2;负极:混合稀土氢合金(LaNiH x)或钛镍合金(MH x)。
电池反应:M N Ni5H6+6NiOH M z Ni+6Ni (OH)2储氢合金:在一定条件下可逆的吸收放出H2的新型合金。
20. 海洋性环境下钢铁主要发生电化学腐蚀,其阴极电极反应主要是什么反应?控制步骤是什么?答:①阴极反应为吸氧反应:O2+4H++4e— 2H2O②控制步骤:氧的扩散步骤21. 何谓电解提取?何谓电解精炼?举例说明两者之间的区别?答:①电解提取:直接利用通电的方式提取电解质中的金属。
②电解精炼:利用电解方法将含有金属的物质进行提纯。
③区别:电解提取采用不溶性阳极,如以Pt为电极,电解Al 2O3得到Al ;电解精炼采用可溶性阳极,如以粗铜为阳极,用以精炼.22. 试叙述赫尔槽的结构特点和在电镀中的用途。
答:特点:阴极各个部位与阳极的距离不同,有近端与远端,其电流密度不同。
用途:①确定渡液各组分的合适含量;②确定渡液中添加剂或杂质的大致含量;③可用于选择不同的操作条件,如改变为温度,pH值、电流密度23. 与其它阴极过程相比,金属电沉积有何特点?答:①液相传质,反应粒子向电极表面迁移;② 前置转化,发生化学转化反应;③电荷传递,反应粒子还原为吸附态金属原子;④电结晶,吸附态金属原子形成晶体。
24. 采用钢铁电极以丙稀氰为主要原料电合成己二氰,写出阴极和阳极反应?答:阴极:2CH2=CHCN+2H++2e— NC(CH2)4CN 阳极:H20—20—1/2O2+2H+25. 碱性锌氧化银电池以锌粉为负极,以氧化银粉(Ag20)压制成正极,电解液为饱和了锌酸盐的浓碱溶液试写出其正极反应,负极反应,电池反应。
答:正极:负极:总反应:26. 试述有关化学电源主要性能的概念,如电动势、开路电压、工作电压、截止电压。
答:①电动势E:电池两极在断路且处于可逆平衡状态时两极电势之差。
②开路电压U:电池两极在断路时的稳定电极电势之差。
③工作电压V: 有电流通过外电路时,两极的电势差。
④截止电压:放电时,电压下降到不宜继续放电的最低工作电压。
⑤数值:E>U> V截止电压27. 防止钢铁腐蚀主要措施有?答:①阴极保护法中的外加电流法;②涂防锈漆;③镀上惰性金属镀层;④用缓蚀剂加以保护28. 什么是析氢腐蚀和耗氧腐蚀?答:①析氢腐蚀:以H"还原反应为阴极,生成“ 的过程。
②耗氧腐蚀:消耗O的还原反应为阴极,生成OH或HO的过程。
碱性介质:2HO+2e=H+2OH (析氢)1/2O 2+2e+HO=2OH(耗氧)酸性介质:2H h+2e-=H l (析氢)2H ++1/2Q+2e=HO(耗氧)29. 阴极保护的方法有哪几种,画图并简述一下各种方法,也可举例说明。
答:①外加电流法:在电解质中加入辅助电极,将需要保护的金属基体连接到外电源负极,调节施加电流,从而保护金属。
图示,把阴极极化曲线的电流调到a点,对应的腐蚀电流I corr '即I a 变小,若调制b点,则为0,起到对阴极的保护。
②牺牲阳极法:在金属基体上附上更活泼的金属,构成短路的原电池,活泼金属为阳极,不断溶解,阴极得到保护,例:钢板上镀锌,防止被海水腐蚀。
30. 发生钝化的金属或合金具有的一些特点?有哪几种主要的钝化理论?答:①特点:形成致密氧化膜,隔离腐蚀介质,包括Al。
Cr、Ti。
②理论:成相膜理论和吸附理论。
31. 什么叫缓冲剂,其防蚀机理如何?答:①缓蚀剂:加入到一定介质中能明显抑制金属腐蚀的少量物质。
②机理:形成氧化膜促进钝化;形成沉淀膜;形成吸附膜32. 金属离子还原继而形成结晶层的电结晶一般过程由哪些基本步骤组成及次序?答:①溶液中的离子向电极表面扩散一②电子迁移反应—③失去溶剂化外壳,形成吸附原子—④ 吸附原子经表面扩散,到缺陷等位置一⑤电还原的金属原子聚集,核化—⑥结合到晶格中,核化生长—⑦沉积物的结晶及形态发展31、什么是电解的电流效率和电能效率?两者区别是?n I =n E=区别:电流效率反映副反应的程度大小,电能效率反映能量的利用率32. 简述电解冶金的方法,并说出电解冶金与火法冶金比较有哪些特点?答:①电解治金可分为水溶液电解,熔盐电解,有机溶剂电解。