010-1硫酸标准溶液配置和标定记录
- 格式:docx
- 大小:14.93 KB
- 文档页数:1
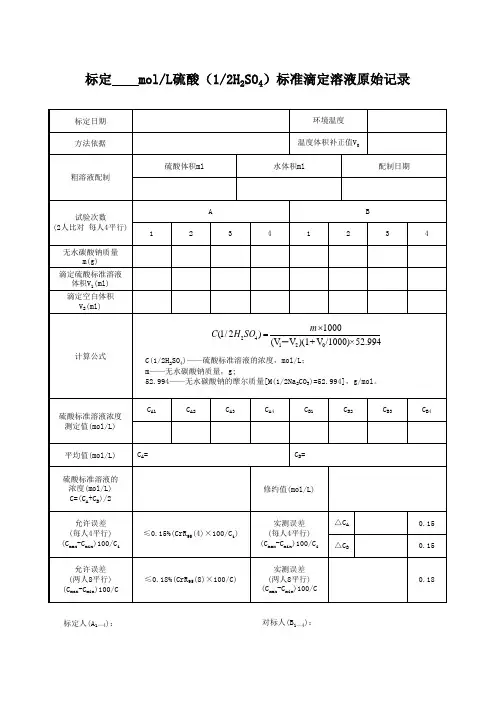
硫酸标准溶液的配制和标定
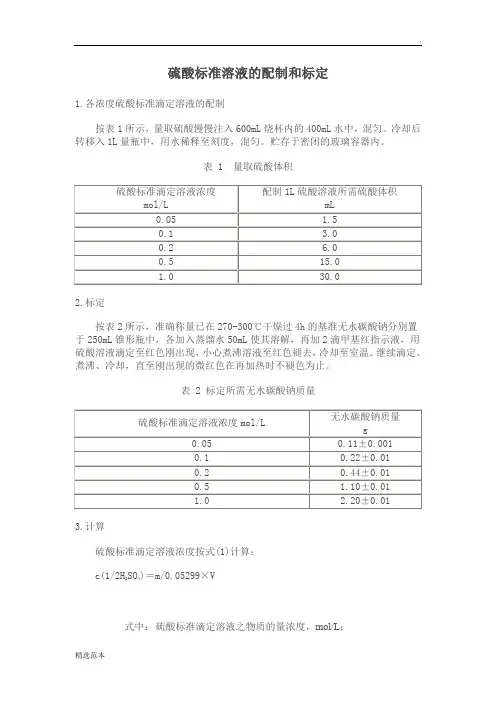
1.各浓度硫酸标准滴定溶液的配制
按表1所示,量取硫酸慢慢注入600mL烧杯内的400mL水中,混匀。
冷却后转移入1L量瓶中,用水稀释至刻度,混匀。
贮存于密闭的玻璃容器内。
表 1 量取硫酸体积
2.标定
按表2所示,准确称量已在270-300℃干燥过4h的基准无水碳酸钠分别置于250mL锥形瓶中,各加入蒸馏水50mL使其溶解,再加2滴甲基红指示液,用硫酸溶液滴定至红色刚出现,小心煮沸溶液至红色褪去,冷却至室温。
继续滴定、煮沸、冷却,直至刚出现的微红色在再加热时不褪色为止。
表 2 标定所需无水碳酸钠质量
3.计算
硫酸标准滴定溶液浓度按式(1)计算:
c(1/2H
2SO
4
)=m/0.05299×V
式中:硫酸标准滴定溶液之物质的量浓度,mol/L;
c(1/2H2SO4)──
m──称量无水碳酸钠质量,g;
V──滴定用去硫酸溶液实际体积,mL;
0.05299──与1.00mL硫酸标准滴定溶液〔c(1/2H2SO4)=1.000mol/L〕相
当的以克表示的无水碳酸钠的质量。
4.精密度
做五次平行测定。
取平行测定的算术平均值为测定结果。
五次平行测定的极差,应小于表3规定的容许差r。
表3 硫酸标准滴定溶液标定的容许差
硫酸标准滴定溶液每月重新标定一次。

硫酸标准溶液的配制和标定国标标题:深度探讨硫酸标准溶液的配制和标定国标一、引言在化学实验中,硫酸标准溶液的配制和标定国标是非常重要的步骤,它涉及到实验数据的准确性和可靠性。
本文将从硫酸标准溶液的概念和意义、配制方法、标定国标的步骤和意义等方面进行深入探讨。
二、硫酸标准溶液的概念和意义硫酸标准溶液是指已知浓度的硫酸溶液,在化学分析和实验中被用作滴定试剂或标定试剂。
配制硫酸标准溶液的目的是为了保证实验数据的准确性和可靠性,因为只有准确的标准溶液才能得到准确的实验结果。
硫酸标准溶液的浓度一般用摩尔浓度表示,其单位为mol/L。
三、硫酸标准溶液的配制方法配制硫酸标准溶液的方法主要包括称量、稀释和混合。
首先需根据所需的浓度和体积计算出所需的硫酸的质量,并用天平称量出相应的硫酸。
然后将硫酸置于容量瓶中,并用去离子水稀释至刻度线。
通过充分混合使得溶液均匀。
在配制过程中,需要注意天平的准确性和容量瓶的清洁程度。
四、硫酸标准溶液的标定国标的步骤和意义标定国标是指用已知浓度和体积的溶液对标准物质进行测定,以确定其溶液的浓度和体积。
标定国标的步骤主要包括称量、定容、逐滴加入、记录终点等。
标定国标的意义在于验证硫酸标准溶液的浓度是否准确,并通过计算修正因子来提高实验数据的准确性。
五、个人观点和理解从事化学实验多年,我深知硫酸标准溶液的配制和标定国标对实验数据的影响。
只有严格按照国家标准的要求进行配制和标定,才能保证实验数据的准确性和可靠性。
在日常工作中,我将充分重视硫酸标准溶液的配制和标定工作,以确保实验数据的科学性和可靠性。
六、总结通过本文的论述,我们可以更深入地了解硫酸标准溶液的配制和标定国标的重要性和方法。
只有认真对待硫酸标准溶液的配制和标定国标,才能保证实验数据的准确性和可靠性,为科学研究和生产提供可靠的数据支持。
在此,我们需要明确硫酸标准溶液配制和标定国标的重要性,并且按照规定的步骤和方法来执行此工作。
只有严格遵守相关规定和要求,才能保证实验数据的可靠性和准确性。

硫酸标准溶液的配制和标定
硫酸标准溶液的配制和标定步骤如下:
1. 准备硫酸和去离子水。
选择高纯度的浓硫酸(约98%)和
去离子水,同时准备精密的量杯、烧瓶和磁力搅拌器等实验装置。
2. 根据所需浓度和体积计算出所需硫酸的量。
例如,要配制
1mol/L的硫酸标准溶液,需将1mol的硫酸加入到1L的去离
子水中。
同时还需注意硫酸的密度,不同浓度的硫酸密度会略有差异。
3. 将所需量的硫酸加入到预先准备好的去离子水中,搅拌均匀,直到硫酸完全溶解。
4. 记录溶液的实际体积和浓度。
使用pH计或酸度计等仪器测
定硫酸标准溶液的pH值或酸度,从而计算出硫酸的浓度。
同
时还需记录溶液的温度和大气压力等实验条件。
5. 根据实际计算的硫酸浓度和体积值,对配制的硫酸标准溶液进行标定,确保浓度值的准确性和可靠性。
需要注意的是,硫酸是一种强酸,在操作过程中要注意安全,避免接触皮肤、吸入气体或者溅入眼睛。
同时还需注意实验室卫生和废弃物的处理。

硫酸标准溶液的配制与标定硫酸标准溶液是化学实验室中常用的一种溶液,用于测定其他物质的浓度,是化学分析中的重要试剂。
正确的配制和标定硫酸标准溶液对于化学实验的准确性和可靠性至关重要。
本文将介绍硫酸标准溶液的配制和标定方法,希望能够对化学实验工作者有所帮助。
1. 配制硫酸标准溶液。
首先,我们需要准备一定质量分数的硫酸溶液作为原料。
将一定质量分数的硫酸溶液定量移入容量瓶中,用去离子水稀释至刻度线,摇匀即得到一定浓度的硫酸溶液。
然后,取适量的硫酸溶液,用去离子水稀释至容量,得到所需浓度的硫酸标准溶液。
2. 标定硫酸标准溶液。
在标定硫酸标准溶液之前,首先要准备好所需的试剂和仪器,包括酚酞指示剂、标定瓶、移液管等。
然后按照标定方法,取适量的硫酸标准溶液放入标定瓶中,加入适量的酚酞指示剂,用氢氧化钠溶液标定至终点,记录所耗用的氢氧化钠溶液的体积。
根据反应方程式,计算出硫酸标准溶液的浓度。
3. 注意事项。
在配制和标定硫酸标准溶液时,需要注意以下几点:(1)实验操作要严格按照标准化学实验操作规程进行,确保实验过程的准确性和可重复性。
(2)所使用的试剂和仪器必须干净,无杂质,以免影响实验结果。
(3)在标定时,要严格控制试剂的用量和反应条件,确保标定结果的准确性。
(4)在配制和标定硫酸标准溶液时,要注意化学品的安全使用,避免发生意外事故。
总之,硫酸标准溶液的配制和标定是化学实验中的重要环节,正确的操作方法和严格的实验控制条件对于实验结果的准确性和可靠性至关重要。
希望本文所介绍的方法能够为化学实验工作者提供一些帮助,确保实验结果的准确性和可靠性。

硫酸的标定实验报告硫酸标准溶液配制与标定硫酸标准溶液配制与标定配制:称取上述规定定量的于270-300℃灼烧至恒重的基准无水碳酸钠,称准至0.0001g。
溶于50ml水中,加10滴溴甲酚绿-甲基红混合指示剂,用配好的硫酸溶液滴定至溶液由绿色变为暗红色,煮沸2min,冷却后继续滴定至溶液再呈暗红色。
同样做空白试验,计算:C(1/2H2SO4)=m/[(V1-V2)*0.05299)]V1--------硫酸之用量,mlV2--------空白试验硫酸之用量,ml0.05299-------于1.0000ml硫酸标准溶液相当的以克表示的无水碳酸钠的质量比较方法:量取30.00-35.00ml上述规定浓度的氢氧化钠标准溶液,加50ml 无二氧化碳的水及2滴酚酞指示剂(10g/l),用配好的硫酸溶液滴定,近终点时加热至80度,继续滴定至溶液呈粉红色。
计算:C(1/2H2SO4)=v1*c1/vV1--------氢氧化钠标准溶液之用量,mlV----------硫酸之用量,mlC1----------氢氧化钠标准溶液之物质的量浓度,mol/l氢氧化钠标准溶液的配制与标定配制:称取100g氢氧化钠,溶于100ml水中,摇匀,注入聚乙烯容器,密闭放置至溶液清亮,用塑料管虹吸下述规定体积的上层清液,注入1000ml无二氧化碳的水称取上述规定的量于105-110℃烘至恒重的基准邻苯二甲酸氢钾,称准至0.0001g。
溶于上述规定体积的无二氧化碳的水中,加2滴酚酞指示剂(10g/l),用配好的氢氧化钠溶液滴定至粉红色,同样作空白试验,计算:C(NaOH)=m/[(V1-V0)*0.2042]V0------(转载于: 写论文网:硫酸的标定实验报告)空白试验氢氧化钠溶液之用量,mlV1------氢氧化钠溶液之用量,ml0.2042-----于1.00ml氢氧化钠标准溶液相当的以克表示的邻苯二甲酸氢钾的质量比较方法:量取30.00-35.00ml上述规定浓度的盐酸标准溶液,加50ml无二氧化碳的水及2滴酚酞指示剂(10g/l),用配好的硫酸溶液滴定,近终点时加热至80度,继续滴定至溶液呈粉红色。
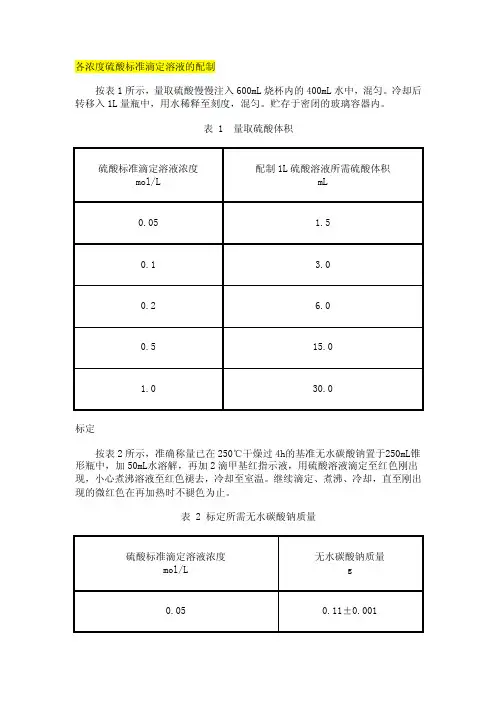
各浓度硫酸标准滴定溶液的配制
按表1所示,量取硫酸慢慢注入600mL烧杯内的400m L水中,混匀。
冷却后转移入1L量瓶中,用水稀释至刻度,混匀。
贮存于密闭的玻璃容器内。
表 1 量取硫酸体积
标定
按表2所示,准确称量已在250℃干燥过4h的基准无水碳酸钠置于250mL锥形瓶中,加50mL水溶解,再加2滴甲基红指示液,用硫酸溶液滴定至红色刚出现,小心煮沸溶液至红色褪去,冷却至室温。
继续滴定、煮沸、冷却,直至刚出现的微红色在再加热时不褪色为止。
表 2 标定所需无水碳酸钠质量
计算
硫酸标准滴定溶液浓度按式(1)计算:
c(1/2H2SO4)=m/0.05299×V (1)
式中:
硫酸标准滴定溶液之物质的量浓度,mol/L;
c(1/2H2SO4)──
m──称量无水碳酸钠质量,g;
V──滴定用去硫酸溶液实际体积,mL;
0.05299──与1.00mL硫酸标准滴定溶液〔c(1/2H2SO4)=1.000mol/L〕相
当的以克表示的无水碳酸钠的质量。
精密度
做五次平行测定。
取平行测定的算术平均值为测定结果。
五次平行测定的极差,应小于表3规定的容许差r。
表3 硫酸标准滴定溶液标定的容许差
稳定性
硫酸标准滴定溶液每月重新标定一次。

硫酸标准溶液的配制和标定1.各浓度硫酸标准滴定溶液的配制按表1所示,量取硫酸慢慢注入600mL烧杯内的400mL水中,混匀。
冷却后转移入1L量瓶中,用水稀释至刻度,混匀。
贮存于密闭的玻璃容器内。
表 1 量取硫酸体积硫酸标准滴定溶液浓度mol/L 配制1L硫酸溶液所需硫酸体积mL0.05 1.50.1 3.00.2 6.00.5 15.01.0 30.02.标定按表2所示,准确称量已在270-300℃干燥过4h的基准无水碳酸钠分别置于250mL锥形瓶中,各加入蒸馏水50mL使其溶解,再加2滴甲基红指示液,用硫酸溶液滴定至红色刚出现,小心煮沸溶液至红色褪去,冷却至室温。
继续滴定、煮沸、冷却,直至刚出现的微红色在再加热时不褪色为止。
表 2 标定所需无水碳酸钠质量硫酸标准滴定溶液浓度mol/L 无水碳酸钠质量g0.05 0.11±0.0010.1 0.22±0.010.2 0.44±0.010.5 1.10±0.011.02.20±0.013.计算硫酸标准滴定溶液浓度按式(1)计算:c(1/2H2SO4)=m/0.05299×V式中:硫酸标准滴定溶液之物质的量浓度,mol/L;c(1/2H2SO4)──m──称量无水碳酸钠质量,g;V──滴定用去硫酸溶液实际体积,mL;0.05299──与1.00mL硫酸标准滴定溶液〔c(1/2H2SO4)=1.000mol/L〕相当的以克表示的无水碳酸钠的质量。
4.精密度做五次平行测定。
取平行测定的算术平均值为测定结果。
五次平行测定的极差,应小于表3规定的容许差r。
表3 硫酸标准滴定溶液标定的容许差c,mol/L 0.05 0.1 0.2 0.5 1.0r,mol/L 0.000 200 0.000 30 0.000 40 0.001 00 0.002 0 硫酸标准滴定溶液每月重新标定一次。
硫酸标准溶液的配制和标定
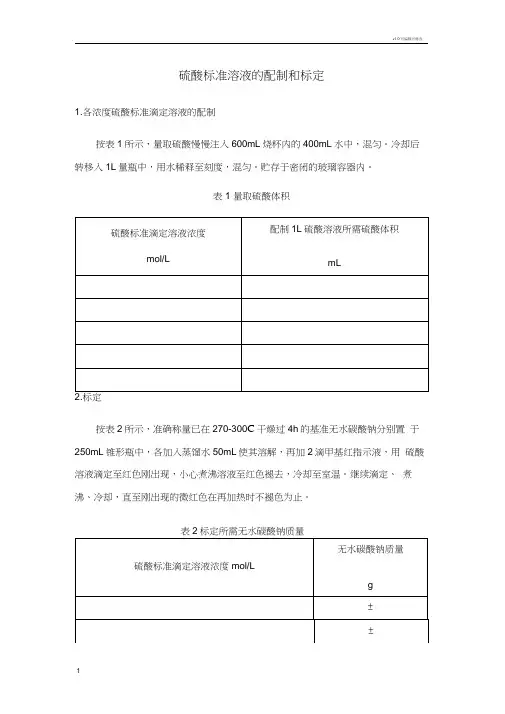
1.各浓度硫酸标准滴定溶液的配制
按表1所示,量取硫酸慢慢注入600mL烧杯内的400mL水中,混匀。
冷却后转移入1L量瓶中,用水稀释至刻度,混匀。
贮存于密闭的玻璃容器内。
表1 量取硫酸体积
按表2所示,准确称量已在270-300C干燥过4h的基准无水碳酸钠分别置于250mL锥形瓶中,各加入蒸馏水50mL使其溶解,再加2滴甲基红指示液,用硫酸溶液滴定至红色刚出现,小心煮沸溶液至红色褪去,冷却至室温。
继续滴定、煮沸、冷却,直至刚出现的微红色在再加热时不褪色为止。
表2标定所需无水碳酸钠质量
硫酸标准滴定溶液浓度按式(1)计算:
c(1/2H 2SQ) = m/xv
式中:硫酸标准滴定溶液之物质的量浓度,mol/L ;
C(1/2H2SG)——
m 称量无水碳酸钠质量,g;
V—滴定用去硫酸溶液实际体积,mL
——与硫酸标准滴定溶液〔C(1/2H2SQ) = L〕相当的以克表示的无水碳酸钠的质量。
4.精密度
做五次平行测定。
取平行测定的算术平均值为测定结果。
五次平行测定的极差,应小于表3规定的容许差r。
表3硫酸标准滴定溶液标定的容许差
硫酸标准滴定溶液每月重新标定一次。
硫酸标准溶液的配制和标定
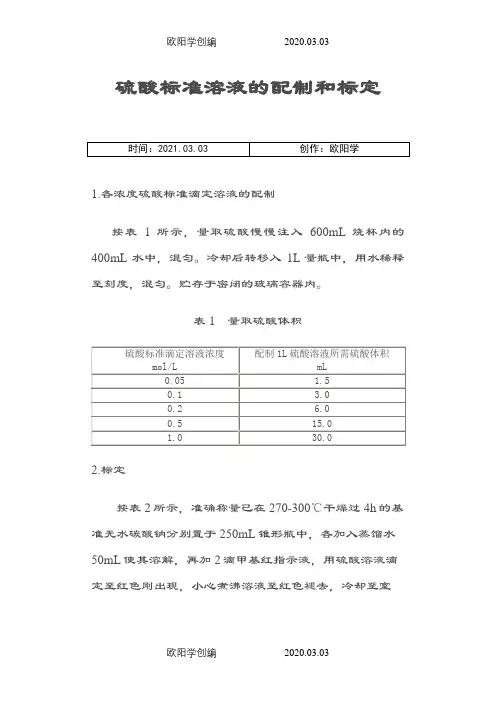
1.各浓度硫酸标准滴定溶液的配制
按表1所示,量取硫酸慢慢注入600mL烧杯内的400mL水中,混匀。
冷却后转移入1L量瓶中,用水稀释至刻度,混匀。
贮存于密闭的玻璃容器内。
表 1量取硫酸体积
2.标定
按表2所示,准确称量已在270-300℃干燥过4h的基准无水碳酸钠分别置于250mL锥形瓶中,各加入蒸馏水50mL使其溶解,再加2滴甲基红指示液,用硫酸溶液滴定至红色刚出现,小心煮沸溶液至红色褪去,冷却至室
温。
继续滴定、煮沸、冷却,直至刚出现的微红色在再加热时不褪色为止。
表 2 标定所需无水碳酸钠质量
3.计算
硫酸标准滴定溶液浓度按式(1)计算:
c(1/2H2SO4)=m/0.05299×V
式中:
硫酸标准滴定溶液之物质的量浓度,mol/L;
c(1/2H2SO4)──
m──称量无水碳酸钠质量,g;
V──滴定用去硫酸溶液实际体积,mL;
0.05299──与1.00mL硫酸标准滴定溶液〔c(1/2H2SO4)=
1.000mol/L〕相当的以克表示的无水碳酸钠的质量。
4.精密度
做五次平行测定。
取平行测定的算术平均值为测定结果。
五次平行测定的极差,应小于表3规定的容许差r。
表3硫酸标准滴定溶液标定的容许差
硫酸标准滴定溶液每月重新标定一次。
硫酸标准溶液的标定
硫酸标准溶液是化学实验中常用的一种溶液,其浓度的准确性
对实验结果具有重要影响。
因此,对硫酸标准溶液进行标定是非常
必要的。
本文将介绍硫酸标准溶液的标定方法及实验步骤。
首先,准备硫酸标准溶液。
在实验室中,通常使用的是
0.1mol/L的硫酸标准溶液。
在准备过程中,需要使用精密天平称取
一定质量的硫酸固体,并溶解于一定体积的去离子水中,最终将其
稀释至所需体积。
在操作过程中,需注意溶解度、稀释倍数等因素,以确保制备出的标准溶液浓度准确。
其次,进行硫酸标准溶液的标定。
标定的目的是确定标准溶液
的准确浓度,一般采用酸碱滴定法。
在标定过程中,需使用已知浓
度的氢氧化钠溶液作为滴定液,通过滴定反应的终点来确定硫酸标
准溶液的浓度。
在操作中,需注意滴定管的使用、滴定终点的判定、滴定过程中溶液的搅拌等因素,以确保标定结果的准确性。
最后,记录实验数据并计算出硫酸标准溶液的准确浓度。
在标
定过程中,需记录滴定液的用量、滴定终点的体积、反应当量等数据,并进行数据处理和计算,最终得出硫酸标准溶液的准确浓度。
在记录和计算过程中,需注意数据的准确性和计算方法的正确性,以确保标定结果的可靠性。
总之,硫酸标准溶液的标定是化学实验中重要的一环,其准确性直接影响到实验结果的可靠性。
在进行标定实验时,需严格按照实验步骤操作,并注意操作细节,以确保标定结果的准确性和可靠性。
希望本文介绍的硫酸标准溶液的标定方法能对实验工作有所帮助。
硫酸标准溶液的配制和标定
1.各浓度硫酸标准滴定溶液的配制
按表1所示,量取硫酸慢慢注入600mL烧杯内的400mL 水中,混匀。
冷却后转移入1L量瓶中,用水稀释至刻度,混匀。
贮存于密闭的玻璃容器内。
表 1 量取硫酸体积
2.标定
按表2所示,准确称量已在270-300℃干燥过4h的基准无水碳酸钠分别置于250mL锥形瓶中,各加入蒸馏水50mL
使其溶解,再加2滴甲基红指示液,用硫酸溶液滴定至红色刚出现,小心煮沸溶液至红色褪去,冷却至室温。
继续滴定、煮沸、冷却,直至刚出现的微红色在再加热时不褪色为止。
表 2 标定所需无水碳酸钠质量
3.计算
硫酸标准滴定溶液浓度按式(1)计算:
c(1/2H2SO4)=m/0.05299×V
式中:
硫酸标准滴定溶液之物质的量浓度,mol/L;
c(1/2H2SO4)──
m──称量无水碳酸钠质量,g;
V──滴定用去硫酸溶液实际体积,mL;
0.05299──与1.00mL硫酸标准滴定溶液〔c(1/2H2SO4)=1.000mol/L〕
相当的以克表示的无水碳酸钠的质量。
4.精密度
做五次平行测定。
取平行测定的算术平均值为测定结果。
五次平行测定的极差,应小于表3规定的容许差r。
表3 硫酸标准滴定溶液标定的容许差
硫酸标准滴定溶液每月重新标定一次。
硫酸标准溶液的标定硫酸标准溶液的标定是化学实验中常见的一项重要工作,它可以用于测定其他物质的浓度和定量分析。
在进行硫酸标准溶液的标定时,需要严格按照标定方法进行操作,以确保标定结果的准确性和可靠性。
下面将介绍硫酸标准溶液的标定方法及实验步骤。
首先,准备好所需的实验器材和试剂,包括天平、容量瓶、移液管、PH计、硫酸、指示剂等。
然后按照以下步骤进行硫酸标准溶液的标定:1. 称取一定质量的硫酸固体,溶解于一定体积的去离子水中,得到一定浓度的硫酸溶液。
2. 取一定体积的硫酸溶液,加入适量的指示剂,通常使用酚酞或甲基橙作为指示剂。
3. 使用标定管或移液管向硫酸溶液中滴加氢氧化钠溶液,直至溶液呈现颜色转变。
根据颜色变化的终点,确定滴定终点。
4. 记录滴定所需的氢氧化钠溶液体积V(ml)。
5. 根据滴定方程式,计算出硫酸的浓度C(mol/L)。
在进行硫酸标准溶液的标定时,需要注意以下几点:1. 实验操作要严格按照标定方法进行,避免操作失误对标定结果造成影响。
2. 实验器材和试剂要保持干净,避免杂质的影响。
3. 在滴定过程中,要缓慢滴加氢氧化钠溶液,直至出现颜色转变,避免过量滴定造成误差。
4. 滴定前后要对实验数据进行记录和核对,确保数据的准确性。
5. 根据实验结果计算出硫酸的浓度,并进行数据处理和分析,得出最终的标定结果。
通过以上步骤和注意事项,我们可以完成硫酸标准溶液的标定工作,得到准确可靠的标定结果。
硫酸标准溶液的标定是化学实验中重要的一环,它对于化学分析和定量分析具有重要意义,因此在进行标定时需要严格按照标定方法进行操作,以确保实验结果的准确性和可靠性。
硫酸标准溶液的标定硫酸标准溶液的标定是化学实验中常见的一项重要操作,它是为了确定硫酸溶液的确切浓度,以便在实验中准确地进行配制和使用。
硫酸标准溶液的标定需要严格按照实验步骤进行,下面将详细介绍硫酸标准溶液的标定方法。
首先,准备好所需的实验器材和试剂。
实验器材包括天平、烧杯、移液管、容量瓶等,试剂包括硫酸溶液、指示剂等。
其次,按照一定比例将已知浓度的硫酸溶液定量移入容量瓶中。
在移液管的帮助下,将硫酸溶液缓慢地加入容量瓶中,直至接近刻度线。
然后,使用滴定管逐滴加入指示剂,直至出现颜色变化。
接着,利用标定瓶配制出一定浓度的氢氧化钠溶液。
将已知浓度的氢氧化钠溶液定量移入容量瓶中,同样使用滴定管逐滴加入指示剂,直至出现颜色变化。
然后,进行滴定操作。
将已标定好的氢氧化钠溶液滴定到硫酸溶液中,直至出现颜色变化。
记录滴定前后的体积差值,并根据滴定方程式计算出硫酸溶液的浓度。
最后,进行数据处理和结果分析。
根据实验数据计算出硫酸溶液的准确浓度,并进行误差分析,以确定实验结果的可靠性。
在进行硫酸标准溶液的标定时,需要注意以下几点,一是实验操作要准确无误,避免因操作失误导致实验结果的偏差;二是实验器材要清洁干净,以免杂质影响实验结果;三是实验过程中要注意安全,避免发生意外。
总之,硫酸标准溶液的标定是一项重要的化学实验操作,它需要严格按照实验步骤进行,并且要注意实验操作的准确性和安全性。
只有通过严谨的实验操作和准确的数据处理,才能得到可靠的实验结果,为后续实验工作提供准确的数据支持。
硫酸标准溶液的配制和标定
1.各浓度硫酸标准滴定溶液的配制
按表1所示,量取硫酸慢慢注入600mL烧杯内的400mL水中,混匀。
冷却后转移入1L量瓶中,用水稀释至刻度,混匀。
贮存于密闭的玻璃容器内。
表 1 量取硫酸体积
2.标定
按表2所示,准确称量已在270-300℃干燥过4h的基准无水碳酸钠分别置于250mL锥形瓶中,各加入蒸馏水50mL使其溶解,再加2滴甲基红指示液,用硫酸溶液滴定至红色刚出现,小心煮沸溶液至红色褪去,冷却至室温。
继续滴定、煮沸、冷却,直至刚出现的微红色在再加热时不褪色为止。
表 2 标定所需无水碳酸钠质量
3.计算
硫酸标准滴定溶液浓度按式(1)计算:
c(1/2H
2SO
4
)=m/0.05299×V
式中:
c(1/2H2SO4)──
硫酸标准滴定溶液之物质的量浓度,mol/L;
m──称量无水碳酸钠质量,g;
V──滴定用去硫酸溶液实际体积,mL;
0.05299──与1.00mL硫酸标准滴定溶液〔c(1/2H2SO4)=1.000mol/L〕相
当的以克表示的无水碳酸钠的质量。
4.精密度
做五次平行测定。
取平行测定的算术平均值为测定结果。
五次平行测定的极差,应小于表3规定的容许差r。
表3 硫酸标准滴定溶液标定的容许差
硫酸标准滴定溶液每月重新标定一次。
硫酸标准溶液配制与标定配制:称取上述规定定量的于270-300℃灼烧至恒重的基准无水碳酸钠,称准至0.0001g。
溶于50ml水中,加10滴溴甲酚绿-甲基红混合指示剂,用配好的硫酸溶液滴定至溶液由绿色变为暗红色,煮沸2min,冷却后继续滴定至溶液再呈暗红色。
同样做空白试验,计算:C(1/2H2SO4)=m/[(V1-V2)*0.05299)]V1--------硫酸之用量,mlV2--------空白试验硫酸之用量,ml0.05299-------于1.0000ml硫酸标准溶液相当的以克表示的无水碳酸钠的质量比较方法:量取30.00-35.00ml上述规定浓度的氢氧化钠标准溶液,加50ml无二氧化碳的水及2滴酚酞指示剂(10g/l),用配好的硫酸溶液滴定,近终点时加热至80度,继续滴定至溶液呈粉红色。
计算:C(1/2H2SO4)=v1*c1/vV1--------氢氧化钠标准溶液之用量,mlV----------硫酸之用量,mlC1----------氢氧化钠标准溶液之物质的量浓度,mol/l氢氧化钠标准溶液的配制与标定配制:称取100g氢氧化钠,溶于100ml水中,摇匀,注入聚乙烯容器,密闭放置至溶液清亮,用塑料管虹吸下述规定体积的上层清液,注入1000ml无二氧化碳的水称取上述规定的量于105-110℃烘至恒重的基准邻苯二甲酸氢钾,称准至0.0001g。
溶于上述规定体积的无二氧化碳的水中,加2滴酚酞指示剂(10g/l),用配好的氢氧化钠溶液滴定至粉红色,同样作空白试验,计算:C(NaOH)=m/[(V1-V0)*0.2042]V0------空白试验氢氧化钠溶液之用量,mlV1------氢氧化钠溶液之用量,ml0.2042-----于1.00ml氢氧化钠标准溶液相当的以克表示的邻苯二甲酸氢钾的质量比较方法:量取30.00-35.00ml上述规定浓度的盐酸标准溶液,加50ml无二氧化碳的水及2滴酚酞指示剂(10g/l),用配好的硫酸溶液滴定,近终点时加热至80度,继续滴定至溶液呈粉红色。