基础有机化学反应总结【2020年】
- 格式:doc
- 大小:3.18 MB
- 文档页数:82
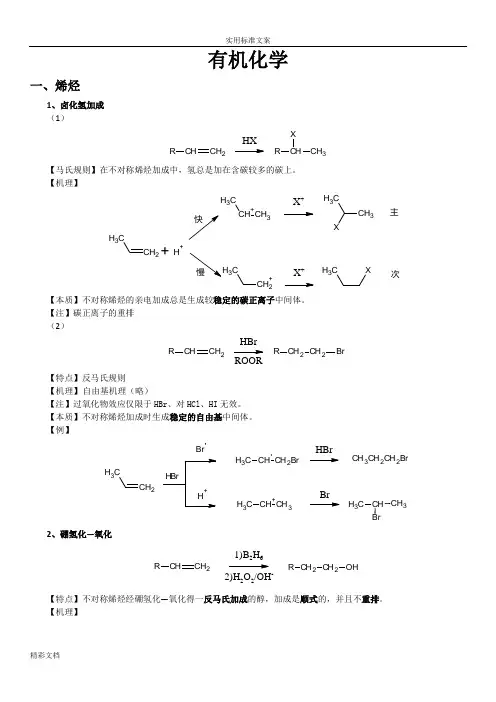
有机化学一、烯烃1、卤化氢加成 (1)CHCH 2RHXCH CH 3RX【马氏规则】在不对称烯烃加成中,氢总是加在含碳较多的碳上。
【机理】CH 2CH 3CH +CH 3CH 3X +CH 3CH 3+H +CH 2+C3X +CH 3X主次【本质】不对称烯烃的亲电加成总是生成较稳定的碳正离子中间体。
【注】碳正离子的重排 (2)CHCH 2RCH 2CH 2R BrHBrROOR【特点】反马氏规则 【机理】 自由基机理(略)【注】过氧化物效应仅限于HBr 、对HCl 、HI 无效。
【本质】不对称烯烃加成时生成稳定的自由基中间体。
【例】CH 2CH3BrCH CH 2BrC H 3CH +CH 3C H 3HBrBrCH 3CH 2CH 2BrCH CH 3C H 32、硼氢化—氧化CHCH 2R CH 2CH 2R OH1)B 2H 62)H 2O 2/OH-【特点】不对称烯烃经硼氢化—氧化得一反马氏加成的醇,加成是顺式的,并且不重排。
【机理】2CH33H323H32CH CH2CH32CH CH=CH(CH3CH2CH2)3-H3CH2CH2C22CH3CH2OCH2CH2CH33CH2CH2C2CH2CH3+O H-OHB-OCH2CH2CH3CH2CH2CH3H3CH2CH2B OCH2CH2CH3CH2CH2CH32CH2CH3HOO-B(OCH2CH2CH3)3B(OCH2CH2CH3)3+3NaOH3NaOH3HOCH2CH2CH33+Na3BO32【例】CH31)BH32)H2O2/OH-CH3HHOH3、X2加成C CBr/CClC CBrBr【机理】CCC CBrBrCBr+C CBrOH2+-H+C CBrOH【注】通过机理可以看出,反应先形成三元环的溴鎓正离子,然后亲和试剂进攻从背面进攻,不难看出是反式加成。
不对称的烯烃,亲核试剂进攻主要取决于空间效应。
【特点】反式加成 4、烯烃的氧化1)稀冷高锰酸钾氧化成邻二醇。

⼤学有机化学⼈名反应总结有机化学⼀、烯烃1、卤化氢加成(1)【马⽒规则】在不对称烯烃加成中,氢总是加在含碳较多的碳上。
【机理】【本质】不对称烯烃的亲电加成总是⽣成较稳定的碳正离⼦中间体。
【注】碳正离⼦的重排(2)【特点】反马⽒规则【机理】⾃由基机理(略)【注】过氧化物效应仅限于HBr 、对HCl 、HI ⽆效。
【本质】不对称烯烃加成时⽣成稳定的⾃由基中间体。
【例】2、硼氢化—氧化【特点】不对称烯烃经硼氢化—氧化得⼀反马⽒加成的醇,加成是顺式的,并且不重排。
【机理】【例】 3、X 2加成【机理】【注】通过机理可以看出,反应先形成三元环的溴鎓正离⼦,然后亲和试剂进攻从背⾯进攻,不难看出是反式加成。
不对称的烯烃,亲核试剂进攻主要取决于空间效应。
【特点】反式加成 4、烯烃的氧化1)稀冷⾼锰酸钾氧化成邻⼆醇。
3H 33H3稀冷KMnO433M n OOH 2O 3H 33H 3 2)热浓酸性⾼锰酸钾氧化3)臭氧氧化 4)过氧酸氧化 5、烯烃的复分解反应【例】 6、共轭⼆烯烃 1)卤化氢加成2)狄尔斯-阿德尔(Diels-Alder )反应【描述】共轭⼆烯烃和烯烃在加热的条件下很容易⽣成环状的1,4加成产物。
【例】⼆、脂环烃1、环丙烷的化学反应【描述】三元环由于张⼒⽽不稳定,易发⽣加成反应开环,类似碳碳双键。
【特点】环烷烃都有抗氧化性,可⽤于区分不饱和化合物。
【注】遵循马⽒规则【例】2、环烷烃制备1)武兹(Wurtz)反应【描述】通过碱⾦属脱去卤素,制备环烷烃。
【例】2)卡宾①卡宾的⽣成A、多卤代物的α消除B、由某些双键化合物的分解②卡宾与烯烃的加成反应【特点】顺式加成,构型保持【例】③类卡宾【描述】类卡宾是⼀类在反应中能起到卡宾作⽤的⾮卡宾类化合物,最常⽤的类卡宾是ICH2ZnI。
【特点】顺式加成,构型保持【例】三、炔烃1、还原成烯烃1)、顺式加成2)、反式加成2、亲电加成1)、加X2【机理】中间体Br+R2 R1【特点】反式加成2)、加HXRRHBr R Br(⼀摩尔的卤化氢主要为反式加成)3)、加H2O【机理】【特点】炔烃⽔合符合马式规则。

大学化学有机反应知识点归纳总结一、酯化反应酯化反应是有机化学中常见的一类反应,通过酸催化或酶催化,酸酐和醇经过酯键的形成得到酯。
酯化反应一般可分为缩水醛酸酯化反应和缩水醇酸酯化反应两种。
二、加成反应加成反应是反应物中的两个分子结合在一起,形成一个新的分子。
常见的有机加成反应有烯烃的加氢、烯烃的加烃、烷烃的卤素化等。
三、醇的氧化反应醇的氧化反应是将醇氧化为酮或醛的反应。
常用的氧化剂有酸性高碘酸钾、酸性高锰酸钾等。
醇的氧化反应可根据氧化程度分为完全氧化和不完全氧化两种。
四、取代反应取代反应是指有机化合物中的一个原子或基团被另一个原子或基团所取代的反应。
常见的取代反应有卤代烃的取代反应、芳香族化合物的取代反应等。
五、缩合反应缩合反应是指两个或多个分子结合在一起生成一个较大的分子。
常见的缩合反应有醛和胺的缩合反应、葡萄糖和果糖的缩合反应等。
六、醛醇互变反应醛醇互变反应是指醇与醛之间可以相互转化的反应。
常见的醛醇互变反应有醇缩醛反应和醛缩醇反应。
七、重排反应重排反应是指在有机分子结构中,原子或基团的位置发生改变,但分子中的原子数量保持不变的反应。
常见的重排反应有醇的重排反应、酯的重排反应等。
八、裂解反应裂解反应是指有机分子中的键发生断裂,从一个分子裂解为两个或多个新的分子。
常见的裂解反应有烷烃的裂解反应、醇的裂解反应等。
九、加成裂解反应加成裂解反应是指有机分子中的化学键同时发生断裂和新键的形成。
常见的加成裂解反应有醇的加成裂解反应、双键加成裂解反应等。
十、亲核取代反应亲核取代反应是指分子中的一个亲核试剂取代了原有分子中的一个基团的反应。
常见的亲核取代反应有卤代烃的亲核取代反应、醇的亲核取代反应等。
总结:大学化学中的有机反应涵盖了酯化反应、加成反应、醇的氧化反应、取代反应、缩合反应、醛醇互变反应、重排反应、裂解反应、加成裂解反应和亲核取代反应等多个知识点。
这些反应在有机合成和有机化学研究中扮演着重要的角色,对于理解有机化学反应机理和设计合成路线具有重要意义。

有机化学反应类型总结有机化学反应类型总结1、?取代反应(1)能发生取代反应的官能团有:醇羟基(-OH)、卤原子(-X)、羧基(-COOH)、酯基(-COO-)、肽键(-CONH-)等。
(2)能发生取代反应的有机物种类如下图所示:加成反应1.能发生加成反应的官能团:双键、三键、苯环、羰基(醛、酮)等。
2.加成反应有两个特点:反应发生在不饱和的键上,不饱和键中不稳定的共价键断裂,然后不饱和原子与其它原子或原子团以共价键结合。
加成反应后生成物只有一种(不同于取代反应)。
说明:1.羧基和酯基中的碳氧双键不能发生加成反应。
2.醛、酮的羰基只能与H2发生加成反应。
3.共轭二烯有两种不同的加成形式。
3、消去反应(1)能发生消去反应的物质:醇、卤代烃;能发生消去反应的官能团有:醇羟基、卤素原子。
(2)反应机理:相邻消去发生消去反应,必须是与羟基或卤素原子直接相连的碳原子的邻位碳上必须有氢原子,否则不能发生消去反应。
如CH3OH,没有邻位碳原子,不能发生消去反应。
4、聚合反应(1)加聚反应:烯烃加聚的基本规律:(2)缩聚反应:(1)二元羧酸和二元醇的缩聚,如合成聚酯纤维:(2)醇酸的酯化缩聚:(3)氨基与羧基的缩聚(1)氨基酸的缩聚,如合成聚酰胺6:(2)二元羧酸和二元胺的缩聚:nHOOC-(CH2)4-COOH+nNH2(CH2)6NH2=[CO(CH2)4CONH(CH2)6NH]n+2nH2O5、氧化反应与还原反应1.氧化反应就是有机物分子里“加氧”或“去氢”的反应。
能发生氧化反应的物质和官能团:烯(碳碳双键)、醇、酚、苯的同系物、含醛基的物质等。
烯(碳碳双键)、炔(碳碳叁键)、苯的同系物的氧化反应都主要指的是它们能够使酸性高锰酸钾溶液褪色,被酸性高锰酸钾溶液所氧化。
含醛基的物质(包括醛、甲酸、甲酸盐、甲酸酯、葡萄糖、麦芽糖等)的氧化反应,指银镜反应及这些物质与新制氢氧化铜悬浊液的反应。
要注意把握这类反应中官能团的变化及化学方程式的基本形式2.还原反应是有机物分子里“加氢”或“去氧”的反应,其中加氢反应又属加成反应。

化学有机化学反应知识点清单与总结题型总结技巧在学习有机化学反应时,掌握反应的知识点和总结题型的技巧非常重要。
有机化学反应知识点清单和总结题型的技巧可以帮助我们更好地理解和应用有机化学反应。
一、有机化学反应知识点清单1. 加成反应:双键或三键断裂,两个或多个原子或官能团结合形成新化合物。
2. 氧化还原反应:涉及电子转移,氧化剂接受电子,还原剂失去电子。
3. 消除反应:双键或三键的形成,同时断开化学键。
4. 取代反应:氢或其他官能团在有机化合物中被另一官能团取代。
5. 还原反应:还原剂将有机化合物还原成较低的氧化态。
6. 加氢反应:氢气加到有机化合物上,生成相应的饱和化合物。
7. 氢解反应:有机化合物在加热或加压的条件下被氢气分解为较低的烃。
8. 缩合反应:两个或多个分子结合成大分子。
二、总结题型总结技巧1. 反应类型判断题在解答题目时,首先要根据反应物和产物之间的化学键的形成和断裂来判断反应类型。
加成反应时,会有新的化学键形成;消除反应时,会有化学键断裂;取代反应时,会有官能团的替换等。
2. 题目理解和分析在阅读题目时,要仔细理解题目的要求,明确所给条件,然后分析并比较反应特性,最后确定所需的性质或化合物。
3. 分析反应机理在解答有机化学反应机理题时,根据反应条件和反应物的结构,可以通过分析反应的步骤来确定反应机理。
从中间产物和过渡态中推断出反应物和产物的关系。
4. 反应规律总结在解答有机化学反应题时,要将题目中出现的关键知识点进行总结,归纳反应规律和特点。
通过积累和总结,可以更好地理解和应用有机化学反应。
5. 反应机制推导在某些有机化学反应中,需要根据实验结果推导出反应的机制。
通过分析起始物质和中间产物之间的关系,根据反应过程中的原子和官能团重新组合来推导反应机制。
6. 反应方程式书写解答有机化学反应题目时,要注意书写离子和官能团的正负电荷,并准确无误地书写反应物和产物,以避免混淆和错误。
总结:有机化学反应知识点清单和总结题型的技巧对于学习和应用有机化学反应非常重要。

大学有机化学反应总结1. 引言大学有机化学是化学专业中的重要课程之一,也是学习有机化学基础知识和反应机理的关键。
本文旨在对大学有机化学中常见的反应进行总结和归纳,以便帮助学生更好地掌握和理解这些反应。
2. 化学键的类型在有机化学中,化学键的类型决定了分子的性质和反应的发生。
常见的化学键类型包括:•单键:共享一对电子,如碳-碳单键(C-C)和碳-氢单键(C-H)。
•双键:共享两对电子,如碳-碳双键(C=C)和碳-氧双键(C=O)。
•三键:共享三对电子,如碳-碳三键(C≡C)和碳-氮三键(C≡N)。
3. 有机反应的类型有机反应可以根据不同的变化和转化方式进行分类。
以下是几种常见的有机反应类型:3.1 取代反应取代反应是指一个原子或官能团被另一个原子或官能团代替的反应。
常见的取代反应包括卤代烃的取代反应和醇的酸碱反应。
3.1.1 卤代烃的取代反应卤代烃的取代反应常见的机理有亲核取代和电子亲合取代。
其中,亲核取代是指亲核试剂攻击卤代烃的卤素原子,如氯离子(Cl-)。
电子亲合取代是指电子亲和试剂攻击卤代烃的电子丰富部位。
3.1.2 醇的酸碱反应醇的酸碱反应是指醇与酸或碱反应生成相应的酯或盐。
这类反应常用于有机合成中,例如酯化反应和醇的酸催化裂解。
3.2 加成反应加成反应是指两个或更多的分子结合在一起形成一个新的分子的反应。
常见的加成反应包括烯烃的加成反应和醛/酮的加成反应。
3.2.1 烯烃的加成反应烯烃的加成反应是指烯烃分子中的双键和其他物质发生加成反应,生成环烷化合物或其他加成产物。
3.2.2 醛/酮的加成反应醛/酮的加成反应是指醛或酮分子的羰基与其他物质的亲电试剂发生加成反应,生成醇或其他加成产物。
3.3 消除反应消除反应是指一个分子中的两个官能团结合成一个较大的官能团并释放一个小分子的反应。
常见的消除反应包括脱水反应和脱酸反应。
3.3.1 脱水反应脱水反应是指通过除去水分子来形成双键或环状结构的反应。
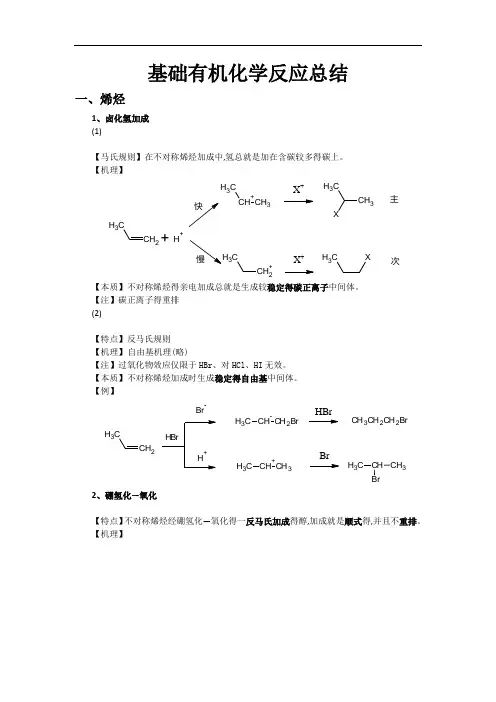
基础有机化学反应总结一、烯烃1、卤化氢加成 (1)【马氏规则】在不对称烯烃加成中,氢总就是加在含碳较多得碳上。
【机理】CH 2CH 3+CH 3CH 3X +CH 3CH 3+H +CH 2+C3X +CH 3X主次【本质】不对称烯烃得亲电加成总就是生成较稳定得碳正离子中间体。
【注】碳正离子得重排 (2)【特点】反马氏规则 【机理】 自由基机理(略)【注】过氧化物效应仅限于HBr 、对HCl 、HI 无效。
【本质】不对称烯烃加成时生成稳定得自由基中间体。
【例】CH 2CH3BrCH CH 2BrC H 3CH +CH 3C H 3HBrBrCH 3CH 2CH 2BrCH CH 3C H 32、硼氢化—氧化【特点】不对称烯烃经硼氢化—氧化得一反马氏加成得醇,加成就是顺式得,并且不重排。
【机理】2CH 33H 323H 32CH CH 2CH 3HBH 2CH CH=CH (CH 3CH 2CH 2)3-H 3CH 2CH 2C22CH 3CH 2OCH2CH 2CH 3H 3CH 2CH 2C2CH 2CH 3+OH -OHB-OCH 2CH 2CH 3CH 2CH 2CH 3H 3CH 2CH 2CBOCH 2CH 2CH 3CH 2CH 2CH 32CH 2CH 3HOO -B(OCH 2CH 2CH 3)3B(OCH 2CH 2CH 3)3+3NaOH 3NaOH3HOCH 2CH 2CH 33+Na 3BO 32【例】3、X 2加成【机理】CCCC Br BrCBr +CC Br OH 2+-H +CC Br OH【注】通过机理可以瞧出,反应先形成三元环得溴鎓正离子,然后亲与试剂进攻从背面进攻,不难瞧出就是反式加成。
不对称得烯烃,亲核试剂进攻主要取决于空间效应。
【特点】反式加成 4、烯烃得氧化1)稀冷高锰酸钾氧化成邻二醇。
3H 33H3稀冷KMnO433M n O OO H 2O 3H 33H 3 2)热浓酸性高锰酸钾氧化C C H R R 2R 1KMnO 4H+CRR 1O +R 2CO3)臭氧氧化4)过氧酸氧化5、烯烃得复分解反应【例】OC H 22C 6H 5OC 6H5+C H 2CH 26、共轭二烯烃 1)卤化氢加成CH CH 2HXCH 3XCH 2CH 3X高温1,4加成为主低温1,2加成为主2)狄尔斯-阿德尔(Diels-Alder)反应【描述】共轭二烯烃与烯烃在加热得条件下很容易生成环状得1,4加成产物。

有机化学反应机理总结有机化学反应机理是有机化学研究的重要内容之一,它揭示了有机化合物在反应过程中的分子结构变化和反应速率规律。
通过对有机反应机理的研究,我们可以更好地理解和预测有机化学反应的发生过程,为有机合成化学和药物设计提供理论依据。
下面我们将对常见的有机化学反应机理进行总结和归纳。
1. 加成反应。
加成反应是有机化学中最基本的反应类型之一,它是指两个或多个单体分子中的双键或三键断裂,然后原子或原子团以共价键的方式结合形成新的分子。
加成反应可分为电子亲和性和电子排斥性两种机理。
电子亲和性加成反应是指亲电试剂攻击双键或三键,形成中间离子,最后被亲核试剂攻击生成产物。
电子排斥性加成反应是指亲核试剂攻击双键或三键,生成中间离子,然后被亲电试剂攻击生成产物。
2. 消除反应。
消除反应是有机化学中另一种重要的反应类型,它是指有机分子中的两个邻近原子或原子团通过共价键的方式脱离分子,生成双键或三键。
消除反应可分为β-消除、α-消除和γ-消除等不同机理,其中最常见的是β-消除反应。
β-消除反应是指邻位原子或原子团与相邻的氢原子脱离,生成双键或三键。
3. 取代反应。
取代反应是有机化学中最常见的反应类型之一,它是指有机分子中的一个原子或原子团被另一个原子或原子团取代。
取代反应可分为亲核取代和亲电取代两种机理。
亲核取代是指亲核试剂攻击有机分子中的一个原子或原子团,将其取代生成新的产物。
亲电取代是指亲电试剂攻击有机分子中的一个原子或原子团,将其取代生成新的产物。
4. 加成-消除反应。
加成-消除反应是一种复合反应类型,它是指有机分子中的双键或三键发生加成反应生成中间产物,然后再发生消除反应生成最终产物。
加成-消除反应的机理比较复杂,通常需要通过实验数据和理论计算来揭示其反应过程和产物结构。
总的来说,有机化学反应机理的研究对于我们理解和掌握有机反应规律具有重要意义。
通过深入学习和掌握有机反应机理,我们可以更好地设计和优化有机合成路线,提高有机合成的效率和选择性,为新药物的研发和合成提供理论指导。

有机化学基础知识点归纳总结6篇第1篇示例:有机化学是研究有机物的组成、结构、性质、变化规律和合成方法的科学。
有机化学基础知识是理解和掌握整个有机化学体系的基础,是有机化学学习的重要环节。
接下来,我们将对有机化学基础知识点进行归纳总结,帮助大家更好地理解和掌握这一重要学科。
一、有机物的命名有机物的命名是有机化学的基础,也是有机化学学习的第一步。
有机物的命名方法繁多,常见的包括IUPAC命名法、通用命名法和结构式命名法等。
IUPAC命名法是最为严谨和规范的命名方法,它遵循一定的命名规则,能够准确地标识出有机物的结构和性质。
有机物的结构包括分子式、结构式和空间构型等。
分子式表明了有机物中各种元素的种类和原子数目,结构式则表明了有机物分子中各原子的连接方式和空间位置,空间构型则描述了有机物分子的立体结构和立体构型。
掌握有机物的结构对于理解其性质和反应具有重要意义。
有机物具有多种多样的性质,包括物理性质和化学性质。
物理性质包括熔点、沸点、溶解度等,化学性质包括燃烧、氧化、还原、加成、消除等。
不同的有机物具有不同的性质,这些性质决定了有机物在自然界中的存在形式和化学行为。
有机化学是一个极为重要的合成化学领域,合成有机化合物是有机化学的核心内容之一。
有机物的合成方法繁多,包括物质合成法、加成反应、消除反应、取代反应、氧化还原反应等。
掌握有机物的合成方法对于有机化学的学习具有至关重要的意义。
六、有机物的衍生物有机物的衍生物是指通过对原有有机物进行化学反应得到的新化合物。
有机物的衍生物包括同分异构体、立体异构体、环化合物、功能化合物等。
了解有机物的衍生物对于理解有机化学的结构和性质具有重要意义。
有机物在生活和工业生产中具有广泛的应用,包括医药、农药、染料、塑料、涂料、合成纤维等。
了解有机物的应用对于学习有机化学的意义重大,它能够帮助我们更好地理解和应用有机化学知识。
第2篇示例:有机化学是化学的重要分支之一,研究碳元素及其化合物的结构、性质、反应等规律。

有机化学反应知识点总结1.烷烃●氧化●自动氧化●燃烧●异构化●热裂●卤化自由基反应●硝化●磺化氯磺化2.环烷烃●与卤素●自由基取代●加成离子型●与HX●催化加氢●不被氧化3.烯烃●催化氢化顺式加成●亲电加成●卤素环鎓离子中间体反式加成●次卤酸环鎓离子中间体马氏规则●氢卤酸碳正离子中间体(顺反加成,重排)马氏规则反马氏规则●硫酸,水,有机酸,醇,酚碳正离子●硼氢化四中心过渡态→顺式加成 B进攻小空阻→反马氏●氧化(H2O2/OH-/H2O)→醇●还原→烷烃●羟汞化-脱汞Hg(OCOCH3)2,NaBH4 马氏规则●自由基加成HBr 过氧化物 hv●氧化●环氧化-开环→反式邻二醇有机过酸酸/碱●高锰酸钾●稀、冷→顺式邻二醇●酸/碱、加热→氧化裂解●四氧化锇→顺式邻二醇●臭氧化-水解●O3●水解●还原水解→醛/酮Zn/H2O;CH3SCH3;H2/Pd;LiAlH4;NaBH4●α-H卤化自由基取代烯丙位自由基稳定●X2 500-600℃/hv●NBS/NCS●与卡宾反应●单线态卡宾●三线态卡宾●类卡宾●加聚反应4.炔烃●末端炔氢酸性●NaNH2/NH3(i)得到亲核试剂: RX C=O●[Ag(NH3)2]+HCl HNO3 CN-/H2O 还原提纯●[Cu(NH3)2]+●亲电加成●卤素反式(环正离子中间体),马氏规则●HX顺/反式(碳正离子中间体),两侧均为R时反式;马氏规则●H2O马氏规则,烯醇式互变酮式●H2SO4 H3PO4催化碳正离子中间体●Hg2+/H+催化汞鎓离子中间体●硼氢化●氧化H2O2/OH-顺式水合,反马氏●还原●自由基加成过氧化物(链引发剂)●亲核加成端炔C,碳负离子中间体●HCN●活泼氢-OH,-SH,-NH2,=NH,-CONH2,-COOH●还原●催化加氢●强还原剂Pd,Pt,Ni●弱还原剂顺式加成●Lindlar催化剂(Pd-CaCO3-PbO)●Pd-BaSO4,吡啶●碱金属与液氨反式加成●氢化锂铝反式加成●氧化→-COOH●KMnO4●O3/H2O2/Hg2+●聚合●链●环三聚成苯 #5.共轭烯烃●亲电加成●1,2-加成动力学●1,4-加成热力学●Diels-Alder反应周环反应,Δ,可逆给电子基双烯体+吸电子基亲双烯体优亲双烯体顺反构型保持内型产物优先产物取代基邻对位优●聚合反应6.苯●亲电取代定位效应:给诱,吸诱,给共,吸共,卤素加成-消除机理●硝化反应HNO3/H2SO4=1:2●卤化反应X2/Lewis酸 F2,I2特殊反应●磺化反应浓硫酸,发烟硫酸弱酸恢复●Friedel-Crafts反应●傅-克烷基化碳正离子重排多烷基化可逆●RX/AlCl3●RCH=CH2/H+●ROH/HF●傅-克酰基化不可逆,无重排,无多元●RCOCL/AlCl3●(RCO)2O/AlCl3●RCOOH/H2SO4●Blanc氯甲基化HCHO/HCl/无水ZnCl2●Gattermann-Koch反应→芳醛Lewis酸,加压CuCl,CO/HCl(1:1)●还原反应●催化氢化H2,Pt Pd Ni Ru Rb●Birch还原Na/NH3(l)/CH3CH2OH●加成反应3Cl3 Δ/P/hv●氧化反应不为高锰酸钾、重铬酸钾所氧化●O2/V2O5/Δ→顺丁烯二酸酐●苯甲位性质●碳负离子反应●碳正离子反应●SN1取代●SN2取代●自由基反应X2/hv NBS/过氧化物●侧链氧化●强氧化(KMnO4,K2Cr2O7,HNO3)→-COOH含α-H的苯环侧链●温和氧化●Etard反应ArCH3 (CrO2Cl2)→ArCHO●Kornblum反应ArCH2X (DMSO,NaHCO3)→ArCHO●卤苯●与金属有机化合物●芳香亲核取代NaNH2/NH3(l) 苯炔中间体机理(消除-加成机理)●邻对位被吸电子基取代卤苯,卤素易亲核取代7.稠环芳烃●萘●亲电取代●硝化●卤代●磺化●低温α-位动力学●高温β-位热力学●酰基化●CS2溶剂→α-位●C6H5NO2溶剂→β-位●氧化●CrO3/HOAc●O2/V2O5/Δ●H2O2●催化氢化●一取代萘亲电取代定位●蒽、菲活泼,9.10位●亲电取代●催化氢化●氧化→醌8.卤代烃●亲核取代机理:Sn1;Sn2 反应活性●水解→醇●碱●水(溶剂解)●醇解→醚●碱●醇(溶剂解)●氨解●NaHS●NaSR●NaCN延长碳链●RC≡CNa●AgNO3鉴别卤代烃●-CH(COOEt)2●NaX'●β-消除区域选择性(Zaitev规则)立体选择性(反式共平面)机理:E1;E2 反应活性●与金属反应●Mg→格氏试剂●格氏试剂亲核取代偶联反应●格氏试剂与活泼氢反应●H2O●HX●HOR'●HC≡CR'●NH3●R'COOH●格氏试剂与醛、酮反应●格氏试剂与酯反应●格氏试剂与环氧乙烷反应●格氏试剂与CO2反应●格氏试剂与O2反应●NaWurtz反应●Li→有机锂→二烷基铜锂●亲核偶联●与活泼氢●与CO2、O2●还原反应●LiAlH4保留双键●NaBH4保留双键●Zn/HCl●HI●催化氢化●Na/NH3保留双键及构型●氧化反应●DMSO(二甲基亚砜)→R-CHO9.醇●醇羟基上的H 酸性●电离●与碱金属→亲核试剂●与氢氧化钠→亲核试剂●醇羟基上的O●碱性●亲核性——酯化反应●与有机酸加成-消除机理碳正离子机理酰基正离子机理●与含氧无机酸●硝酸●亚硝酸●硫酸●与羧酸衍生物●酰卤●酸酐●胺/氨●酯酯交换●亲核取代●HX机理:SN1,SN2 Lucas试剂及应用邻基参与效应●PX3,PX5重排●SOCl2不重拍●→构型保持●+吡啶→构型翻转●分子间脱水(H2SO4/140℃)低温利SN1●β-消除(H2SO4或HPO3/180℃)分子内脱水,高温利E1●氧化有α-H者●KMnO4/MnO2●稀、冷、中性KMnO4→不反应●酸性/Δ KMnO4●1°R-OH→羧酸●2°R-OH→酮●3°R-OH→裂解成酮●新制MnO2→醛(不饱和键保留)●铬酸●强氧化●Na2Cr2O7+H2SO41°R-OH→羧酸 2°R-OH→酮●温和氧化→醛不饱和键保留●Sareett试剂(CrO3+吡啶)●Jones试剂(CrO3+稀H2SO4)●PCC试剂(CrO3+HCl+吡啶)●硝酸●1°ROH→羧酸●2°ROH,3°ROH→浓硝酸,裂解●环醇→二元酸●Oppenauer氧化Al[OC(CH3)3]3→选择性醇/酮H交换●Pfitzner-Moffatt试剂氧化→醛二甲亚砜+二环己基碳二亚胺●脱氢Cu或CuCrO4或Pd/300℃●多元醇特殊性质●邻二醇●络合金属离子(Cu2+)●氧化邻二醇→断裂为二羰基化合物●H5IO6●Pb(OAc)4/CH3COOH或C6H6●NaIO4●频哪醇重排10.酚●酚羟基●酸性●NaOH●碱性极弱●亲核性较低●酯化催化剂:碱,质子酸●酰卤●酸酐●醚化●Williamson醚合成●RX●CH3OSO2OCH3●CH2NO2●Clainsen重排芳香,脂肪●Fires重排●芳环上亲电取代●卤化●多卤代●单卤代降低温度小极性或非极性溶剂酸性条件次氯酸叔丁酯●磺化●硝化亚硝化●Friedel-Crafts反应●烷基化●酰基化●Reimer-Tiemann反应→邻对位甲酰化(苯甲醛)CHCl3/NaOH/60℃●Kolbe-Schmitt反应→邻对位羧酸NaOH—CO2(高压)—H+●羟甲基化反应→邻对位羟甲基化HCHO/H+●偶联反应→对位偶氮苯ArN2+X-11.醚●自动氧化自由基反应●碱性→佯盐●亲核取代 HIC-O键断裂顺序●Claisen重排●烯基型醚稀酸→醛/酮●1,2-环氧乙烷开环●酸性 SN2机理,SN1区位选择性Nu-多取代C 构型翻转●碱性 SN2机理Nu-小空阻C 构型翻转●冠醚12.醛&酮●羰基亲核加成●含氧亲核试剂●H2O→偕二醇●ROH→半缩醛(酮)→缩醛(酮) [碱与氧化剂稳定,酸不稳定→恢复羰基]催化剂:对甲苯磺酸,HCl●含硫亲核试剂●NaHSO3(过量、饱和)醛脂肪族甲基酮 C8以下环酮●RSH→缩硫醛(酮)H2/NaneyNi→二甲基●Schiff试剂(品红+SO2)●含碳亲核试剂●HCN→α-羟基腈醛脂肪族甲基酮 C8以下环酮●炔化物→α-炔基醇●金属有机化合物→醇一次加成●Witting试剂(磷Ylide)→烯烃●含氮亲核试剂●胺●一级胺→亚胺●二级胺→烯胺●氨●胺衍生物●α-H反应酸性烯醇化→烯醇盐(区位选择)●α-H卤化●酸催化●碱催化●卤仿反应α-甲基酮,α-甲基醇●烷基化 RX●酮(仲胺参与)●醛(亚胺参与)●羟醛缩合(Aldol反应)酸催化碱催化自身缩合定向缩合●Michael加成(1,4-加成)含α-H的醛/酮+α-不饱和醛/酮●Perkin缩合芳香醛+酸酐(酸酐对应盐/Δ)→反式β-芳基-α-不饱和羧酸●Mannich反应含α-H的酮+甲醛+胺●氧化●一般氧化高锰酸钾、重铬酸钾、铬酸、过酸、过氧化氢、氧化银、溴…●醛→羧酸●酮 Null●特殊●醛●自氧化自由基●Fehling试剂(新制氢氧化铜络合物)→羧酸盐+砖红色氧化亚铜醛、α-羟基酮、α-醛酮芳香醛不反应●Tollens试剂(银氨离子)→羧酸盐+银镜●酮●Baeyer-Villiger氧化重排(过酸)迁移顺序●还原●→-C-OH●催化氢化顺式,小空阻侧●氢化金属化合物●LiAlH4C=C、C≡C保留●NaBH4C=C、C≡C保留●B2H6C=O>C=C●Meerwein-Pronndorf-Verley还原(异丙醇铝/异丙醇)C=C、C≡C保留●活泼金属●单分子还原●双分子还原[Mg/苯,Na/NH3(l)]→频哪醇孤立C=C不还原,共轭时优先还原●→-CH2●Clenmmensen还原 Zn-Hg/浓HCl●Wolff-Kishner还原●Wolff-Kishner-黄鸣龙还原C=C、C≡C保留●歧化 Cannizzaro反应(浓OH-)分子间自身,交叉,定向(甲醛总被氧化)分子内●安息香缩合苯甲醛+CN-●Darzen反应酮+XCH2COOR'→环氧化酯→(OH-/H2O,H3O/Δ)多一个碳的醛●聚合反应●不饱和醛、酮●烯酮●羰基的加成(活泼H)互变●格氏试剂●聚合体反应●β-丙内酯开环●酸性中性●碱性,强酸性●α,β-不饱和醛酮●加成反应●1,4-加成氨及其衍生物HX H2SO4 HCN H2O ROH 二烷基铜锂格氏试剂与酮Michael加成●1,2-加成RNa RLi 格氏试剂与醛●3,4-加成X2 H2O●还原●醌●对苯醌●加成●1,2-加成●氮亲核试剂●格氏试剂●1,4-加成HCN,HX,CH3OH,胺●还原●Diiels-Alder反应●羟基取代醛酮●α-OH取代●互变●氧化●与苯肼反应●与H5IO6反应●β-OH取代●脱水●γ/δ-OH取代●分子内亲核取代→环状半缩醛13.羧酸●酸性NaOH,KOH,Na2CO3,NH3·H2O●酰基碳上的亲核取代——酰化●酯化 ROH RX加成-消除碳正离子中间体酰基正离子中间体●与无机酰卤SOCl2 PCl3 PCl5●与氨或胺亦可酸碱反应●氨→互变成腈●胺→脱水缩合●与金属有机化合物●格氏试剂→羧酸镁盐无意义●有机锂→酮●还原●催化氢化●LiAlH4●BH3●脱羧自由基●Kolbe法电解●Hunsdicker反应→R-BrRCOOAg+Br2 (CCl4/Δ)●Cristal反应→R-BrHgO+Br2●Kochi反应●二元羧酸脱水与脱羧Blanc规则●α-H的反应 Hell-Volhard-Zelinsky反应PBr3 一、二、三卤代●不饱和羧酸●α,β-不饱和●1,4-亲核加成●Diels-Alder反应14.取代羧酸●卤代酸●α-X●亲核取代NaOH/H2O,NH3,NaCN/H+●β-X●卤代烃消除●γ,δ,ε -X●内酯化●醇酸●酸性●脱水●α- →半交酯→交酯●β- →消除成烯(共轭)●γ,δ - →内酯(分子内)●>ε- →聚酯(分子间)●与醛反应(亲核加成)●α-醇酸与金属离子→螯合物●降解脱羧,成酮●α-醇酸●稀H2SO4●浓H2SO4●β-醇酸●酚酸●羰基酸●乙醛酸水合●丙酮酸降解●乙酰乙酸●4-戊酮酸●氨基酸●两性与等电点●脱羧●脱水缩合●显色反应●β-酮酸酯●酸性●酮式与烯醇式互变●分解●酮式分解→酯水解稀碱●酸式分解→亲核加成-消除,脱羧浓碱●作为亲核试剂●烃化●酰化●Knoevenagel反应弱碱催化●Micheal加成●乙酰乙酸乙酯合成法●丙二酸二乙酯合成法15.羧酸衍生物●酰基碳上的亲核取代反应性:I>Br>Cl>-OCOOR>-OR>-OH>-NH2>-NHR●水解→羧酸酸性,碱性酰卤>酸酐>酯,易酰胺难●酯水解的机理●亲核加成-消除●碳正离子●酰基正离子●腈→酰胺→羧酸●醇解→酯酰卤>酸酐,易酯>酰胺>腈,难●酯交换反应及应用●氨解→酰胺均易●酸解●与金属有机化合物反应●酰卤●格氏试剂,有机锂→少量得酮,过量得3°ROH●二烷基铜锂→酮●有机镉化物→酮●酯,腈格氏试剂,有机锂→少量得酮,过量得3°ROH●酰胺NH2活泼氢先反应,浪费●酸酐→酮→醇浪费●还原●催化氢化●酰卤●强烈还原——H2/Pd→RCH2OH●温和还原Rosenmund还原——H2/Pd-BaSO4/硫/喹啉→RCHO●酸酐 ..H2/Pd●酯 CuO·CuCrO4,200-300℃,10-30MPa苯环不受影响●酰胺 H2/CuCr氧化物/高温高压●腈 H2/Ni/NH3(l)/高温高压●金属氢化物●酰卤,酸酐,酯→RCH2OH●LiAlH4/乙醚●LiBH4/THF●NaBH4/THF●酰胺 LiAlH4/乙醚●1°→RCH2NH2●2°→RCH2NHR'●3°●氧化剂过量→RCH2CR'R''●氧化剂不过量→RCHO●腈→RCH2NH2LiAlH4●特殊●二元环酐(NaBH4)→内酯●酰卤[ AlLi(t-BuO)3H ]→醛●酯的特殊还原——Bouveault-Blanc还原(Na/ROH)→醛+醇●酰卤专属反应●α-H卤代X2/H+●酯的专属反应●Claisen酯缩合→β-羰基酯C2H5ONa/C2H5OH●混合酯缩合●Dieckmann反应二酸酯(Na/甲苯/C2H5OH)→β-羰基酯环五、六元环稳定●酮酯缩合●酮醇缩合 2酯→β-羟基酮Na/N2,Ph-CH3,Δ●热裂→羧酸+烯400-500℃●Reformatsky反应β-卤代酸酯+醛/酮(Zn)→β-羟基酸酯●酰胺专属性质●酸碱性●脱水→腈P2O5或SOCl2或Δ●Hofmann降级→胺X2/NaOH→NaXO●Gabriel合成法亚酰胺制备伯胺●腈专属反应●水解→酰胺→羧酸●Ritter反应16.有机含氮化合物●胺●脂肪胺●碱性碱性判断分离纯化●酸性LDA制备●亲核性●烷基化(Hofmann烷基化) R-XSN2●酰基化(伯胺,仲胺)●羧酸衍生物——酰卤,酸酐,酯保护氨基,结构鉴定●磺酰氯 Hinsberg反应鉴别结构,分离纯化●亚硝化●叔胺→N-亚硝铵盐●仲胺→N-亚硝胺●伯胺→重氮盐→碳正离子●取代●消除●重排●Tiffeneau-Demjanov重排类似频哪醇●与醛/酮反应●伯胺→亚胺●仲胺→烯胺●还原性●伯胺→亚硝基化合物→硝基化合物●仲胺→羟胺●叔胺→氧化胺●Cope消除β-H的氧化胺Δ→烯烃+羟胺●芳香胺●极弱碱性●芳香亲核取代活化,邻对位改变活性→铵盐改变定位→酰化●卤化→三卤代无cat.●磺化,硝化,酰基化注意N上的H竞争反应●重氮化NaNO2,H+,H2O,0-5℃●伯芳胺→芳香重氮盐●仲芳胺→N-R基-N-亚硝基苯胺●叔芳胺→对亚硝基苯胺●还原性●氨基氧化●1°→硝基化合物●2°→羟胺●3°→氧化胺●苯环氧化复杂醌式结构●MnO2/H2SO4/10℃→醌●季铵盐与季铵碱●制备●Hofmann烷基化●Ag2O/H2O●Hofmann消除Hofmann规则●硝基化合物●脂肪族●还原反应→-NH2●酸性还原系统 Fe/Zn/Sn+HCl●催化氢化●酸性α-H●Henry反应碳负离子与羰基化合物缩合●与亚硝酸反应●1°→硝肟酸+NaOH→红色溶液●2°→假硝醇+NaOH→蓝色溶液●3° null●芳香族●还原→→-NH2●酸性系统→-NH2●中性系统→-NHOHNH4Cl,CH3CH2OH●碱性系统→氧化偶氮苯,偶氮苯,氢化偶氮苯Zn/NaOH●催化氢化●亲电取代钝化,间位定位●亲核取代卤苯亲核取代●重氮化合物●重氮甲烷●碱性●与含活泼氢者反应●亲核性●与醛/酮反应●与酰卤反应 Arndt-Eister合成法●亲电反应●1,3-偶极环加成反应→环丙烷及其衍生物●生成卡宾●芳香族●酸性●亲核取代反应●被OH取代PhN2+SO4H- H2O H+/Δ●被卤素取代●F Schiemann反应●Cl Br●Olah反应●Sandmeger反应CuX●Gattermann反应Cu●IKI/Δ●被CN取代●Sandmeger反应CuCN+KCN●Gattermann反应Cu+KCN●被硝基取代●Gattermann反应NaNO2+H2O+Cu●被H取代●H2PO3+H2O●HCHO+NaOH●还原反应●偶联反应活泼芳环●二烷基芳胺●芳香伯胺、仲胺●酚●偶氮化合物●芳香族●异构化●弱碱性●联苯胺重排●氧化→氧化偶氮苯→对羟基偶氮苯过氧酸 H+●脂肪族●叠氮化合物●还原→-NH3●Curtius重排酰胺叠氮→胺(少一个C)●Schmidt重排●氮烯17.杂环化合物●五元杂环●一个杂原子——吡咯、呋喃、噻吩●芳香性●亲电取代α-位吡咯>呋喃>噻吩●卤代●Br2 Cl2→多卤代●SO2Cl/Et2O/0℃,Br2/环二乙醚/0℃,Br2/AcOH,NBS,NCS→一卤代●噻吩+I2/HgO/苯/0℃→一碘代●磺化吡啶三氧化硫噻吩可直接磺化●硝化乙酰基硝酸酯●偶联芳香重氮盐●傅-克酰基化●傅-克烷基化→混合物●加成●催化加氢●Diels-Alder反应●吡咯特有性质●极弱碱性●酸性与碱反应得N+●N+作为亲核试剂RX, RCOX, CO2/H2O●瑞默尔-悌曼反应→α-醛CHCl3/NaOH●衍生物α-呋喃甲醛●醛●催化加氢●氧化●无α-H的醛●康尼扎罗●安息香缩合●交叉羟醛缩合●Perkin反应●一个杂原子的苯并杂环——吲哚,异吲哚●亲电取代3-位●2个杂原子●咪唑●酸性强于吡咯●碱性强于吡咯●六元杂环●一个杂原子——吡啶●碱性●亲核性N●CH3I●RX●酰卤●SO3●亲电取代β-位●卤代200℃●硝化HNO3/H2SO4/KNO3/300℃●磺化发烟H2SO4/HgSO4/230℃●亲核取代α-位●Chichibabin反应NaNH2/NH3●C6H5Li●3,4-卤代吡啶+氨水/160℃→4-取代●氧化●较苯难氧化●被过氧化物氧化产物取代定位γ-●还原●催化氢化●Na/C2H5OH●侧链α-H缩合反应●芳香醛●CH3I●一个杂原子的苯并杂环——喹啉,异喹啉●亲电取代苯环5,8-位●亲核取代●喹啉 2(主),4-位●异喹啉 1位●氧化还原●侧链α-H18.周环反应●电环化反应●4n●基态Δ→顺旋●激发态hν→对旋●4n+2●基态Δ→对旋●激发态hν→顺旋●环加成反应基态Δ●Diels-Alder反应●1,3-偶极环加成反应●σ迁移反应●[1,j]●H迁移●基态●同面5 9 13(4n+1C)●异面3 7 11 (4n-1C)●激发态●同面 4n-1●异面4n+1●C迁移●基态●构型保持●同面4n+1●异面4n-1●构型翻转●同面4n-1●异面4n+1●激发态●构型保持●同面4n-1●异面4n+1●构型翻转●同面4n+1●异面4n-1 ●[i,j]●[3,3]σ迁移●cope重排●claisen重排。

有机化学基础知识点整理烷基化反应与烷化反应机制【有机化学基础知识点整理】烷基化反应与烷化反应机制烷基化反应是有机化学中一类重要的反应,主要涉及底物中的氢原子被烷基基团取代的过程。
烷化反应机制则是指在此类反应中所形成的反应中间体和过渡态的详细变化过程。
本文将整理烷基化反应的几个基础知识点,并探讨其中常见的烷化反应机制。
一、烷基化反应的基本概念烷基化反应是有机化学中最为常见和广泛应用的一类反应,其中最常见的就是烷基磺酸盐的合成。
其原理是通过引入一个“烷基基团”,将底物中的氢原子取代。
烷基化反应可以形成新的碳-碳键或碳-氧键,产生新的有机化合物。
二、烷基化反应的分类烷基化反应根据反应过程的类型和反应底物的不同,可以分为以下几类:1.质子接受型烷基化反应:底物中的质子被烷基离子或烷基金属试剂取代。
2.质子捐赠型烷基化反应:底物中的烷基基团将质子给予另一分子,形成新的碳-碳键。
3.亲电取代型烷基化反应:底物中的亲电试剂与烷基基团发生亲电取代反应。
4.自由基烷基化反应:底物中的烷基离子与自由基试剂发生反应,形成新的碳-碳键。
三、常见的烷化反应机制1.质子接受型烷基化反应机制:在质子接受型烷基化反应中,底物中的质子被烷基离子或烷基金属试剂取代。
这类反应通常采用强碱作为反应试剂,如氢氧化钠(NaOH)。
反应机理如下:底物 + 烷基离子/烷基金属试剂→ 产物 + 相应的离子/金属盐该反应机制属于亲核取代反应,质子首先被碱中的氢氧根离子去质子化,然后进一步与烷基离子或金属离子发生亲核取代反应,最终形成新的碳-碳键。
2.自由基烷基化反应机制:在自由基烷基化反应中,底物中的烷基离子与自由基试剂发生反应,形成新的碳-碳键。
这类反应通常通过热、光或自由基引发剂来产生自由基,如过氧化氢(H2O2)或过氧化苯甲酰(Benzoyl peroxide)。
反应机理如下:底物 + 自由基试剂→ 产物该反应机制属于自由基取代反应,首先由自由基引发剂产生自由基,然后自由基与底物反应,形成新的碳-碳键。
基础有机化学反应总结一、烯烃1、卤化氢加成 (1)CHCH 2RHXCH 3RX【马氏规则】在不对称烯烃加成中,氢总是加在含碳较多的碳上。
【机理】CH 2CH 3+CH 3CH 3X +CH 3CH 3+H +CH 2+C3X +CH 3X主次【本质】不对称烯烃的亲电加成总是生成较稳定的碳正离子中间体。
【注】碳正离子的重排 (2)CHCH 2RCH 2CH 2R BrHBrROOR【特点】反马氏规则 【机理】 自由基机理(略)【注】过氧化物效应仅限于HBr 、对HCl 、HI 无效。
【本质】不对称烯烃加成时生成稳定的自由基中间体。
【例】CH 2CH3BrCH CH 2BrC H 3CH +CH 3C H 3HBrBrCH 3CH 2CH 2BrCH CH 3C H 32、硼氢化—氧化CHCH 2R CH 2CH 2R OH1)B 2H 62)H 2O 2/OH-【特点】不对称烯烃经硼氢化—氧化得一反马氏加成的醇,加成是顺式的,并且不重排。
【机理】2CH 33H 323H 32CH CH 2CH 32CH CH=CH (CH 3CH 2CH 2)3-H 3CH 2CH 2C22CH 3CH 2OCH 2CH 2CH 3H 3CH 2CH 2C2CH 2CH 3+OH -OHB-OC H 2CH 2CH 3CH 2CH 2CH 3H 3CH 2CH 2BOC H 2CH 2CH 3CH 2CH 2CH 3H 2CH 2CH 3HOO -B(OCH 2CH 2CH 3)3B(OCH 2CH 2CH 3)3+3NaOH 3NaOH3HOC H 2CH 2CH 33+Na 3BO 32【例】CH 31)BH 32)H 2O 2/OH-CH 3HH OH3、X 2加成C CBr /CCl CC Br【机理】CC CC Br BrC CBr +CC Br OH 2+-H +CC Br OH【注】通过机理可以看出,反应先形成三元环的溴鎓正离子,然后亲和试剂进攻从背面进攻,不难看出是反式加成。
12020高考理综化学精品专题(六)—有机方程式总结(必修部分)(一)烷烃(甲烷)燃烧氧化:CH 4 +2O 2CO 2 + 2H 2O 李比希氧化:CH 4 +4 CuOCO 2 + 2H 2O + 4Cu 取代反应:CH 4 + Cl 2CH 3Cl + HCl CH 4 + 2Cl 2CH 2Cl 2 + 2HCl CH 4 + 3Cl 2CHCl 3+ 3HCl CH 4 + 4Cl 2CCl 4 + 4HCl 分解反应:CH 4C + 2H 2(二)烯烃(乙烯)燃烧氧化:C 2H 4 + 3O 22CO 2 + 2H 2O 强氧化剂氧化:5CH 2=CH 2+12KMnO 4+18H 2SO 4 10CO 2 + 12MnSO 4+6K 2SO 4+28H 2O 加成反应:CH 2=CH 2 + Br 2CH 2BrCH 2Br CH 2=CH 2 +H 2CH 3CH 3 CH 2=CH 2 + H 2OCH 3CH 2OH CH 2=CH 2 +HClCH 3CH 2Cl(三)芳香烃(苯)燃烧氧化:2C 6H 6+15O 212CO 2 + 6H 2O 不能被强氧化剂高锰酸钾氧化取代反应: + Br 2+ HBr +HO -NO 2+ H 2O (50℃—60℃) + HO -SO 3H(苯磺酸) + H 2O (70℃—80℃) 加成反应:+ 3H 2 (环己烷是非平面结构)(四)、石油和煤石油的综合利用(你知道分馏、裂化、裂解、催化重整之间的区别吗?)裂化反应:C 16H 34C 8H 18 + C 8H 16 C 8H 18C 4H 10 + C 4H 8 C 4H 10C 2H 6 + C 2H 4 C 4H 10CH 4 + C 3H 62煤的综合利用(你知道干馏、液化、气化之间的区别吗?)煤的气化反应:C+H2O(g)CO+H2(注意区别:CO+ H2O(g) CO2+H2)煤的间接液化:①先气化C+H2O(g)CO+H2②再液化CO+2H2CH3OH煤的直接液化:煤+H2液体燃料(五)、醇类(乙醇)置换反应:2CH3CH2OH + 2Na 2CH3CH2ONa + H2↑消去反应:CH3CH2OH CH2=CH2↑ + H2O氧化反应(三种氧化)燃烧氧化:CH3CH2OH + 3O22CO 2 + 3H20催化氧化:<1> 2Cu + O2 2 CuO <2> CH3CH2OH + CuO CH3CHO + H2O + Cu强氧化剂氧化:5CH3CH2OH+4KMnO4+6H2SO45CH3COOH+ 4MnSO4+2K2SO4+11H2O 取代反应:(三种取代)酯化CH3CH2OH+CH3COOH CH3COO OCH2CH3 +H2O成醚:2CH3CH2OH CH3CH2OCH2CH3 + H2O生成卤代烃:CH3CH2OH+HBr CH3CH2Br+H2O(六)、羧酸和酯(乙酸和乙酸乙酯)弱酸性(指示剂变色、活泼金属、金属氧化物、碱和盐五个方面)酯化反应:水解反应:(注意酸性可逆,碱性不可逆)CH3COOCH2CH3 + H2O CH3COOH + CH3CH2OHCH3COOCH2CH3 + NaOH CH3COONa + CH3CH2OH。
高考化学有机化学反应基础知识全面总结在高考化学中,有机化学反应是一个重要的考点。
掌握好有机化学反应的基础知识,对于理解和解决相关问题至关重要。
下面就让我们一起来全面总结一下高考化学中常见的有机化学反应。
一、取代反应取代反应是指有机物分子中的某些原子或原子团被其他原子或原子团所替代的反应。
常见的取代反应有以下几种:1、卤代反应烷烃在光照条件下与卤素单质(如氯气、溴气)发生取代反应,生成卤代烃和卤化氢。
例如,甲烷与氯气在光照下发生反应:CH₄+Cl₂ → CH₃Cl + HCl 。
2、硝化反应苯与浓硝酸、浓硫酸在加热条件下发生硝化反应,生成硝基苯和水。
3、酯化反应羧酸与醇在浓硫酸催化下发生酯化反应,生成酯和水。
例如,乙酸与乙醇反应:CH₃COOH + C₂H₅OH ⇌ CH₃COOC₂H₅+ H₂O 。
4、水解反应酯、卤代烃等在一定条件下发生水解反应,酯水解生成羧酸和醇,卤代烃水解生成醇和卤化氢。
二、加成反应加成反应是指有机物分子中不饱和键(双键或三键)两端的原子与其他原子或原子团直接结合生成新化合物的反应。
1、与氢气的加成烯烃、炔烃、苯及其同系物等在一定条件下与氢气发生加成反应,使不饱和键变为饱和键。
例如,乙烯与氢气反应:CH₂=CH₂+ H₂→ CH₃CH₃。
2、与卤素单质的加成烯烃、炔烃等与卤素单质发生加成反应。
3、与卤化氢的加成烯烃、炔烃等与卤化氢发生加成反应。
三、消去反应消去反应是指在一定条件下,有机物分子脱去小分子(如 H₂O 、HX 等)生成不饱和化合物的反应。
醇在浓硫酸、加热条件下发生消去反应生成烯烃。
例如,乙醇在浓硫酸作用下加热到 170℃发生消去反应:C₂H₅OH → CH₂=CH₂↑ +H₂O 。
卤代烃在氢氧化钠的醇溶液、加热条件下发生消去反应生成烯烃。
四、氧化反应1、燃烧有机物在氧气中燃烧,生成二氧化碳和水。
2、催化氧化醇在铜或银作催化剂、加热条件下被氧化为醛或酮。
例如,乙醇被氧化为乙醛:2CH₃CH₂OH + O₂ → 2CH₃CHO + 2H₂O 。
高一化学必修2有机化学反应知识点总结有机化学是化学中的重要分支,它研究碳和氢以及它们之间的化合物的性质、结构、合成及其反应。
以下是高一化学必修2有机化学反应的一些重要知识点总结:反应类型1. 代谢反应:有机物分解产生能量和新的有机物。
2. 燃烧反应:有机物与氧气在高温下反应,产生二氧化碳和水。
3. 加成反应:两个或多个化合物反应生成一个新的化合物。
4. 酯化反应:酸与醇反应生成酯和水。
5. 酰基化反应:酸酐与醇反应生成酯和水。
6. 酯水解反应:酯与水反应生成醇和酸。
7. 醚化反应:醇与醇反应生成醚和水。
8. 醚水解反应:醚与水反应生成醇和醇。
9. 锯齿反应:有机物中的碳骨架被分解成两个部分,然后重新连接成一个新的化合物。
10. 缩合反应:两个或多个分子结合成一个较大的分子。
常见有机化合物反应醇的氧化反应醇的氧化反应可以将醇氧化为酮或醛,具体反应条件取决于醇的结构。
常用的氧化剂包括酸性高锰酸钾(KMnO4)、酸性高铬酸钾(K2Cr2O7)等。
烷烃的卤代反应烷烃可以与卤素发生取代反应,生成卤代烃。
反应条件包括适当温度和光照。
酸酐与醇的酯化反应酸酐与醇反应生成酯和水,反应通常需要催化剂。
常见的催化剂有硫酸和盐酸等。
醇的缩合反应两个或多个醇分子可以发生缩合反应,生成较大的分子。
此类反应通常需要酸性条件和适当温度。
酮与醛的加成反应酮与醛可以发生加成反应,产生一个新的酮或醇。
常见的加成试剂包括氢氨基钠(NaBH3CN)等。
这些是高一化学必修2有机化学反应的一些重要知识点总结,希望对你有所帮助!。
有机反应知识点总结一、有机反应的分类有机反应可以根据反映的化学实质及过程特点分为不同的类型。
一般来说,有机反应可以分为以下几种类型:1. 加成反应加成反应是指两个不饱和化合物中的碳—碳双键或者碳—碳三键之间的共价键断裂,然后与其它物质中的原子或者原子团形成新的键的反应。
例如:在上面的反应中,1,3-丁二烯和Br2反应,生成1,4-二溴丁烷。
2. 消除反应消除反应是指分子中的两个原子团(通常是氢原子与氢氯酸根、质子与醇酸根或者氢替换基与羟基等)之间的离子键断裂,原来结合在一起的分子中的原子或者原子团离开,从而从分子中除去一个分子的过程。
例如:在上面的反应中,氢氧化钠与氯丙酮反应,生成丙烯醇。
3. 取代反应取代反应是指一个有机分子中的原子团或者原子被另一个原子团或者原子所取代的过程。
例如:在上面的反应中,氯甲烷与氢氧化钠反应,生成甲醇。
4. 重排反应重排反应是指有机分子分子中化学键的原子在分子内重新排列的过程,生成不同的有机化合物。
在上面的反应中,氯丙烷受热发生重排反应,生成异丙烯和丙烷。
5. 加氢反应加氢反应是指有机分子中的碳—碳双键或者碳—碳三键上的原子与氢原子反应的过程,也就是加氢的过程。
例如:在上面的反应中,丙烯与氢气反应,生成丙烷。
6. 氧化反应氧化反应是指有机分子中的原子或者原子团失去电子与氧原子或者其他含氧的物质发生反应的过程。
例如:在上面的反应中,2-丁醇与酸性高锰酸钾反应,生成丁酸。
7. 还原反应还原反应是指有机分子中的原子或者原子团与氢原子或者氢离子发生反应的过程。
例如:在上面的反应中,苯酮与水合肼反应,生成苯甲酸。
二、有机反应知识点总结1. 共轭体系的稳定性在有机化学中,共轭体系的稳定性对很多有机反应的进行起着决定性作用。
共轭体系是指一个分子内含有两个或者两个以上的π键,这些π键相邻并且共享一个或者多个的原子,形成一个扩展的共轭体系。
共轭体系的稳定性对于很多有机反应起着决定性的作用。