臭氧的性质
- 格式:doc
- 大小:37.50 KB
- 文档页数:4
臭氧物理性质
在常温常压下,较低浓度的臭氧是无色气体。
当浓度达到15%时,呈现出淡蓝色。
臭氧可溶于水,在常温常压下臭氧在水中的溶解度比氧气高约13倍,比空气高25倍。
但臭氧水溶液的稳定性受水中所含杂质的影响较大,特别是有金属离子存在时,臭氧可迅速分解为氧气。
在纯水中分解较慢。
臭氧的密度是2.14g·l(0°C,0.1MP)。
沸点是-111°C,熔点是-192°C。
臭氧分子结构是不稳定的,它在水中比在空气中更容易自行分解。
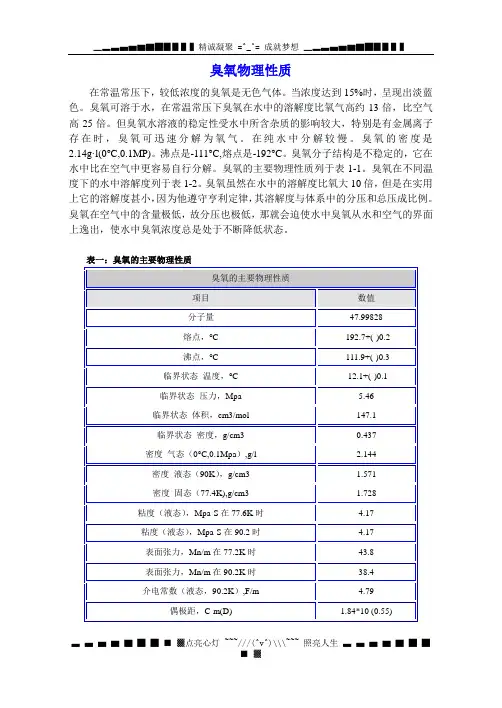
臭氧的主要物理性质列于表1-1。
臭氧在不同温度下的水中溶解度列于表1-2。
臭氧虽然在水中的溶解度比氧大10倍,但是在实用上它的溶解度甚小,因为他遵守亨利定律,其溶解度与体系中的分压和总压成比例。
臭氧在空气中的含量极低,故分压也极低,那就会迫使水中臭氧从水和空气的界面上逸出,使水中臭氧浓度总是处于不断降低状态。
表一:臭氧的主要物理性质
表二:臭氧在水中的溶解度。

o3氧气符号O3氧气符号是什么?O3氧气符号是指三个氧原子结合在一起形成的分子,也称为臭氧。
其化学式为O3,其中“O”代表氧元素。
O3的物理和化学性质物理性质:1. 外观:无色有刺激性气味的气体。
2. 密度:1.66 g/L。
3. 熔点:-192.2℃。
4. 沸点:-111.9℃。
化学性质:1. 氧化剂:臭氧具有很强的氧化能力,可以将许多物质(如二次污染物和细菌)分解成无害的物质。
2. 强还原剂:臭氧可以将许多有机物(如苯、甲醛等)分解成较小的分子,从而去除异味和有害物质。
3. 亲电性强:臭氧具有很强的亲电性,可以与许多有机物发生反应,形成活性中间体,从而去除异味和有害物质。
4. 反应活泼:臭氧与水反应生成一种强酸——亚硝酸(HNO2),这种反应被称为“湿法臭氧”。
O3的应用1. 水处理:臭氧可以用于水处理,去除水中的异味、色度和有机物质。
2. 空气治理:臭氧可以用于空气治理,去除空气中的二次污染物和细菌。
3. 化学合成:臭氧可以用于化学合成,如合成酮、醛等有机化合物。
4. 医疗卫生:臭氧可以用于医疗卫生,如治疗皮肤病、口腔炎等。
5. 食品加工:臭氧可以用于食品加工,如去除食品中的异味和杀菌消毒等。
6. 工业生产:臭氧可以用于工业生产,如制造高温橡胶、涂料等。
O3与环境保护1. 去除有害物质:臭氧具有很强的氧化能力和亲电性,可以将许多有害物质(如二次污染物、细菌)分解成无害的物质,从而减少对环境的污染。
2. 降低温室效应:臭氧属于大气中的重要组分之一,可以吸收紫外线,从而减少地球表面的温度升高,降低温室效应。
3. 保护大气层:臭氧层是保护地球大气层的重要组成部分之一,可以防止紫外线对地球的损害。
4. 推动环保产业发展:臭氧技术在环境保护中的应用越来越广泛,推动了环保产业的发展和经济的繁荣。
结论O3氧气符号是指三个氧原子结合在一起形成的分子,也称为臭氧。
其具有很强的化学性质和广泛的应用领域,在环境保护和经济发展中都起到了重要作用。

臭氧的性质臭氧(OZONE),分子式O 3,分子量47.9982(≈48),在常温下为蓝色气体,有类似鱼腥的气味。
臭氧的理化数据:在标准状况下,密度2.144g/L。
由于接近地面的干燥空气,密度为1.293g/L,因此臭氧密度是空气的1.658倍。
在-195.4 0 C时,液态臭氧密度为1.164g/ml。
临界温度为-12.1 0 C,临界压力为5.45×10 6帕。
在冷水中的溶解度比氧气约大10倍。
空气中含有0.02PPm左右的臭氧。
一般情况下,空气中1PPm臭氧可取2.14mg/m 3,水中1PPm臭氧为1mg/L。
长期呼吸>0.1PPm臭氧,对人体有害。
臭氧浓度在0.02PPm时,嗅觉敏锐者能感觉到,称“感觉临界点”;0.15PPm时,一般人能嗅出,称“嗅觉临界值”(亦为卫生标准点);1-10PPm为“刺激范围”;10PPm以上为“中毒范围”。
臭氧不稳定,在高温时会迅速分解,在常温下会缓慢分解为(氧气),在1%的臭氧水溶液中半衰期约16分钟,在空气中的半衰期约25分钟。
臭氧的不稳定性使其很难实现瓶装贮存,一般只能利用臭氧发生器现场生产,随产随用。
臭氧是比氧气更强的氧化剂,且可以在较低温度下进行氧化。
所以,臭氧的一切应用(消毒、灭菌、水净化、漂白、作氧化剂等)本质上都是利用其强氧化能力。
由上可知,臭氧的强氧化性、常温作用性,特别是其“工作”后能还原为氧气,是其应用经久不衰,备受人类青脒的三大原因。
纯臭氧在受撞击、磨擦时会发生爆炸而分解,含高浓度臭氧溶液加热时易发生爆炸,但只要注意避免,此类事故即不易发生(至于臭氧对人体的毒害,臭氧问世150余年来,尚无一例中毒死亡的报告)。
臭氧用于空气消毒时,消毒现场不应有高浓度易燃易爆气体。
臭氧与水同存时为强烈漂白剂,其作用比氯气(Cl 2)、双氧水(H 2 O 2)、二氧化硫(SO 2)快得多。
臭氧的获得:臭氧可通过高压放电、电晕放电、化学等方法获得。

高三地理臭氧知识点总结臭氧是地球大气层中一种重要的气体成分,它在保护地球生命的过程中扮演着极为重要的角色。
以下是高三地理中关于臭氧的知识点总结。
一、臭氧的定义和特性臭氧(O3)是一种由三个氧原子组成的气体,具有强烈的氧化性。
与氧气(O2)相比,臭氧分子更加不稳定,容易分解为氧气和自由氧原子。
二、臭氧的分布和形成臭氧主要分布在地球大气层的同温层和对流层中。
同温层臭氧主要以臭氧层的形式存在于平流层,而对流层臭氧则分布较为零散。
臭氧形成有两种主要机制:自然形成和人为形成。
自然形成的臭氧主要是通过紫外线照射下氧气分子发生光解反应生成;而人为形成的臭氧主要是由于大气污染物的排放和化学反应而产生。
三、臭氧层的作用和保护臭氧层在地球大气层中扮演着重要的保护层,主要具有以下作用:1.吸收紫外线:臭氧层可以吸收大部分太阳紫外线,保护地球表面的生物免受紫外线的伤害;2.调节气候:臭氧层的存在可以吸收和反射太阳的热量,对地球气候起到调节作用;3.维持生态平衡:臭氧层的保护对维持生态系统的稳定和平衡具有重要意义。
四、臭氧层破坏和问题然而,随着人类活动的增加和工业化进程的加快,地球大气层中的臭氧层出现了一系列问题和破坏现象:1.臭氧空洞:大气异常富含臭氧空洞,是指臭氧浓度明显低于正常情况的区域。
臭氧空洞主要是由人为因素引起的,如氯氟烃类化合物(CFCs)的排放;2.紫外线辐射增强:臭氧空洞导致紫外线辐射进一步增强,对人类和生物造成较大的伤害;3.气候变化:臭氧层的破坏也会对地球气候产生重要影响,如增加温室效应、加剧全球变暖等。
五、应对臭氧层问题的措施为了减轻和防止臭氧层的破坏,国际社会采取了一系列措施:1.国际合作与政策制定:各国共同努力,签署并执行国际协议和公约,限制和减少有害物质的排放;2.减少化学物质使用:鼓励研究和开发代替性物质,减少有害物质的使用;3.环境教育与意识提升:加强公众对臭氧破坏问题的认识和理解,提高环保意识,倡导低碳环保生活方式。

臭氧的化学性质
臭氧很不稳定,在常温下即可分解为氧气。
臭氧、氯和二氧化氢的氧化势(还原电位)分别是2.07、1.36、1.28伏特,可见臭氧在处理水中是氧化力量最强的一种。
臭氧的氧化作用导致不饱和的有机分子的破裂。
使臭氧分子结合在有机分子的双键上,生成臭氧化物。
臭氧化物的自发性分裂产生一个羧基化合物和带有酸性和碱性基的两性离子,后者是不稳定的,可分解成酸和醛。
臭氧与有机物反应
臭氧与有机物以三种不同的方式反应:一是普通化学反应;二是生成过氧化物;三是发生臭氧分解或生成臭氧化物。
如有害物质二甲苯与臭氧反应后,生成无毒的水及二氧化碳。
所谓臭氧分解是指臭氧在与极性有机化合物的反应,是在有机化合物原来的双键的位置上发生反应,把其分子分裂为二。
由于臭氧的氧化力极强,不但可以杀菌,而且还可以除去水中的色味等有机物,这是它的优点,然而它的自发性分解性、性能不稳,只能随用随生产,不适于储存和输送,这是它的缺点。
当然,如果从净化水和净化空气的角度来看,由于其分解快而没有残留物质存在,又可以说成是臭氧的一大优点。
臭氧与无机物反应
除铂、金、铱、氟以外,臭氧几乎可与元素周期表中的所有元素反应。
臭氧可与K、Na反应生成氧化物或过氧化物,在臭氧化物中的阴离子O3实质上是游离基。
臭氧可以将过渡金属元素氧化到较高或最高氧化态,形成更难溶的氧化物,人们常利用此性质把污水中的Fe2+、Mn2+及Pb、Ag、Cd、 Hg、Ni等重金属离子除去。
此外,可燃物在臭氧中燃烧比在氧气中燃烧更加猛烈,可获得更高的温度。

臭氧的物理性质臭氧是一种具有独特刺激性气味的有色气体,通常是深蓝色或紫色,因具有很强的氧化性,因而被广泛应用于各个领域。
以下是臭氧的一些重要的物理性质。
1. 臭氧的化学式为O3,是由三个氧原子组成的一种不稳定分子。
臭氧的分子量为47.998 g/mol,比分子量为32.00 g/mol的O2大得多。
2. 臭氧具有很强的氧化性,可与许多物质发生反应,例如氧化亚氮、硫化氢等。
它还可以与有机物反应,形成具有臭味的挥发性有机化合物。
这种氧化反应在大气中发挥着重要的作用,可消除毒性气体,并净化空气。
3. 臭氧是一种混合物,通常含有臭氧、氧、氮、水蒸气和一些杂质气体。
臭氧在大气中的浓度很低,通常在10~20 ppb(亿分之一)的水平。
4. 臭氧比空气密度大2倍左右,因此可以与空气分离。
它是非常有害的,因此需要在合适的场所存储和处理。
5. 臭氧的沸点很低,只有-111.9℃,因此它是一种易挥发的气体。
在室温下,臭氧呈现为深蓝色或紫色气体。
由于它是一种强氧化剂,因此不稳定,容易分解成氧气。
其分解反应的速度很快,而且加热会加速分解的速度。
6. 臭氧的电学特性非常突出。
它是一种优秀的绝缘体和电介质,能够承受高电压和电弧放电。
臭氧的导电率极低,可用于隔离工业过程和高电压开关。
7. 臭氧的分子结构样式类似于三角形。
它的极性很强,因此具有很好的溶解性。
臭氧可以溶解在许多有机溶剂中,如乙醇、丙酮、甲醇、石油醚等。
综上所述,臭氧是一种具有重要化学特性的气体,天然界中存在的浓度极低,但它在各个领域如污水处理、空气净化、医疗卫生等方面的应用也越来越广泛。
同时,臭氧也具有较高的危害性,需要特别注意使用和处理,确保安全。


臭氧的科普知识一、概述臭氧(O3)是大气中的一种重要成分,它主要存在于平流层,对流层中的臭氧对人类生活有重要影响。
臭氧对人类生存环境的影响主要表现在以下几个方面:1.太阳辐射吸收:臭氧吸收太阳辐射中的紫外线,为地球表面提供了防护。
2.气候影响:平流层中的臭氧对地球表面温度和气候变化有一定影响。
3.空气质量:低层臭氧对空气质量有重要影响,高浓度的臭氧会对人体健康造成危害。
二、化学性质臭氧的化学性质非常活泼,很容易与其它物质发生反应。
在大气中,臭氧主要与一些气态污染物发生反应,将它们转化为无害或低害的物质。
同时,臭氧也会与一些自然界的物质发生反应,如植物表面、土壤和水中的物质。
三、影响低层臭氧的形成主要是由于人类活动产生的污染物在阳光的作用下氧化而产生的。
这些污染物主要包括氮氧化物(NOₓ)、挥发性有机物(VOCs)等。
因此,控制这些污染物的排放对于减少低层臭氧污染至关重要。
四、利用和保护臭氧在工业、农业、环保等领域有广泛的应用,如用于水的消毒、空气的净化、漂白等方面。
然而,过量的臭氧会对人体健康造成危害,因此需要采取措施控制臭氧的浓度。
为了保护臭氧层,国际社会签订了蒙特利尔议定书,限制使用那些可能导致臭氧层破裂的物质,如CFCs(氯氟烃)。
此外,我们也可以通过减少污染物排放、使用环保能源等方式来减少臭氧的排放,保护我们的大气环境。
五、防护措施由于臭氧具有强烈的氧化性,长期接触高浓度的臭氧会对人体造成伤害,如引起呼吸系统问题、眼睛不适等。
因此,在臭氧浓度较高的环境中,我们需要采取适当的防护措施:1.避免长时间在户外活动:尤其在日照强烈、气温较高的日子,应尽量减少户外活动时间。
2.佩戴防护口罩:选择N95或更高级别口罩,过滤由臭氧引起的空气污染。
3.减少汽车出行:尽量选择公共交通工具,减少汽车尾气排放。
4.室内空气净化:使用空气净化器,过滤进入室内的污染空气。
5.定期关注空气质量预报:根据预报调整出行和活动计划。
臭氧有哪些物化性质?
臭氧既是一种强氧化剂,亦是一种消毒剂。
臭氧作为消毒剂,能杀菌和灭病毒,反应快,投量少,适应性强,pH值在5.6~9.8,水温在0~37℃范围内变化时,对消毒效果影响很少。
臭氧作为氧化剂能去除水中色、臭、味和氧化水中可溶性亚铁、二价锰盐类、氰化物、硫化物、亚硝酸盐等。
分解水中溶解性有机物,有助于水的絮凝作用,强化水的澄清、沉淀和过滤效果,提高处理后的出水水质。
下面介绍臭氧的化学性质。
臭氧(O3)是一种不稳定的具有特殊“新鲜”气味的气体,它是氧的同素异形体,每个分子中含有3个氧原子,常温常压下是一种不稳定的淡蓝色气体,并能自行分解为氧气。
臭氧是良好的氧化剂,具有很强的氧化能力,在天然元素中仅次于氟。
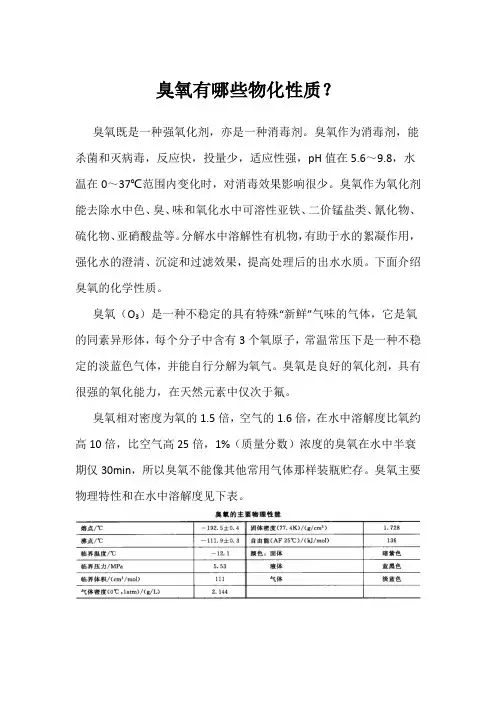
臭氧相对密度为氧的1.5倍,空气的1.6倍,在水中溶解度比氧约高10倍,比空气高25倍,1%(质量分数)浓度的臭氧在水中半衰期仅30min,所以臭氧不能像其他常用气体那样装瓶贮存。
臭氧主要物理特性和在水中溶解度见下表。
臭氧与水中无机物反应,是放出一个性质活泼的氧原子使无机物氧化,同时放出一个氧分子,臭氧化有机物一般认为先生成过氧化物或羟基。

臭氧的概述、化学性质一、概述臭氧是有毒、淡蓝色、不稳定和具有潜在爆炸性的气体。
在很低的温度下,它是暗蓝色的液体或固体。
其沸点为-111.3℃二、化学性质臭氧的氧化能力仅次于氟。
它能将大多数无机化合物氧化成它们的最高氧化态。
铁、锰和铬离子均可被定量地氧化成各自相应的最高氧化态。
臭氧加成到烯烃的双键上,随后,生成的臭载化物分解.这一过程很久以来一直被看做是氧化离解的最可靠的实验室方法。
借此可以给双键定位。
由于在臭氧化物完全离解之前可以移出氧化剂(臭氧),因而可以分离出初级离解产物,这是臭氧分解反应的重要优点所在。
在实验室中,臭氧分解已经广泛使用于结构分析。
在工业上也用于生产醛和酸。
该方法的应用在某种程度上受到下列事实的限制,即许多臭氧化物具有爆炸性。
通常在低温下工作(在下列溶剂中,氯氟甲烷、乙烷、乙酸乙酯、四氧化碳或氯苯乙烷),并且只是在溶液中进行臭氧化物的生成和分解而不是试图分离出臭氧化物,就可以避免爆炸。
在合成可的松和其它激素的工业过程中,已经利用臭氧分解来使烯烃侧链降解。
臭氧还被用于油酸氧化制壬二酸和壬酸。
臭氧的物理性质臭氧的应用目前,很多供水机构都在进行大量研究,将采用臭氧净水法取代氯气消毒法作为饮水消毒的有效手段。
1kg臭氧可以处理1000m 的水,处理范围包括对水消毒、脱臭、去味以及氧化水中的有机化合物等等。
迄今为止,欧洲已有1000多套采用臭氧净化的水处理装置。
瑞士的布郎一包维瑞工业集团已开始生产工业化规模的臭氧发生器,用以大规模地生产这种气体。
臭氧的制造是通过“无声放电”过程来实现的,这个过程可用电进行自动控制。
现在已生产出若干额定功率在450kW以上的装置。
工业化规模的生产涉及到放电过程的控制及采用自动化操作,以便连续地制造出臭氧。
布朗—包维瑞公司为德国提供的位于西普林根的最大臭氧生产装置,是一个应用臭氧净化水技术的极好例子。
在德国南部各州的生活供水中,绝大部分是采用臭氧净水法处理的,这套大型化生产装置,每小时可生产出53kg的臭氧,每天可处理约67万m 的生活用水。

臭氧的知识臭氧(ozone)是一种强氧化剂和催化剂,具有广谱、高效的杀菌作用。
臭氧用于消毒已有近百年的历史,目前臭氧主要用于饮水消毒、污水处理、空气消毒、食品保鲜、冷藏冷冻物品除菌、医院消毒、家庭消毒等方面,在工农业中的应用也日趋广泛和深入。
一、理化性质臭氧是由三个氧原子组成的氧的同素异形体,常态下为淡蓝色气体,有特殊的刺激性,臭氧在水中的溶解度为3%,是氧的10倍,臭氧不稳定,易分解,在水中臭氧的半衰期与温度和PH值有关,PH值越高,分解越快;温度越高,分解也越快,在20℃,PH为7.6时半衰期约为21~22min。
臭氧具有极强的氧化能力,其标准氧化还原电位达2.07V。
这种强氧化性对微生物具有较强的杀灭作用。
由于臭氧的不稳定性和毒性使其应用受限,现在新型臭氧发生方法的产生使它在消毒领域内的应用范围不断拓宽。
二、对微生物的杀灭作用臭氧是一种高效消毒剂,可以杀灭各种微生物。
(一)对细菌繁殖体臭氧对细菌繁殖体具有较好的杀灭作用,但不同细菌对臭氧的抵抗力不同,敏感菌和抗力强的细菌之间杀灭浓度相差2倍。
臭氧对表面上污染的细菌繁殖体的杀灭效果国内研究较多,李綏晶等(1997)报道在温度为20~25℃,RH为48%的条件下,臭氧对表面上的大肠杆菌作用30min(浓度为0.258mg/L)。
可杀灭99.9%~99.99%。
而林辉等(1995)的试验结果显示,臭氧浓度为0.49 mg/L,作用60min时可杀灭物体表面99.99%的金葡菌和大肠杆菌。
郭兰英等对光氧消毒仪(利用紫外线照射压缩空气产生臭氧)的表面消毒效果进行检测,臭氧浓度为9.37min/m³,作用5min,可杀灭大肠杆菌99.9%、金葡菌99.8%以上,作用30min(浓度78.64mg/m³),两者杀灭率均达99.99%。
(二)对细菌芽孢臭氧对空气、水中和表面上的芽孢均有杀灭作用,用管式臭氧发生器对气溶胶中的枯草杆菌黑色变种芽孢进行消毒,在18~24℃,RH为90%~95%,15min的杀灭率就达99.94%,用沿面放电等离子体臭氧发生器作用15min可把99.9%的枯草杆菌黑色变种芽孢杀灭,20min杀灭率达100%。
臭氧(O3)是一种具有强氧化性的分子,在大气层中起着重要的作用。
本文将从分子结构、化学性质、制备方法以及应用等方面对臭氧进行介绍。
一、分子结构臭氧分子的分子式为O3,由三个氧原子组成。
与氧分子(O2)相比,臭氧分子结构更为复杂,呈现出较大的扭曲度和角度变化。
臭氧分子的形状可以描述为一种“V”形,三个氧原子的键角为117.5°,其中一个氧原子与两个相邻的氧原子形成单键,与另一个相邻氧原子形成双键。
这种结构使臭氧分子具有较高的反应活性和氧化能力。
二、化学性质臭氧具有强氧化性,能够与多种物质发生反应,产生氧化或分解作用。
臭氧分子的反应性与其电子云分布和形状密切相关,其中最主要的反应方式是臭氧分子发生自身分解反应,生成两个氧分子和自由基O。
另外,臭氧也可以与其他物质如有机物、硫化物、亚硝酸盐等进行反应,产生氧化或分解作用。
此外,臭氧还具有较好的杀菌能力,在水处理、污染治理等领域得到广泛应用。
三、制备方法目前,臭氧主要通过电晕放电法、紫外线辐射法和冷等离子体法等方式进行制备。
1. 电晕放电法电晕放电法是一种将氧分子转化为臭氧的常用方法。
该方法利用电场作用,将氧分子加以激发,使其发生电离和激发态跃迁,最终形成臭氧分子。
电晕放电法操作简单,设备成本低廉,目前在污染治理、卫生消毒等方面得到广泛应用。
2. 紫外线辐射法紫外线辐射法是一种利用紫外线辐射将氧分子转化为臭氧的方法。
该方法通过紫外线照射氧分子,使其分子结构发生改变,形成臭氧分子。
这种方法适用于小规模生产制备,但能耗较高,不适用于大规模生产。
3. 冷等离子体法冷等离子体法是一种新兴的制备臭氧的方法。
该方法通过将氧分子置于冷等离子体中,使其跃迁到激发态,产生高能量电子和自由基,最终形成臭氧分子。
这种方法操作简单,能耗低,适用于大规模生产。
四、应用领域臭氧在各种领域有着广泛的应用,主要包括以下方面:1. 污染治理:臭氧能够有效分解有机物和气态污染物,对空气污染、水处理等具有良好的治理效果。
臭氧的知识点总结一、臭氧的形成1.1 臭氧的形成途径臭氧的主要形成途径有两种,一种是紫外光照射下的氧分子产生的单质氧,再通过化学反应与另外一个氧分子结合形成臭氧;另一种形成途径是通过一氧化氮的光解作用形成的自由基与氧分子反应形成臭氧。
1.2 影响臭氧形成的因素紫外光照射是臭氧形成的必要条件,所以当大气中的紫外线辐射量增大时,可以促进臭氧的形成;而气象条件也对臭氧的形成起到了一定的影响。
二、臭氧的性质2.1 物理性质臭氧是无色的,有刺激性气味的气体,它的融点是-192.5℃,沸点是-110℃,密度是0.00143g/cm3;2.2 化学性质臭氧是一种强氧化剂,它可以与许多物质发生化学反应,如与双键、三键形成过氧化物、与还原剂反应等。
三、臭氧的应用3.1 水处理领域利用臭氧的氧化性,可以将水中的有机物、氨氮等污染物氧化分解,从而实现水的净化;3.2 医疗领域利用臭氧具有杀菌、消毒的特性,可以应用于医院手术室、血液透析器等的消毒;3.3 废水处理领域臭氧可以将废水中的有机物、重金属等进行氧化还原反应,从而实现废水的净化。
四、臭氧的危害4.1 对人体的危害臭氧对人体的呼吸系统、眼睛等有一定的刺激作用,长时间暴露在高浓度的臭氧环境下会导致人体出现呼吸困难等症状;4.2 对环境的危害臭氧是一种强氧化剂,在大气中参与了许多气体和颗粒物的反应,导致了大气的污染,影响了空气质量。
五、臭氧的监测与控制5.1 监测方法目前常用的臭氧监测方法有分光光度法、紫外吸收法等;5.2 控制措施控制臭氧的方法主要有控制空气中的有机物排放,减少不必要的紫外线辐射等。
六、臭氧层的保护6.1 臭氧层的功能臭氧层的主要功能是吸收99%的紫外线,保护地球上的生物免受紫外线的伤害;6.2 臭氧层破坏的原因主要是由于温室气体的排放增多、氟氯烃类化合物的排放等所导致的。
七、臭氧的管理7.1 国际上的管理在国际上,有关臭氧的管理主要是通过国际公约,如蒙特利尔议定书等来进行的;7.2 国内的管理在国内,臭氧的管理主要是由环保部门来负责,通过监测、控制等手段来进行管理。
臭氧是不是易燃易爆气体臭氧是指由三个氧原子组成的气体分子,化学式为O3。
它是一种具有强氧化性的氧化剂,能杀灭大量病菌和病毒,并能处理各种废气和净化水源。
但对于它是否易燃易爆,我们需要对臭氧的特性和物理化学性质进行深入了解。
臭氧的物理化学性质臭氧是一种无色气体,在温度和压力正常的情况下,它的气体密度大于空气,容易被紫外线分解为氧气。
臭氧在常温下是稳定的,但是在高温和高压下会发生爆炸,释放大量氧气,从而对环境和人类造成伤害。
因此,其在工业生产和使用过程中需要严格控制和防止。
臭氧的分解因受温度、压力、湿度等因素影响较大,难以在常温和常压下稳定存在,易分解产生氧气,而氧气对于燃烧有强氧化性,能促进火源燃烧,这也是臭氧易燃易爆的重要原因之一。
臭氧对人体健康的影响臭氧具有一定的有害性,能对人体健康造成伤害。
对于工作在臭氧环境下的职业人员来说,长时间暴露在臭氧环境下,会出现头痛、头晕、乏力、心悸等症状,严重时会引起呼吸困难和胸痛等,并影响心脏、肺、中枢神经系统等器官的功能。
特别是儿童、老年人和患有呼吸系统疾病的人群更容易受到臭氧的伤害。
防范臭氧的方法在工业生产和使用臭氧的过程中,需要加强安全监管,防范臭氧的爆炸、中毒等事故发生。
具体防范措施如下:1.在生产现场建立完善的安全防护体系,采取必要的安全措施和器具。
2.严格控制生产设备的温度和压力,在生产过程中涉及到高温、高压和易爆颗粒物的,需要设置可燃气体探测器和温度/压力传感器等监控设备。
3.加强对员工的安全教育和技术培训,让操作人员了解臭氧的特性和安全操作规范,提高安全意识和技能水平。
4.优化生产工艺,减少臭氧产生的量和浓度,从根源上避免或减少安全隐患。
结论臭氧是一种稳定的无色气体,但在高温、高压下易发生爆炸,并会释放大量氧气,从而对环境和人类造成威胁。
因此,在工业生产和使用过程中,需要加强安全监管并采取必要的防范措施,保护人类和环境的安全。
认识臭氧卫生部《消毒技术规范》—臭氧臭氧又名三子氧,分子式为 O3,分子量为 48.00 。
一、理化特性:臭氧在常温下为带蓝色的爆炸性气体,有特臭,为已知最强的氧化剂,密度为 1.658( 空气 =1) 。
臭氧气体经冷处理后可呈液状,其液体密度为 1.71 ,沸点为 -112.3 ℃ , 在水中溶解度比氧高,但因分压较低,故在平时使用温度与压力下,只能得到每升数毫克的溶液,含臭氧的溶液,温热时会爆炸。
臭氧的稳定性极差,在常温下可自行分解为氧,在270 ℃ 高温下可立即转化为氧。
1% 水溶液在常温大气中半衰期为 16 分钟,所以臭氧不能像其它工业气体一样可以用瓶贮存,一般为现场生产,立即使用。
二、杀菌作用:臭氧是一种广谱杀菌剂,可杀灭细菌繁殖体和芽孢、病毒、真菌等,并可破坏肉毒杆菌毒素。
臭氧在水中杀菌迅速较氯快。
三、影响杀菌作用的因素:① PH:用臭氧水溶液消毒时,若PH增高,则所需浓度必须增加。
② 湿度:用臭氧熏蒸消毒时,相对湿度高则效果好,低则效果差,对干燥菌体几乎无杀菌作用。
③ 温度:温度降低有利于臭氧的溶解,可增强其消毒作用,甚至在0℃ 亦能保持较好的杀菌效果,如水温为4-6℃ 时,臭氧杀菌用量为100,水温10-21℃ 时为160,水温36-38℃ 时则为320,有机物可降低其杀菌作用。
四、毒性:空气中臭氧浓度达0 .01-0.02mg/L 时即可嗅知:浓度达到 1mg/L 时,可引起呼吸加速、变、胸闷等症状,在2 .5-5mg/L 时,可引起脉搏加速,疲倦、头痛,停留1小时可发生肺气肿,以至死亡,作业现场空气中容许的阀限值为0 .2mg/m3.五、腐蚀性:臭氧为强氧化剂 , 可损坏多种物品 , 浓度越高对物品损害越重 , 可使铜片出现绿色锈斑 , 特别是使橡胶老化 , 色变暗 , 弹性降低 , 以致变脆 , 断裂 , 使织物漂白褪色 .六、稳定性 : 臭氧稳定性极差,常温下即可自行分解为氧,停止发生后,通风30-60分钟后,其浓度与大气水平一样.七、使用范围:在消毒方面,臭氧的用途主要有以下几种:1、液体消毒:饮用水、工业生活污水和饮料水的净化消毒.2、物体表面消毒,饮食用具、理发工具、食品加工用具、衣物、钱币、票券等放密闭箱内消毒.3、防腐保存:蔬菜水果蛋类鱼肉类干鲜土特产,水产品加工,贮存和冷藏等.八、使用方法:1、液体消毒:臭氧消毒饮用水时,其用量取决于水质,应由实验确定精确值,比较清洁的水,一般应加臭氧0.5-1mg/L,作用5-10分钟后,水中保持臭氧浓度为0.1-0.5mg/L;对于污染比较严重的饮用水,臭氧用量可增至3-6 mg/L。
臭氧过氧化氢臭氧和过氧化氢是两种常见的氧化剂,它们在很多领域都有广泛的应用。
本文将分别介绍臭氧和过氧化氢的性质、制备方法以及它们在环境净化、医疗和工业领域中的应用。
一、臭氧1. 性质臭氧(O3)是一种具有强氧化性的气体,具有刺激性的气味,可以溶于水和有机溶剂。
臭氧是一种不稳定的物质,在常温下会分解成氧气,因此无法长期储存。
2. 制备方法臭氧可以通过紫外光或电晕放电将氧气(O2)分解产生。
在紫外光作用下,氧分子吸收能量后会发生异构化,生成臭氧。
而电晕放电则是通过高压电场使氧气分子发生电离和激发,从而形成臭氧。
3. 应用领域臭氧具有强氧化性和杀菌性,因此在环境净化和水处理领域有广泛应用。
臭氧可以被用于净化室内空气、水处理以及处理工业废水和废气。
此外,臭氧还可以被用于医疗领域,例如用于治疗伤口感染、消毒和灭菌等。
二、过氧化氢1. 性质过氧化氢(H2O2)是一种无色液体,具有刺激性的气味。
过氧化氢在常温下是相对稳定的,但遇到阳光、高温或金属催化剂时会分解放出氧气,因此需要储存和使用时要注意安全。
2. 制备方法过氧化氢可以通过将氢气(H2)与氧气(O2)在催化剂的作用下反应生成。
常见的制备方法包括电解法、氧化法和蒸气相法等。
3. 应用领域过氧化氢具有强氧化性和杀菌性,因此在医疗和工业领域有广泛应用。
在医疗领域,过氧化氢可以被用于消毒、灭菌以及伤口的清洁和治疗。
在工业领域,过氧化氢可以被用于漂白、废水处理以及有机合成等。
臭氧和过氧化氢是两种常见的氧化剂,它们具有强氧化性和杀菌性,在环境净化、医疗和工业领域有广泛的应用。
臭氧可以通过紫外光或电晕放电制备,而过氧化氢可以通过氢气与氧气的反应制备。
臭氧和过氧化氢的制备方法和应用领域各有不同,但它们都能发挥重要的作用。
希望本文能对读者对臭氧和过氧化氢有更深入的了解。
臭氧的性质
臭氧(OZONE),分子式O 3 ,分子量47.9982(≈48),在常温下为蓝色气体,有类似鱼腥的气
味。
臭氧的理化数据:
在标准状况下,密度 2.144g/L。
由于接近地面的干燥空气,密度为1.293g/L,因此臭氧密度是空气的1.658倍。
在-195.4 0 C时,液态臭氧密度为1.164g/ml。
临界温度为-12.1 0 C,临界压力为5.45×10 6 帕。
在冷水中的溶解度比氧气约大10倍。
空气中含有0.02PPm左右的臭氧。
一般情况下,空气中1PPm臭氧可取2.14mg/m 3 ,水中1PPm臭氧为1mg/L。
长期呼吸>0.1PPm臭氧,对人体有害。
臭氧浓度在0.02PPm时,嗅觉敏锐者能感觉到,称“感觉临界点”;0.15PPm时,一般人能嗅出,称“嗅觉临界值”(亦为卫生标准点);1-10PPm为“刺激范围”;10PPm以上为“中毒范围”。
臭氧不稳定,在高温时会迅速分解,在常温下会缓慢分解为(氧气),在1%的臭氧水溶液中半衰期约16分钟,在空气中的半衰期约25分钟。
臭氧的不稳定性使其很难实现瓶装贮存,一般只能利用臭氧发生器现场生产,随产随用。
臭氧是比氧气更强的氧化剂,且可以在较低温度下进行氧化。
所以,臭氧的一切应用(消毒、灭菌、水净化、漂白、作氧化剂等)本质上都是利用其强氧化能力。
由上可知,臭氧的强氧化性、常温作用性,特别是其“工作”后能还原为氧气,是其应用经久不衰,备受人类青脒的三大原因。
纯臭氧在受撞击、磨擦时会发生爆炸而分解,含高浓度臭氧溶液加热时易发生爆炸,但只要注意避免,此类事故即不易发生(至于臭氧对人体的毒害,臭氧问世150余年来,尚无一例中毒死亡的报告)。
臭氧用于空气消毒时,消毒现场不应有高浓度易燃易爆气体。
臭氧与水同存时为强烈漂白剂,其作用比氯气(Cl 2 )、双氧水(H 2 O 2 )、二氧化硫(SO 2 )快得多。
臭氧的获得:
臭氧可通过高压放电、电晕放电、化学等方法获得。
利用高压电离(或化学、光化学反应),使空气中的部分氧气分解聚合为臭氧,是氧的同素异形转变过程;亦可利用电解水法获得。
臭氧的广泛用途
臭氧主要应用于消毒灭菌(对空气、物体和水)和污水处理(环境治理)[详见第三章《臭氧的应用领域》。
此外,它还有漂白、水脱色、除异味、参加工业氧化反应、治疗疾病等许多特别用途。
臭氧消毒灭菌机理:
臭氧是一种强氧化剂,臭氧灭菌过程属生物化学氧化反应,O 3 灭菌有以下三种方式:
臭氧能氧化分解细菌内部氧化葡萄糖所必须的酶,使细菌灭活死亡。
直接与细菌、病毒作用,破坏它们的细胞壁和DNA和RNA,细菌的新陈代谢受到破坏,导致死亡。
(DNA——核糖核酸;RNA——脱氧核糖核酸。
病毒是由蛋白质包裹着一种核酸的大分子;病毒只含一种核酸。
摘自《微
生物学基础》,化工出版社1994版)。
渗透胞膜组织,侵入细胞膜内作用于外膜的脂蛋白和内部的脂多糖,使细菌发生透性畸变,溶解死亡。
消毒灭菌的很多优势
臭氧灭菌具有很多优点:
●高效性和广谱性
臭氧灭菌属溶菌级,杀菌彻底,无残留,杀菌广谱,可杀灭细菌繁殖体和芽孢、病毒、真菌等,并可破坏肉毒杆菌毒素,O 3 不仅对各种细菌有极强的杀灭作用,对杀死霉菌也很有效。
绿色灭菌,无任何污染
臭氧稳定性差,很快自行分解为氧气和单个氧原子。
单个氧原子又自行结合为氧分子,不存在任何有毒残留物,所以称无污染消毒灭菌剂。
●无死角
臭氧为气体,能迅速弥漫到整个灭菌空间,灭菌无死角。
消毒灭菌类型划分:
消毒灭菌根据其作用原理可分为:
抑菌如冰箱,通过改变环境温度抑制细菌生长,但细菌生存能力,适应能力很强,会很快适应并大量繁殖。
杀菌如紫外线、化学熏蒸,只能通过破坏细菌的外壳,使细菌死亡,而残余在细菌体内部(寄生)的病毒会快速繁殖。
溶菌如臭氧,能干净彻底地杀灭细菌和寄生的病毒,并且能将它们溶解为菌丝,使细菌彻底失去生命条件。
(注:抑菌、杀菌、溶菌概念,摘自《微生物学基础》1994版P-9)
臭氧对热原的杀灭作用:
热原属病毒,臭氧不仅可以直接杀灭病毒,还可以通过杀灭病毒所寄生的细菌和微生物的方式将热原杀灭。
消毒级别和消毒级别的具体规定
消毒级别即“洁净级别”。
各国GMP对洁净室中空气浮游菌及表面细菌有严格的规定,如USP(美国药典)1991年10月对洁净级别提出了建议(即洁净环境中的细菌允许值)。
见下表:细菌允许值
注:CFU——菌落数;inch 2 ——平方英寸
臭氧消毒灭菌对环境的要求:
本公司生产的臭氧化设备,由于工作电压低、结构紧凑、可靠性好,所以对使用环境(空气湿度、灰粒等)无苛刻要求。
比传统的高电压产生臭氧设备对环境的要求简单得多。
但本公司臭氧发生器不宜在以下场所使用:
(1)有易燃、易爆气体直接接触的场所(如需使用应预先进行气体置转换);
(2)粉尘过多的场所;
(3)50 0 C以上或-20 0 C以下的场所。
传统的消毒灭菌方法及其优缺点介绍
在空气和物体表面灭菌方面:
●紫外线优点是价格便宜,安装更换方便。
但缺点较多:
不彻底紫外线灭菌属杀菌级,不能干净彻底的杀灭细菌对病毒基本没有杀灭作用。
对霉菌的作用很差,是大肠杆菌的几十分之一。
有死角紫外线杀菌,光线照射不到的地方没有效果。
超过紫外灯光源1.5米以外的范围基本无效。
有衰退紫外线的杀菌能力随时间的增加而减退。
穿透力极弱紫外线穿透力极弱,一张纸、一层布,甚至灰尘和湿度都影响效果,只适用于表面杀菌。
●化学熏蒸利用甲醛、环氧乙烷等消毒液蒸发产生气体来熏蒸,这种方法的优点是具有一定的长效性。
缺点是:
不彻底化学熏蒸同样存在着不彻底的弊端,细菌的繁殖是惊人的;如大肠杆菌在37 0 C条件下,单个细菌24小时后可产生4722*10 21 个后代(《废水处理手册》,P-126,美国国家环保局编),采用化学熏蒸因杀菌不彻底,留下“祸根”,杀菌之后时间不长,细菌就繁殖超标。
对抗药性强的细菌和病毒效果更差,甚至无效。
工作量大无残留污染损害人体健康,有较重的令人难以忍受异味。
B、在饮用水消毒方面有:
紫外线紫外线对水消毒不仅存在和空气相同的缺点,并且对芽孢没有杀灭作用;另外紫外线消毒水处理水量小,质量检测大多细菌超标,国家已明令禁止。
●加氯气(CL 2 )缺点是:
经氯消毒的水存在残余污染,对人体有伤害,并有异味。
可能产生氯化氢等化合物,其中一些是已知的致癌化合物。
●加次氯酸盐缺点是:存在残余毒素(二次污染)。
臭氧灭菌的缺点及防范:
(1)臭氧对物体有氧化性,主要是对天然橡胶或天然橡胶制品以及铜制品(有水汽存在时)有一定的腐蚀。
对于其他材料因臭氧灭菌时间短腐蚀微弱可忽略不计。
(2)臭氧发生器工作时,不宜导入超过爆炸极限的易燃性气体。
(3)臭氧的穿透力弱,对物体纵深处细菌杀灭能力低。
臭氧消毒具有优越的性能
在消毒这方面,臭氧具有优越的性能,主要是高效性——臭氧消毒自产自销。
消毒时臭氧发生器产生一定量的臭氧,在相对密封的环境下工作,克服了紫外线杀菌只能直来直去,存在的消毒死角的问题,同时还具有很强的除霉、腥、臭等异味的功能;高洁性——臭氧可自然分解为氧气,不存在任何残留,解决了化学消毒剂消毒时,残留物的二次污染问题,同时省去了消毒结束后再次清洁的麻烦;方便性——臭氧杀菌如同使用电视机一样方便,只要看明白说明书,按照步骤操作即可.。