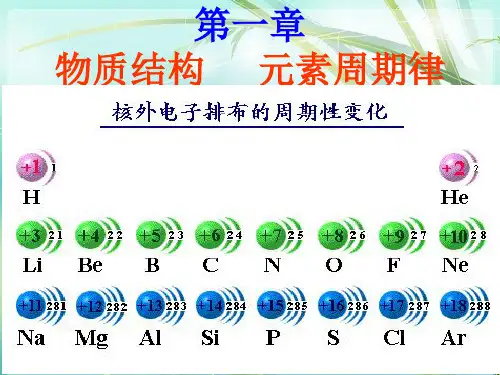
例如:NaCl、KCl、NH4Cl、NaOH等。
共价键 1、定义:原子间通过共用电子对所形 成的相互作用。
2、形成元素: 1)同种或不同种非金属元素结合; 2)部分金属元素元素原子与非金属元素, 如AlCl3 ;BeCl2 ; 3、共价化合物:以共用电子对形成分子 的化合物。 4、共价键的存在:HCl、H2等,一些 离子化合物中,如NaOH、Na2O2等。
分子结构和化学键
用电子式表示离子键、共价键的形成过程
.+
2+
H.
H × ×H
离子键和共价键的比较
离子键
共价键
成键微粒 阴、阳离子
原子
成键本质 静电作用
表示方法 Na+ [:C·l·:]··
成键元素 活泼金属与活 泼非金属元素
共用电子对
·· ··
H
C··l ··
同种或不同价化合 子化合物中 物及部分离子化合物中
性
卤素的性质
名
相似形
递变性
称 最外层 物理 化学 电子 熔点 沸点 密度 化学
电子数 性质 性质 层数
性质
氟
氯 溴 碘
7
单质 的熔, 沸点 较低, 颜色 较深
单质 具有 强的 氧化
性
逐 渐 增 多
逐 渐 升 高
非 逐逐金 渐渐属 升增性 高大逐
渐 减 弱
五、化学键
定义:相邻的两个或多个原子(或离子)
5、共价键可分为极性键和非极性键。 如:H—Cl、H—F键等为极性键;H—
H、Cl—Cl键等为非极性键。
电子式:
元素符号周围用“•”或“×”来表示原
子的最外层电子(价电子)的式子叫做电
子式。
H︰H
‥ H︰‥N︰H