高考化学考点硫及其重要化合物
- 格式:pptx
- 大小:869.02 KB
- 文档页数:13

高考化学硫知识点总结化学是高考科目之一,对于学生来说,掌握化学知识是非常重要的。
其中,硫元素是化学中的重要一环。
本文将对高考化学中与硫相关的知识点进行总结和归纳。
一、硫的性质和用途硫的原子序数为16,位于氧的下方,属于周期表的第16族。
硫是一种黄色固体,在常温下呈现出异味。
硫的主要存在形式为硫化物,如硫化氢、硫代硫酸盐等。
硫在化学反应中可以表现出特殊的性质,如与氧反应生成二氧化硫,与金属反应生成对应的硫化物。
硫在工业上有着广泛的应用,其中最重要的是在肥料和药物制剂中的应用。
硫肥可以提高农作物的产量和品质,同时还可以作为某些蛋白质和药物的原料。
此外,硫还可以用于橡胶工业、皮革工业、油脂工业等许多领域。
二、硫的氧化态和离子化合物根据硫的氧化态,硫化物可以分为低价态和高价态。
低价态的硫化物中硫的氧化态为-2,如硫化氢(H2S)、硫化镁(MgS)等。
高价态的硫化物中硫的氧化态大于-2,如二氧化硫(SO2)、二氧化硫(SO3)等。
硫的离子化合物也是化学中的重要内容。
硫在离子中的氧化态取决于与硫结合的其他元素的氧化态。
比如,硫与氧结合成硫酸根离子(SO42-),硫的氧化态为+6;而硫与氢结合成硫氢离子(HS-),硫的氧化态为-1。
三、硫的还原性和氧化性硫具有较好的还原性和氧化性,这对于它在化学反应中起着重要的作用。
在还原反应中,硫可以被氢气还原为硫化氢:S + H2 → H2S在氧化反应中,硫可以与金属反应生成硫化物:S + 2M → MS2硫的这种性质使得它在许多工业和生活中都有着广泛的应用,比如制造火柴和火药、脱硫等。
四、硫的环境污染和防治虽然硫是一种重要的元素,但过量的硫却会对环境和人体健康造成危害。
硫在大气中生成二氧化硫,会导致空气污染和酸雨的发生。
同时,硫也会通过水体、土壤等途径进入生态系统,对生态环境造成破坏。
为了减少硫的环境污染,需要采取相应的措施。
其中,使用脱硫装置对工业废气进行处理是一种常见的方法。
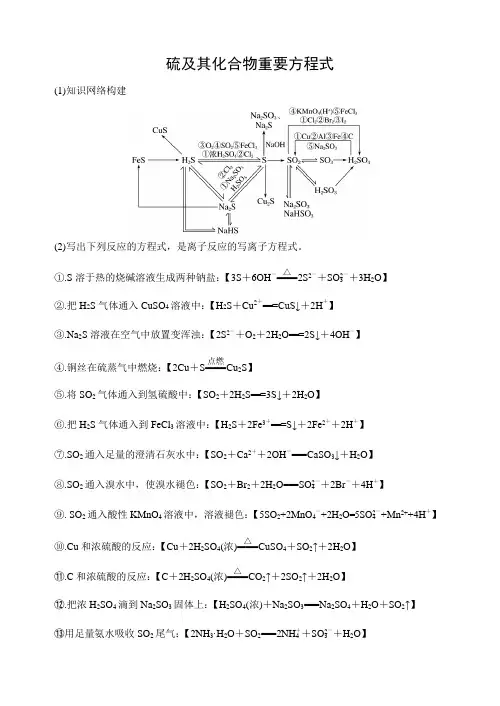
硫及其化合物重要方程式
(1)知识网络构建
(2)写出下列反应的方程式,是离子反应的写离子方程式。
①.S 溶于热的烧碱溶液生成两种钠盐:【3S +6OH -=====△2S 2-+SO 2-3+3H 2O 】 ②.把H 2S 气体通入CuSO 4溶液中:【H 2S +Cu 2+===CuS↓+2H +】 ③.Na 2S 溶液在空气中放置变浑浊:【2S 2-+O 2+2H 2O===2S↓+4OH -】 ④.铜丝在硫蒸气中燃烧:【2Cu +S =====点燃
Cu 2S 】
⑤.将SO 2气体通入到氢硫酸中:【SO 2+2H 2S===3S↓+2H 2O 】 ⑥.把H 2S 气体通入到FeCl 3溶液中:【H 2S +2Fe 3+===S↓+2Fe 2++2H +】 ⑦.SO 2通入足量的澄清石灰水中:【SO 2+Ca 2++2OH -===CaSO 3↓+H 2O 】 ⑧.SO 2通入溴水中,使溴水褪色:【SO 2+Br 2+2H 2O===SO 2-4+2Br -+4H +】
⑨. SO 2通入酸性KMnO 4溶液中,溶液褪色:【5SO 2+2MnO 4-+2H 2O=5SO 2-4+Mn 2++4H +】 ⑩.Cu 和浓硫酸的反应:【Cu +2H 2SO 4(浓)=====△CuSO 4+SO 2↑+2H 2O 】 ⑪.C 和浓硫酸的反应:【C +2H 2SO 4(浓)=====△CO 2↑+2SO 2↑+2H 2O 】 ⑫.把浓H 2SO 4滴到Na 2SO 3固体上:【H 2SO 4(浓)+Na 2SO 3===Na 2SO 4+H 2O +SO 2↑】 ⑬用足量氨水吸收SO 2尾气:【2NH 3·H 2O +SO 2===2NH +4+SO 2-3+H 2O 】。
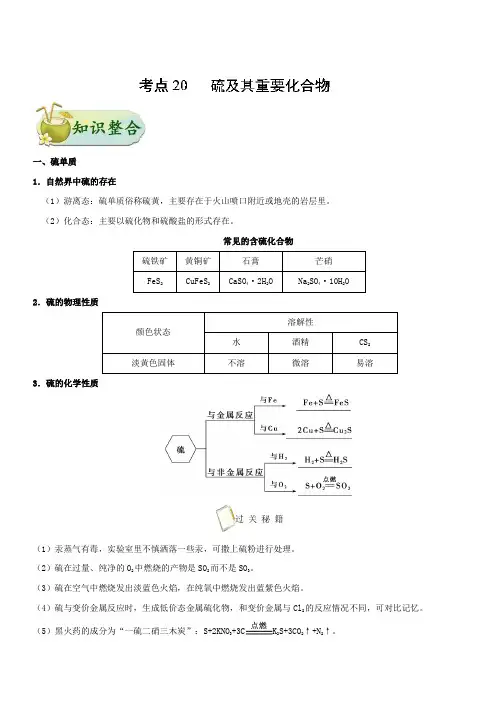
一、硫单质1.自然界中硫的存在(1)游离态:硫单质俗称硫黄,主要存在于火山喷口附近或地壳的岩层里。
(2)化合态:主要以硫化物和硫酸盐的形式存在。
常见的含硫化合物2.硫的物理性质溶解性颜色状态水酒精CS2淡黄色固体不溶微溶易溶3.硫的化学性质过关秘籍(1)汞蒸气有毒,实验室里不慎洒落一些汞,可撒上硫粉进行处理。
(2)硫在过量、纯净的O2中燃烧的产物是SO2而不是SO3。
(3)硫在空气中燃烧发出淡蓝色火焰,在纯氧中燃烧发出蓝紫色火焰。
(4)硫与变价金属反应时,生成低价态金属硫化物,和变价金属与Cl2的反应情况不同,可对比记忆。
(5)黑火药的成分为“一硫二硝三木炭”:S+2KNO3+3C K2S+3CO2↑+N2↑。
二、硫的氧化物——二氧化硫和三氧化硫1.二氧化硫(1)物理性质(2)化学性质①酸性氧化物的通性a.与水反应:SO 2+H2O H2SO3b.使指示剂变色:SO2能使紫色石蕊溶液变红c.与碱反应:NaOH足量:SO2+2NaOH Na2SO3+H2ONaOH不足量:SO2+NaOH NaHSO3d.与碱性氧化物反应:SO2+CaO CaSO3②氧化性:2H2S+SO23S↓+2H2O(产生淡黄色沉淀)③还原性a.与O2反应:2SO2+O22SO3b.与X2(Cl2、Br2、I2)的水溶液反应:SO2+X2+2H2O2HX+H2SO4c.可被酸性KMnO4溶液、K2Cr2O7溶液、H2O2、Fe3+等氧化。
④漂白性:SO2能漂白某些有色物质(如品红溶液),但不能使紫色石蕊溶液等指示剂褪色。
(3)检验将气体通入品红溶液后,溶液褪色,加热后溶液又恢复到红色则可验证该气体是SO2。
注意“加热”是必不可少的步骤,因为氯气也能使品红溶液褪色,但加热后溶液不会重新变红色。
2.三氧化硫(1)物理性质常温常压下为无色、易挥发的液体,熔点为16.8 ℃,沸点为44.8 ℃。
(2)化学性质:酸性氧化物的通性三、硫酸的性质和23SO -、24SO -的检验 1.硫酸的性质干燥注意:(1)浓硫酸的稀释方法:将浓硫酸沿器壁慢慢注入水中,并用玻璃棒不断搅拌。

高考化学硫单质及其化合物必背知识点高考化学硫单质及其化合物必背知识点硫单质及其化合物是高考重点考察的知识点,它有哪些关键的地方需要考生们记住呢?下面是店铺为大家精心推荐的高考化学硫单质及其化合物必背知识点,希望能够对您有所帮助。
(一)硫单质的反应(非金属性弱于卤素、氧和氮)1.硫与氧气反应(只生成二氧化硫,不生成三氧化硫)2.硫与氢气加热反应3.硫与铜反应(生成+1价铜化合物,即硫化亚铜)4.硫与铁反应,(生成+2价铁化合物,即硫化亚铁)5.硫与汞常温反应,生成HgS(撒落后无法收集的汞珠应撒上硫粉,防止汞蒸气中毒)7.硫与强碱溶液反应生成硫化物和亚硫酸盐(试管上粘附的硫除了可用CS2洗涤以外,还可以用NaOH溶液来洗)3S+6NaOH=2Na2S+Na2SO3+3H2O(二)二氧化硫或亚硫酸的反应(弱氧化性,强还原性,酸性氧化物)1.氧化硫化氢2.被氧气氧化(工业制硫酸时用催化剂;空气中的二氧化硫在某些悬浮尘埃和阳光作用下被氧气氧化成三氧化硫,并溶解于雨雪中成为酸性降水。
)3被卤素氧化SO2+Cl2+2H2O==H2SO4+2HCl4.与水反应5.与碱性氧化物反应6.与碱反应7.有漂白性(与有机色质化合成无色物质,生成的无色物质不太稳定,受热或时日一久便返色)(三)硫酸性质用途小结1.强酸性(1)、与碱反应(2)、与碱性氧化物反应(除锈;制硫酸铜等盐)(3)、与弱酸盐反应(制某些弱酸或酸式盐)(4)、与活泼金属反应(制氢气)2.浓硫酸的吸水性(作气体干燥剂;)3.浓硫酸的脱水性(使木条、纸片、蔗糖等炭化;乙醇脱水制乙烯)4.浓硫酸的强氧化性(1)、使铁、铝等金属钝化;(2)、与不活泼金属铜反应(加热)(3)、与木炭反应(加热)(4)、制乙烯时使反应混合液变黑5.高沸点(不挥发性)(制挥发性酸)(1)、制氯化氢气体(2)、制硝酸(HNO3易溶,用浓硫酸)实验室制二氧化碳一般不用硫酸,因另一反应物通常用块状石灰石,反应生成的硫酸钙溶解度小易裹在表面阻碍反应的进一步进行。

高中化学硫及其化合物知识大全1、硫元素的存在:硫元素最外层电子数为6个,化学性质较活泼,容易得到2个电子呈-2价或者与其他非金属元素结合成呈+4价、+6价化合物。
硫元素在自然界中既有游离态, 又有化合态。
(如火山口中的硫就以游离态存在)2、硫单质:①物质性质:俗称硫磺,淡黄色固体,不溶于水,微溶于酒精,易溶于二硫化碳,熔点低。
②化学性质:S+O2 ===(点燃) SO2(空气中点燃淡蓝色火焰,纯氧中为蓝紫色)Fe+SFeS 2Cu+SCu2S 2Na+S=Na2SHg+S==HgS(汞滴处理)3S+6NaOH(浓)2Na2S+Na2SO3+3H2O(洗硫)3、二氧化硫(SO2)(1)物理性质:有刺激性气味有毒气体, 可溶于水(1:40),易液化。
(2)化学性质:①SO2能与水反应:SO2+H2O H2SO3亚硫酸为中强酸,此反应为可逆反应。
可逆反应定义:在相同条件下,正逆方向同时进行的反应。
(关键词:相同条件下)②SO2为酸性氧化物,可与碱反应生成盐和水。
a、与NaOH溶液反应:SO2(少量)+2NaOH=Na2SO3+H2OSO2(过量)+NaOH=NaHSO3对比CO2与碱反应:CO2(少量)+Ca(OH)2=CaCO3↓(白色)+H2O2CO2(过量)+Ca(OH)2=Ca(HCO3)2(可溶)将SO2逐渐通入Ca(OH)2溶液中先有白色沉淀生成,后沉淀消失,与CO2逐渐通入Ca(OH)2溶液实验现象相同,故不能用石灰水来鉴别SO2和CO2。
能使石灰水变浑浊的无色无味的气体一定是二氧化碳,这说法是对的,因为SO2是有刺激性气味的气体。
b、SO2将通入酚酞变红的溶液,溶液颜色褪去,体现了SO2和水反应生成亚硫酸,是酸性氧化物的性质,而不是漂白性,SO2不能漂白指示剂。
③SO2具有强还原性,能与强氧化剂(如酸性KMnO4溶液、Cl2、O2(催化剂:粉尘、V2O5)等)反应。
SO2能使酸性KMnO4溶液、新制氯水褪色,显示了SO2的强还原性(不是SO2的漂白性)。


高考化学关于硫知识点硫是我们常见的一种元素,它在自然界中广泛存在,并且在多个领域中都发挥着重要的作用。
在高考化学中,硫也是一个重要的考点。
下面我们将深入探讨一些关于硫的知识点,以帮助同学们更好地准备高考。
1. 硫的性质硫是一种非金属元素,它的原子符号为S,原子序数为16。
硫有非常特殊的性质,其中最为明显的就是它的颜色。
硫可以表现出黄色的颜色,常说的硫黄就是指黄色的硫。
此外,硫还具有非常强烈的气味,有一种特殊的臭味。
这也是我们在生活中经常闻到的硫磺味的来源。
2. 硫的存在形式硫在自然界中以多种形式存在。
其中最常见的就是硫矿石,如黄铁矿和硫化铜等。
此外,硫还存在于许多矿石中,如辉绿石、黄铜矿等。
除此之外,硫还以硫酸、硫酸盐的形式存在于天然水、土壤和生物体内。
3. 与硫有关的化合物硫与其他元素组成了许多重要的化合物。
其中最著名的就是二氧化硫(SO2)和三氧化硫(SO3)。
二氧化硫是一种无色气体,具有刺激性气味。
它是大气中污染物的重要成分,也是酸雨的主要原因之一。
三氧化硫则是硫酸的前体,在工业生产中有着重要的应用。
此外,硫还与氢、氧、碳、氮等元素形成了类似硫醇、硫醚、硫酮和硫脲等多种有机化合物。
这些有机硫化合物在生命体中具有重要的生物学功能,如充当生物催化剂、维持生物膜的完整性等。
4. 硫的化学反应硫在化学反应中也表现出一些特殊的性质。
例如,硫和氧气可以发生化学反应生成二氧化硫。
在这个反应中,硫的化合价由0增加到+4,氧化了。
这个反应是许多火山喷发和燃烧过程中的重要反应。
另外,硫还可以与氢气反应生成硫化氢。
这是一种具有刺激性气味的气体,也是很多硫化物的常见产物。
5. 硫的应用由于硫的特殊性质和广泛存在,它在多个领域中有着重要的应用。
其中最常见的就是化肥生产和硫酸制造。
硫酸是一种重要的工业原料,广泛用于化工、冶金、环保等行业。
此外,硫还可以用于生产橡胶、染料、药品等。
在生物体中,硫也是不可或缺的元素之一。


第19讲 硫及其化合物【课程标准】 1.掌握硫及其重要化合物的主要化学性质及应用。
2.了解硫的氧化物对大气的污染与防治。
考点一 硫单质的性质1.自然界中的硫形态,游离态火山喷口附近或地壳的岩层里,化合态主要以硫化物和硫酸盐的形式存在 2.物理性质3.化学性质(1)氧化性:(0价→-2价)(2)还原性:(0价→+4价) S +O 2=====点燃SO 2(3)与碱发生歧化反应(如NaOH 溶液): 3S +6NaOH=====△2Na 2S +Na 2SO 3+3H 2O 。
[正误辨析]1.硫在自然界中仅以化合态存在( )2.硫在空气中燃烧的产物是SO 2,在纯氧中燃烧的产物是SO 3( ) 3.硫与铁粉和铜粉分别反应,都可生成二价金属硫化物( )4.等质量的S 6和S 8分子分别与足量的KOH 反应,消耗KOH 的物质的量相同( ) 5.常温下硫单质主要以S 8形式存在,加热时S 8转化为S 6、S 4、S 2属于物理变化( )6.汞蒸气有毒,实验室里不慎洒落一些汞,可撒上硫粉进行处理( ) 答案:1.× 2.× 3.× 4.√ 5.× 6.√正误判断(1)(2022·山东卷)“能化……银、铜、铁,奇物”,石硫黄(S)表现氧化性( ) (2)(2019·浙江卷)硫元素在自然界中的存在形式有硫单质、硫化物和硫酸盐等( ) 答案:(1)√ (2)√硫是生物必需的营养元素之一,下列关于自然界中硫循环(如图所示)说法正确的是( )A .含硫杆菌及好氧/厌氧菌促进了硫的循环B .硫循环中硫的化合物均为无机物C .上述硫循环中硫元素均被氧化D .烧煤时加石灰石,可减少酸雨及温室气体的排放 答案:A解析:硫酸盐和亚硫酸盐等在含硫杆菌及好氧/厌氧菌作用下缓慢转化成植物R 1-S -R 2,含硫杆菌及好氧/厌氧菌促进了硫的循环,故A 正确;硫循环中硫的化合物有含硫的有机物,不全是无机物,故B 错误;含硫杆菌及好氧/厌氧菌将硫酸盐、亚硫酸盐中的硫还原成R 1-S -R 2,硫循环中硫元素有时被氧化,有时被还原,故C 错误;烧煤时加石灰石,CaCO 3+SO 2=====△CaSO 3+CO 2可减少酸雨,除上述反应外石灰石分解生成二氧化碳,会增加温室气体的排放,故D 错误。


知识清单12硫及其重要化合物知识点01单质硫的性质及应用知识点03亚硫酸、亚硫酸盐和硫代硫酸盐知识点05硫酸根离子的检验知识点02硫氧化物的结构、性质和制备知识点04浓硫酸的性质与应用知识点01单质硫的性质及应用1.硫的结构(1)原子结构示意图,离子结构示意图(2)性质:在反应中容易得到2个电子形成最外层8电子稳定结构,表现氧化性(3)常见化合价:-2,0,+4和+62.硫元素的自然存在(1)游离态:主要存在于火山喷口附近或地壳的岩层里。
(2)化合态:主要以硫化物和硫酸盐的形式存在。
硫铁矿黄铜矿石膏芒硝FeS 2CuFeS 2CaSO 4·2H 2ONa 2SO 4·10H 2O3.硫的同素异形体(1)单斜硫、斜方硫和正交硫(2)S 8的结构①化学键/mol :8②S 原子的杂化方式:sp 3③分子极性:非极性分子4.硫单质物理性质(1)色、态:黄色或淡黄色的固体,俗称硫黄(2)溶解性:不溶于水,微溶于酒精,易溶于二硫化碳5.弱氧化性:Fe ------→S加热FeS ;Cu -----→S加热Cu 2S 6.燃烧反应(1)反应:S+O 2SO 2;S ---------→过量O 2点燃SO 2(2)氧气浓度不同,产物相同,现象不同①空气:产生微弱的淡蓝色火焰②氧气:产生明亮的蓝紫色火焰易错点:硫的易错知识点(1)单质硫燃烧时,产物只能是SO 2,无论O 2的量是否充足,均不会生成SO 3。
(2)硫单质的氧化性较弱,与变价金属反应时一般生成低价态金属硫化物(和Cl 2与变价金属的反应情况相反),如FeS 、Cu 2S 等。
(3)等量的硫在空气中完全燃烧比在氧气中完全燃烧放热多(光能少)(4)汞蒸气有毒,实验室里不慎洒落一些汞,可撒上硫粉进行处理。
(5)实验室中,残留在试管内壁上的硫可用CS 2溶解除去,也可用热的NaOH 溶液除去,反应化学方程式为3S+6NaOH2Na 2S+Na 2SO 3+3H 2O 。
第24讲硫及其化合物的相互转化[复习目标] 1.能从物质类别、硫的化合价变化理解硫及其化合物的转化关系。
2.掌握硫及其重要化合物的性质及制备方案。
1.同价态硫的化合物之间的转化关系(1)+4价硫的化合物之间的转化写出①的离子方程式:HSO -3+H +===SO 2↑+H 2O ;写出②的离子方程式:HSO -3+OH -===SO 2-3+H 2O ;写出③的化学方程式:2NaHSO 3=====△Na 2SO 3+SO 2↑+H 2O ;写出④的化学方程式:Na 2SO 3+SO 2+H 2O===2NaHSO 3。
(2)-2价硫的化合物之间的转化氢硫酸(H 2S)是二元酸,与酸式盐(NaHS)、正盐(Na 2S)之间的转化关系,跟H 2SO 3、亚硫酸氢盐、亚硫酸盐之间的转化关系相似。
①写出硫氢化钠(NaHS)与NaOH 反应的离子方程式:HS -+OH -===H 2O +S 2-。
②写出NaHS 与HCl 反应的离子方程式:HS -+H +===H 2S ↑。
2.不同价态硫的转化是通过氧化还原反应实现的当硫元素的化合价升高或降低时,一般升高或降低到其相邻的价态,即台阶式升降,可用下图表示:如:H 2S ①O 2 不足④H 2、△S ②O 2⑤H 2S SO 2――→③O 2SO 3写出③④⑤反应的化学方程式:③2SO 2+O 2催化剂△2SO 3;④S +H 2=====△H 2S ;⑤SO 2+2H 2S===3S +2H 2O 。
注意(1)同种元素相邻价态的粒子间不发生氧化还原反应,如S 和H 2S 、S 和SO 2、SO 2和浓硫酸之间不发生氧化还原反应。
(2)当硫元素的高价态粒子与低价态粒子反应时,一般生成中间价态,如2Na 2S +Na 2SO 3+3H 2SO 4===3Na 2SO 4+3S ↓+3H 2O 。
一、硫的循环转化1.硫是生物必需的营养元素之一,下列关于自然界中硫循环(如图所示)的说法正确的是()A .含硫杆菌及好氧/厌氧菌促进了硫的循环B .硫循环中含硫化合物均为无机物C .上述硫循环中硫元素均被氧化D .烧煤时加石灰石,可减少酸雨及温室气体的排放答案A 解析硫酸盐和亚硫酸盐等在含硫杆菌及好氧/厌氧菌作用下缓慢转化成植物R 1—S—R 2,含硫杆菌及好氧/厌氧菌促进了硫的循环,故A 正确;硫循环中含硫化合物有有机物,如R 1—S—R 2,也有无机物,如SO 2,故B 错误;硫循环中硫元素有的被氧化,有的被还原,故C 错误;烧煤时加石灰石,可减少SO 2的排放,但不会减少温室气体的排放,故D 错误。
2023高考化学一轮复习知识点:硫单质及其化合物1500字硫(S)是一种常见的非金属元素,具有多种物理和化学性质。
硫单质的化学式为S8,它的存在形式可以是黄色晶体、橙黄色粉末或者黄褐色透明胶状物。
硫单质的制备方法主要有以下两种:1. 从天然硫矿中提取:硫矿是指含有大量硫的矿石,常见的硫矿有辉硫矿、硫铁矿等。
硫矿中的硫经过矿石破碎、矿石浮选等工艺处理后,可以得到纯净的硫单质。
2. 通过加热硫化物:硫单质可以通过加热金属硫化物来制备。
例如,将铁与硫粉末混合加热,铁与硫反应生成硫化铁,然后再通过加热硫化铁来制备硫。
硫单质具有以下几个重要的化学性质:1. 燃烧性质:硫单质可以在氧气中燃烧,产生二氧化硫(SO2)气体。
硫燃烧的化学方程式为:S + O2 → SO22. 溶解性质:硫单质几乎不溶于水,但可以溶解于有机溶剂如二硫化碳(CS2)。
硫和二氧化硫在水中的溶解度较小,而在二硫化碳中的溶解度较大。
3. 氧化性:硫单质具有较强的氧化性。
例如,硫可以与金属反应生成金属的硫化物。
硫化物是一类重要的化合物,如FeS、CuS等。
硫化物是硫与其他元素形成的化合物。
硫化物具有广泛的应用,例如在金属冶炼、化工工艺、能源生产等领域中都有重要的作用。
一些常见的硫化物有:1. 硫化氢(H2S):是一种无色、有刺激性气味的气体,具有强烈的毒性。
硫化氢广泛存在于天然气、石油等矿物资源中。
2. 二硫化碳(CS2):是一种无色液体,具有强烈的挥发性和可燃性。
它广泛应用于橡胶工业、农药生产等领域。
3. 三硫化二磷(P2S3):是一种黄色固体,是一种常用的农药成分。
4. 二硫化锌(ZnS):是一种白色固体,常用于制备发光材料。
此外,硫还可以形成一些含氧化合物,如亚硫酸(H2SO3)、硫酸(H2SO4)等。
硫酸是一种广泛应用的化学品,具有强酸性和腐蚀性。
总之,硫单质及其化合物是化学中重要的一类物质。
理解硫的性质及其与其他元素的反应,对于理解硫化物的合成和应用具有重要的意义。
硫及其化合物【考情分析】1.了解硫及其重要化合物的制备方法,掌握其主要化学性质及其应用。
2.了解硫的氧化物对环境的影响。
【核心素养分析】1.变化观念与平衡思想:从硫的化合价变化认识硫及其化合物的相互转化及应用。
2.科学探究与创新意识:从不同的角度探究硫及其重要化合物的性质及制备实验方案,并进行实验操作验证。
3.科学态度与社会责任:关注与SO2有关的污染和环境保护,具有可持续发展意识和绿色化学观念。
【重点知识梳理】知识点一 硫及其氧化物的性质 一、硫单质的性质及应用 1.硫元素的存在形态(1)游离态:在火山口附近或地壳的岩层例存在 (2)化合态:以硫化物和硫酸盐的形式存在 2.硫单质的物理性质硫单质俗称硫黄,是一种淡黄色固体;不溶于水,微溶于酒精,易溶于CS 2;有多种同素异形体,如单斜硫、斜方硫等。
3.硫单质的化学性质 (1)S 的氧化性S 与Fe 、Cu 、Hg 反应的化学方程式依次为Fe +S=====△FeS 、2Cu +S=====△Cu 2S 、S +Hg===HgS(此反应适用于除去室内洒落的Hg)。
(2)S 的还原性①S 与O 2反应的化学方程式为S +O 2=====点燃SO 2,在空气中燃烧火焰为淡蓝色。
②与强氧化剂反应(如浓硫酸)的化学方程式为S +2H 2SO 4(浓)=====△3SO 2↑+2H 2O 。
(3)S 与NaOH 溶液反应的化学方程式为3S +6NaOH=====△2Na 2S +Na 2SO 3+3H 2O ,该反应中硫既是氧化剂,又是还原剂,此反应可用于除去试管内黏附的S 。
【特别提醒】①硫与变价金属反应时,生成低价态金属硫化物(如Cu 2S 、FeS)。
②汞蒸气有毒,实验室里不慎洒落一些汞,可撒上硫粉进行处理。
二、硫的氧化物(SO 2、SO 3)的性质及应用 1.二氧化硫(SO 2) (1)物理性质二氧化硫是无色、有刺激性气味的有毒气体,是大气污染物之一;易溶于水,通常状况下,1体积水溶解约40体积SO 2。