第七章 相平衡原理
- 格式:ppt
- 大小:2.28 MB
- 文档页数:83


1、几个基本概念一、相平衡:在一定的条件下,当一个多相系统中各相的性质和数量均不随时间变化时,称此系统处于相平衡。
此时从宏观上看,没有物质由一相向另一相的净迁移,但从微观上看,不同相间分子转移并未停止,只是两个方向的迁移速率相同而已。
二、吉布斯函数:G=H 一TS ,亦称为吉布斯自由能。
G 是一个由H 和T ,S 组合得到的物理量,它具有能量的量纲。
由于H ,S ,T 都是 状态函数,因而G 也必是一个状态函数。
三、化学势:在一个热力系统中,温度是热量传递的驱动力,压力是功传递的驱动力,化学势则是在各相之间或在某给定相的各部分之间质量传递的驱力。
()()()()i j n V S i i j n V S i i j n V S i i j n V S i i j j j j n G n A n H n U ≠≠≠≠⎪⎪⎭⎫ ⎝⎛∂∂=⎪⎪⎭⎫ ⎝⎛∂∂=⎪⎪⎭⎫ ⎝⎛∂∂=⎪⎪⎭⎫ ⎝⎛∂∂=,,,,,,,,μ四、吉布斯方程众所周知,确定质量和成分不变的简单可压缩系统的热力学状态需要两个独立参数。
但是,对于可变成分的系统,显然还需要确定成分。
例如,如果用S 和V 为独立变量,则成分固定的封闭的势力学能是U=U(S,V)成分变化的开口系统,U 还应该是r 种不同组元的物质的量n 1,n 2,···n r 的函数,即U=U(S,V , n 1,n 2,···n r )所以开口体系的热力学能的全微分是()i r i i j n V S i n S n V dn n U dV V U dS S U dU j ∑=≠⎪⎪⎭⎫ ⎝⎛∂∂+⎪⎭⎫ ⎝⎛∂∂+⎪⎭⎫ ⎝⎛∂∂=1,,,,式中n 表示所有组分的物质的量保持常数,即成分不变,而下标n j (j ≠i)表示除n i 之外所有其他组分的n 保持常数。
当在微分过程中所有组分的n 保持不变时,则有T S U n V =⎪⎭⎫ ⎝⎛∂∂, 和p V U nS -=⎪⎭⎫ ⎝⎛∂∂, 而组元i 的化学势()i j n V S i i j n U ≠⎪⎪⎭⎫⎝⎛∂∂=,,μ 因此U 的全微分可写为∑=+-=ri ii dn pdV TdS dU 1μ (4.3) 同样,多组元系统的其它广延参数,也是不同组元的物质的量n 1,n 2,···n r 的函数。
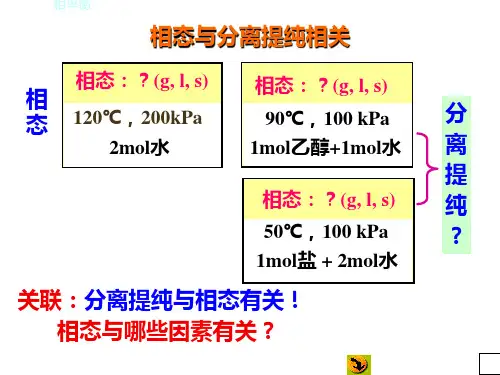


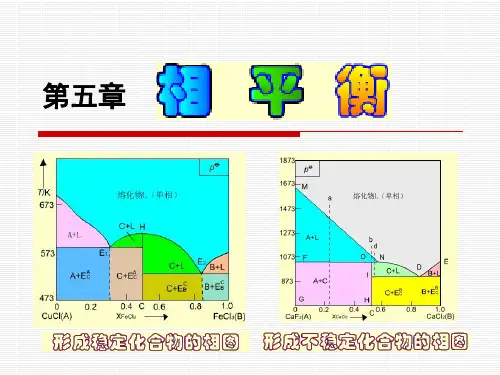

物理化学相平衡在我们生活的这个世界里,物质以各种各样的形式存在着,它们之间的相互转化和共存遵循着一定的规律,这就是物理化学中的相平衡。
相平衡研究的是在不同条件下,物质的不同相之间的平衡关系。
它不仅是物理化学的重要组成部分,也在许多实际领域,如化工、材料科学、地质科学等,发挥着关键作用。
让我们先来理解一下什么是“相”。
简单来说,相是指系统中物理性质和化学性质完全均匀的部分。
比如说,一杯水就是一个单相系统,因为水的性质在整个杯子中是均匀的。
但如果在水里加入油,就形成了水相和油相两个不同的相。
相平衡的概念可以通过一些常见的现象来理解。
比如,在一个封闭的容器中,水会不断蒸发变成水蒸气,而水蒸气也会不断凝结成水。
当蒸发和凝结的速率相等时,就达到了气液两相的平衡状态。
再比如,在冬天,湖面上的水会结冰,而冰和水在一定温度下能够稳定共存,这也是一种相平衡。
那么,相平衡是如何实现的呢?这就涉及到热力学的知识。
热力学第一定律告诉我们能量是守恒的,而热力学第二定律则指出了自发过程的方向和限度。
在相平衡中,系统的自由能会达到最小值,从而使得相的组成和性质保持稳定。
相律是描述相平衡系统的重要规律。
它由吉布斯提出,表达式为 F= C P + 2 ,其中 F 表示自由度,C 表示组分数,P 表示相数。
自由度是指在不改变相的种类和数目时,可以独立改变的强度性质的数目,比如温度、压力、浓度等。
通过相律,我们可以对相平衡系统进行分析和计算。
比如说,对于一个单组分系统,如水的气液平衡,组分数 C = 1 ,相数 P = 2 (气相和液相),那么自由度 F = 1 2 + 2 = 1 。
这意味着在温度和压力两个变量中,只有一个可以独立变化。
比如,在一定压力下,水的沸点是固定的,改变压力,沸点也会随之改变。
多组分系统的相平衡就更加复杂了。
以盐水溶液为例,盐和水构成了两个组分。
当盐的浓度不同时,可能会出现不同的相态,如溶液相、固相(盐结晶)等。




1相平衡热力学原理对平衡系相统的应用本章任务(1) 相平衡系统的普遍规律(2) 各种系统的具体相平衡情况重点:二组分系统的相平衡情况第一节一、 相的概念相: 在系统中物理性质和化学性质完全均匀的部分。
相间有界面越过相界面有些性质发生突变。
注意: 由于气体能无限混合,所以,一个系统中无论有多少种气体,只能形成一个气相。
一个系统可以有一个液相或两个液相,一般不会超过三个液相存在。
如果系统中所含的不同种固体达到了分子程度的均匀混合,就形成固溶体,一种固 溶体是一个固相。
二、物种数和组分数系统中所含的化学物质数称为系统的物种数,用符号S 表示。
注意:不同聚集态的同一种化学物质不能算两个物种,如水喝水蒸气其物种数S=1不是2。
足以表示系统中各相组成所需要的最少独立物种数称为系统的组分数,用符号C 表示。
无化学变化 组分数=物种数有化学变化 有浓度关系限制 组分数=物种数- 独立化学平衡数- 独立浓度关系注意:一个系统的物种数可以随人们考虑问题的不同而不同,但平衡系统中的组分数却是确定不变的。
三、自由度(degree of freedom )确定平衡系统的状态所必须的独立强度变量的数目称为自由度,用字母 f 表示。
这些强度变量通常是压力、温度和浓度等。
如果已指定某个强度变量,除该变量以外的其它强度变量数称为条件自由度,用 表示。
例如:指定了压力指定了压力和温度四、多相系统平衡的一般条件(1) 热平衡(2) 力学平衡(3) 相平衡(4) 化学平衡§5.3 相 律某平衡系统中有 S 个相,需要多少强度变量才能确定系统的状态?表示每一个相的组成需要的浓度变量为表示所有各相组成需要的浓度变量为加上温度和压力两个变量,则变量总数为根据化学势相等导出联系浓度变量的方程式数为根据自由度的定义 *1f f =-**2f f =-1S -(1)S -Φ(1)2S -+Φ(1)S -Φ{}{}(1)2(1)f S S ΦΦ=-+--这是相律的一种表示形式(1)若化学反应中有R 个独立的化学平衡(2)系统的强度性质还要满足R ‘ 附加条件,例如浓度限制条件则相律表示式为令:相律为C 称为独立组分数 它的数值等于系统中所有物种数 S 减去系统中独立的化学平衡数 R ,再减去各物种间的强度因数的限制条件R'。
相平衡的应用学生姓名卢贝贝学号********** 所属学院化学化工学院专业化学工艺日期2014年11月相平衡的应用摘要相平衡是传质分离过程和热质传递过程的理论基础之一。
化学化工生产中对产品进行分离、提纯时离不开蒸馏、结晶、萃取等各种单元操作,而这些单元操作的基础就是相平衡原理。
随着化学的不断发展,相平衡的应用也越来越广泛。
关键词:相平衡应用蒸馏结晶萃取引言相平衡是指在一定的温度和压力下,在体系中各相的组成和性质不再随时间而发生变化。
当体系达到相平衡时,各相之间的温度、压力和逸度相等[1]。
宏观来看,相平衡时,各相之间的物质将停止迁移,这时各相的组成和性质将不随时间而变化。
微观来看,在任一时刻各相之间物质的传入传出量相等,即各相之间物质的传递量为零。
相平衡是一个动态的平衡过程[2]。
相平衡的研究非常重要,因为相平衡是平衡级分离过程的理论基础,也是化工热力学中的重要组成部分。
相平衡确定了化工单元操作中平衡级分离过程的传质推动力和分离极限,并为确定设备的结构尺寸和操作条件提供必要的基础数据[3]。
按照相平衡时物质存在状态的不同,主要有气液平衡,液液平衡,固液平衡,固固平衡等,它们是精馏,吸收,萃取和结晶等化工单元操作的基础[4]。
相律是吉布斯根据热力学原理得出的,主要目的是确定系统的自由度数,及独立变量个数,它用于确定相平衡系统中能够独立改变的变量个数。
F=C-P+2 (1-1)其中:F-自由度数C-组分数P-相数相平衡的判据:含有π个相和N个组分的体系达到平衡时(1-2)由逸度的定义dG i =du =RTdlnf i(等温)和上式可得(1-3)系统达到相平衡时,除各项的温度、压力相同外,各个组分在各个相中的逸度应相等。
1、相平衡在萃取中的应用液液相平衡的测定方法[5]主要有二种。
第一是液液平衡釜法,这种方法应用较多,可以测定共轭相的数据;第二是浊点法,这种方法应用较少,此法只能测定互溶度的数据,无法得到共轭相的组成。