三态变化
- 格式:ppt
- 大小:2.62 MB
- 文档页数:35
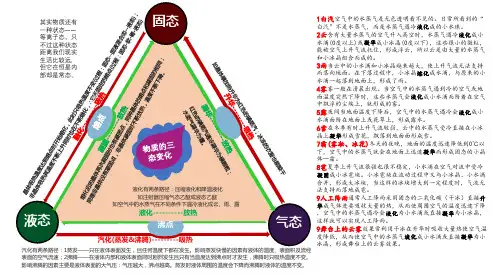


科学教案物质的三态变化科学教案:物质的三态变化【引言】物质是构成我们周围世界的基本组成部分,其存在的形式可以分为固态、液态和气态三种。
本教案将围绕物质的三态变化展开讲解,帮助学生们更好地理解和掌握这一重要概念。
【第一部分】固态(1)概述:固态是物质最常见的状态之一。
在固态中,原子或分子之间的距离相对固定,只发生微小的振动。
(2)性质:固态具有一定的形状和体积。
其中,晶体结构的固体具有清晰的几何形状,如盐和糖;而非晶体结构的固体会表现出无规则的形状,如玻璃和胶体。
(3)变化:固态物质的变化主要包括热胀冷缩、熔化和凝固。
(4)示例:以水为例,介绍冰的特性和冰的熔化过程。
【第二部分】液态(1)概述:液态是物质的另一种常见状态。
在液态中,原子或分子之间的距离比固态更大,允许它们自由移动。
(2)性质:液态物质没有固定的形状,但有固定的体积。
液体具有流动性、不可压缩性和表面张力等特性。
(3)变化:液态物质主要经历汽化、冷凝和蒸发等变化过程。
(4)示例:介绍水的特性、水的沸腾现象以及水蒸气的形成。
【第三部分】气态(1)概述:气态是物质的第三种状态。
在气态中,原子或分子之间的距离更大,它们具有高度的自由运动性。
(2)性质:气态物质既没有固定的形状,也没有固定的体积。
气体具有可压缩性和扩散性等特点。
(3)变化:气态物质的变化包括压缩、膨胀、液化和气化等过程。
(4)示例:介绍空气的成分、气体的流动和气体的液化实验。
【第四部分】物质间的相互转化(1)概述:物质的三态之间可以进行相互转化,这是由于原子和分子间相互作用的不同。
(2)相变图:引入相变图的概念,解释不同物质在不同温度和压力下的相变规律。
(3)示例实验:通过一系列简单的实验,如加热冰块、冷却水蒸气等,帮助学生们观察和理解物质的相变过程。
【总结】通过本教案的学习,学生们可以深入了解物质的三态及相互转化的基本概念。
同时,通过实验的参与,学生们能够更直观地感受到物质的性质和变化过程,提高他们的科学素养和实验能力。

探索物质的三态变化及其原理物质的三态变化指的是固态、液态和气态之间的相互转化过程。
这些变化是由于物质分子间的相互作用力的改变所导致的。
本文将探索物质的三态变化及其原理。
一、固态固态是物质最稳定的状态。
在固态中,物质的分子紧密地排列在一起,分子之间的相互作用力很强。
固体的形状和体积是固定的,分子只能做微小的振动运动。
固态的物质具有一定的硬度和弹性,能够保持自己的形状。
固态物质的三态变化原理是由于温度的改变引起的。
当温度升高时,固体的分子运动加剧,分子之间的相互作用力减弱。
当温度降低时,分子的振动减弱,分子之间的相互作用力增强。
当固态物质受到极低的温度或者其他外力的作用时,可能会发生相变,从固态转变为其他的态。
二、液态液态是介于固态和气态之间的状态。
在液态中,物质的分子之间的相互作用力较弱,分子之间存在着一定的间隙。
液体具有一定的流动性和变形性,可以自由流动而不被限制的形状。
液态物质的体积是不固定的,但其形状受到容器的限制。
液态物质的三态变化原理同样是由于温度的改变。
当温度升高时,液体的分子之间的相互作用力减弱,分子运动的速度增加,液体会逐渐转变为气体。
当温度降低时,液体的分子之间的作用力增加,分子运动减缓,从而形成固态。
三、气态气态是物质最具自由性的状态。
在气态中,物质的分子间的相互作用力最弱,分子间存在着较大的间隔。
气体具有较高的可压缩性和无固定形状。
气体的体积和形状完全受到容器的限制。
气态物质的三态变化原理同样是由于温度的改变。
当温度升高时,气体分子的运动速度增加,分子之间的相互作用力减弱,气体的体积会扩大,压力也会增加。
当温度降低时,气体分子的运动减缓,分子之间的相互作用力增强,气体的体积会缩小,压力也会降低。
总结起来,物质的三态变化是由于温度的变化而引起的。
固态物质在温度升高时会转变为液态,再升高温度则转变为气态;液态物质在温度升高时转变为气态,温度降低则转变为固态;气态物质在温度降低时转变为液态,再降低温度则转变为固态。

物质的三态变化与特点物质存在着三种基本的物态,即固体、液体和气体。
这些物态的存在形式和性质各不相同,经过加热或降温等外部条件的改变,物质可以在这三种态之间相互转化。
本文将深入探讨物质的三态变化以及它们各自的特点。
一、固体态固体是物质最常见的存在形态。
固体的分子间有着紧密的联系,呈现出一定的排列结构。
它们的运动状态比较有序,分子之间的距离相对较近,分子振动幅度较小。
固体的特点是形状稳定、体积固定不变。
这意味着无论如何外力作用,固体的形状和体积都不会发生变化。
固体具有较高的密度,因为分子之间距离相对较小,占据的空间较小。
此外,固体还具有较高的弹性,可以在受到外力作用后恢复到原来的形状。
固体的特性还包括融点和熔解热。
当固体受热至一定温度时,分子的振动增强,反应速度加快,最终进入液体态。
这个温度被称为固体的融点。
同时,固体融化过程释放或吸收的能量被称为熔解热。
二、液体态液体是物质的另一种常见物态。
液体分子之间的相互作用力较固体较弱,因此液体分子具有较大的自由度和流动性。
液体分子的运动方式是无规则的,呈现出较为松散的排列状态。
液体的主要特征是形状可变,但体积固定。
液体的自由度较高,分子之间的空隙相对较大,能够自由流动,并沿着较低位能的方向聚集。
这也导致液体有较高的表面张力,即液体表面会呈现出一定的膜状结构。
液体的特性还包括沸点和汽化热。
当液体受热至一定温度时,分子热运动加剧,液体逐渐转化为气体态。
这个温度被称为液体的沸点。
在这一过程中,液体吸收或释放的能量被称为汽化热。
三、气体态气体是物质的第三种常见物态,为分子运动最为剧烈且无定形的状态。
气体分子的运动速度较快,分子间相互作用力较弱甚至可以忽略不计。
气体分子呈现出无规则运动,以高速正常碰撞为主。
气体的最为显著的特点是形状和体积都可变。
气体可以根据容器的形状和大小自由扩散和蔓延。
气体分子之间的距离较远,几乎可以忽略其空间占据。
气体的密度较低,分子之间的空隙相对较大。


小学科学物质的三态变化物质是组成一切物体的基本单位,它可以存在于三个不同的态:固态、液态和气态。
这种状态的改变称为物质的三态变化。
在这篇文章中,我们将探讨物质的三态变化,并了解它们在日常生活中的应用。
一、固态固态是物质最常见的状态之一。
在这个状态下,物质的分子或原子紧密地排列在一起,并保持相对稳定的形状和体积。
晶体是一种常见的固态物质,例如糖和盐。
固态物质的分子之间存在着吸引力,因此它们只能做微小的振动。
冰是水的固态形式,它的分子会以规则的方式排列在一起,形成六角形的结构。
由于存在着分子之间的相互作用力,冰的体积处于稳定状态。
固态物质可能会发生溶解、熔化或蒸发等变化。
例如,将一块糖放入水中,它会逐渐溶解,使水变甜。
这是固态物质向液态转变的过程。
二、液态液态是物质的另一种常见状态。
在液态中,物质的分子或原子之间的相互作用力较弱,使得它们可以自由地移动。
液体的形状会适应其所处的容器,并在容器中占据一定的体积。
水是最常见的液态物质之一。
当我们将冰暴露在室温下时,它会融化成水。
水分子在液态下会有较大的运动空间,可以相互流动,因此水可以流动。
液态物质可以通过冷却变成固态,通过升温变成气态。
例如,将水放入冰箱冷冻室中,它会逐渐冷却并形成冰块。
相反,如果我们加热水,它会逐渐转化为蒸汽。
三、气态气态是物质最自由的状态。
在气态下,物质的分子或原子之间的相互作用力非常弱,使得它们可以快速、自由地移动。
气体没有固定的形状和体积,而是填充整个容器。
空气就是我们周围最常见的气态物质。
空气中的气体分子非常活跃,不断碰撞和运动。
在气压的作用下,气体会填充其所在的容器,并且可以均匀地分布到空间中。
气态物质可以通过降温或增加压力变成液态,或者通过加热变成等离子态。
例如,当我们冷却水蒸气时,它会变成水滴。
相反,当我们加热水,它会变成水蒸气。
物质的三态变化在我们的日常生活中无处不在。
例如,当我们把冰块放在室温下时,它会逐渐融化成水。

探索科学奥秘物质的三态变化物质的三态变化是科学中一个重要的研究领域,涉及到固态、液态和气态三种不同形态下物质的性质和相互转化规律。
通过对三态变化的探索,我们可以深入了解物质的本质和规律,为科学技术的发展提供理论依据和实践指导。
本文将探讨固态、液态和气态三种态的特征和转化过程。
一、固态:稳定有序的结构固态物质是我们日常生活中最常见的一种状态。
它的特征是分子或原子紧密排列,保持相对稳定的形态和固定的体积。
在固态下,物质的分子或原子只是微小的振动,不断发生着热运动。
固态物质具有一定的强度和硬度,常见的有金属、陶瓷等。
根据不同的结构,固态又可以分为晶体和非晶体两种。
二、液态:无固定形状的流动体液态是物质的第二态,其特点是分子或原子自由度较大,可以互相流动。
在液态下,物质的分子或原子之间的相互作用力较弱,排列较为松散,没有固定的形状。
液体具有较大的体积和流动性,可以适应不同的容器形状。
液态物质常见的有水、酒精等。
在液态中,我们还可以观察到一些特殊的现象,例如液体的表面张力和毛细管现象。
液体的表面张力使得液面在接触到固体边界时会出现弯曲,形成弹性形状。
毛细管现象则是液体在细小管道中产生的上升或下降现象,由液体与固体边界的相互作用力引起。
三、气态:无固定体积的扩散态气态是物质的第三态,气体的特征是分子或原子自由度最大,能够充满整个容器。
气体的分子或原子之间相互作用力较弱,几乎没有相互约束,故呈现出高度的能量运动、无固定形状和无固定体积等特性。
常见的气体有空气、氮气等。
气态物质在一定的温度和压强下可以凝结成液体或固体。
这个过程被称为气体的凝聚,常见的凝聚形式有冷凝、冷冻和沉积等。
反过来,液体和固体物质在一定条件下也可以变成气体,这个过程称为气化。
气化的方式有蒸发、沸腾和升华等。
通过调节温度和压强等外界条件,可以使物质在不同的状态之间转化。
例如,当我们把固态物质加热时,分子或原子的振动加剧,克服相互作用力后,物质从固态变成液态;当温度进一步升高时,物质则从液态转化为气态。

物质的三态变化及示意图解物质是构成宇宙万物的基本要素,它可以存在于不同的形态,即固态、液态和气态。
这三种态的变化是物质的基本特性之一,它们之间的转变在我们的日常生活中无处不在。
本文将探讨物质的三态变化,并通过示意图解来帮助读者更好地理解这一过程。
固态是物质最常见的一种形态。
在固态中,分子或原子之间的相互作用力很强,使得它们紧密地排列在一起。
固态物质具有固定的形状和体积,而且它们的分子或原子只能做微小的振动。
一个常见的例子是冰,当水的温度降到0摄氏度以下时,水分子之间的相互作用力会使得它们排列成规则的晶体结构,形成冰的固态。
液态是物质的另一种常见形态。
在液态中,分子或原子之间的相互作用力较弱,使得它们可以自由地移动和流动。
液态物质具有固定的体积,但没有固定的形状,可以适应容器的形状。
水是一个典型的液态物质,当温度升高时,水分子的热运动增强,相互作用力减弱,水从固态转变为液态。
气态是物质的第三种常见形态。
在气态中,分子或原子之间的相互作用力非常弱,它们具有高度的自由度,可以在容器中自由运动。
气态物质不仅没有固定的形状,也没有固定的体积,可以充满整个容器。
例如,水在加热到100摄氏度时,会发生沸腾,水分子的热运动足够强大,使得水分子逃离液体表面,形成气体状态的水蒸气。
这些物质的三态变化之间可以通过加热或降温来实现。
当物质受到热量的加热时,分子或原子的热运动增强,相互作用力减弱,从而导致物质的相变。
相反,当物质受到冷却时,分子或原子的热运动减弱,相互作用力增强,也会导致物质的相变。
为了更好地理解物质的三态变化,我们可以通过示意图解来帮助我们形象地呈现这一过程。
下图是一个简单的示意图,展示了水在不同温度下的三态变化。
[示意图]图中的示意图分为三个部分,分别代表了水在固态、液态和气态下的形态。
在低温下,水以固态存在,分子紧密排列,形成冰的晶体结构。
当温度升高时,水从固态转变为液态,分子之间的相互作用力减弱,水分子可以自由地移动和流动。

物质的三态变化生活中的应用例子
物质的三态变化指的是固体、液体和气体之间的相互转化。
这种变化在日常生活中十分常见,以下是一些应用例子:
1. 冰块融化成水:当冰块处于室温下时,它会逐渐变成水,这是因为室温下的热量导致了固体冰的分子振动加剧,从而使其变成液态的水。
2. 饮用水沸腾:将水加热到一定温度时,它会发生沸腾现象,这是因为水中的分子振动增强,从而形成气泡并逸出水面。
3. 冰淇淋融化:在热天里,冰淇淋会很快融化,这是因为它的温度超过了室温,进而导致了固态冰淇淋变成了液态。
4. 蒸发干衣服:将湿衣服晾干的过程中,水会逐渐从液态转变成气态并散发到空气中,这就是蒸发的过程。
5. 吹风机吹干头发:吹风机通过发热将水蒸发,从而将头发上的水分转变成了水蒸气,使头发变得干燥。
总之,物质的三态变化在日常生活中无处不在,我们需要了解这些现象,才能更好地掌握和运用它们。
- 1 -。

物质的三态变化物质是由原子或分子组成的,其性质和状态会随着温度和压力的变化而改变。
在常见的条件下,物质可以存在于固态、液态和气态这三种不同的状态。
这种状态的转变称为物质的三态变化,本文将探讨固态、液态和气态的特征及它们之间的相互转化过程。
固态是物质最常见的状态之一。
在固态中,物质的分子或原子之间保持着紧密排列的结构。
它们振动的幅度很小,只限于一个固定的位置。
这种特性使得固体具有相对稳定的形状和体积。
经典的例子是冰,它由水分子构成,当温度降低到0摄氏度以下时,水的分子开始缓慢地结晶并形成冰晶体。
此时,水变成了固态。
固体的分子或原子之间的吸引力很强,因此固体具有较高的密度和较低的压缩性。
液态是物质的另一种常见状态。
在液态中,物质的分子或原子之间的排列相对较为松散。
由于分子之间的相互作用力较弱,它们可以自由地在相对固定的空间内移动。
这使得液体具有较高的流动性和可变的形状。
例如,当将冰加热到0摄氏度以上时,冰开始融化,水分子之间的结构逐渐解开,并形成流动的状态。
液体具有较高的密度和较低的压缩性,但相对于固体来说,液体的形状和体积可以根据容器的形状和大小而改变。
气态是物质的第三种常见状态。
在气态中,物质的分子或原子之间的距离较远,它们以高速运动并相互之间几乎没有相互作用。
气体的分子或原子可以在容器内任意自由地移动,并且它们会不断地碰撞和迅速弥散。
当物质受热而被加热到一定温度时,分子或原子的动能增加,使它们跳出原来的束缚,从而转变成气体。
与固体和液体相比,气体具有较低的密度和较高的压缩性。
此外,气体的形状和体积都会根据容器的形状和大小而自由变化。
三态之间的相互转化过程可以通过改变温度和压力来实现。
这些变化过程包括固态到液态的熔化、液态到固态的凝固、液态到气态的汽化、气态到液态的液化、固态到气态的升华以及气态到固态的凝华。
这些相变过程不仅与物质的性质有关,还受到外部条件的影响。
总结起来,固态、液态和气态是物质三种常见的状态。
三态变化的名称一、三态变化的概念三态变化是指物质在不同温度下经历的三种不同状态的变化,包括固态、液态和气态。
在不同的温度条件下,物质的分子之间的相互作用力发生变化,导致物质的状态发生改变。
二、固态的特征与变化固态是物质最常见的状态之一,它具有以下特征:1. 分子之间的相互作用力较强,分子排列紧密,形成有序结构;2. 固体具有一定的形状和体积,不易被外界的力所改变;3. 固体的分子运动范围较小,只能做微小的振动。
固态物质在温度变化下也会发生变化,其中最常见的现象是熔化和凝固。
当温度升高时,固体受到的热能增加,分子的振动增强,相互作用力减弱,最终导致固体熔化为液体。
而当温度降低时,固体受到的热能减少,分子的振动减弱,相互作用力增强,最终导致液体凝固为固体。
三、液态的特征与变化液态是物质在一定温度范围内的状态,它具有以下特征:1. 分子之间的相互作用力较弱,分子排列无序;2. 液体具有一定的形状和体积,可以被外界的力所改变;3. 液体的分子运动范围较大,可以自由流动。
液态物质在温度变化下也会发生变化,其中最常见的现象是沸腾和凝结。
当温度升高时,液体受到的热能增加,分子的运动速度增快,最终导致液体沸腾为气体。
而当温度降低时,液体受到的热能减少,分子的运动速度减慢,最终导致气体凝结为液体。
四、气态的特征与变化气态是物质在较高温度或较低压力下的状态,它具有以下特征:1. 分子之间的相互作用力很弱,分子排列无序,分子之间距离较远;2. 气体没有固定的形状和体积,可以被外界的力所改变;3. 气体的分子运动范围很大,可以自由扩散。
气态物质在温度变化下也会发生变化,其中最常见的现象是汽化和凝结。
当温度升高时,气体受到的热能增加,分子的运动速度增快,最终导致液体汽化为气体。
而当温度降低时,气体受到的热能减少,分子的运动速度减慢,最终导致气体凝结为液体。
五、三态变化的应用三态变化在日常生活和工业生产中有着广泛的应用。
1. 冷冻食品:冷冻食品的制作过程中,液态食材经过冷冻处理转化为固态,以延长食品的保质期。
物质的三态变化及相关性质物质是构成我们周围物体的基本元素,它们可以以不同的方式组合和变化。
在我们日常生活中,我们经常会遇到物质的三态变化,即固态、液态和气态。
这三种态的变化与物质的性质密切相关,下面将分别对各个态的特征及其性质进行探讨。
一、固态固态是物质最常见的状态之一。
在固态下,物质的分子之间相互吸引形成了稳定的结构。
这种结构使得物质能够维持一定的形状和体积。
固态的物质通常是硬的,而且在常温下具有一定的弹性。
固态物质还具有以下特性:1. 熔点:固态物质在升温时会达到一定的温度,称为熔点。
熔点通常是物质由固态转变为液态的临界温度。
不同物质的熔点各不相同,这取决于其分子之间的相互作用力。
2. 硬度:固态物质的硬度是指其抵抗外力的能力。
硬度与物质的化学成分和结构密切相关。
例如,金属通常具有较高的硬度,而一些晶体物质也可以具有很高的硬度。
3. 可塑性:固态物质具有可塑性,这意味着它可以被变形而不破坏。
这一特性使得我们可以通过加工技术来制造各种不同的固态物品。
二、液态当物质的温度超过其熔点时,它会从固态变为液态。
液态物质的分子之间的相互作用力较弱,无法保持固态的结构。
因此,液态物质具有以下特征:1. 定容不定形:液态物质的体积可变,但质量保持不变。
它们可以适应容器的形状,并且可以通过改变温度和压力来改变其体积。
2. 表面张力:液体分子之间的相互作用力导致液面上形成表面张力。
这种张力使得液体呈现出一定的薄膜性质,如水滴在平面上的形态。
3. 倾向于自我调节:液体有自我调节的能力,当在一个容器中时,它会自动平均分布并填满容器。
三、气态当物质的温度超过其沸点时,它会从液态变为气态。
气态物质具有以下特征:1. 可压缩性:气体分子之间的相互作用力较弱,使得气体具有可压缩性。
通过增加或减少压力,我们可以改变气体的体积。
2. 扩散性:在开放空间中,气体分子会自动向各个方向扩散。
这是因为气体分子的运动速度足够快,能够克服彼此之间的相互作用力。
物质的三态变化是如何发生的?
物质的三态变化,包括固态、液态和气态,是物质在不同条件下的状态转变。
这些转变是根据物质的分子间相互作用和运动规律发生的。
固态
固态是物质的一种状态,其特点是分子紧密排列,形成固定的结晶格点。
在固态下,分子的运动受限,只能在位移较小的范围内振动。
固态的物质保持其形状和体积,不容易流动。
固态转变成液态的过程称为熔化,需要向物质提供足够的能量使分子克服相互间的吸引力,从而跳出原有的结晶格点。
液态
液态是物质的另一种状态,其特点是分子的排列无序,密度较高,分子可以自由移动。
在液态下,物质可以流动,并且有一定的表面张力。
液态转变成固态的过程称为凝固,需要从物质中提取能量,使分子重新排列成固定的结晶格点。
液态转变成气态的过程称为汽化,需要提供足够的能量,使分子克服相互作用力,从液体表面脱离进入气态。
气态
气态是物质的第三种状态,分子间相互作用较弱,分子的运动是自由的。
在气态下,物质具有较低的密度和较高的压缩性,可以充满。
气态转变成液态的过程称为液化,需要从气体中提取足够的能量,使分子之间的相互作用增强,从而使分子聚集成液滴或液体表面。
气态转变成固态的过程称为凝华,需要从气体中提取能量,使分子重新排列成固定的结晶格点。
总结
物质的三态变化是根据物质的分子间相互作用和运动规律发生的。
固态、液态和气态之间的转变是通过吸收或释放能量来实现的,分别称为熔化、凝固、汽化、液化和凝华。
理解物质的三态变化有
助于我们认识物质的性质和行为。
物质的三态变化物质是组成一切事物的基本要素,其性质随着温度和压力的改变而发生变化。
在日常生活中,我们常常遇到物质的三态变化,即固态、液态和气态。
本文将从微观和宏观的角度,介绍物质在不同态之间的变化过程以及相关的性质。
一、固态固态是物质最常见的状态之一。
在固态下,物质的分子或原子紧密排列,并通过强力相互作用保持着相对固定的位置。
这种有序的排列使得固态物质具有一定的形状和体积。
此外,固态物质还具有较低的动能,其分子或原子只是在振动,而无法自由移动。
固态物质的熔点和沸点较高,因此在一定温度范围内,固态物质稳定存在。
我们可以通过加热或降低温度来改变固态物质的性质。
当固态物质受热时,分子或原子的振动加剧,最终达到熔点,固态物质开始转变为液态。
二、液态液态是指物质的分子或原子相对于固态而言存在更大的自由度。
在液态下,物质的分子间距离稍大,能够自由移动。
因此,液态物质没有固定的形状,而是适应容器的形状,并且具有一定的体积。
液态物质的熔点和沸点介于固态和气态之间,相对较低。
当液态物质受热时,分子的运动速度增加,逐渐超过液态物质的吸引力,产生蒸发现象。
这是物质从液态向气态的转变过程。
三、气态气态是指物质的分子或原子具有较高的动能,能够克服物质间的相互作用力,自由运动的状态。
在气态下,分子之间的距离很大,分子的运动速度也非常快,使得气态物质具有高度的扩散性和可压缩性。
气态物质的熔点和沸点相对较低,当气态物质受冷或加压时,分子的运动速度减慢,逐渐聚集,形成液态或固态。
物质的三态变化是一个连续的过程,通过调节温度和压力,我们可以使物质在不同态之间相互转变。
例如,冰在适当的温度下受热会融化成水,水在适当的温度下受热会变成蒸汽,而蒸汽在适当的温度下受冷会凝结成液态水或固态冰。
除了通过温度和压力的改变,物质的三态变化还受到其他因素的影响,如环境条件和化学物质的作用。
例如,加入盐可以使水的沸点升高,使其变得更难沸腾。
这种实际应用使物质的三态变化更加复杂和丰富。