电子转移步骤动力学完整版
- 格式:ppt
- 大小:317.00 KB
- 文档页数:20

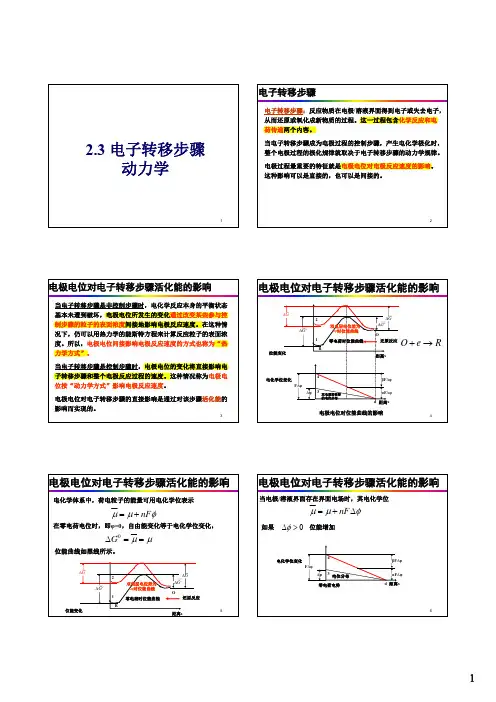
电极电位对电子转移步骤活化能的影响电极电位对电子转移步骤活化能的影响电极电位对电子转移步骤活化能的影响
电极电位对电子转移步骤活化能的影响
电极电位对电子转移步骤活化能的影响
G
∆
0G F αϕ∆+
同一个电极上发生的还原反应和氧化反应的绝对速度与电极电位交换电流密度交换电流密度
交换电流密度交换电流密度
交换电流密度交换电流密度
交换电流密度稳态电化学极化规律稳态电化学极化规律稳态电化学极化规律
稳态电化学极化规律
η
高过电位下的电化学极化规律
2.3 2.3
高过电位下的电化学极化规律
电极反应以一定的速度进行时,电化学过电位的大小取决于电极
混合控制时的动力学规律已知混合控制时的动力学规律
i i
RT RT
i i
RT RT i i
RT RT
i i RT RT。

第六章电子转移步骤动力学电子转移是指电子从一个原子或分子向另一个原子或分子的跃迁。
这个转移过程可以通过多种方式发生,比如离子交换、电子传递等。
在化学反应中,电子转移步骤是非常重要的,对反应速率和产物选择性有着显著影响。
因此,研究电子转移步骤动力学是理解和控制化学反应的关键。
电子转移过程中,电子的跃迁通常伴随着原子或分子的几何变化。
这种几何变化可以通过分子轨道理论和能带理论等方法进行描述。
通过这些理论,我们可以计算得到电子转移过程的能垒和反应路径,并进一步分析其动力学特性。
在电子转移步骤的动力学研究中,我们经常使用催化剂来促进转移过程。
催化剂可以提供一个较低的能垒,从而加速反应速率。
催化剂通常通过与反应物形成配位键或中间体来实现对反应的加速作用。
通过研究催化剂的结构和反应机理,我们可以深入理解电子转移步骤的动力学行为。
另一个重要的研究方法是通过动力学实验来研究电子转移步骤。
动力学实验的基本原理是测量反应速率随时间的变化。
通过改变反应条件,如温度、压力和浓度等,我们可以探究电子转移步骤的温度和压力依赖性,以及反应物浓度对反应速率的影响。
通过这些实验数据,我们可以确定反应的速率常数和反应级数,并进一步分析反应机理。
除了实验研究,理论计算也在电子转移步骤动力学研究中发挥了重要作用。
量子力学和分子动力学模拟等计算方法可以提供详细的分子层面的信息,如反应势能面、反应路径和能量障碍等。
通过理论计算,我们可以预测反应速率常数、反应物选择性和反应动力学行为,为实验研究提供重要参考。
总之,电子转移步骤动力学研究是理解和控制化学反应的重要手段。
通过研究电子转移过程的动力学特性,可以揭示反应机理和反应条件对反应速率和产物选择性的影响。
这一领域的研究对于发展新型催化剂、设计高效反应体系以及理解生命现象等具有重要意义。






化学反应中的电子转移反应动力学研究化学反应中的电子转移反应动力学研究在现代化学领域中扮演着重要的角色。
了解反应速率和能量变化的动力学过程对于设计新的催化剂、预测催化反应的效率以及优化反应条件具有重要作用。
本文将介绍电子转移反应的动力学研究方法与应用。
一、电子转移反应的基本概念电子转移反应是指在化学反应中,电子从一个物质转移到另一个物质的过程。
这种反应通常发生在氧化还原反应中,其中一个物质失去电子(被氧化),而另一个物质获得电子(被还原)。
电子转移反应的动力学研究主要关注反应速率以及反应路径中的能量变化。
二、电子转移反应动力学研究方法1. 光谱学方法光谱学方法是电子转移反应动力学研究中常用的方法。
通过测量反应物和产物之间的吸收、发射或散射光谱,可以获得反应过程中电子能级的信息。
例如,紫外可见吸收光谱、荧光光谱和拉曼光谱等可以用于研究电子转移反应过程中的能量变化以及反应物和产物之间的电子转移路径。
2. 电化学方法电化学方法是另一种用于电子转移反应动力学研究的常用方法。
电化学实验可以通过测量电流和电势的变化来研究反应物和产物之间的电子转移过程。
其中,循环伏安法、计时电流法和旋转圆盘电极法等常用技术可以用于测定电子转移反应的速率常数和电子转移动力学参数。
3. 分子动力学模拟方法分子动力学模拟方法是近年来发展起来的一种重要的电子转移反应动力学研究方法。
这种方法通过在计算机上模拟器件分子系统的动力学过程,可以获得电子转移过程中的能量变化和反应速率常数等信息。
分子动力学模拟方法可以提供原子级别的细节,对于研究复杂的电子转移反应机理非常有价值。
三、电子转移反应动力学研究的应用1. 催化剂的设计与优化电子转移反应动力学研究对于催化剂的设计和优化至关重要。
了解反应的动力学特性可以帮助科学家确定催化剂的合适活性位点和优化催化反应的条件,从而提高反应的选择性和效率。
2. 化学反应速率预测电子转移反应动力学研究可以提供反应速率常数和反应路径的信息,使得科学家能够预测和解释化学反应的速率。

