高中化学 专题1 第2单元 研究物质的实验方法(第1课时)导学案2 苏教版必修1
- 格式:doc
- 大小:57.02 KB
- 文档页数:4


高中化学《研究物质的实验方法》教案2苏教版必修1第二单元第2课时常见物质的检验一、学习目标1.学会Cl-、SO42-、CO32-、NH4+等离子检验的实验技能,能用焰色反应法、离子检验法设计简单的实验方案探究某些常见物质的组成成分。
2.初步认识实验方案设计、实验现象分析等在化学学习和科学研究中的应用。
3.初步学会独立或与同学合作完成实验,记录实验现象,并学会主动交流。
逐步形成良好的实验习惯。
二、教学重点及难点常见离子检验的实验技能;设计简单的探究实验方案。
三、设计思路化学研究中,人们经常根据某些特征性质、特征反应、特征现象和特征条件对物质进行检验,以确定物质的组成。
学生已经掌握了一定的物质检验知识,但不够系统化,需进一步总结和提炼。
本节课选择Cl-、SO42-、CO32-、NH4+等常见离子作为检验对象,复习总结初中化学知识,学习常见物质的检验方法,介绍现代分析测试方法,从而让学生了解物质检验方法的多样性,进一步认识到物质检验过程中防止干扰的设计、多种物质检验方案的设计及操作技能。
教学时,首先让学生明确物质检验的意义和价值,并初步明确进行物质检验的依据或策略,教学过程中充分发挥学生的自主性。
其次,根据教学目标创设相应的情景,提出具体的任务。
四、教学过程[导入] 物质的检验是一个重要的工作。
如为保证公平竞赛,在大型运动会上会进行兴奋剂检测;检查身体时对血糖血脂的检验;质检员对生产的产品质量标准的检验,等等。
[情景]“资料链接”——由某抗秧苗病菌的农药袋上的标签可知,该农药含有碳酸铵和硫酸铜两种成分。
如何通过实验确证该农药中含有铵根离子、碳酸根离子和硫酸根离子呢?指出所用的试剂、预期将观察到的现象以及反应的化学方程式。
[实验] 完成课本“活动与探究”栏目中的实验1-4。
各个实验中,依次观察到什么现象?出现这些现象的根本原因是什么?明确NH4+、Cl—、SO42—等离子的检验所采用的试剂和方法等:NH4+:加浓NaOH溶液,加热,产生能使湿润的红色石蕊试纸变蓝的气体;Cl—:滴加硝酸银溶液和稀硝酸,生成不溶于稀硝酸的白色沉淀;SO42—:滴加BaCl2溶液和稀盐酸,生成不溶于稀盐酸的白色沉淀。
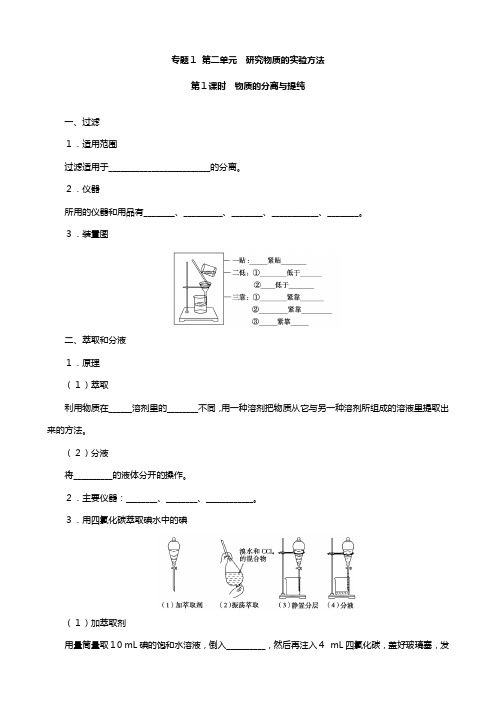
专题1第二单元研究物质的实验方法第1课时物质的分离与提纯一、过滤1.适用范围过滤适用于__________________________的分离。
2.仪器所用的仪器和用品有________、__________、________、____________、________。
3.装置图二、萃取和分液1.原理(1)萃取利用物质在______溶剂里的________不同,用一种溶剂把物质从它与另一种溶剂所组成的溶液里提取出来的方法。
(2)分液将__________的液体分开的操作。
2.主要仪器:________、________、____________。
3.用四氯化碳萃取碘水中的碘(1)加萃取剂用量筒量取10 mL碘的饱和水溶液,倒入__________,然后再注入4mL四氯化碳,盖好玻璃塞,发现溶液分层。
__________在下层。
(2)振荡萃取用右手压住分液漏斗______,左手握住______部分,把分液漏斗倒转过来振荡,使两种液体充分接触;振荡后打开活塞,使漏斗内气体放出。
(3)静置分层将分液漏斗放在铁架台上静置,液体分层。
上层为____,无色;下层为_________,____色。
(4)分液待液体分层后,将分液漏斗上的________打开(或使塞上的________对准_________),再将分液漏斗下面的________拧开,使下层液体沿__________流下。
上层液体从分液漏斗________倒出。
三、蒸馏1.概念将液态物质加热至________,使之汽化,然后将蒸汽重新________为液态的操作过程。
2.原理利用混合物中各组分的________不同,除去液态混合物中__________、__________或__________的杂质的方法。
3.制取蒸馏水仪器及装置图知识点1过滤的方法和应用1.进行过滤操作应选用的一组仪器是()A.滤纸、烧杯、试管夹、漏斗、玻璃棒B.烧杯、酒精灯、试管、漏斗C.漏斗、玻璃棒、烧杯、铁架台、滤纸D.玻璃棒、滤纸、烧瓶、漏斗、铁架台2.下列混合物能用过滤法分离的是()A.汽油和水B.食盐和蔗糖C.泥沙和食盐D.铜粉和铝粉3.某学生发现滴瓶中的溶液有悬浮物,拟用如图所示操作进行过滤,操作上错误的地方有()A.4处B.3处C.2处D.1处知识点2萃取与分液的应用4.下列混合物的分离和提纯方法中,主要是从溶解性的角度考虑的是()A.蒸发B.蒸馏C.过滤D.萃取5.在使用分液漏斗进行分液时,正确的操作是()A.上层液体经漏斗下方活塞放出B.分离液体时,将漏斗拿在手上进行分离C.分离液体时,分液漏斗上的小孔与大气相通时打开活塞D.分液漏斗中盛装的是液体,振荡后不必扭开活塞把气体放出6.将体积比为1∶2的四氯化碳和碘水在试管中充分混合后静置。

第二单元研究物质的实验方法(两课时)【名言警句】勤奋成就学业,态度决定一切.一、物质的分离和提纯【学海导航】1、通过学习,能够掌握物质分离和提纯的常用方法2、能够对一些混合物进行分离和提纯操作【主干知识】物质的分离和提纯的常用方法根据混合物中各物质溶解性、沸点、被吸附性能及在不同溶剂中溶解性的不同,可以选用过滤和结晶、蒸馏(或分馏)、纸上层析、萃取和分液等方法进行分离和提纯。
注意:不同的分离方法都有一定的适用范围,要根据不同混合物的性质选择合适的方法进行分离,且有时需要多种方法配合使用。
(1)过滤:适用于混合物的分离, 过滤注意点:【实验探究1】请设计实验方案:如何将含有硫酸钠,氯化镁和泥沙等杂质的粗食盐提纯?(2)结晶: 适用于【实验探究2】现有氯化钾和硝酸钾的固体混合物50克,其中氯化钾的质量分数为10%,请设计实验方案提纯硝酸钾?(3)萃取是指所用主要仪器,萃取剂要求一是,二是.常用萃取剂有。
(酒精不能作为萃取剂)【实验探究3】溴水呈色,加CCl4振荡静置后, 上层下层。
碘水中加CCl4, 振荡静置后,上层下层。
(4)分液: 适用于混合物的分离【实验探究4】如何分离CCl4和水的混合物?(5) 蒸馏:蒸馏是利用互溶的液体混合物中各组分沸点不同(通常沸点需相差30℃以上)进行分离提纯的操作。
其过程是:蒸馏分为蒸馏蒸馏等。
【实验探究5】如何将含有Fe3+的自来水提纯?蒸馏操作注意事项:(6)层析:适用于【实验探究6】红、蓝墨水混合物中的不同色的分离:【课堂探究】例1.某溶液含有较多的Na2SO4和少量的Fe2(SO4)3。
若用该溶液制取芒硝(Na2SO4·10H2O),可选择的操作有(1)加适量H2SO4溶液;(2)加金属钠;(3)结晶;(4)加过量NaOH溶液;(5)加强热脱结晶水;(6)过滤。
正确的操作步骤是()A.(2)(6)(3) B.(4)(6)(1)(3) C.(4)(6)(3)(5) D.(2)(6)(1)(3)(5)例2.下列溶剂能溶解单质碘和溴,但不能把碘和溴从碘水和溴水中提取出来的是A.苯B.汽油C.酒精D.四氯化碳【巩固练习】1.欲将食盐固体与碘的混合物分开,最好的方法是A.溶解、过滤B.溶解、过滤、蒸发C.溶解、加AgNO3、过滤D.升华(碘加热后由固态直接变为气态)2.进行分液操作时,下列实验仪器一定不会用到的是( )A 锥形瓶 B分液漏斗C烧杯 D 温度计3.不能从溴水中提取溴的试剂是()A.酒精B.汽油C.烧碱溶液D.四氯化碳45.下列各组溶液,不用其他试剂......,就可将它们区别开的是()A.盐酸氢氧化钠碳酸钠硫酸铜B.盐酸硝酸银氯化钠硝酸钠C.氢氧化钠硫酸镁碳酸钠硫酸氢钠D.氯化钡硫酸钠氯化钙硝酸钙6.实验室用固态不纯氯化钠(含少量NH4HCO3和Na2SO4杂质)制取纯净氯化钠溶液。

专题一第二单元研究物质的实验方法教学案课时二第2单元研究物质的实验方法课时2【教学目标】:1、学会Cl、SO产、co产、NH;等离子检验的实验技能。
2、能川焰色反应法、离子检验法设计简单的实验方案来探究某些常见物质的纽成成分。
【教学重难点】:Cl、SO产、CO产、NH:等离子的检验。
【知识回顾】一、己知硫酸倾、氯化银既不溶于水,也不溶于酸;碳酸锁、碳酸银不溶于水,却可溶于酸,完成下列化学方程式:1、向碳酸钠溶液中滴加硝酸银溶液,再滴加稀硝酸:2、向氯化钠溶液屮滴加硝酸银溶液,再滴加稀硝酸:3、向碳酸钠溶液屮滴加氯化强溶液,再滴加稀盐酸:4、向碳酸钠溶液屮滴加澄清的石灰水:5、向碳酸钠溶液屮加入稀盐酸:6、向硫酸钠溶液中滴加川硝酸酸化了的氯化顿溶液:7、向硝酸银溶液中滴加川硝酸酸化了的氯化顿溶液:8、氯化钱溶液与氢氧化钠溶液共热:二、碳酸盐的检验方法:__________________________________________________________ o通过化V方程式举例说明:【教学过程与内容】K引言1在生活、生产及化学研究中,人们经常甜要根据不同的原了、分了或离了的某些特征反应对物质进行检验,以确定物质的组成。
如,根据纤维在火焰上燃烧的气味,确定该纤维是否为蛋白质纤维等。
一、常见物质或离子的检验:K活动与探究1氯化彼、硫酸讓、氯化钾、硫酸钾屮所含离子的检验方法:(探究实验一):取两支试管,分别加入2讥氯化钱、硫酸钱溶液,再各加入2mL氢氧化钠,加热, 将湿润的红色石蕊试纸靠近试管口,观察试纸的颜色变化。
现象:原理:1、总结:钱盐(NHC的检验方法:钱盐与强碱共热,能放出具有刺激性气味且能使湿润的红色石蕊试纸变蓝的气休(探究实验二):取两支试管,分别加入氯化钱、氯化钾,再各加硝酸银,观察实验现象。
现象:原理:2、总结:氯离子(CO的检验方法:与硝酸银溶液反应,牛•成不溶于稀硝酸的口色沉淀。

常见物质的检验【学习目标】1学会NH4、CI-、so4-、co3-等离子的检验方法;掌握焰色反应及常见离子的特征焰色;2 •能用焰色反应法、离子检验法设计简单的实验方案探究物质的组成。
【新课引入】在日常生活中,我们常需要测定物质的组成,确定它是哪种物质,即进行物质的检验。
请同学们回忆下,初中我们接触过哪些物质的检验。
【实验探究11 NH4C L (NH4)2SO4 KCl和K2SO4均可用作化肥。
下列实验将帮助我们探究这几种盐中所含离子的检验方法。
实验1:取两支试管,分别加入2mLNH4CI和(NH4)2SO4溶液,再各加入2mLNaOH溶液,加热试管,将湿润的红色石蕊试纸靠近试管口,闻气味及观察试纸颜色的变化。
实验现象:____________________________ ,反应方程式:____________________________实验2 :取两支试管,分别加入2mLNH4CI和KCI溶液,各滴几滴稀HNO3再各滴几滴AgNO3实验现象:____________________________ ,反应方程式:____________________________思考:加入稀硝酸的作用是什么?____________________________________________________实验3:取两支试管,分别加入2mL(NH4)2SO4和K2SO4溶液,各滴几滴稀HCI,再各滴几滴BaCI2。
实验现象: ______________________________________ ,反应方程式:____________________________思考:稀HCI的作用是什么?___________________________________________________能否用硝酸来排除干扰?为什么?_______________________________________________________—、常见离子的检验NH4的检验实验原理:铵盐与强碱溶液在加热时发生下列反应:NH4CI+ NaOH—_________________ ___ , (NH4)2SO4+ NaOH- __________________ _,NH3的检验_________________________________________________________________________ 。
第二单元 研究物质的实验方法第一课时 物质的分离与提纯一、物质的分离与提纯1.物质的分离:将混合物中各物质通过物理变化或化学变化把各成分彼此分开的过程。
2.物质的提纯:把混合物中的杂质除去,得到纯净物的过程。
二、分离和提纯的常用方法过滤、蒸发、结晶和重结晶、萃取和分液、蒸馏 1.过滤过滤是分离 液体和不溶性固体 混合物最常用的方法之一,主要是除去液体中的 难溶性组分,过滤装置如图:(1)过滤时用到的玻璃仪器有: 烧杯 、漏斗 、 玻璃棒 。
(2)过滤的操作要点①一贴:滤纸紧贴 漏斗 内壁;②二低: 滤纸 边缘应略低于漏斗边缘, 滤液液面 应略低于滤纸的边缘;③三靠:向漏斗中倾倒液体时,烧杯的尖嘴应与玻璃棒接触;玻璃棒的底端应和漏斗的 三层滤纸 处轻轻接触;漏斗颈的末端应与 烧杯内壁 相接触。
2.蒸发蒸发是将溶液加热,使溶液受热汽化,从溶液中分离出固体物质的方法。
蒸发可得晶体,也用于浓缩溶液。
蒸发装置如图:(1)蒸发时用到的仪器有: 蒸发皿 、 玻璃棒 、 酒精灯 、铁架台 。
(2)在进行蒸发操作时要注意以下问题①实验结束后,不能将蒸发皿直接放在 实验台桌面 上,以免烫坏 桌面 或遇实验台上的冷水引起蒸发皿炸裂;②当蒸发到析出大量 晶体 、剩余少量 溶液 时,应停止 加热 ,利用 余热 蒸干,以防止晶体过热迸溅。
3.结晶和重结晶 (1)冷却法将热的饱和溶液慢慢冷却后析出晶体,此法适用于溶解度 随温度变化比较大 ,如KNO3。
物质分离与提纯的原则 不增:不增加新杂质 不减:不减少被提纯的物质易分离:被提纯物质与杂质易分离易复原:被提纯物质要容易复原常用哪些方法分离、提纯物质?(1)物理方法:过滤、结晶、升华、蒸馏、萃取、分液、溶解等。
(2)化学方法:沉淀、置换、加热、分解等。
蒸发操作中要注意哪些安全事项?(1)蒸发皿中液体的量不能超过其容积的。
(2)蒸发过程中必须用玻璃棒不断搅拌,防止局部温度过高而使液体飞溅。
第二单元研究物质的实验方法课时1物质的分离和提纯[学习目标]1.初步了解根据混合物的性质,选择不同的分离方法对物质进行分离。
2.初步学会过滤、重结晶、蒸馏和分馏、萃取和分离,层析等分离物质的实验技能,能独立完成一些简单物质的分离和提纯的实验操作。
[知识梳理]1.现实世界中的各种物质,绝大多数都是物,人们需要其中某一种物质时,就必须将其。
你在初中化学中已学过的混合物的分离方法有。
2.现若有氯化钠和硝酸钾的混合物,可将它们分离开来的方法是,具体做法依次是。
3.现若有含泥沙的粗食盐,提纯食盐的方法是。
若有含硫酸钠、氯化镁和泥沙的粗食盐,提纯食盐的方法是4.若欲把稀碘水中的单质碘浓缩于CCl4中,可采取的方法是,具体做法是。
5.蒸馏常用于分离。
蒸馏过程中,温度计的位置是,加入碎瓷片的作用是,装置中各仪器的安装顺序的方向是从到,从到。
冷却水的流向是口进,口出。
6.人们可根据__________________,采取适当的方式将混合物中各物质分离开来。
不溶性固体与水的混合物,如___ ___,可用____ __方法分离。
可溶性固体与水的混合物,如___ ___,可用__ ____方法分离。
易溶固体与难溶固体的混合物,如___ ___,可通过__________方法分离;两种可溶性固体,若它们的溶解度随温度变化不同,如___ ___,可通过_________________方法将其分离;两种互不相溶的液体,如___ ___,可通过____________方法分离。
两种互相溶解但沸点不同的液体,如____ ____,可通过____________方法分离。
若混合物中各成分被某种固体吸附的难易不同,则可用____________方法分离。
若欲将极稀的溶液变成较浓的溶液,可采取的方法是_________________________。
胶体与溶液的混合物,可用______________方法分离。
[例题分析]例1. 现有氯化钠、硫酸钡、氯化钙三种固体的混合物,试关于它们回答下列问题:(1)若属于氯化钠固体中含有硫酸钡和氯化钙杂质,试述怎样将杂质除去。