水碘检测方法
- 格式:doc
- 大小:80.50 KB
- 文档页数:6

实验步骤(水碘)1、打开主机---打开电脑---双击桌面软件快捷方式----单击“仪器设置”---点击刷新显示COM口后点击连接----当显示“已连接”后证明电脑与主机通讯正常,此处需注意“测试样类型,仪器默认尿碘测试,需要改为水碘,然后仪器会有提示需要转换仪器后面的光度计开关”,2、单击“当前运行”---点击“复位”(注意复位时三根取液管需要悬空放置)---复位完成后开始“酸洗”点击确定,然后跳出是否烘干水浴池点击“否”(酸洗时需要在样品盘第一位放一根装有三分之一稀盐酸的试管)----然后在“复位”(同上)----复位完成时点击“水洗”同样不烘干。
然后点击“仪器设置”界面选择“抽水选项启动”,待溢水口有水流出时点击“抽水停止”按钮,接着设定加热炉温度为30℃后即可进行水碘实验。
再就可以准备实验-----取好样品(1000ul)----准备好所需要的足量的试剂。
3、标曲依次由高到低摆放至样品架中(前6位为固定标曲),样品最好有序摆放,以便于数据处理。
摆放好之后就可以选定浓度(0-100ug/l)---选好样品位数----点击“复位”---将三根取液管插入所对应的试剂瓶底部然后拧紧接头。
4、检查纯水桶,自来水桶中液位是否充足。
检查废液桶,样品废液瓶中的废液,要是太多就及时处理。
5、实验前的检查,准备都已经做好了之后就可以直接开始实验----点击“运行”确认运行该浓度的实验。
-----开始之后就可以在“实验数据”中填写对应的样品编号(双击出现“可编辑”后才能输入;此软件也可以直接下拉,需同名称有序序号,如:沙河市儿童1,沙河市儿童2,用鼠标选中第一位第二位有序下拉则会自动填充。
)。
输入完成后等待试验结束在后台中调取实验数据。
6、实验结束后数据查看在桌面“”该文件夹中的“实验数据”文件夹里按照时间查找最新实验数据可直接打印。
7、试验结束后如果说还要继续实验需要重新重复“复位”---“水洗”---“复位”后方可进行下一批实验(仪器会提醒你做注意事项,);如果说本次实验结束后仪器要长时间放置,则需要进行“复位”---“酸洗”---“复位”---“水洗”----“复位”----关机。

高碘地区地下水碘离子的检测本次实验采用离子色谱法对某高碘地区地下水中的碘离子进行了检测1.1 样品处理水样经0.45Um滤膜过滤,上机测试。
1.2 实验部分(1)仪器与试剂YC3000型离子色谱仪、脱气机、高效阴离子色谱柱、ASCD阴离子抑制电导池碳酸钠、碳酸氢钠(优级纯,科密欧试剂有限公司)碘化钾等优级纯试剂(2)测试条件淋洗液Na2CO3∕NaHCo3体系,流速LOmLZmin,柱压2.3MPa,室温,电导32,电流67mAo(3)实验内容(一)标准溶液配置与标准曲线制作:①碘化钾标准试剂预先在烘箱干燥至恒重,称取适量,精确至0.0002g,置于100mL容量瓶中,加入约70mL的超纯水,待试样溶解后定容至刻度,得到浓度为Lomg∕mL的标准溶液。
②精确移取LOmL碘离子标准溶液置于100mL容量瓶,加入二次去离子水稀释至刻度,得到10mg∕L的碘离子工作标准溶液。
③分别移取适量体积的碘离子工作标准溶液,置于10OmL容量瓶中,用二次去离子水定容至刻度,得到浓度由低到高的系列线性标准溶液。
④将上述线性标准溶液按浓度由低到高依次上机测试,并绘制标准工作曲线。
(二)水样测试经0.45Um滤膜过滤,上机测试。
(三)数据处理采用外标法进行数据处理,测得水样中碘离子的浓度。
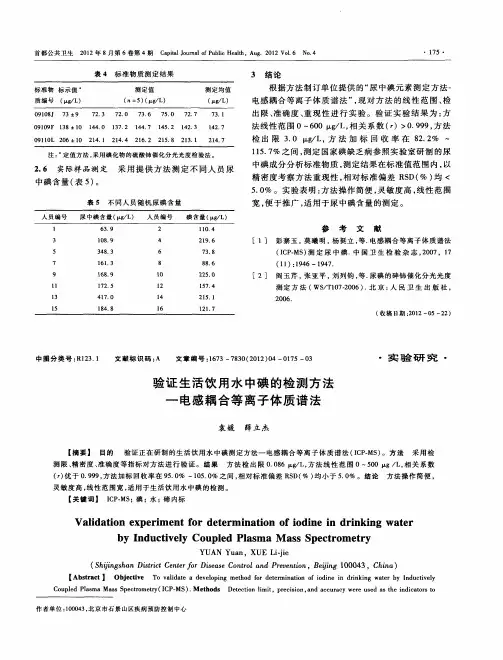
1.3 结果分析(1)碘离子标准谱图(2)标准曲线校正因孑:f0=1.55986E-6,fl=2.02749E-U相关系数:0.999394,200.0004,000,0003,800,0003.600,0003,400,0003,200,000:3,000,000;2,800,000:2.600,000:2,400,000:nn∩:1.4 结论本次实验采用离子色谱法测定某高碘地区地下水样中的碘离子含量。
该方法方便、可行,数据较为可靠。
检测数据:碘离子浓度0.176mg∕L°。




水中碘化物的测定方法离子色谱法检测水中碘化物其原理是采集的水样随着淋洗液进入阴离子分离柱,分离出的碘离子用电导检测器检测,根据碘离子保留时间定性,采用外标法进行定量。
当水样体积为250ul时此方法的检出限为0.002mg/L。
检测所需仪器1.离子色谱仪(具有电导检测器)。
2.色谱柱:阴离子分离柱和阴离子保护柱。
3.连续自再生的阴离子膜抑制器或同等性能抑制器。
4.一次性注射器:5ml。
5.微孔滤膜过滤器。
6.聚乙烯瓶或棕色玻璃瓶:500ml。
7.阳离子交换柱、固相萃取柱8.实验室常用仪器及设备检测所需试剂1.碘化钾(KI):优级纯,临用前在110℃烘干至恒重。
2.氢氧化钾(KOH):优级纯。
3.氢氧化钠(NaOH):优级纯。
4.碘化物标准贮备液1000mg/L称取1.3080g碘化钾,用水溶解并定容至1000ml;于4℃冷藏、避光可保存一年。
或使用市售有证标准溶液。
5.碘化物标准中间液100mg/L移取1000ml碘化物标准贮备液,用水稀释定容至100m,临用现配。
6.碘化物标准使用液10mg/L移取1000n碘化物标准中间液(55,用水稀释定容至100m,临用现配。
7.氢氧化钾溶液40 mmol/L称取22g8氢氧化钾(52),用水溶解并定容至100n0混,贮存于聚乙烯瓶中备用。
8.氢氧化钠饱和溶液在室温下取适量的氢氧化钠固体溶解于100ml水中,搅拌使其溶解,再继续加入氢氧化钠固体进行搅拌,直至有固体析出不再继续溶解为止,静置后取出澄清溶液备用。
9.高纯度氮气。
10.水系微孔滤膜0.45um水样的保存检测水样在采集时需要用聚乙烯瓶或棕色玻璃瓶,然后加入氢氧化钠饱和溶液调节pH。
将水样pH调节至12。
采集完成后要尽快检测,如果不能及时检测可以在0-4℃环境下进行保存,保存时间不超过24h。
采集后的水样要经过0.45um水系微孔滤膜进行过滤,弃去10ml初滤液,将剩余的滤液保存待测。
具体检测步骤1.色谱检测参考条件根据检测仪器说明书设定仪器。


生活饮用水中碘化物的检测方法(国家碘缺乏病参照实验室推荐方法)●本方法规定了用硫酸铈催化分光光度法测定生活应用水及其水源中碘化物的含量。
●本方法适用于生活饮用水及其水源中碘化物的测定。
●本方法可以测定0~10 μg/L (I-),0~100 μg/L (I-)和100~600 μg/L (I-)范围碘化物。
1. 原理利用碘对砷铈氧化还原反应的催化作用:H3AsO3 + 2Ce4+ + H2O→H3AsO4 + 2Ce3+ + 2H+反应中黄色的Ce4+被还原成无色的Ce3+,碘含量越高,反应速度越快,剩余的Ce4+则越少。
控制反应温度和时间,在一定波长下测定体系中剩余的Ce4+的吸光度,求出碘含量.2. 仪器2.1 超级恒温水浴箱:30℃±0.2℃2.2数显分光光度计:1cm比色杯2.3 玻璃试管:15 mm⨯120 mm或15 mm⨯150 mm2.4秒表3. 试剂(本标准所使用的试剂纯度除特别指明外均为分析纯)3.1浓硫酸(H2SO4,优级纯)3.2氢氧化钠(NaOH,优级纯)3.3三氧化二砷(As2O3)3.4氯化钠(NaCl,优级纯)3.5硫酸铈铵(Ce(NH4)4(SO4)4.4H2O)3.6碘化钾(KI,优级纯)3.7过硫酸铵(H8N2O8S2)3.8去离子水(H2O,应符合GB/T 6682二级水规格,电导率≤1.0 μs/cm)4. 溶液配制4.1硫酸溶液[c(H2SO4)=2.5 mol/L]:取140 mL浓硫酸[优级纯,ρ20=1.84]缓慢加入到700 mL去离子水中,冷却后用水稀释至1L。
4.2低浓度水碘(范围:0~10 μg/L)测定所需溶液(1)过硫酸铵溶液[c(H8N2O8S2)=0.5 mol/L]:称取57.05 g 过硫酸铵(H8N2O8S2),溶于500 mL去离子水中。
置冰箱(4℃)避光保存, 至少稳定1个月。
(2)亚砷酸溶液Ⅰ[c(H3AsO3)=0.060 mol/L]:称取5.9340 g 三氧化二砷(As2O3)、20.0 g氯化钠(优级纯)和2.0 g氢氧化钠置于1L的烧杯中,加水约500 mL,加热至完全溶解后冷至室温,再缓慢加入350 mL 2.5 mol/L硫酸溶液(1.4.1),冷至室温后用水稀释至1L,贮于棕色瓶中室温放置,可保存数月。

工厂废水测试碘含量标准
在工业废水处理中,碘含量的测试是一个重要的环节,因为碘是衡量水质污染物含量的一个重要指标。
在测试工业废水中碘的含量时,通常会使用碘量法。
碘量法是一种直接或间接测定水中碘含量的方法,其原理是通过测定水中的碘与硫代硫酸钠反应生成的碘的量,来计算出水中碘的含量。
具体的测试步骤如下:
1. 取一定量的废水样品,加入硫酸酸化,使其中的碘离子转化为游离碘。
2. 然后加入淀粉溶液,如果水中含有碘,就会使淀粉变为蓝色,这是碘的量就可以通过比色法来确定。
3. 计算出废水中的碘含量。
具体的测试标准会根据你的测试目的和环境要求来确定。
如果你的废水是生活废水,那么可能需要参考生活污水的排放标准。
如果你的废水是工业废水,那么可能需要参考工业废水的排放标准。
无论是哪种废水,都要求碘的含量不能超过规定的标准。

生活饮用水中碘化物的检测方法1.电位滴定法:这是一种常用的测定方法,通过测定溶液的电位变化来确定溶液中碘化物的含量。
首先,将样品经过预处理后,用硝酸将样品中的碘化物转化为碘酸盐。
然后,将样品溶液与电极连接在一起,通过向样品中滴定一定浓度的亚硝酸钠溶液来观察溶液的电位变化。
当溶液中的碘化物被亚硝酸钠滴定完后,电位突然下降,此时记录电位变化的体积,根据计算公式可以得到样品中碘化物的含量。
2.荧光法:荧光法是一种快速、灵敏、无污染的检测方法。
该方法利用吸收光谱和荧光光谱的差异来判断样品中碘化物的含量。
首先,将样品与一种特定的荧光染料反应生成荧光复合物,然后对该复合物进行荧光测量。
根据荧光的强度来确定样品中碘化物的含量。
3.离子色谱法:离子色谱法是一种常用的检测水中离子的方法之一、这种方法可用于测定饮用水中碘离子的含量。
首先,将样品中的离子通过离子交换柱分离,然后通过检测器检测离子的浓度。
根据样品中离子的峰面积或峰高来计算样品中碘化物的含量。
4.高效液相色谱法:这是一种高效、灵敏的检测方法,也可用于测定饮用水中碘化物的含量。
该方法利用高效液相色谱仪对样品中的碘化物进行分离和测量,在分离过程中使用特定的流动相和柱温来实现高效的分离。
通过仪器测量样品中离子的峰面积或峰高,根据标准曲线来计算样品中碘化物的含量。
需要注意的是,在进行碘化物的检测时,需要对水样进行适当的预处理以去除可能干扰的物质。
例如,可以通过氯仿提取法提取碘化物,并用硫酸钾和氯仿洗涤去除可能的干扰物质。
此外,在进行碘化物的检测过程中,需要仪器和试剂的标定、校准以确保结果的准确性和可靠性。
总结而言,生活饮用水中碘化物的检测方法多种多样,每种方法都有其特点和适用范围。
在选择合适的检测方法时,需要考虑样品的性质、检测的灵敏度和准确性要求以及实验条件等因素,并根据实际情况选择合适的方法。
海水中碘含量的测定方法
海水中碘含量的测定方法有多种,以下提供两种常见的方法:
方法一:
1.酸化煮沸:取适量海水,加入硫酸酸化,煮沸蒸发至干,除去水,再加入硫酸酸化,通入高纯氮驱赶出其中的碘,通入吸收液中。
2.氧化:加入适量氧化剂,将碘氧化成碘离子。
3.滴定:用标准溶液滴定吸收液中的碘离子,根据消耗的标准溶液体积计算出海水中碘的含量。
方法二:
1.采集一定体积的海水,加入适量的氢氧化钠溶液,将碘离子转化为碘酸根离子。
2.用标准溶液滴定生成的碘酸根离子,根据消耗的标准溶液体积计算出海水中碘的含量。
以上方法仅供参考,具体操作请按照专业人士的指导进行。
水中碘含量标准检测方法1. 碘是人体必需的微量元素之一,在水中的适量含量对人体健康至关重要,因此需要标准化的检测方法来确定水中的碘含量是否符合安全标准。
2. 传统的水中碘含量检测方法包括化学分析法和物理分析法。
3. 化学分析法是指利用化学试剂和反应原理来测定水中碘的含量,常采用的方法有吸光光度法、滴定法和原子吸收光谱法。
4. 吸光光度法是基于碘与特定试剂之间的光化学反应,通过测量溶液在特定波长处的吸光度来确定碘的含量。
5. 滴定法是通过加入已知浓度的反应溶液到待测溶液中,根据滴定反应的终点变化来确定碘的含量。
6. 原子吸收光谱法则是通过光谱仪测量碘在特定波长处的吸光度,然后根据标准曲线来计算出碘的含量。
7. 物理分析法是指利用物理性质或仪器设备来测定水中的碘含量,常使用的方法有电化学法和光谱法。
8. 电化学法是通过测量溶液中氧化还原反应的电流强度或电位来确定碘的含量,常采用的方法有极谱法和电位滴定法。
9. 光谱法是利用碘溶液在特定波长处的吸光度与碘的含量成正比关系,通过光度计或分光光度计来测量吸光度。
10. 标准的水中碘含量检测方法应该具备准确、快速、灵敏和可靠的特点,以确保结果的准确性和可重复性。
11. 选择合适的检测方法需要考虑样品的特性、目标检测碘的浓度范围、仪器设备的可用性和实验条件等因素。
12. 在进行水中碘含量检测之前,需要对样品进行预处理,如过滤、稀释或提取等,以消除对测量结果的干扰。
13. 检测前需要准备标准溶液,根据已知浓度的标准物质制备一系列浓度递增的碘溶液,用于构建标准曲线和校准仪器。
14. 校准仪器是指通过测量标准溶液的吸光度或电流强度来调整仪器的灵敏度和准确性,以确保检测结果的精准度。
15. 标准曲线是根据已知浓度的标准溶液的吸光度或电流强度与其浓度之间的关系绘制而成,用于计算待测样品中碘的含量。
16. 检测过程中需要注意测量条件的控制,如温度、pH值、光线强度等因素,以确保实验结果的准确性和可靠性。
方法发表在《中国地方病学杂志》2007年第26卷第3期,333-336。
生活饮用水中碘化物的检测方法
本方法规定了用硫酸铈催化分光光度法测定生活饮用水及其水源中碘化物的含量。
本方法适用于生活饮用水及其水源中碘化物的测定。
本方法可以测定碘含量在0~10 μg/L (I-),0~100 μg/L (I-)和100~600 μg/L (I-)范围的碘化物。
本方法最低检测质量浓度为0.2 μg/L (I-),若取2ml水样,最低检测质量为0.4ng。
1. 原理
利用碘对砷铈氧化还原反应的催化作用:
H3AsO3 + 2Ce4+ + H2O→H3AsO4 + 2Ce3+ + 2H+
反应中黄色的Ce4+被亚砷酸还原成无色的Ce3+,碘含量越高,反应速度越快,剩余的Ce4+则越少。
控制反应温度和时间,在一定波长下测定体系中剩余的Ce4+的吸光度,求出碘含量。
2. 仪器
2.1 超级恒温水浴箱:30℃0.2℃
2.2 数显分光光度计:1cm比色杯
2.3 消解仪
2.4 移液器
2.5 玻璃试管:15 mm120 mm或15 mm150 mm
2.6 秒表
3. 试剂(本标准所使用的试剂纯度除特别指明外均为分析纯)
3.1浓硫酸(H2SO4,优级纯)
3.2氢氧化钠(NaOH,优级纯)
3.3三氧化二砷(As2O3)
3.4氯化钠(NaCl,优级纯)
3.5硫酸铈铵(Ce(NH4)4(SO4)
4.4H2O)
3.6碘化钾(KI,优级纯)
3.7过硫酸铵(H8N2O8S2)
3.8去离子水(H2O,应符合GB/T 6682二级水规格,电导率1.0 s/cm)
4. 溶液配制
4.1硫酸溶液[c(H2SO4)=2.5 mol/L]:取140 mL浓硫酸[优级纯,
ρ20=1.84]缓慢加入到700 mL去离子水中,冷却后用水稀释至
1L。
4.2低浓度水碘(范围:0~10 μg/L)测定所需试剂的配制
过硫酸铵溶液[c(H8N2O8S2)=0.50 mol/L]:称取57.1 g 过硫酸铵(H8N2O8S2),定溶于500 mL去离子水中。
置冰箱(4℃)避光保存, 至少稳定1个月。
亚砷酸溶液Ⅰ[c(H3AsO3)=0.060 mol/L]:称取5.9 g 三氧化二砷(As2O3)、20.0 g氯化钠(优级纯)和2.0 g氢氧化钠置于1L的烧杯中,加水约500 mL,加热至完全溶解后冷至室温,再缓慢加入350 mL 2.5 mol/L硫酸溶液(1.4.1),冷至室温后用水稀释至1L,贮于棕色瓶中室温放置,可保存数月。
硫酸铈铵溶液Ⅰ[c(Ce4+)=0.012 mol/L]:称取8.0 g硫酸铈铵(Ce(NH4)4(SO4)4.4H2O)溶于700 mL 2.5mol/L硫酸溶液(1.4.1),用水稀释至1L,贮于棕色瓶中避光室温放置, 可保存数月。
4.3中浓度水碘(范围:0~100 μg/L)测定所需溶液
亚砷酸溶液Ⅱ[c(H3AsO3)=0.10 mol/L]:称取10.0 g 三氧化二砷(As2O3)、25.0 g氯化钠(优级纯)和2.0 g氢氧化钠置于1L的
烧杯中,加水约500 mL,加热至完全溶解后冷至室温,再缓慢
加入200 mL 2.5 mol/L硫酸溶液(1.4.1),冷至室温后用水稀释
至1L,贮于棕色瓶中室温放置,可保存数月。
硫酸铈铵溶液Ⅱ[c(Ce4+)=0.053 mol/L]:称取35.4 g硫酸铈铵溶于490 mL 2.5 mol/L硫酸溶液(1.4.1),用水稀释至1L,贮于棕色瓶
中避光室温放置, 可保存数月。
4.4高浓度水碘(范围:100~600 μg/L)测定所需溶液
亚砷酸溶液Ⅲ[c(H3AsO3)=0.060 mol/L]:称取6.0 g 三氧化二砷(As2O3)、18.0 g氯化钠(优级纯)和2.0 g氢氧化钠置于1L的
烧杯中,加水约500 mL,加热至完全溶解后冷至室温,再缓慢
加入160 mL 2.5 mol/L硫酸溶液(1.4.1),冷至室温后用水稀释
至1L,贮于棕色瓶中室温放置,可保存数月。
硫酸铈铵溶液Ⅲ[c(Ce4+)=0.053 mol/L]:称取35.4 g硫酸铈铵溶于490 mL 2.5 mol/L硫酸溶液(1.4.1),用水稀释至1L,贮于棕色瓶
中避光室温放置, 可保存数月。
4.5碘标准溶液:
贮备液:准确称取经硅胶干燥器干燥24 h的碘化钾0.1308 g于烧杯中,用0.1%NaOH溶液溶解,定量移入1000 mL容量瓶,再用
0.1%NaOH溶液稀释至刻度。
此溶液1 mL含碘100 g。
置冰箱
(4℃)内可保存半年以上。
中间溶液Ⅰ:临用时吸取10.00 mL贮备液置于100 mL容量瓶中,用
0.1%NaOH水溶液稀释至刻度,此溶液1mL含碘10 g。
中间溶液Ⅱ:临用时吸取10.00 mL中间溶液Ⅰ置于100 mL容量瓶中,用0.1%NaOH水溶液稀释至刻度,此溶液1mL含碘1g。
中间溶液Ⅲ: 临用时吸取10.00 mL碘标准中间溶液Ⅱ置于100 mL容量瓶中, 用0.1%NaOH水溶液稀释至刻度. 此溶液碘浓度为
100 μg/L。
高浓度水碘标准应用系列溶液:临用时吸取碘标准中间溶液Ⅰ1.00,
2.00,
3.00,
4.00,
5.00,
6.00 mL分别置于100 mL容量瓶中,
用0.1%NaOH水溶液稀释至刻度。
此标准系列溶液的碘浓度分
别为100,200,300,400,500,600 μg/L。
中浓度水碘标准应用系列溶液:临用时吸取碘标准中间溶液Ⅱ0,
2.00,4.00, 6.00, 8.00,10.00 mL分别置于100 mL容量瓶中,
用0.1%NaOH水溶液稀释至刻度。
此标准系列溶液的碘浓度分
别为0, 20, 40, 60, 80,100 μg/L。
低浓度水碘标准应用系列溶液:临用时吸取碘标准中间溶液Ⅲ0,
2.00,4.00,6.00,8.00,10.00 mL分别置于100 mL容量瓶中,
用0.1%NaOH水溶液稀释至刻度。
此标准系列溶液的碘浓度分
别为0, 2, 4, 6, 8,10 μg/L。
5.分析步骤
5.1 低浓度水碘(范围0~10 μg/L)的测定
分别取碘标准应用系列溶液及水样各2.0 mL置于玻璃试管中,各管加入0.5 mL 0.5 mol/L过硫酸铵溶液,混匀后置于消化控温加热装
置中,于100℃消化20分钟(通风橱不是必需的),取下冷却至
室温.
各管加入1.0 mL亚砷酸溶液Ⅰ,充分混匀后置于30℃恒温水浴中温浴15min。
使用秒表计时,依顺序每管间隔15-30秒向各管准确加入0.5 mL硫酸铈铵溶液Ⅰ,立即混匀,放回水浴中。
待第一管加入硫酸铈铵溶液Ⅰ后准确反应30min时,依顺序每管间隔15-30秒于405 nm波长下,用1 cm比色杯,测定各管的吸光度。
样品碘含量的计算:碘浓度C与测得的吸光度A之间的定量关系为C=
a +
b lnA(或lgA), 计算出标准曲线的回归方程,将样品的吸光度
值代入此方程,求出样品的碘浓度。
5.2中浓度水碘(范围:0~100 μg/L)的测定
分别取碘标准应用系列溶液及水样各1.0 mL置于玻璃试管中,然后加入2.5 mL亚砷酸溶液Ⅱ,充分混匀后置于30℃恒温水浴中温浴
15min。
使用秒表计时,依顺序每管间隔15~30秒向各管准确加入0.5 mL硫酸铈铵溶液Ⅱ,立即混匀,放回水浴中。
待第一管加入硫酸铈铵溶液Ⅱ后准确反应15min时,依顺序每管间隔15~30秒于420 nm波长下,用1cm比色杯,测定各管的吸光
度。
样品碘含量的计算:碘浓度C与测得的吸光度A之间的定量关系为C=
a +
b lnA(或lgA), 计算出标准曲线的回归方程, 将样品的吸光
度值代入此方程,求出样品的碘浓度。
5.3高浓度水碘(范围:100~600 μg/L)的测定
分别取碘标准应用系列溶液及水样各0.2 mL置于玻璃试管中,然后加入3.5 mL亚砷酸溶液Ⅲ,充分混匀后置于30℃恒温水浴中温浴
15min。
使用秒表计时,依顺序每管间隔15~30秒向各管准确加入0.5 mL硫酸铈铵溶液Ⅲ,立即混匀,放回水浴中。
待第一管加入硫酸铈铵溶液Ⅲ后准确反应15min时,依顺序每管间隔15~30秒于405 nm波长下,用1cm比色杯,测定各管的吸光度。
样品碘含量的计算:碘浓度C与测得的吸光度A之间的定量关系为C=
a +
b lnA(或lgA), 计算出标准曲线的回归方程, 将样品的吸光
度值代入此方程,求出样品的碘浓度。
省、地市级碘缺乏病实验室水碘外质控考核结果报表省份:检测单位:
检测方法:
说明
1. 上表为省、地市两级碘缺乏病实验室水碘外质控考核报表,本次考核发放2个考核样。
请将考核样贮存于4℃冰箱内保存,检测前轻轻摇匀,拧开塑料瓶盖后小心开启铝箔即可进行检测。
2. 请参加考核的实验室采用“适合缺碘及高碘地区水碘检测的方法研究”(中国地方病学杂志,2007,26(3):333-336)中0-100ug/L范围的测定方法进行检测,共检测三次,分三个工作日完成,每次进行平行检测,结果填入上表。
请同时填报任意一次检测的标准曲线吸光度值。
3. 请省级实验室将本省省级和地市级实验室水碘检测结果汇总,于2016年4月12日前上报至国家碘缺乏病参照实验室。